卒中后尿失禁患者应用盆底肌电刺激联合Kegel运动的康复效果观察
王丽萍, 聂玉琴, 朱爱丽
(1新疆医科大学护理学院, 乌鲁木齐 830063; 2新疆医科大学第五附属医院口腔科, 乌鲁木齐 830011;新疆医科大学第二附属医院3护理部, 4妇科, 乌鲁木齐 830092)
尿失禁是脑卒中后常见并发症,表现为膀胱失去控制,患者无意识排尿[1]。脑卒中后尿失禁(Post-stroke urinary incontinence,PSUI)患病率可达32%~79%[2],严重影响患者的生活质量。有研究发现,44%和38%的患者在脑卒中后3个月和12个月被诊断出尿失禁[3]。PSUI患者自理水平普遍较低,常出现焦虑、沮丧、尴尬等心理反应,从而导致患者社会参与度及生活质量下降[4]。有研究报道,盆底肌电刺激和凯格尔(Kegel)运动治疗尿失禁均有较好的疗效[5-6],但评价盆底肌电刺激联合Kegel运动治疗脑卒中尿失禁的报道很少。基于此,本研究通过观察盆底肌电刺激联合Kegel运动治疗脑卒中后尿失禁的效果,以期为PSUI患者的康复治疗提供新的治疗依据,现报道如下。
1 资料与方法
1.1 一般资料选择2021年7月至2022年7月在新疆医科大学第二附属医院经颅脑CT或MRI检查确诊的脑卒中后尿失禁患者100例。纳入标准:(1)符合脑卒中及尿失禁诊断标准;(2)确定是卒中后出现尿失禁症状;(3)年龄在45岁以上;(4)意识清楚,病情稳定,能够配合治疗;(5)患者及家属均同意,并签署知情同意书。排除标准:(1)既往患尿失禁、非脑卒中导致的尿失禁;(2)合并严重失语、意识或认知障碍的患者;(3)伴有尿路感染的患者;(4)合并有肝、肾、心等脏器严重原发性疾病者。按随机数字表法分为观察组、对照组,各50例。观察组:女性28例,男性22例,年龄47~82岁,平均(65.48±9.57)岁;对照组:女性30例,男性20例,年龄46~88岁,平均(66.38±10.33)岁。两组患者年龄、性别比较,差异无统计学意义(P>0.05)。本研究通过新疆医科大学第二附属医院伦理委员会批准,所有患者签署知情同意书。
1.2 方法
1.2.1 对照组 (1)用药护理:根据医嘱行脑血管疾病及其他伴随疾病的常规药物治疗。(2)饮食护理:摄入清淡、低盐低脂、易消化的食物,同时补充蛋白质。(3)心理护理:与患者建立信任关系,向患者进行尿失禁相关知识健康宣教,指导患者进行放松训练,使其树立战胜疾病的信心。(4)行为疗法:按照患者实际情况及饮水习惯,制定饮水计划,定时定量饮水(日饮水量控制在1 500~2 000 mL),避免饮用浓茶和咖啡,定时排尿,并逐渐延长排尿间隔时间。治疗4周后进行效果评价。
1.2.2 观察组 在对照组基础上采用盆底肌电刺激联合Kegel训练:(1)采用生物反馈电刺激治疗仪(上海诺诚电气股份有限公司,型号XCH-C1/C2)进行电刺激治疗,主要技术参数:频率5~100 Hz,电流强度0~25 mA,波宽200~500 us。嘱患者治疗前排空大小便,女性患者取仰卧位,双腿稍屈曲(男性患者取侧卧位),将感应电极片贴于患者腹部,电极用0.9%生理盐水浸湿后置入阴道(女性)或肛门(男性)。在医师指导下制定针对性的治疗方案,明确电刺激模式,刺激电流大小以患者能感到肌肉收缩或跳动为准。每日1次,每次40 min,前20 min被动进行电刺激治疗,后20 min进行生物反馈刺激,根据设备语音提示及可视的图形进行主动训练,10次为1个疗程。共做2个疗程。(2)采用凯格尔(Kegel)运动增强盆底肌肉肌力。嘱患者运动前排空膀胱,主动收缩、夹紧尿道口与肛门,然后再放松[7]。每次收缩5~10 s,继而放松5~10 s,重复动作20次为1次完整练习,每日进行2~3次,站立、仰卧、俯卧、坐位以及步行时均可进行训练。前3次由护理人员指导完成,之后由患者自行完成。治疗4周后进行效果评价。
1.3 观察指标
1.3.1 24 h排尿情况 根据中国康复医学会康复护理专业委员会制定的《神经源性膀胱指南版》指导患者详细记录24 h排尿情况,包括24 h排尿次数和24 h尿失禁次数。
1.3.2 盆底肌表面肌电评估(Glazer)[8]总得分 由生物反馈电刺激治疗仪测出,Glazer评估包括5个阶段:前静息阶段、快速收缩阶段、紧张收缩阶段、耐力收缩阶段及后静息阶段。Glazer总得分越低,表示盆底肌肉功能越差。
1.3.3 尿失禁生活质量问卷(Incontinence quality of life questionnaire,I-QOL)[9]评分I-QOL包括行为的限制、心理的影响、社会障碍,共22个条目。每个条目根据严重程度按1~5分评分,总分0~100分;得分越低,表示尿失禁程度越严重,对生活影响越大。
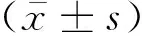
2 结果
2.1 两组患者24 h排尿次数和尿失禁次数比较观察组7例患者治疗中自动退出,另有1例因治疗中感到口干而终止;对照组5例患者未完成治疗。最终,观察组42例(男性17例,女性25例),对照组45例(男性19例,女性26例)完成研究。治疗前两组患者24 h排尿次数、24 h尿失禁次数比较差异无统计学意义(P>0.05)。治疗后观察组24 h排尿次数、24 h尿失禁次数显著低于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组患者24 h排尿情况比较(次,
2.2 两组患者Glazer评估总得分比较两组患者治疗前Glazer评估总得分比较差异无统计学意义(P>0.05)。治疗后观察组Glazer评估总得分显著高于对照组,差异有统计学意义(P<0.05),见表2。

表2 两组患者Glazer评估总得分比较[分, M(P25,P75)]
2.3 尿失禁生活质量问卷(I-QOL)得分比较两组患者治疗前I-QOL得分比较差异无统计学意义(P>0.05)。治疗后观察组I-QOL得分明显高于对照组,差异有统计学意义(P<0.05),见表3。

表3 两组患者I-QOL评分比较[分, M(P25,P75)]
3 讨论
PSUI的主要原因是尿道括约肌损伤和神经功能障碍[10]。脑卒中后会导致抑制排尿反射减弱或消失,继而引起膀胱功能亢进而出现尿频、尿急和尿失禁等症状[11-13]。盆底肌主要由肛门括约肌、肛提肌及尿道括约肌等组成,脑卒中后可引起盆底肌肉麻痹或无力而导致尿失禁[14]。盆底肌电刺激(Pelvic floor electrical stimulation,PES)采用电流刺激盆底肌群,可有效提高盆底肌力,相关动物实验表明电刺激阴部神经能够促进压力性尿失禁大鼠的神经再生[15-16]。近年,已有将电刺激原理应用到PSUI治疗的报道[17-18]。
本研究结果显示,治疗后观察组24 h排尿次数、24 h尿失禁次数显著低于对照组,观察组Glazer评估总得分明显高于对照组,说明观察组效果优于对照组。同时,观察组患者每次尿量也有增加。研究中个别患者Glazer总得分无变化,但阶段得分有提高,可认为治疗依然有效。分析其原因,观察组较对照组康复机制更加明确,因为PES可直接刺激盆底肌群,提升神经肌肉兴奋性,唤醒盆底肌神经,抑制逼尿肌收缩,提高盆底肌抗疲劳肌纤维比例[19];生物反馈电刺激过程中,大脑皮层可接受到反馈信息,从而控制并协调排尿反射。且患者接受生物反馈电刺激治疗时,可直观看到肌电图曲线,这在很大程度上提高了患者的主动性。本研究还显示,治疗后观察组I-QOL得分明显高于对照组。可能是因为观察组患者经治疗后,24 h排尿频次、尿失禁次数均明显减少,对日常外出、穿衣、饮食、甚至性生活都有积极的作用,从而提高了患者生活质量。
临床中,多数PSUI不被重视,尿失禁管理通常被描述为一个护理问题,采取一般护理,效果欠佳[20-21]。本研究结果显示,盆底肌电刺激联合Kegel运动较常规康复方法更具优势,但本研究也存在一定局限性,如样本量少、随访时间短、入选样本未按脑卒中类型或病变部位进行分类等。今后需设计更加严谨的试验方案,进一步观察盆底肌电刺激联合Kegel运动对PSUI患者的康复效果。
综上,在常规护理的基础上,采用盆底肌电刺激联合Kegel运动能够有效改善PSUI患者尿失禁症状,提高患者生活质量,且患者易接受,值得临床推广。

