中药配方颗粒汤剂与传统汤剂一致性评价存在的问题及建议*
麻利杰,姚静,路露,侯富国,岳佑凇,谢梦迪,王艳丽,李学林,刘瑞新
(1.河南中医药大学药学院,郑州 450046;2.河南中医药大学第一附属医院药学部,郑州 450000;3.河南省中药临床应用、评价与转化工程研究中心,郑州 450000;4.河南中医药大学呼吸疾病中医药防治省部共建协同创新中心,郑州 450046;5.河南省中药临床药学中医药重点实验室,郑州 450000)
中药配方颗粒汤剂是传统汤剂临床应用的有力补充[1-2]。开展二者的一致性评价对于解决二者是否等效的争议、促进中药配方颗粒合理应用以及推进中药国际化都具有非常重要的意义。
近年来,已经有许多学者借鉴化学仿制药一致性评价开展了中药配方颗粒汤剂与传统汤剂一致性评价[3],一定程度上促进了中药配方颗粒的良性发展。但目前二者的评价没有明确流程和统一标准,开展二者一致性评价时应该优先选择单味药还是复方、配方颗粒应该选择自制还是市售、评价时应该选择单方面对比还是多方面比较等问题一直争议不断。因此,尽管已经有很多学者从多方面、多角度对比了二者的一致性,但目前二者是否等效、等效范围多大、不等效时应如何处理等问题仍无定论。
笔者在本文拟以二者一致性评价流程为主线,通过梳理二者一致性评价过程中存在的问题,并针对有争议的问题进行分析,再基于真实世界中药配方颗粒的合理应用提出有争议问题的解决方案,对二者等效范围、不等效时的解决方法提出初步建议,以期初步构建一套完整、合理的一致性评价流程,为二者及其他中药制剂一致性评价研究提供参考,为推动中药配方颗粒及其他中药剂型合理应用提供参考。
1 化学药物一致性评价概述及中药配方颗粒汤剂一致性评价特点与需求
1.1化学药物一致性评价概述 化学药物的一致性评价又称化学药品一致性评价,系指仿制化学药品的质量和疗效应与原研药品保持一致,包括杂质谱一致、稳定性一致及体内外溶出规律一致[4]。该评价是提高仿制药品质量、降低患者用药费用、提高药品有效性、提升医疗行业发展质量以及推动供给侧结构改革的重要途径[5]。其最早起源于美国1968年提出的药物有效性实施项目,随后日本、欧盟等国家和地区也相继开展[3],我国化学药物一致性评价工作起步较晚[6],迄今为止仅有十余年的历史。
1.2中药配方颗粒汤剂与传统汤剂一致性评价的特点与需求 相较于化学仿制药物的一致性评价,中药配方颗粒汤剂与传统汤剂一致性评价主要包括以下特点:①评价层次和指标选择相对复杂;②评价体系和相关标准亟待完善;③个性化评价相对重要;④原料来源对评价结果影响较大[7-8]。
根据上述特点,中药配方颗粒汤剂与传统汤剂的一致性评价应满足以下需求:①基于中医药的“整体观”思想开展综合分析,合理选择评价层次和指标;②建立完善的评价体系和相关评价标准;③在共性化一致性评价的基础上开展个性化一致性评价;④对两类对象的原料来源情况作出明确规定。
2 中药配方颗粒汤剂与传统汤剂一致性评价现状及存在问题
2.1评价现状 目前二者的一致性评价依据评价流程的不同阶段可分为不同的类别,具体如下:①依据研究载体的不同可分为单味药研究和复方研究[9];②依据原料来源不同可分为来源批次一致的研究和来源批次不一致的研究;③依据研究内容不同可分为化学成分研究、药理药效研究和临床疗效研究;④依据研究结果不同可分为二者具有一致性的研究、配方颗粒汤剂优于传统汤剂的研究和配方颗粒汤剂次于传统汤剂的研究[10-11]。当以单味药为载体时,研究内容主要以化学成分和药理药效研究为主;当以复方为载体时,研究内容主要以化学成分和临床疗效研究为主[12-13]。笔者总结了2020—2021年度进行过一致性评价的配方颗粒品种,并按照发表先后顺序进行了整理,结果发现其中以单味药为载体进行的研究共27个,内容为化学成分和药理药效的研究占比100%;以复方为载体的研究共57个,包括化学成分和临床疗效研究共占比89.47%。具体见表1。
2.2存在的问题
2.2.1现阶段开展一致性评价的先后及主次不明 当下二者的一致性评价研究依据研究载体的不同主要可分为两类:一是以单味药为研究载体,比较配方颗粒汤剂与传统汤剂质量的一致性;二是以某一复方为研究载体,比较单煎配方颗粒混合后制备的配方颗粒汤剂与合煎传统汤剂的质量一致性[103]。然而,现阶段应以哪类研究载体为主,优先开展哪部分研究内容仍无明确定论。既有学者认为单味药的质量统一是当前研究的主要内容,以单味药为载体开展了一致性评价[31,102];也有学者认为单煎与合煎的差异是目前评价的重心,以复方为载体比较二者的一致性[104]。但由表1数据可知,总体上复方研究多于单味药,二者比例约为2:1。
2.2.2饮片和配方颗粒的来源批次是否需要统一未明确 近年来,随着二者一致性评价范围的扩大,饮片和配方颗粒的来源批次是否应保持统一也逐渐成为研究者关注的焦点。既有学者进行了来源批次统一的中药配方颗粒汤剂与传统汤剂一致性评价[40,104],也有学者基于真实世界对比了来源批次不统一的中药配方颗粒汤剂与传统汤剂的一致性[21,31,35,96]。但目前二者来源批次是否应当统一尚未明确,统一或不统一时二者的来源批次如何选择等问题也众说纷纭。
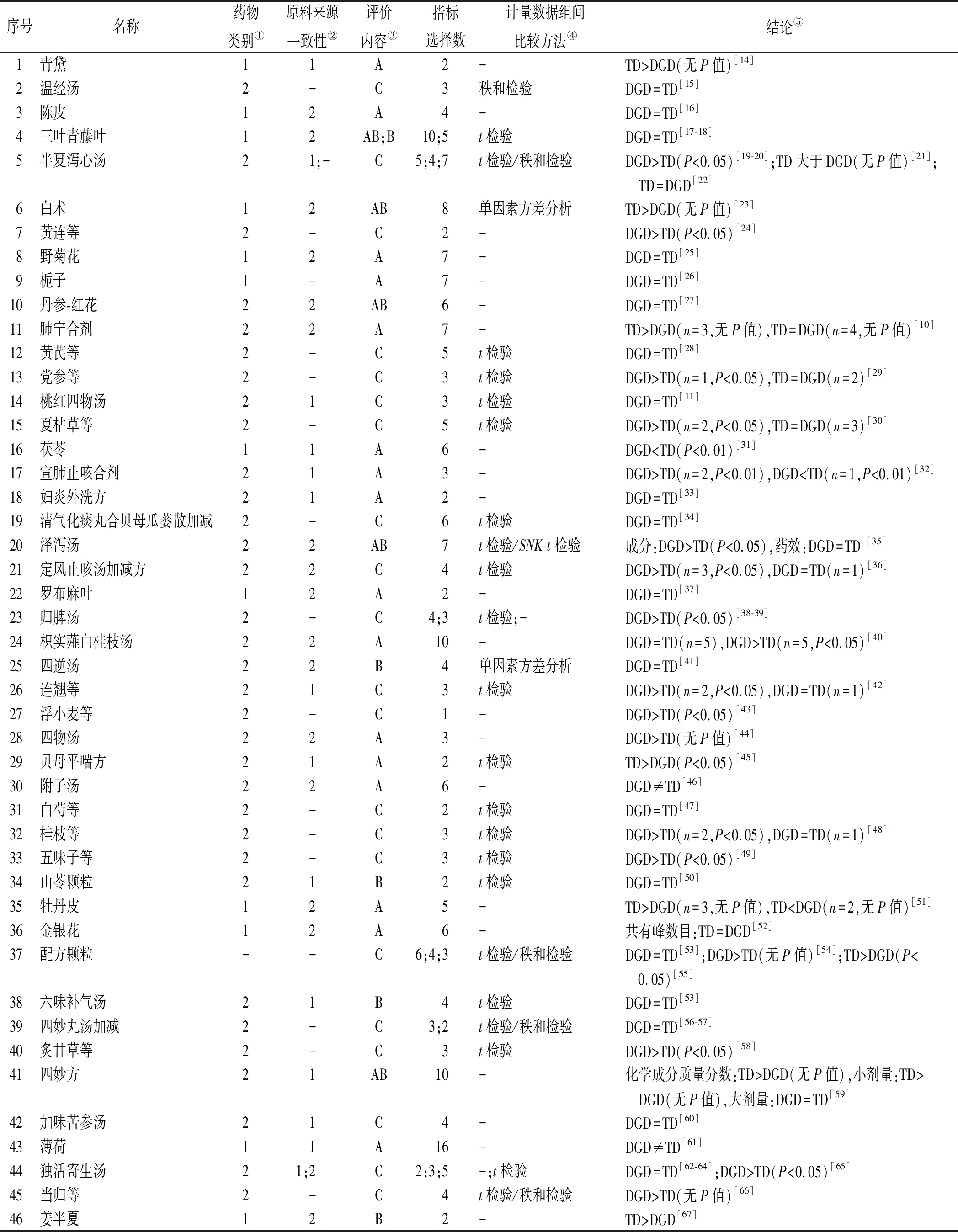
表1 2020—2021年度中药配方颗粒汤剂与传统汤剂一致性评价
2.2.3评价品种的数目与类型可能存在局限性和不均衡性 首先,进行过一致性评价的配方颗粒品种较少。以单味中药配方颗粒汤剂为例,尽管国家颁布了196种单味中药配方颗粒的标准(截至2022年4月),但过去十年已进行过评价的配方颗粒数目不足50%(表2)。其次,评价品种的类型比例存在一定失衡[105-107]。笔者在中国知网(CNKI)上以“ 配方颗粒”为关键词检索2017—2022年进行过一致性评价的中药配方颗粒品种,结果共有40余种配方颗粒进行了一致性评价,而动物药和矿物药均只有1种,分别为广地龙和自然铜,其余均为植物药。
2.2.4评价层次和指标的选择缺乏系统性 首先,对于单味中药配方颗粒汤剂而言,目前大部分学者仅针对化学成分或药理作用等单一方面进行评价,仅有少数学者从化学成分、药理药效等多方面综合比较二者的一致性[108-109],如2020—2021年仅有7%配方颗粒品种进行了综合对比(表1)。其次,中药配方颗粒汤剂成分众多,性质复杂,单味中药配方颗粒汤剂往往具有多种药理作用。然而,部分学者在比较二者药理作用时,往往基于实验的复杂程度去选择指标,而非依据药物的物质基础。再者,单味中药配方颗粒大多并非只具有一种主要功效,当其具有多种功效时,部分学者仅选取个别指标进行研究,其做法是否恰当仍值得进一步探讨。
2.2.5缺乏个性化评价方法与模式 现有评价方法的主要特点为共性化,缺乏适合配方颗粒品种本身特点的个性化评价方法的参与。以成分的评价为例,现阶段主要通过现代科学仪器测定指标性/代表性成分的种类、含量或特征图谱的相似度来对比二者成分的一致性[110-111],但对于某些有效性成分为微量元素的配方颗粒,按照共性化的方法去评价其汤剂与传统汤剂的一致性是不恰当的。此外,不同品种的配方颗粒性质存在较大差异,其评价方法类型的主次也应有所区别,如对于有效成分明确的植物药和有效成分不明确的动物药或矿物药,评价方法类型的主次必然存在一定差异。
2.2.6数据处理方法不尽合理 目前二者一致性评价中对计量资料主要采用t检验来判断二者是否存在差异及差异程度。然而,少有学者关注到该检验的前提条件,即数据近似符合正态分布,也极少有学者会在处理相关数据时对数据进行正态性检验[112]。导致的直接结果就是尽管中药配方颗粒汤剂与传统汤剂一致性评价研究已经有很多,但其中可靠性较强的研究数目有多少无从知晓。
2.2.7评价标准亟待完善 目前对于二者化学成分一致性评价的研究主要包括:①指纹图谱相似度;②化学成分种类和数目;③《中华人民共和国药典》(以下简称《中国药典》)和国家标准规定的指标性成分含量、重金属及有害元素含量;④除指标性成分以外的代表性成分含量。对药理作用一致性评价的研究主要包括对实验动物的疗效差异和实验细胞的作用强弱。尽管部分文献已提出了配方颗粒汤剂与传统汤剂指标性成分含量、生物活性的一致性范围,但该范围是否合理仍有待进一步阐明,指纹图谱的相似度、化学成分种类和数目等指标的一致性范围也函待确定。
2.2.8评价结果缺乏深入分析 提出二者一致性评价是为了指导临床合理用药,促进中药配方颗粒合理应用,并非单纯比较二者孰优孰劣。然而,目前部分研究中对于二者的比较仅限于得出谁好谁坏的结果,并未对结果进行延伸分析和进一步探讨,尤其是在二者临床合理应用方面。
3 中药配方颗粒汤剂与传统汤剂一致性评价建议
3.1明确现阶段一致性评价的先后及主次 现阶段应以评价单味中药配方颗粒汤剂与传统汤剂质量的一致性为主,以评价复方单煎与合煎的一致性为辅。优先评价单味中药配方颗粒汤剂与传统汤剂的一致性,原因如下:①尽管与单味药相比,复方在临床上应用更广泛,但单味中药配方颗粒是复方汤剂的重要组成,其质量在一定程度上影响着复方汤剂,只有保证了单味药质量,复方单煎与合煎的对比研究才更有意义。②若先研究复方单煎和合煎的一致性,在单味药质量尚未统一的前提下,会增加结果的不确定性,当得到不一致的结果时,难以确定是单煎与合煎的差异还是单味药质量问题所致。因此,在今后的一段时期内,应以评价单味中药配方颗粒汤剂与传统汤剂质量一致性为主,在单味药质量一致性研究取得进展后,复方单煎与合煎的一致性才有可能成为未来某一阶段的研究重点。若在现阶段探讨复方单煎与合煎的差异,则应遵循由易到难的原则,按照小复方(药对)到大复方的顺序进行研究,并对复方中的每一味药物进行评价。
3.2明确饮片和配方颗粒来源批次是否应统一 配方颗粒汤剂与传统汤剂进行一致性评价时饮片和配方颗粒的来源批次不要求必须统一。尽管来源批次的统一可消除原料差异造成的影响,是理想状态下的最佳选择。但患者在真实世界中拿到同一或相近来源批次的中药饮片和由其制备的配方颗粒的概率极低,所以此类比较实质在一定程度上脱离了临床实际。因此,评价时不应要求配方颗粒和饮片的来源批次具有一致性,而应选择来源于真实世界的饮片和配方颗粒即可。
目前中药配方颗粒汤剂与传统汤剂一致性评价的文献中配方颗粒的来源主要包括三方面:①医疗机构购买;②配方颗粒厂家提供;③自制。当原料批次不统一时,第二和第三种来源便可排除,同时考虑到多数患者获取配方颗粒的渠道仅为第一种,因此,在评价时应选择第一种来源的中药配方颗粒。但为降低实验误差,保证评价的可靠性与合理性,评价时从医疗机构购买的某一厂家的配方颗粒批次不应少于3批;对于中药饮片而言,文献中其来源主要包括:①医疗机构;②饮片公司;③药材市场(自行炮制);④配方颗粒厂家。当原料批次不统一时,第四种来源便可排除,同时考虑到当前市场上中药材质量良莠不齐的现状,评价时优先选择前两种来源。作为参比对象,饮片应具有广泛代表性,其批次建议为10~15批为宜,所有中药饮片均应进行《中国药典》项下的相关检查,以确保饮片质量。
3.3丰富和适当均衡评价品种的数目与类型 首先,应增加评价品种的数目,且优先针对已有国家/省标准的、尚未开展评价的大宗中药配方颗粒品种,如薏苡仁颗粒、炙甘草颗粒等。同时还应遵循由简入繁的原则,先对无挥发性的中药配方颗粒进行评价,再过渡到含有挥发性成分的配方颗粒品种;先从有明确药理药效指标的配方颗粒进行评价,再过渡到药理药效指标不太明确的配方颗粒。其次,评价品种的类型也应适当均衡,增加对动物药和矿物药的评价。
3.4系统性选择评价层次和指标 首先,针对中药物质基础复杂、靶点众多的特点,有必要在准确把握药物物质基础的同时,基于中医药整体观念系统性的选择二者一致性研究的层次和指标。针对单一方面的对比研究信服力较弱的现状,可考虑多方面结合进行综合对比,并利用主客观赋权法或其他方法对不同的内容进行加权,综合判断中药配方颗粒汤剂与传统汤剂的一致性。但考虑到真实世界中各研究者所擅长的研究方向有所不同,或难以开展多方面研究。因此,一方面,可加强各课题组之间的合作交流,选择同一来源、批次的中药饮片,依据研究方向的不同分别开展相关研究,最后依据各方面结果综合判断中药配方颗粒汤剂与传统汤剂的等效性;另一方面,可以同一来源、批次的中药饮片开展多方面研究,并建立不同对比方面的判别函数,阐明各对比方面之间的关联性[113],借鉴主成分分析“降维”思想,使配方颗粒汤剂与传统汤剂的单方面对比研究能够表征或预测多方面对比结果。其次,在进行一致性评价时应依据药物的主要物质基础去选择评价指标,确保评价可靠性与合理性,同时对于具有多种功效的中药配方颗粒,也不宜只选择其中部分功效进行评价,而应开展综合分析。
3.5建立个性化评价方法与模式 针对不同类别中药性质差异较大的情况,在共性化对比研究的基础上也应提出中药配方颗粒汤剂与传统汤剂个性化的一致性研究。基于《中国药典》对单味中药饮片的描述,依据是否含有明确成分及明确成分类别选择不同的评价内容,具体如下。
①没有明确代表性成分的一般药物。对于部分矿物药和动物药,如蝉蜕、鳖甲、龟甲等,由于《中国药典》中并未明确其指标性成分,其评价内容应以药理作用为主,以其他内容为辅。
②有明确代表性成分的一般药物。这类药物应以成分一致性为主,以药理作用为辅。对于部分矿物药和动物药,如自然铜、石膏、牡蛎等,可以评价其微量元素含量的一致性为主[114],以药理作用为辅。此外,由于石膏、牡蛎中的重金属极易超标从而对人体产生危害,故重金属含量的一致性也应纳入二者的一致性评价;对于含单一类别成分的植物药,如黄连,应以比较指纹图谱的相似度、指标性成分的含量为主,辅以药理作用进行判断;对于含多成分的植物药,可以通过一测多评法测定代表性成分含量,再结合指纹图谱相似度和药理作用进行判断。
③特殊类中药。对于菌类中药,如茯苓、猪苓等,其水溶性成分可按照常规检测方法测定含量[31],多糖类可对其水解后产生的单糖进行衍生化处理,建立相应的指纹图谱[115];对于包括磁石、赤石脂在内的矿物药,包括商陆、蟾酥等在内的毒性药,包括麝香、鹿茸等在内的贵重药以及包括冰片、薄荷脑在内的结晶性药材,由于这些药物本身不适宜制成中药配方颗粒[116],故不需要或不建议进行一致性评价。
3.6合理选择数据处理方法 在对二者一致性评价过程中的计量数据进行处理时,首先应检验数据正态性,步骤如下:①通过直方图、Q-Q图、P-P图等初步观察数据的正态性;②运用Kolmogorov-Smirnov法(n>50)和Shapiro-Wilk法(n<50)对数据进行正态性检查[117];③依据前两个步骤的结果,得出数据是否符合正态性的结论。当数据近似符合正态分布的情况下,需采用F检验判断样本数据的方差齐性,之后再采用独立样本t检验对实验数据进行处理[117];当数据分布严重偏态时,可采用Mann-WhitneyU检验[117]等非参数检验方法。
3.7完善评价标准 应参照化学仿制药物一致性评价标准与中药配方颗粒相关标准,进一步完善中药配方颗粒汤剂与传统汤剂成分、药理作用以及临床疗效一致的范围。结合现有文献研究结果,笔者认为中药配方颗粒汤剂与传统汤剂一致性评价标准的完善或可从以下几个方面进行考虑:①指纹图谱相似度应设立合适的下限(统一相似度计算方法及相关评价条件的前提下);②以传统汤剂的指标性/代表性化学成分种类为参考,二者化学成分的种类应无明显差异;③以传统汤剂中指标性成分或代表性成分含量的均值为标准,当配方颗粒中相应成分的含量处于“均值±3SD”[118]或其他合理范围内时,认为二者成分具有一致性;④以传统汤剂药理作用的均值为标准,当配方颗粒的药理作用在传统汤剂均值的“80%~125%”或其他合理范围[118]时,认为二者药理作用具有一致性;⑤共有峰峰面积总和与所有峰峰面积和的比值也应在一定范围内,如0.85~1.15或其他合理范围。当超出一致性范围时应对配方颗粒的当量或生产工艺进行适当调整,以保证配方颗粒临床应用的安全性和有效性;而当配方颗粒的成分、药理作用等均与传统汤剂具有一致性时,认为二者具有一致性,在临床上可相互替代使用。
3.8深入分析评价结果 如单味中药配方颗粒汤剂与传统汤剂之间的差异有统计学意义,一方面可采用峰面积加和法、平均倍数法或其他方法对其当量进行校正[31,102],另一方面可改进中药配方颗粒的生产工艺,以提高中药配方颗粒的质量和疗效,进一步确保其临床应用的安全性和有效性。此外,或可考虑该品种中药饮片制成配方颗粒的适宜性[116]。
4 展望
中药配方颗粒作为中医药理论指导下的“新型中药饮片”,是中药剂型改革的重要产物,也是传统汤剂的重要补充。通过不断完善中药配方颗粒汤剂与传统汤剂的一致性评价流程,有望建立一套规范化的评价体系,从而明确传统汤剂与各厂家生产的配方颗粒所制备汤剂之间的等效关系,提高配方颗粒的质量,促进中药配方颗粒的合理应用。此外,中药配方颗粒在剂型上与化学药的颗粒剂具有相似之处,在质量和疗效与传统汤剂一致的基础上,可以以中药配方颗粒汤剂为载体推动传统汤剂与中药饮片走向国际。

