AST-YS08药敏卡片检测酵母菌体外抗真菌药物敏感性的评价*
王苏珍,张羽仪,周春妹,黄声雷,王蓓丽,潘柏申,郭 玮
复旦大学附属中山医院检验科,上海 200032
真菌感染是全球范围内感染性疾病相关死亡的主要因素[1]。侵袭性真菌感染对公共健康构成了重大威胁[2]。严重的真菌感染常继发于哮喘、艾滋病、癌症、器官移植、使用皮质类固醇等[3]。世界卫生组织于2022年针对侵袭性真菌病颁布了第一份真菌重点病原体清单,其中新型隐球菌、白色念珠菌属于严重优先级[4]。
白色念珠菌是医院获得性侵袭性念珠菌病的主要病原体,近年来我国由非白色念珠菌引起的念珠菌血症也有所增加[5]。非白色念珠菌更易产生耐药性,并导致暴发性感染[6],而唑类药物的耐药率上升使得棘白菌素类药物的使用增加[7]。我国隐球菌病发病率也呈上升趋势[5]。常用的治疗新型隐球菌感染的药物包括两性霉素B、5-氟胞嘧啶及氟康唑[8]。针对性预防与经验性治疗是对侵袭性真菌感染高风险人群的重要干预措施[9]。临床微生物实验室提供全面、准确、快速的体外抗真菌药敏试验结果,可指导临床治疗、流行病学研究及监测抗真菌药物耐药率。
目前常见的酵母菌药敏试验方法或试剂有微量肉汤稀释法(BMD法)、纸片扩散法、浓度梯度(Etest)法,以及半自动药敏板条、全自动药敏系统。纸片扩散法成本较低,但有临床折点的药物少[10]。Etest法可提供最低抑菌浓度(MIC),与参考方法具有较好的一致性[11-12],但目前在国内仅限科研用途。半自动药敏板条操作简便,但唑类药物结果判读受主观因素影响较大。AST-YS08真菌药敏卡片(以下简称AST-YS08卡片)作为一种全自动的真菌药敏试验板条,国内对其评估较少,因此本研究以基于美国临床和实验室标准协会(CLSI)的M27-Ed4[13]的BMD法为金标准,评价AST-YS08卡片检测酵母菌药物敏感性的准确性。
1 材料与方法
1.1菌株来源 收集本院2019年3月29日至2022年5月8日临床分离的100株酵母菌菌株,其中白色念珠菌15株、光滑念珠菌19株、热带念珠菌16株、近平滑念珠菌复合群18株(包括近平滑念珠菌11株、拟平滑念珠菌3株、似平滑念珠菌4株)、克柔念珠菌8株、新型隐球菌14株、葡萄牙念珠菌4株、挪威念珠菌2株、希木龙念珠菌1株、季也蒙念珠菌1株、皱褶念珠菌1株、解脂念珠菌1株。本实验经复旦大学附属中山医院医学伦理委员会批准(B2022-376R)。
1.2主要仪器与试剂
1.2.1主要仪器 Vitek 2 Compact全自动鉴定药敏系统(法国生物梅里埃公司)、比浊仪(法国生物梅里埃公司)、Vitek MS质谱仪(法国生物梅里埃公司)、生物安全柜(美国赛默飞公司)、涡旋混匀仪(美国Scientific Industries公司)。
1.2.2主要试剂 沙氏葡萄糖琼脂培养基(美国赛默飞公司);VITEK-MS-FA、VITEK-MS-CHCA基质、盐水、VITEK®2 AST-YS08卡片(法国生物梅里埃公司);RPMI 1640培养基、0.165 mol/L MOPS缓冲液(德国Sigma-Aldrich公司);氟康唑、伏立康唑、两性霉素B、5-氟胞嘧啶(中国食品药品检定研究院);进口注射用醋酸卡泊芬净(美国默沙东公司);注射用米卡芬净钠(安斯泰来制药公司)。
1.3实验方法
1.3.1转种及鉴定 将-80 ℃保存的菌株接种于沙保弱平板二次传代后,使用Vitek MS质谱仪进行鉴定。用于BMD法检测的念珠菌于35 ℃需氧条件下培养24 h、新型隐球菌于35 ℃需氧条件下培养48 h。用于AST-YS08卡片检测的所有菌株按说明书要求,于35 ℃需氧条件下培养18~96 h。
1.3.2BMD法 按照CLSI M27-Ed4[13]文件规定的标准化方法操作。抗菌药物浓度范围依据AST-YS08卡片可报告范围配制,分别为:米卡芬净0.06~8.00 μg/mL,卡泊芬净0.125~16.000 μg/mL,伏立康唑0.25~32.00 μg/mL,两性霉素B 0.125~16.000 μg/mL,氟康唑0.5~64.0 μg/mL,5-氟胞嘧啶1~64 μg/mL。念珠菌在35 ℃条件下孵育24 h后读取药敏结果,新型隐球菌在35 ℃条件下孵育72 h后读取结果。
1.3.3AST-YS08卡片检测 按照该试剂说明书进行操作。
1.3.4试剂质量控制及重复性检测 使用近平滑念珠菌ATCC 22019和克柔念珠菌ATCC 6258对BMD法及AST-YS08卡片进行质量控制检测。采用“3×5”的检测方案,即使用质控菌株连续测试5 d,每日3次,验证该药敏卡片的重复性。
1.3.5收集数据 统计两种检测方法的检测时长、基本一致率(EA)和分类一致率(CA)。EA指两种方法测得的MIC值相差不超过2个浓度梯度占总测定数据的百分比。CA指两种方法的判定结果一致(均为敏感、中介或耐药)的菌株占总测定数据的百分比。显著错误(VME)指BMD法MIC值判定为耐药而AST-YS08卡片判定为敏感;大错误(ME)指BMD法MIC值判定为敏感而AST-YS08卡片判定为耐药;小错误(MiE)指一种方法MIC值判定为中介或剂量依赖性敏感(SDD)而另外一种方法判定为敏感或耐药。

2 结 果
2.1质控 质控菌株检测相应药物测得的MIC值均在规定范围内。重复性试验检测AST-YS08卡片符合率≥90%,符合CNAS-CL02-A005要求。
2.2EA 根据两种方法测得的MIC值计算EA(表1)。检测念珠菌时AST-YS08卡片与BMD法的总EA为87.2%。统计不同药物MIC50和MIC90发现,除AST-YS08卡片测得的卡泊芬净MIC90比BMD法高2个梯度外,其余药物的MIC50、MIC90与BMD法结果相差均在1个梯度内。两种方法测得卡泊芬净MIC值大于1个浓度梯度的菌株共38株,除1株皱褶念珠菌外,其余97.4%菌株(光滑念珠菌13株、近平滑念珠菌复合群12株、克柔念珠菌8株、其他念珠菌5株)AST-YS08卡片检测的卡泊芬净MIC值均偏高。检测培养24 h和48 h的新型隐球菌,AST-YS08卡片与BMD法的总EA分别为96.3%和100.0%。AST-YS08卡片测得的所有药物MIC50、MIC90与BMD法检测结果相差均在1个梯度内,且对培养24 h和48 h的新型隐球菌,AST-YS08卡片与BMD法的EA比较,差异无统计学意义(P=0.495)。
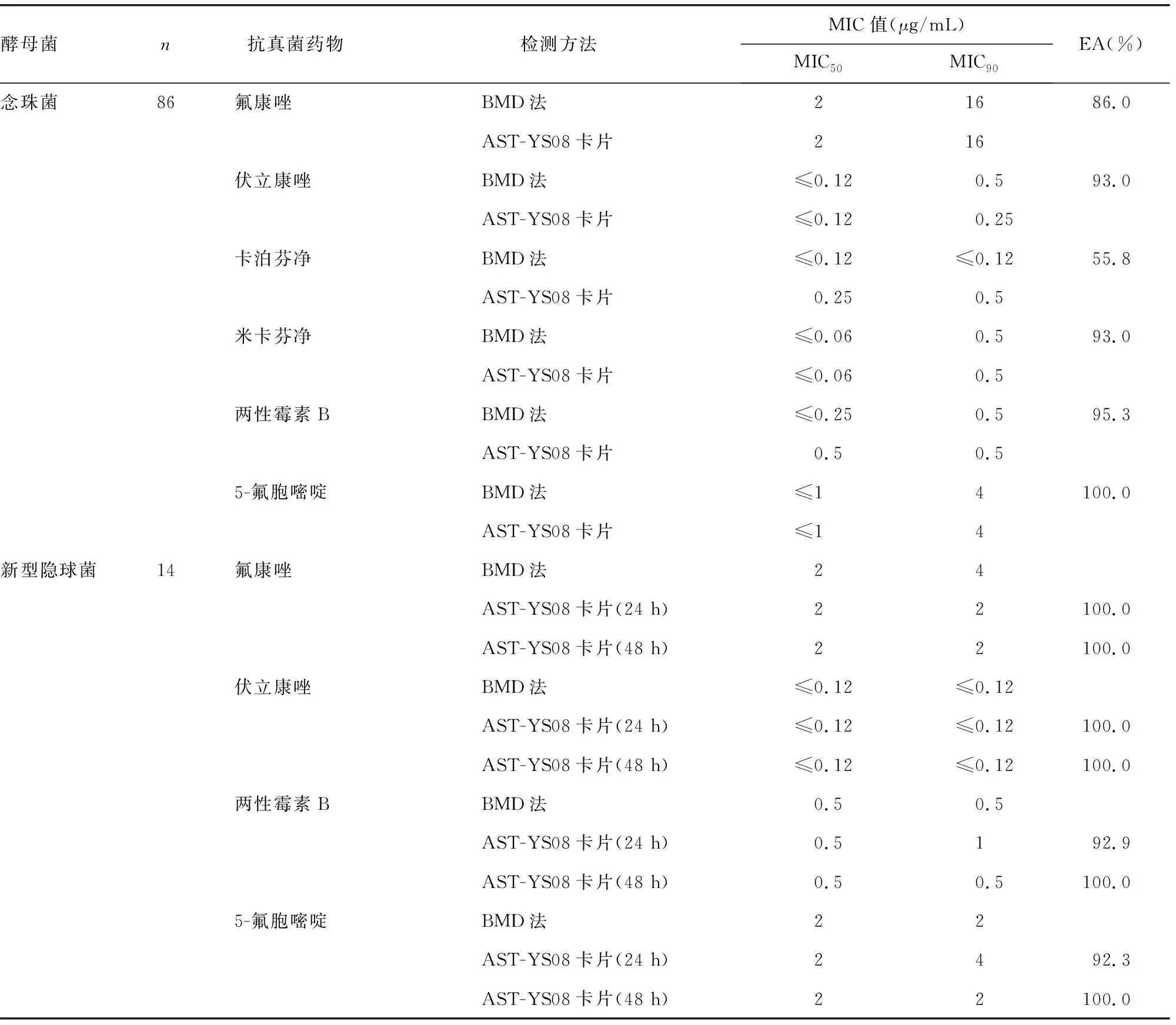
表1 AST-YS08卡片与BMD法检测酵母菌药物敏感性的MIC和EA
2.3CA与敏感性判定错误率 参考CLSI酵母菌敏感性折点及流行病学折点文件,计算CA、VME、ME及MiE的数量和占比,其中分类不一致的菌株及药物见表2。AST-YS08卡片与BMD法的总体CA较高,对近平滑念珠菌复合群及培养48 h的新型隐球菌两种方法的CA为100.0%。所有药物中,检测卡泊芬净时两种方法的CA最低(光滑念珠菌:CA为5.3%;克柔念珠菌:CA为0.0%;其他念珠菌:CA为83.3%),且AST-YS08卡片 MIC值明显高于BMD法。
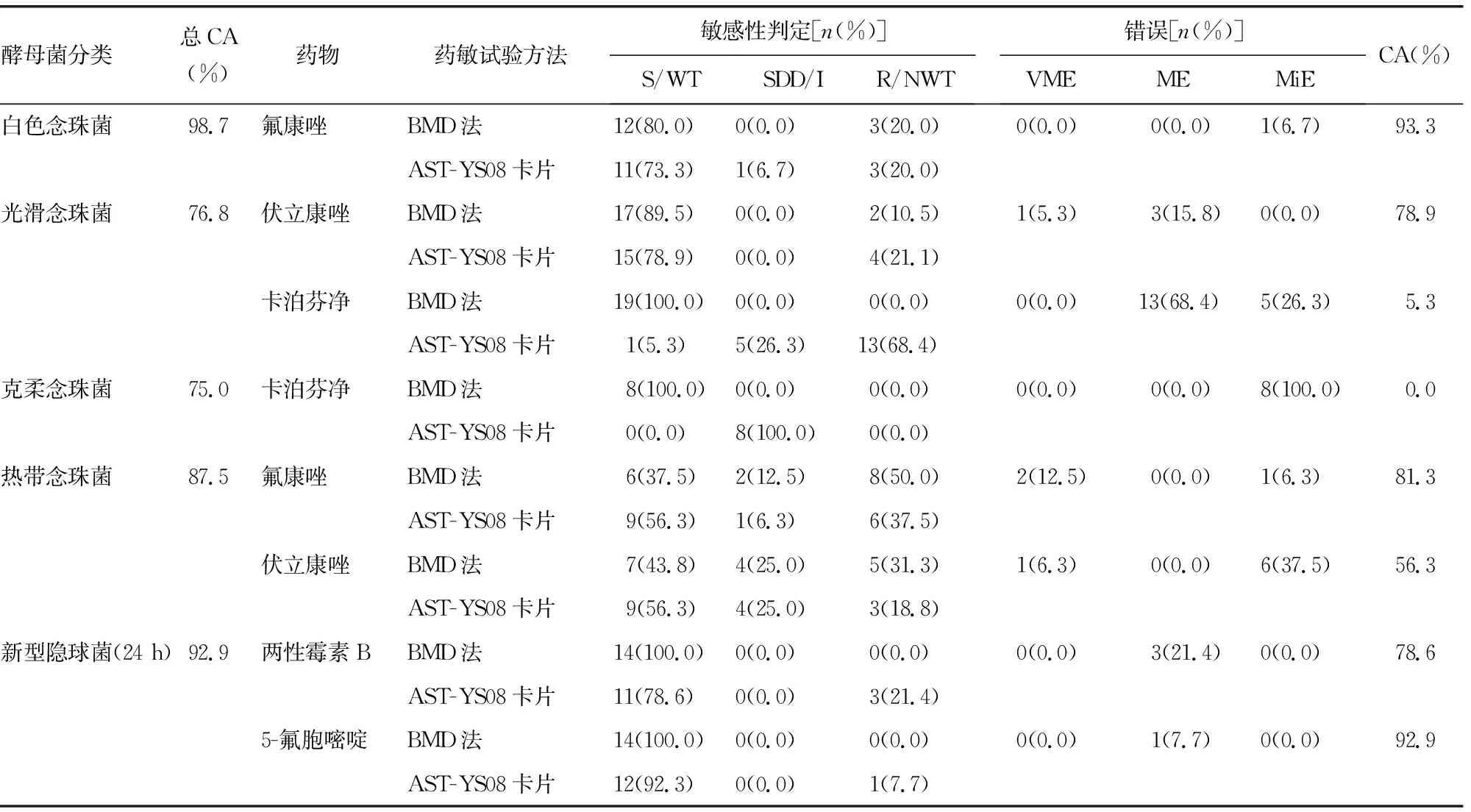
表2 AST-YS08卡片与BMD法检测酵母菌药物敏感性分类不一致菌株的CA及敏感性判定错误率
2.4不同酵母菌之间EA、CA比较 临床常见的酵母菌AST-YS08卡片检测与BMD法的总EA从高到低依次是新型隐球菌(48 h)100.0%、白色念珠菌97.8%、新型隐球菌(24 h)96.3%、热带念珠菌87.5%、近平滑念珠菌复合群85.2%、光滑念珠菌和克柔念珠菌均为83.3%。上述6种酵母菌AST-YS08卡片检测与BMD法检测的总CA从高到低依次是新型隐球菌(48 h)及近平滑念珠菌复合群均为100.0%、白色念珠菌98.7%、新型隐球菌(24 h)92.6%、热带念珠菌87.5%、光滑念珠菌76.8%、克柔念珠菌75.0%。培养48 h与培养24 h的新型隐球菌AST-YS08卡片检测与BMD法的CA比较,差异无统计学意义(P=0.118)。
2.5体外药敏试验时长分析
2.5.1念珠菌检测时长 CLSI M27-Ed4规定的念珠菌BMD法检测所需时长为24 h。AST-YS08卡片检测念珠菌时长为(13.63±2.55)h,其中热带念珠菌[(12.25±0.75)h]、光滑念珠菌[(12.54±1.32)h]、白色念珠菌[(12.60±0.77)h]检测时间较短,而克柔念珠菌[(14.61±1.53)h]、近平滑念珠菌复合群[(14.82±1.07)h]检测时间较长。AST-YS08卡片检测时间比BMD法缩短了约43.2%,检测速度明显提高(P<0.05)。
2.5.2新型隐球菌检测时长 CLSI M27-Ed4规定的新型隐球菌BMD法检测所需时长为70~74 h。AST-YS08卡片对于培养48 h的新型隐球菌检测时长为(20.67±5.13)h,培养24 h的菌株检测时长为(20.31±5.84)h,AST-YS08卡片对两种培养时间的新型隐球菌检测时长比较,差异无统计学意义(P=0.970)。但AST-YS08卡片检测时间比BMD法缩短了约71.5%,检测速度明显提高(P<0.05)。
3 讨 论
使用AST-YS08卡片检测各类念珠菌及多种抗真菌药物时EA均较高,临床常见的5类念珠菌AST-YS08卡片检测与BMD法检测的EA均>80.0%,其中两种方法检测白色念珠菌的EA最高,为97.8%,热带念珠菌为87.5%、近平滑念珠菌复合群为85.2%,而两种方法检测光滑念珠菌和克柔念珠菌EA较低,为83.3%,与HYEYOUNG等[14]研究结果类似。对于各类药物EA的统计发现,除氟康唑为86.0%、卡泊芬净为55.8%外,其余药物两种方法的EA均>90.0%。BURCU等[15]评估了140株念珠菌,与本研究结果接近。而对于卡泊芬净,CRETELLA等[16]研究3种检测方法后发现,相较于Etest法、Sensititre YeastOne,AST-YS08卡片表现更加出色(EA>90%)。
检测念珠菌时AST-YS08卡片与BMD法分类不一致的情况主要集中在氟康唑、伏立康唑和卡泊芬净。如AST-YS08卡片检测卡泊芬净出现“中介”或“耐药”,应谨慎报告。本实验唑类药物结果与RICARDO等[17]、MANUEL等[18]研究结果类似。后者检测了154株临床标本分离株,发现Vitek 2药敏系统检测氟康唑、伏立康唑,均有少量的VME检出。有研究指出,如念珠菌出现卡泊芬净“中介”或“耐药”,需检测米卡芬净/阿尼芬净,对FKS基因进行DNA序列,或将菌株送至参比实验室进行确认。若对阿尼芬净或米卡芬净耐药,或存在FKS热点突变,则认为对所有棘白菌素耐药[11]。本实验数据提示,AST-YS08卡片检测光滑念珠菌、克柔念珠菌时对卡泊芬净结果不理想,数篇文献研究同样发现卡泊芬净体外药敏试验与CLSI标准的BMD法间存在差异[14,19-20],后续可就该卡片卡泊芬净检测MIC值偏高的原因进一步研究。
另外,AST-YS08卡片检测范围不包含拟平滑念珠菌和似平滑念珠菌。CLSI指出如能明确区分为似平滑念珠菌或拟平滑念珠菌,则应使用相应折点而非近平滑念珠菌的折点[11]。近年来近平滑念珠菌感染率逐渐上升,已成为第二或第三位较常见的临床分离念珠菌[21]。有研究指出,似平滑念珠菌和拟平滑念珠菌也可引起血流感染[22]。随着鉴定技术的发展,近平滑念珠菌复合群已经可以被细分到3类不同的念珠菌,而Vitek 2药敏系统并未设置“似平滑念珠菌”“拟平滑念珠菌”的选项,且AST-YS08卡片的伏立康唑浓度范围也不能覆盖似平滑念珠菌折点,有待改进。
AST-YS08卡片检测新型隐球菌时与BMD法的EA较高,且检测培养48 h的新型隐球菌或比培养24 h表现更好。本实验检测培养24 h和48 h的新型隐球菌总EA分别为96.3%和100.0%,唑类药物EA均为100.0%,与LEONARDO等[22]、MIN等[23]研究结果相近。同时,本实验发现培养24 h的新型隐球菌菌株两性霉素B AST-YS08卡片检测与BMD法检测的CA为78.6%,ME%为21.4%,较培养48 h的新型隐球菌菌株CA更低。本研究还发现,1株培养24 h的新型隐球菌菌株AST-YS08卡片检测两性霉素B、5-氟胞嘧啶均比BMD法升高了3个稀释梯度。另外,使用AST-YS08卡片检测其中1株新型隐球菌菌株时,部分药物出现阳性对照孔生长不充分导致无MIC值的情况,培养48 h时有2种药物无结果,培养24 h时有4种药物无结果。由于菌株数量限制,暂未在该卡片检测培养24 h和培养48 h新型隐球菌的性能方面发现明确差异,可作为后续方向进一步研究。
本实验共选取了该卡片使用范围内的多种念珠菌(共计13种,86株)以及新型隐球菌(共14株),包括了酵母菌感染的主要病原体种类。但数种少见酵母菌未评估,例如西弗念珠菌、杜氏念珠菌、产朊念珠菌等,因此对于这些念珠菌,AST-YS08卡片的检测性能还不明确。另外本院未收集到对棘白菌素类耐药的念珠菌,所以无法评估卡泊芬净、米卡芬净对于耐药菌株MIC检测的性能。
综上所述,AST-YS08卡片操作简便,检测时长短,适用范围广,抗真菌药物种类全面,检测念珠菌时,绝大部分药物与BMD法的EA、CA较高。新型隐球菌培养48 h后进行检测,所有药物AST-YS08卡片与BMD法的EA、CA均>90.0%;缩短新型隐球菌培养时间至24 h时,AST-YS08卡片检测与BMD法的EA、CA有所下降,但与培养48 h的结果无明显差异。然而AST-YS08卡片未能区分近平滑念珠菌复合群中的3种念珠菌,且伏立康唑检测范围不能覆盖似平滑念珠菌折点。因此AST-YS08卡片适合在临床实验室中应用于酵母菌体外药物敏感性检测,但对于念珠菌对卡泊芬净非敏感结果需谨慎报告,似平滑念珠菌对伏立康唑的药物敏感性需使用其他方法检测。

