基于2,5-双(四唑)对苯二甲酸3 D含能材料的合成及性质
付思源,祝若倩,吕 磊
(1.延安大学 化学与化工学院,陕西 延安 716000;2.铜川矿业有限公司,陕西 铜川 727000)
自火药发明以来,人类生产生活离不开含能材料(如:枪械子弹、火炮药、烟花爆竹、火箭推进剂),传统的含能材料存在严重的安全性和污染问题,如在制备、存放、运输、使用过程中有较大的安全隐患,同时燃烧产物有毒,污染环境,破坏人类赖以生存的环境,威胁人类的身体健康,因此,急需研究新的含能材料。四唑类材料是高氮含能材料的代表,因其热稳定性好、生成热高、单位质量产气量大、燃烧产物对环境友好、灵敏度低而受到研究者的关注[1-4]。NASROLLAHZADEH 等[5]介绍了四唑作为催化剂、含能材料和有效配体的重要应用,及各种配合物的性能、稳定性、可重复使用性和环保问题。WURZENBERGER 等[6]用四唑配体合成的富氮铜(Ⅱ)双氰胺的配合物,呈现多维结构,具有中等的敏感 性。SUN 等[7]以Ni(ClO4)2·6H2O 和5-(4-吡啶)四唑-2-乙酸为原料,制备的三维网络结构的[Ni(pytza)2]n配位化合物可作为一种潜在的含能材料。NI等[8]制备的5-(4-吡啶基)四唑酯-亚甲基四唑配合物,分解温度高于240 ℃,整个反应过程的平均活化能为137.24 kJ·mol-1,放热过程四唑环打开的反应释放的氮气无污染。
四唑类配体在含能材料制备中是一类非常受欢迎的配体[9-10],文中选用的2,5-双(四唑)对苯二甲酸(H4dtztp)配体的相关研究报道较少。WANG等[11]采用配体H4dtztp 制备出三维蜂窝状骨架的配位聚合物[Ca(dtztp)0.5(DMA)]·2H2O,对其热分解过程和分离乙炔的功能进行了研究,但在含能材料领域尚未见报道。付思源等[12]以La(NO3)·6H2O 和H4dtztp 为原料,制备出具有三维结构的新型配合物{[La2(dtztp)1.5(H2O)5]·DMA·2H2O}n,具有良好的热稳定性。以上2 种配合物中配体与金属离子有着灵活丰富的配位方式,有利于配合物的稳定性。本文以H4dtztp 配体和同周期钙、锰离子为原料,采用溶剂热法[13-14]制备得到2 种新颖结构的配合物,研究配合物的结构、热稳定性、热安全性、反应机理,为配合物在含能材料领域的应用提供基础研究数据。
1 实验部分
1.1 仪器与试剂
Perkin-Elmer 2400 元素分析仪(Thermo Electron SPA 公司);Rigaku Ultima IVX 射线衍射仪(日本理学株式会社公司);Thermo Scientific Nicolet iS20 傅立叶红外光谱仪(Nicolet 公司);STA449F3 同步热分析仪(德国耐驰公司);DHG-9010 电热鼓风干燥箱(中国上海一恒科学仪器有限公司)。
2,5-双(四唑)对苯二甲酸(H4dtztp)(吉林中科研伸科技有限公司);MnSO4·H2O和CaCl2(陕西叁一实验室仪器设备有限公司)。
1.2 配合物的合成
配合物1 的合成:将CaCl2(0.007 8 g)、H4dtztp(0.006 0 g)、DMA(3 mL)和H2O(1 mL)混合,装入25 mL 带有聚四氟乙烯内衬的不锈钢反应釜中,放置在135 ℃的电热鼓风干燥箱中反应70 h。反应结束后,自然冷却至室温,过滤、洗涤后得到无色晶体。配合物(C20N16H26O19Ca4)元素分析(质量分数,%)理论值:C 25.59,H 2.81,N 22.86;实测值:C 25.59,H 2.78,N22.63。IR数据(KBr,cm-1):3 612,3 500,3 118,2 203,1 549,1 478,1 416,1 377,1 311,1 213,1 139,1 035,912,862,801,764,684,637,565,527,457。
配合物2 的合成:将MnSO4·H2O(0.007 8 g)、H4dtztp(0.006 0 g)和H2O(1 mL)混合,依据配合物1的合成步骤合成。配合物(C10N8H16O11Mn2)元素分析(质量分数,%)理论值:C 23.55,H 2.77,N 21.05;实测值:C 23.50,H 2.75,N 20.98。IR 数据(KBr,cm-1):3 398,2 377,2 275,1 846,1 599,1 389,1 153,1 149,1 091,1 049,979,812,623,540。
1.3 红外光谱
2 种配合物的红外光谱如图1 所示。在配合物1 中,1 549 和1 478 cm-1处的吸收峰为羧酸根离子的不对称伸缩振动,1 416、1 377 和1 311 cm-1处的吸收峰为羧酸根离子的对称伸缩振动,推测是配体的羧基完全去质子化,与Ca2+发生配位(图1A)。在配合物2 中,1 599 cm-1处的吸收峰为羧酸根离子的不对称伸缩振动,1 389 cm-1处的吸收峰为羧酸根离子的对称伸缩振动,推测是配体的羧基已完全去质子化,与Mn2+进行了配位(图1B)。
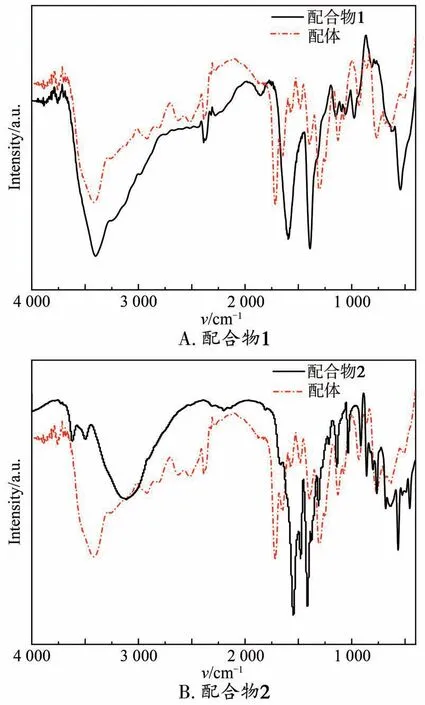
图1 配合物的红外光谱图
1.4 粉末衍射
PXRD 测试的目的是确定配合物的相纯度,配合物1和2的粉末衍射结果如图2所示。由图2可知,配合物的实验谱线与模拟谱线图基本吻合,表明2种配合物样品的相纯度较高[15]。
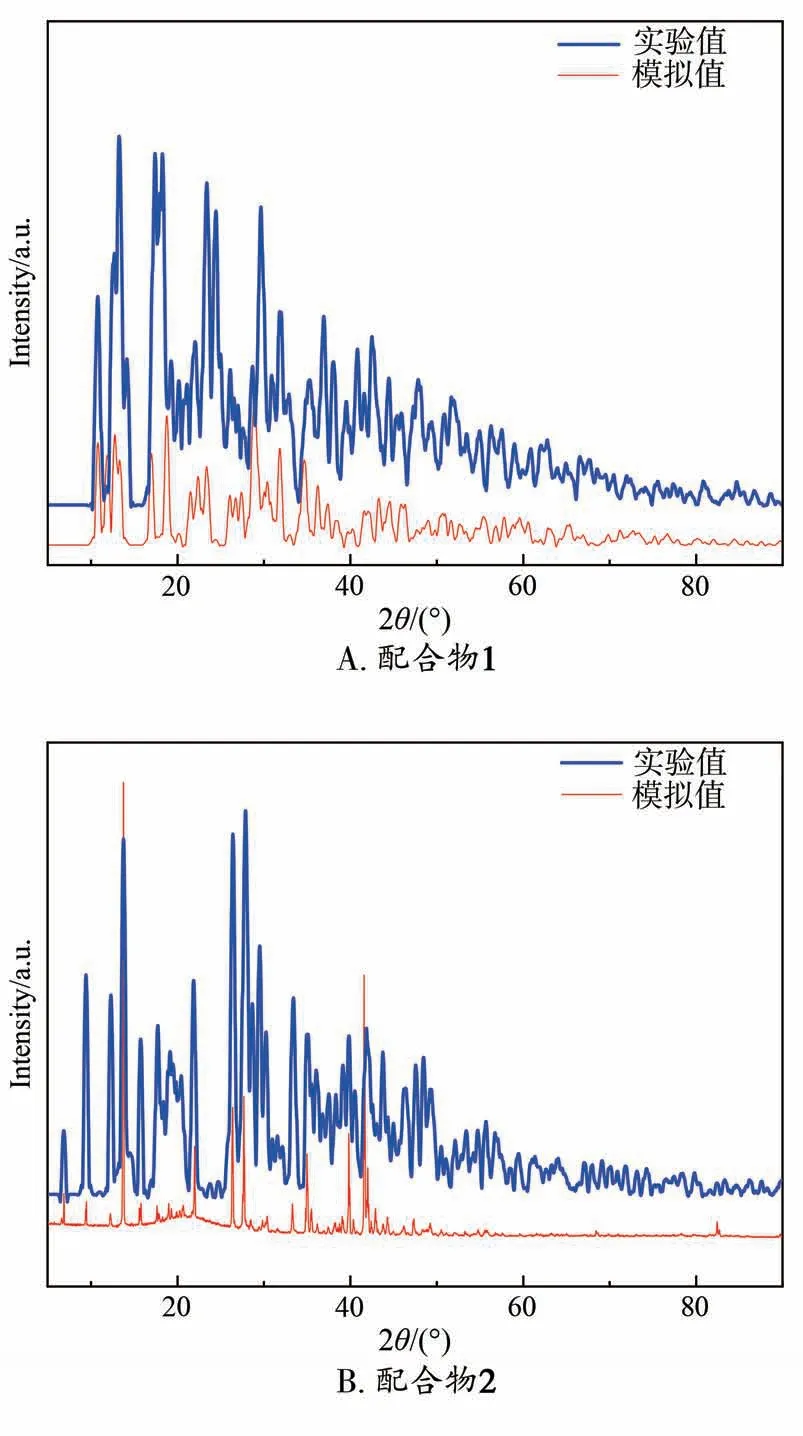
图2 配合物的PXRD谱图
2 结果与讨论
2.1 晶体结构
X 射线单晶衍射分析表明,配合物1 属于三斜晶系,空间群为P-1,晶体密度为1.919 g·cm-3,配合物的不对称单元由2 个Ca(Ⅱ)原子、一个配体分子、10个配位水分子和一个结晶水分子构成。其中Ca(1)与O(1)、O(2)、O(3)、O(4)、O(5)、O(6)、N(3)和N(6)构成八配位,Ca(1)与O的键长范围是0.238 3(2)~0.252 9(3)nm,Ca(1)与N的键长范围是0.258 7(3)~0.303 8(3)nm;Ca(2)与O(1)、O(2)、O(3)、O(4)、O(7)、O(8)、O(9)和N(2)也构成八配位,Ca(2)与O的键长范围是0.235 2(2)~0.259 5(2)nm,Ca(2)与N 的键长是0.260 4(3)nm。将结构延伸至二维空间形成了二维的层状结构,dtztp4-中羧基采用桥连和螯合2 种方式将3 个Ca 原子连接起来,单独的一个dtztp4-配体中N(2)、N(3)、N(6)、O(1)、O(2)、O(3)、O(4)与9 个金属Ca 连接,其中N(2)、N(3)、N(6)来自2 个四唑且均为单齿配位,O(1)、O(2)、O(3)、O(4)来自2个羧酸离子且采用桥连和螯合2种方式将3 个Ca 原子连接起来。配体丰富的配位点和灵活的配位方式构造了配合物空间结构的稳定性及复杂性。此外,配合物中的氢键存在2 种形式,一种是配位的水分子作为电子给体与dtztp4-中的羧基氧原子形成氢键,主要的氢键表现为:O(8)-H(8)...O(10)=0.261 8(6)nm,O(7)-H(7)...O(10)=0.261 8(6)nm,O(5)-H(5)...O(7)#1=0.306 6(3)nm;另一种是与dtztp4-中的四唑中氮原子形成氢键,主要的氢键表现为:O(10)-H(10)...N(1)#3=0.292 0(6)nm,O(9)-H(9)...N(4)#10=0.298 3(7)nm,O(8)-H(8)...N(8)#5=0.337 6(4)nm,O(7)-H(7)...N(5)#5=0.299 1(4)nm,O(5)-H(5)...N(5)#4=0.291 5(4)nm,这些分子内氢键可增强配合物结构的稳定性。并且在三维结构有着宽为0.744 35 nm、长为0.678 65 nm的四面体孔道,如图3所示。
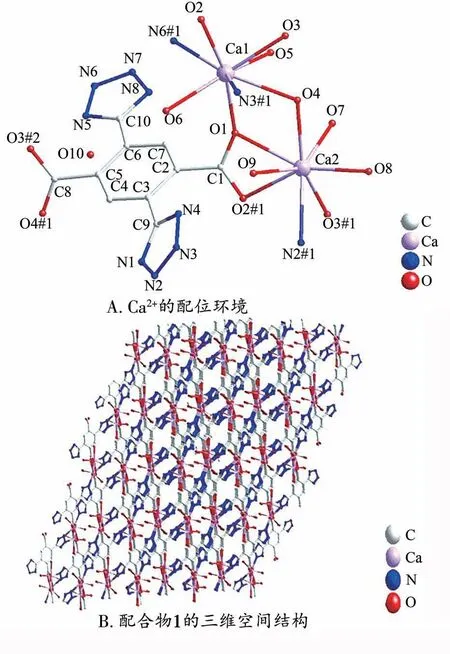
图3 配合物1结构图
X射线单晶衍射分析表明,配合物2属于三斜晶系,空间群为P-1,密度为1.840 g·cm-3,a=0.927 2 nm,b=0.944 2 nm,c=1.256 1 nm,V=96.4 nm3。配合物的不对称单元结构由3x个Mn(Ⅱ)原子、一个配体、6 个配位水分子和一个结晶水分子构成。Mn(1)与Mn(2)、Mn(3)均属于六配位,Mn(1)的6 个配位原子分别是O(1)、O(1#1)、O(11)、O(11#1)、N(1)、N(1#1),其中O(11)、O(11#1)来自配位水分子,其余的4 个配位原子来自配体。与Mn(1)不同的是Mn(2)的6 个配位原子均为氧原子,分别是O(2)、O(3)、O(4)、O(5)、O(6)、O(7),且4 个氧原子来自水分子,另外2 个氧原子来自配体,Mn 与氧原子的键长分别为:Mn(2)-O(2)=0.216 55 nm,Mn(2)-O(3)=0.214 60 nm,Mn(2)-O(4)=0.219 94 nm,Mn(2)-O(5)=0.216 69 nm,Mn(2)-O(6)=0.217 12 nm,Mn(2)-O(7)=0.217 07 nm。Mn(3)和Mn(1)配位原子类似,Mn(3)的配位原子分别为:O(8)、O(8#1)、O(10)、O(10#1)、N(8)、N(8#1),Mn(1)和Mn(3)中的N(1#1)和O(11#1)、N(1)和O(11)、N(8)和O(8)、N(8#1)和O(8#1)分别来自同一配体。配体的羧酸基以顺-反桥式双齿、反式单齿2种配位方式与金属Mn2+键连接,并在a 轴方向延伸形成二维结构,在b、c轴方向延伸形成稳定的三维空间结构,并且在三维结构有着宽为0.927 3 nm、长为2.275 46 nm的四面体孔道,如图4所示。
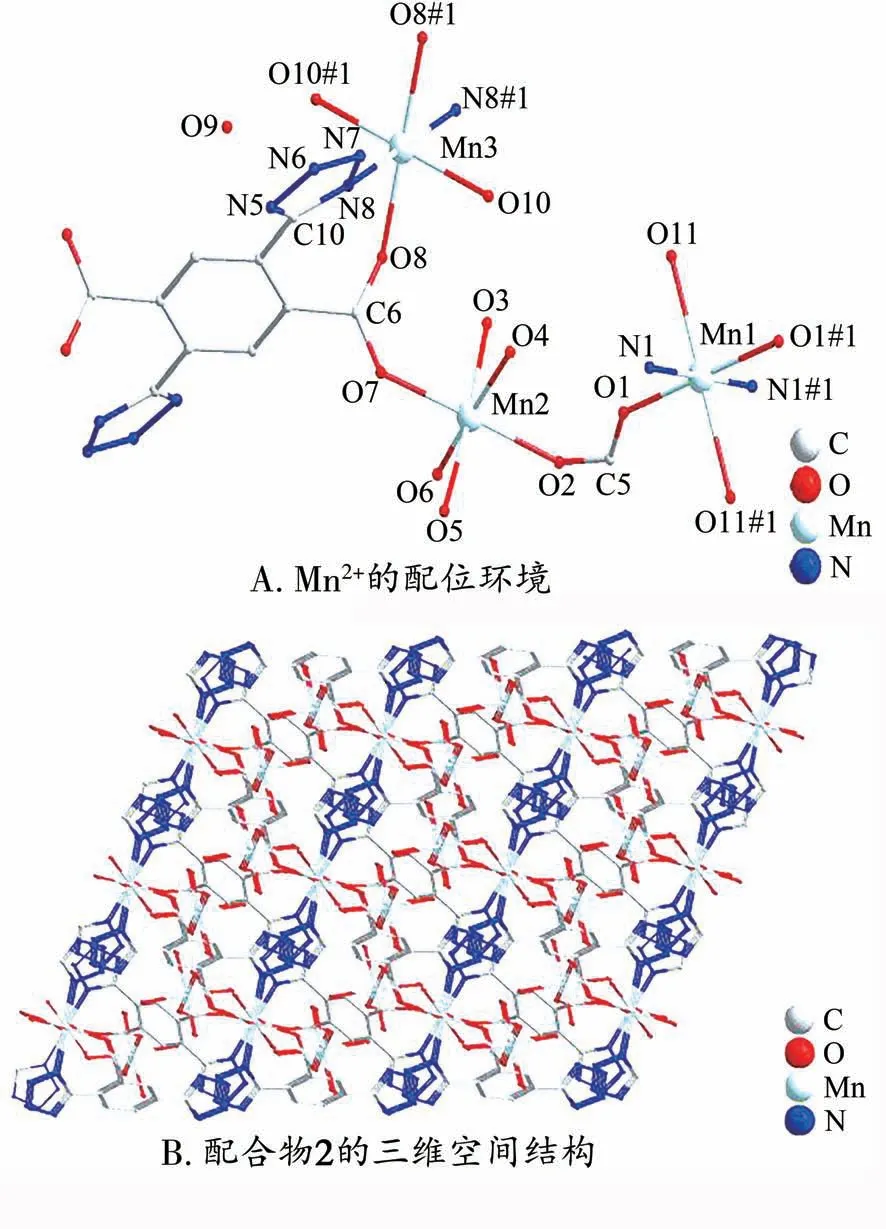
图4 配合物2的结构图
2.2 配合物的热分解
热稳定性是评价含能配合物材料稳定性的一个重要指标,这个指标对于含能材料的现实应用有重要的意义。采用差式扫描热分析(DSC)和热重分析(TG)研究配合物的热分解及质量损失过程,评价含能材料的热稳定性。DSC 和TG 的测试条件是升温速率5 ℃·min-1,流速25 mL·min-1的N2氛围,样品用量10~20 mg,结果如图5所示。
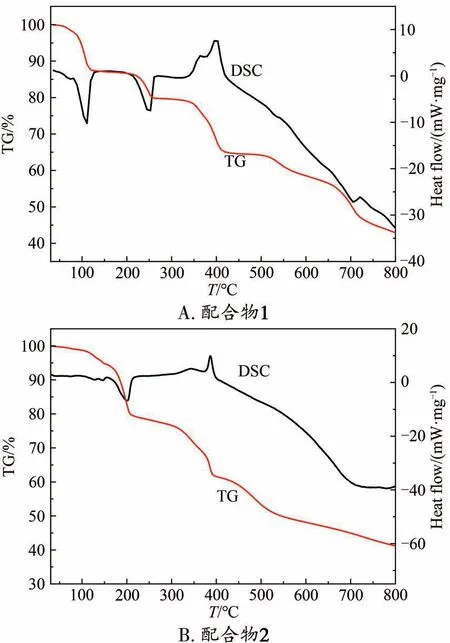
图5 配合物的DSC-TG曲线图
从图5A 可以看出配合物1 的热分解过程为一个放热过程和2 个吸热过程,伴随4 个连续的失重阶段。第一个分解过程属于吸热过程,在80 ℃时配合物1 开始分解直至115 ℃完成,质量损失主要是配位水分子和游离水分子的高温蒸发损失的质量,这一过程的吸热峰温为109 ℃。第二个分解过程也属于吸热过程,配合物1 在204 ℃开始发生分解,这一阶段配合物1 的主体结构开始发生分解,随着温度的升高,主体结构逐渐坍塌,其吸热峰温为249 ℃。第三个分解过程属于放热过程,配合物1的初始分解温度为380 ℃,表现出较好的热稳定性,整个过程总质量损失率为57.99%。表明配合物1有较好的热稳定性。
从图5B 可以看出配合物2 的热分解过程为一个吸热过程和一个放热过程,伴随3 个失重阶段。第一个热分解过程属于吸热过程,配合物2 在104 ℃开始缓慢分解,210 ℃时热分解完成,这一过程的吸热峰温为197 ℃,质量损失主要表现为结晶水和配位水的蒸发损失,分解过程的质量损失率为16.60%。第二个分解过程为放热过程,配合物2 从379 ℃开始热分解,398 ℃停止热分解,事实上在310 ℃时主体结构开始坍塌,表现出较好的热稳定性。这一过程对应的放热峰温是387 ℃,对应质量损失率为10.84%。第三阶段紧接着第二阶段,质量损失率为5.08%。配合物2有较好的热稳定性。
2.3 配合物的非等温动力学
2.3.1 活化能
通过DSC 测试配合物在4 种不同升温速率(5、10、15、20 ℃·min-1)下的DSC 数据来评价配合物非等温动力学的稳定性,结果如图6所示。由图可知4种升温速率下分解温度的峰值,利用Kissinger 法[16]和Ozawa 法[17],计算得到2 种配合物的表观活化能(E)和指前因子(A),如表1 所示。Kissinger 公式(1)和Ozawa公式(2)为
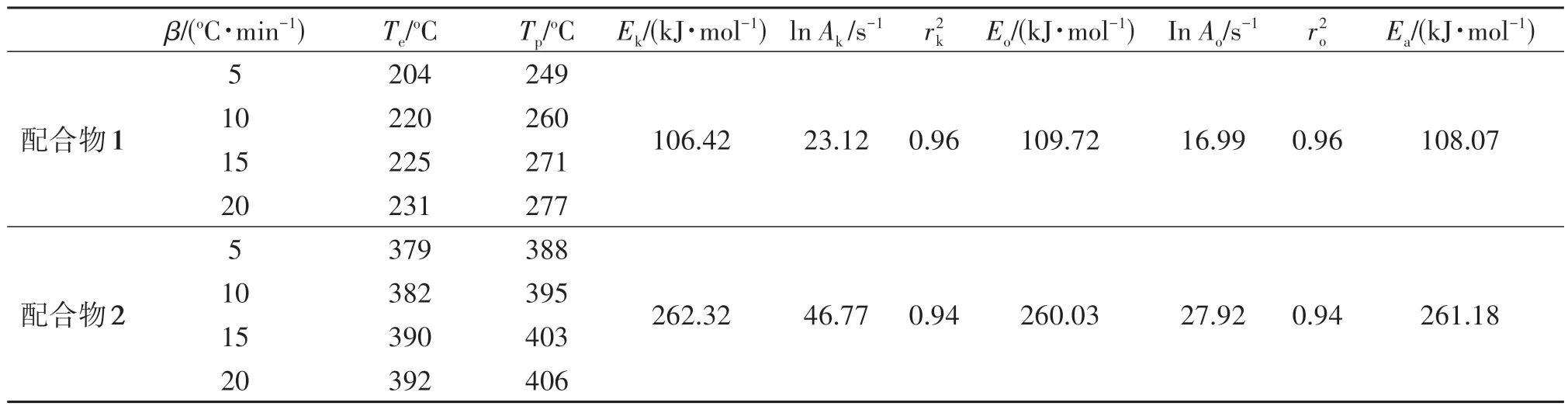
表1 配合物的非等温动力学参数

图6 配合物在5、10、15和20℃ min-1时的DSC曲线图
其中,β为升温速率(℃·min-1);Tp为分解峰值温度(℃);A为指数前因子(s-1);R为气体常数和C为常数;Ek、Eo为表观活化能(K 为Kissinger 法,O 为Ozawa法)(kJ·mol-1)。
Kissinger 法计算过程如下:获取DSC 数据中4个升温速率下的Tp值,然后以1/Tp的数据为X轴,lnβ/Tp2数值为Y轴,进行y=kx+b的线性拟合,从拟合方程中由斜率k=(-E/R)和截距b=ln(AR/E)可求得Ek和lnAk。配合物1 和2 的Kissinger 拟合方程分别为y=-12 799.96x+13.67 和y=-31 551.03x+36.41。Ozawa法计算为:以1/Tp的数据作为X轴,logβ数值为Y轴,进行y=kx+b的线性拟合。配合物1 和2 的拟合方程分别为y=-6 026.78x+12.27 和y=-14 284.21x+22.33,计算得到的相关数据如表1所示。
通过Kissinger 和Ozawa 法计算得到配合物的E结果相近都接近于1,说明计算结果是可靠的。由Ea(Ek和Eo的平均值)和lnAk可得到配合物1和2 的反应机理方程分别为:lnk1=23.123-108.07×103/RT和lnk2=46.77-261.18×103/RT。配合物2的表观活化能高于配合物1,表明配合物2 具有更好的热动力学稳定性。
2.3.2 热爆炸临界温度
TSADT、Tb和TTIT是含能材料常见的热安全参数,是衡量安全性的重要指标,计算过程如式(3)~(7)。
其中,Te为初始分解温度;Tb为热爆炸临界温度值;TTIT为热点火温度;TSADT为发生热爆炸的自加速热分解的最低温度;Te0为β→0 时的初始分解温;Tp0为β→0时的分解峰值温度(℃)。
由Ozawa 法可得到Ee0和Ep0,代入式(5)、(6)、(7)可计算出配合物1 和2 的TSADT分别为186 ℃和371.5 ℃,TTIT分别为189.04 ℃和375.21 ℃,Tb分别为238.56 ℃和382.17 ℃,如表2所示。

表2 配合物的热安全参数 单位:℃
对含能材料而言,发生热爆炸的自加速热分解的最低温度较大、发生热爆炸的临界温度较高或者热着火点温度较大时,材料的安全性更好[18]。由表2 可知配合物2 的TSADT、Tb、TTIT均比配合物1 的高的多,因此配合物2的热安全性更好。
2.3.3 活化焓、活化熵和活化吉布斯自由能
放热分解反应的重要表观热力学参数为活化熵(ΔS≠)、活化焓(ΔH≠)和活化自由能(ΔG≠),根据式(8)~(10)[19]可计算。其中,T=Tp0,A=Ak,Ea=Ek,kB为玻尔兹曼常数(1.381×10-23J·K-1),h为普朗克常数(6.626×10-34J·s)。
计算得到配合物1 和配合物2 的ΔS≠分别为-50.60 和141.97 J·K-1·mol-1,ΔH≠分别为104.47 和259.18 kJ·mol-1,ΔG≠分别为116.33 和205.58 kJ·mol-1(表3)。配合物1 和2 的ΔG≠的值均大于零,属于非自发反应,表明配合物都不会自发放热分解,需要在外界热能的作用下发生分解,且配合物2 的ΔG≠和ΔH≠值较大,说明其吸热分解所需的外界能量较多,在外界刺激条件表现出相对稳定的特性[20]。

表3 配合物的热力学参数
3 结论
四唑类配合物的研究一直是含能材料领域的研究热点,以H4dtztp 为配体,钙、锰金属为中心,通过水热法和溶剂热法,成功地合成了[Ca4(dtztp)2(H2O)10]·H2O 和[Mn2(dtztp)(H2O)6]·H2O 新型含能配合物,2 种配合物均为三斜晶系和P-1 空间群,具有三维结构,配合物1 中存在氢键。配体中四唑基以单齿或多齿的方式与金属离子键连接。与配合物1 相比,金属离子半径小的配合物2 的初始分解温度为361 ℃,主体结构开始坍塌温度为310 ℃,其热稳定性更好;表观活化能为261.18 kJ·mol-1,热动力学稳定性更好;热安全参数TTIT为375.21 ℃,Tb为382.17 ℃,其热安全性更好。综合表明配合物2 更安全,有望成为含能材料的研究热点。

