基于中国医院药物警戒系统的药源性帕金森综合征真实世界研究
任丛丛,贾光伟b,梁良,郭菲,张帆
药源性帕金森综合征(drug-induced Parkinson´s syndromeism,DIP)是由于药物导致纹状体内多巴胺递质含量减少,乙酰胆碱的兴奋作用相对增强而出现的运动障碍、震颤、自主神经功能紊乱等临床表现的综合征[1]。DIP 是典型抗精神病药物的常见不良反应,但临床实践发现某些非典型抗精神病药物、镇静催眠药、钙通道拮抗剂、抗癫痫药等引起的DIP 也不容忽视[2]。DIP 与原发性帕金森综合征(id‑iopathic Parkinson´s syndrome,IPD)的症状相似,通过临床症状鉴别难度大,又比IPD 病情进展快,常以月、周为单位加重[3]。有10%的病人会进展为持续性帕金森综合征[4]。中国医院药物警戒系统(Chi‑nese hospital pharrnacovigilance system,CHPS)由国家药品不良反应监测中心自2016年开始探索建立,目前全国已建立300 家国家级CHPS 监测哨点。本研究利用CHPS 2.0 对聊城市人民医院入院病人进行回顾性研究,探索对DIP开展主动监测的方法,并分析DIP 的人群特征,以期提高临床对DIP 的认识,做到早发现、早诊断、早治疗。
1 资料与方法
1.1 资料来源采用回顾性研究方法,利用CHPS收集聊城市人民医院2019 年1 月至2020 年12 月收入院病人信息,且既往使用一种或一种以上诱发DIP 的中、高风险药物,或有DIP 主要症状的病人作为本研究纳入病例,汇总分析其人口学信息、病史、诊断、诊疗信息、安全性信息、结局信息等内容。本研究符合《世界医学协会赫尔辛基宣言》的相关要求。原治疗方案病人或其近亲属知情同意。
1.2 主动监测方案的制定
1.2.1确定研究药物 本研究根据文献调研从病人的病历、医嘱、体征等信息中通过关键词初步检索,关键词为文献报道的诱发DIP 的19 种中、高风险药物[1-2]。通过初步检索,排除了以上药物中未检索到的(齐拉西酮、阿立哌唑、丁苯那嗪、甲基多巴、喹硫平、左乙拉西坦、桂利嗪)并结合聊城市人民医院实际用药情况,最终确定研究药物为氟桂利嗪、利血平、丙戊酸、曲美他嗪、奥氮平、氟哌啶醇、苯妥英、氯氮平、氯丙嗪、甲氧氯普胺、维拉帕米、地尔硫䓬12 种。
1.2.2生成监测结果 利用CHPS 的药品评价管理功能,检索关键词是“1.2.1”项中确定的研究药物和DIP 主要症状(运动迟缓、行走迟缓、抖动、震颤、肌张力增高、肌强直),CHPS 系统自动预警符合条件的病例,对预警病例的临床症状、治疗药物、体征检查、既往用药4个方面的资料进行分析判断后,生成最终的主动监测结果。
1.3 阳性病例的判断CHPS 报警病例由1 名神经内科医师与1名临床药师,结合病人疾病、既往用药等情况进行人工复核。两人意见不一致时,由研究小组所有成员讨论决定。DIP的临床诊断标准[2]:①既往服用过一种或一种以上可疑药物;②有帕金森病:运动迟缓,并且有静止性震颤或肌强直中的一项;③服用可疑药物之前无帕金森病史,出现症状在服用可疑药物之后。对于既往曾诊断为原发性帕金森病或出现帕金森症状在服用可疑药物之前的则排除DIP。判定为DIP 的,参照我国《药品不良反应监测和管理办法》中五项判定标准,进行相关性评价,相关性评价为“可能”“很可能”“肯定”的病例确定为阳性病例。
1.4 分析方法通过CHPS 提取阳性病例所在科室、病历号、姓名、性别、年龄、临床诊断、怀疑药物、用法用量、实验室检查、影像学检查、既往史、家族史等相关信息。
2 结果
2.1 病例筛查结果2019 年1 月至2020 年12 月,聊城市人民医院共有入院病例244 406 例,本研究共纳入病例36 369 例,其中男性18 906 例(51.98%),女性17 463 例(48.02%);病人年龄(62.64±13.53)岁,年龄范围为0~6 岁有1 例,>6~17 岁213 例,>17~40 岁1 813 例,>40~65 岁16 866例,>65 岁17 476 例。CHPS 预警病例2 488 例,纳入病例的性别及年龄分布情况。
2.2 病例再评价结果在纳入研究的36 369 例病人中,实际使用研究药物的为12 021 例,在CHPS 预警病例2 488 例中,经人工复核后确定阳性病例52例。CHPS 阳性预警率为2.1%(52/2 488),DIP 实际发生率为0.43%(52/12 021)。52 例阳性病例中,关联性评价为可能的10 例,占19.23%(10/52),很可能42例,占80.77%(42/52),肯定0例,占0.00%(0/52)。
2.3 DIP 人群特征分析52 例阳性病例中男性18例,女性34 例,年龄(68.36±12.98)岁。52 例阳性病例性别、年龄、既往史、临床表现、影像学表现、帕金森家族史分析结果见表1。

表1 DIP人群特征分析
2.4 引起DIP 的药物本研究方案中的12 种可能引起DIP 的药物,共有8种药物发生了DIP。未出现由氯丙嗪、甲氧氯普胺、维拉帕米、地尔硫䓬引起的阳性病例。有2例阳性病例是由研究方案之外的药物引起的,分别是阿普唑仑、多奈哌齐各1 例。有7例是由联合使用两种研究药物引起的,DIP 阳性病例的用药时长从1 周至20 年不等,其中,≤1 年 9 例,占17.31%,>1~5 年24 例,占46.15%,>5~10 年 13例,占25.00%,>10 年6 例,占11.54%。DIP 在用药1~5年发生率高,见表2。

表2 DIP阳性病例用药时长和发生率
2.5 DIP 阳性病例临床转归52 例阳性病例中症状未缓解或加重14 例,占26.92%(14/52),症状消失20 例,占38.46%(20/52),症状部分缓解但遗留后遗症18 例,占34.62%(18/52)。52 例阳性病例具体临床转归见表3。
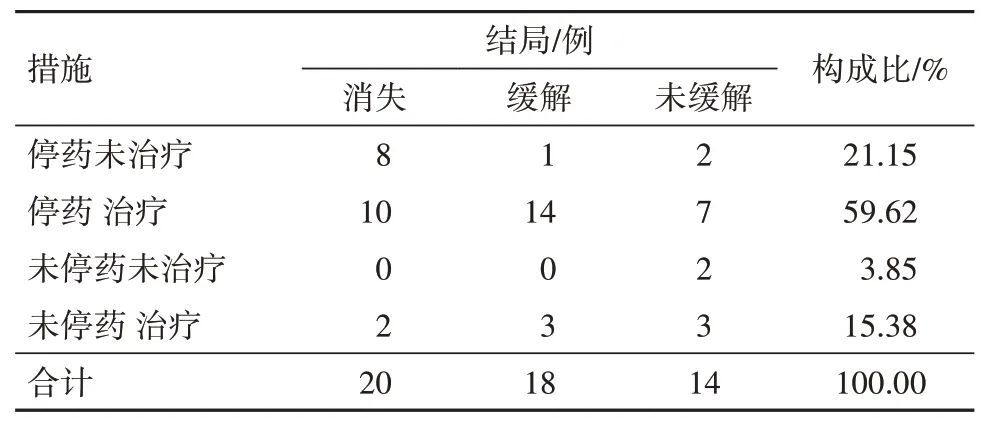
表3 DIP阳性病例临床转归
3 讨论
3.1 CHPS 在ADR 监测方面的优势CHPS 不仅可以全面整合医嘱、病历、检验、检查等诊疗信息,还具有主动监测功能,能辅助监测哨点发现、报告、评价药品不良反应或事件,克服了原有被动监测模式存在的低报、漏报、无法统计发生率、报告偏倚、信号发现迟滞等局限性,可以及时发现罕见、隐匿的不良反应。同时还为以后开展多中心研究、重点监测、药品综合评价创造了条件[5]。以本研究为例,CHPS 回顾性监测244 406 例病人仅用时2 分50 秒,共发现阳性病例52例,而同期聊城市人民医院相关ADR报告数为0。
本研究通过CHPS 计算的DIP 的发生率为0.43%。虽然目前国内外尚无统一、权威的相关数据,Han等[6]研究发现在韩国DIP的发病率为3.3/10 0000人,Savica等[7]一项为期30年的研究显示在美国DIP年平均发病率为3.3/10 0000 人年,女性发病率较高,且随着年龄的增长而增加。本研究所得发生率明显高于上述资料提供的数据,是因为研究人群为暴露于具有高、中DIP风险药物的病人,但也部分反映出我国医务人员对DIP 的认知度较低,同时说明CHPS具有评估、改进医疗机构医疗水平的功能。
除研究方案中的12种药物之外,本研究发现了由阿普唑仑、多奈哌齐引起的DIP 各1 例,筛查其药品说明书发现均未标识可能发生DIP,阿普唑仑说明书标识可致静坐不能、异常不自主运动,多奈哌齐说明书标识可致震颤,文献曾报道1 例脑外伤病人同时使用多奈哌齐和利培酮引起的DIP。尚未有阿普唑仑引起DIP 的报道。可见CHPS 具有辅助发现风险信号的作用。
3.2 DIP 相关危险因素、临床表现、转归本研究显示,年龄>65 岁、女性、缺血性脑病史是DIP 的危险因素。有研究证实,年龄是DIP 的一个持续风险因素[8],而年龄≥65岁是其危险因素之一。本研究显示性别是DIP 的危险因素,多项研究也显示DIP 发病率女性高于男性,这可能与雌激素会抑制多巴胺受体的表达有关[9]。
52 例阳性病例均无IPD 病史/家族史,其DIP 的主要临床表现为肢体或下颌不自主抖动,其次为肌张力增高、行动迟缓、步态不稳、震颤,以双侧肢体阳性症状为主,也有少数病人单侧肢体症状明显,其结果与相关研究一致[10-11]。本研究显示,DIP病人的颅脑CT/MRI 检查结果与未发生相关ADR 的病人存在明显差异,这说明CT/MRI 检查在DIP 与IPD 的鉴别上具有一定意义,这可能有助于DIP 的早期诊断和鉴别,Sung等[12]在3T MRI上采用多巴胺转运体显像鉴别DIP 和IPD,IPD 病人和DIP 病人间的敏感度为100%、特异度为85.0%、准确度为93.9%,这说明3T MRI上采用多巴胺转运体显像对IPD和DIP鉴别有较高准确性,可帮助筛选怀疑有DIP 并需要多巴胺转运体显像的病人。
DIP 一般是急性或亚急性起病,其症状体征一般是可逆性过程,及时停用可疑药物并给予适当对症治疗,4~22 个月内帕金森病症状可完全消失,少数病人可遗留一些轻度帕金森病症状或持续、进展性发展,有的甚至可能持续27个月[13]。本回顾性研究的研究时间至病人出院,最长仅21 d,帕金森症状消失病例为38.46%,部分缓解病例34.62%,尚有10例因病情需要不能停用可疑药物,随访时间短以及因病情需要不能停药可能是导致本研究DIP症状消失率低的主要原因。
3.3 引起DIP 的药物根据药物引起DIP 的风险高低和我院临床实际用药情况,本研究方案纳入12种药物,其中DIP 发生率最高的是复方利血平和丙戊酸盐,前者因其耗竭纹状体内多巴胺的作用,被认为是DIP 高风险药物,但关于复方利血平诱发DIP 的文献报道却很少,本研究复方利血平DIP 发生率2.51%,均发生在服药6 个月以上。相关研究显示丙戊酸盐发生DIP 的风险是5.04%,高于其他抗癫痫药,阳性病人服丙戊酸盐超过3年,研究是在癫痫治疗中心开展的,丙戊酸盐使用率和联合用药率高,这可能是DIP 发生率高于本研究的原因之一[14-15]。DIP是典型抗精神病药物的常见不良反应,发生率高达25%,非典型抗精神病药因为对纹状体的多巴胺受体阻断作用不明显,致锥体外系反应的风险氯氮平<喹硫平<奥氮平[1],本研究中DIP 发生率为奥氮平0.68%、氟哌啶醇0.52%,发现氯氮平风险信号1 例,与文献报道基本一致。钙通道阻滞剂曲美他嗪和氟桂利嗪分子结构中含有哌嗪环,易透过血脑屏障,是致DIP 中度风险药物[16],导致的DIP多为震颤型[17],可能是通过与纹状体内多巴胺D2受体结合诱发或加重帕金森症状[18-19]。因本研究纳入的住院病例均是临时单次使用氯丙嗪注射液或甲氧氯普胺注射液,使用维拉帕米仅23 例,未发现由这3种药物引起的DIP。
本研究中发现了7例因服用两种研究药物导致的DIP,联合用药导致DIP 发生率较使用单一药物明显增加。由于该研究为回顾性的真实世界研究,病史资料中对研究药物的剂量没有具体记录,所以未考察药物剂量对DIP 的影响,这是本研究的不足之处。
本研究中约2/3的阳性病例,其中包括7例因服用两种研究药物导致的DIP,其发生时间均在用药五年之内。有近1/2 阳性病例是发生在用药的1~5年,在此期间DIP发生率较高,据此提示临床医生和药师当病人服用诱发DIP的中、高风险药物时,在初始用药的5 年内需注意监测DIP 的发生,尤其是联合使用两种或以上药物时。
4 结果
本研究中DIP的实际发生率远高于相关文献报道,随着越来越多的药物引起DIP的病例被报道,需要有一种阳性预警率高、标准统一、及时高效可普及的监测方法来代替被动监测,CHPS 能够满足以上要求。
临床对DIP 认知度低。年龄>65 岁、女性、既往缺血性脑病史是发生DIP的危险因素。无IPD病史/家族史、双侧肢体阳性症状、颅脑CT/MRI 检查显示异常有助于DIP 的早期诊断和鉴别,多巴胺活性转运蛋白扫描成像检查,对IPD 和DIP 鉴别有较高准确性。DIP 的发病机制目前尚不明确,可能是黑质纹状体多巴胺D2受体被阻断或递质减少,多巴胺和乙酰胆碱作用失衡而诱导或加重帕金森病的作用[18]。详细询问病史及用药史,严格、仔细的体格检查,对初始使用中、高风险药物病人,尤其是联合使用两种或以上药物病人的药学监护,有助于早期发现DIP。

