基于HPLC指纹图谱结合化学计量学的白及与黄花白及辨识研究
范雪花,王艳丽,侯富国,李 涵,李海洋,姚 静, 3, 5,施钧瀚, 3, 5,桂新景, , 5*,刘瑞新, 4, 5*
基于HPLC指纹图谱结合化学计量学的白及与黄花白及辨识研究
范雪花1,王艳丽2,侯富国1,李 涵1,李海洋1,姚 静2, 3, 5,施钧瀚2, 3, 5,桂新景1, 2, 5*,刘瑞新2, 4, 5*
1. 河南中医药大学,河南 郑州 450046 2. 河南中医药大学第一附属医院,河南 郑州 450000 3. 河南省中药临床应用评价与转化工程研究中心,河南 郑州 450000 4. 河南中医药大学呼吸疾病中医药防治省部共建协同创新中心,河南 郑州 450046 5. 河南省中药临床药学中医药重点实验室,河南 郑州 450000
通过指纹图谱结合化学计量学方法对白及与黄花白及进行辨识研究。采用Shim-pack GIST C18-AQ(250 mm×4.6 mm,5mm)色谱柱,流动相为0.1%磷酸水溶液-乙腈梯度洗脱,检测波长280 nm;体积流量1.0 mL/min;柱温30 ℃;进样量10mL。采用ChemPatternTM软件对白及、黄花白及的指纹图谱数据进行分析,并对其进行相似度评价;采用SIMCA14.1软件进行主成分分析(principal component analysis,PCA)、偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA),对二者进行定性辨识研究。在相似度分析中,45批白及的相似度为0.74~0.97,相似度较好,29批黄花白及的相似度为0.44~0.83,部分黄花白及与白及较为相似;聚类分析与PCA分析结果较为一致,部分样品可分为2类;PLS-DA分析分类效果显著,模型参数Q为0.80,RY为0.85,完全能将两者区分开。通过PLS-DA分析结合VIP值筛选出了影响白及与黄花白及质量差异的8个共有峰,对这8个共有峰进行分析,二者之间除15号峰(militarine)峰面积没有显著性差异外(>0.05),其余7个共有峰峰面积白及均显著小于黄花白及(<0.01)。HPLC指纹图谱结合化学计量学方法能够实现白及与黄花白及的鉴别,可为白及饮片的质量辨识提供参考。
白及;黄花白及;指纹图谱;化学计量学;1, 4-二[4-(葡萄糖氧)-苄基]-2-异丁基苹果酸酯;天麻素;质量辨识
白及为兰科植物白及(Thunb.) Reichb. f.的干燥块茎,具有收敛止血、消肿生肌的功效,临床上常用于治疗咯血、吐血、外伤出血、疮疡肿毒、皮肤皲裂等症[1]。现代药理研究表明,白及对于常见疑难疾病如肿瘤[2,3]、矽肺[4]、肺结核[5]、胃溃疡[6]等具有良好的治疗作用;因其在皮肤皲裂、美白方面有良好的疗效,也被广泛用于医药美容领域[7,8]。黄花白及Schltr.与白及同为白及属植物,在我国南方大部分地区被用作民间药物或白及的替代品,其黄花白及被收录于2010年版《四川省中药材标准》[9]、小白及(实为黄花白及)收录于2009年版《甘肃省中药材标准》[10]和黔白及(实为黄花白及)收录于2003年版《贵州省中药材、民族药材质量标准》[11],其归经及功效记载几乎与《中国药典》2020年版记载等同,但《中国药典》2020年版只收载了白及。鉴于此,有学者研究白及与黄花白及的化成成分指纹图谱后提出二者具有相同或相似化学成分[12,13],将黄花白及充当正品使用有其合理性和必然性。但在药典尚未纳入黄花白及前,其仍是白及的伪品,且市场上多有黄花白及掺入白及中充当正品使用的情况[14],而性状、显微、薄层方法难以分辨二者[15],因此基于其化学成分探讨建立一种定性辨识二者的方法尤为重要。
中药指纹图谱技术能从整体上对中药进行研究,可以全面反映中药中所含的复杂化学成分及相互关系,被广泛用于中药的辨识研究[16-18]。但指纹图谱包含的信息量庞大,需要借助多元统计分析方法来进行更深入的分析[19]。化学计量学是一种通过分析数据,最大限度地提供可用的化学信息的方法,聚类分析、主成分分析、判别分析等化学计量学方法被普遍用于中药的质量评价和鉴定[20]。指纹图谱结合化学计量学的方法可对指纹图谱的数据进行矩阵式整合,对中药的质量差异进行整体描述与合理评价。基于此,本研究利用HPLC法建立白及与黄花白及的指纹图谱,结合化学计量学方法对其指纹图谱进行综合分析,探讨该法用于定性鉴别白及与黄花白及的可行性。
1 仪器与材料
1.1 仪器
UltiMate-3000型高效液相色谱仪,包括紫外检测器等(中国赛默飞世尔科技有限公司);BSA2245-CW型万分之一电子分析天平(德国Sartorius公司);HHS恒温水浴锅(北京科伟永兴仪器有限公司),HK250型科导式超声清洗器(上海科导超声仪器有限公司);JW-2018H型高速离心机;FW-100型高速万能粉碎机(60~180目,北京科伟永兴仪器有限公司);药典筛(四号筛,0.25 μm孔径,浙江上虞市道墟五四仪器厂);0.45 μm微孔滤膜。
1.2 材料
1,4-二[4-(葡萄糖氧)-苄基]-2-异丁基苹果酸酯(militarine)对照品(质量分数≥98%,K18O9B72711,上海源叶生物科技有限公司);天麻素(批号110807-201809,国家食品药品检定研究院),质量分数大于98%;白及对照药材(批号121261-201706,国家食品药品检定研究所)。超纯水、稀乙醇、甲醇、乙腈、磷酸均为色谱纯。
购买白及饮片45批、黄花白及饮片29批,经河南中医药大学第一附属医院施钧瀚副主任药师鉴定白及为兰科植物白及(Thunb.) Reichb. f. 的干燥块茎,符合《中国药典》2020年版规定;黄花白及为兰科植物黄花白及Schltr.的干燥块茎。白及、黄花白及样品信息见表1,其中白及饮片编号S1~S45;黄花白及饮片编号S46~S74。

表1 白及、黄花白及样品信息
2 方法与结果
2.1 色谱条件
色谱柱:Shim-pack GIST C18-AQ柱(250 mm×4.6 mm,5mm);流动相为0.1%磷酸水溶液(A)-乙腈(B);梯度洗脱(0~5 min,5%~20% A;5~10 min,20%~24% A;10~20 min,24%~31.5% A;20~25 min,31.5%~35% A;25~30 min,35%~42% A;30~45min,42%~60% A);体积流量1.0 mL/min;柱温30 ℃;进样量10mL;检测波长280 nm。
2.2 样品溶液的制备
2.2.1 混合对照品溶液的制备 精密称取militarine、天麻素对照品适量,置于10 mL棕色量瓶中,加乙腈-水(3∶97)溶解并定容,制成含militarine 0.906 mg/mL、天麻素1.066 mg/mL的混合溶液,摇匀,即得。
2.2.2 供试品溶液的制备 取饮片适量,粉碎过4号筛,精密称定2.0 g,置于50 mL具塞瓶中,加稀乙醇40 mL,称定质量,超声提取30 min(功率:200 W,频率:40 kHz),取出,放冷,用稀乙醇补足减失的质量,滤过,滤液浓缩至无醇味,残渣加乙腈-水(3∶97)溶解,转移至25 mL量瓶中,用乙腈-水(3∶97)稀释至刻度,摇匀,离心,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 重复性试验 精密称定S14号供试品6份,按照“2.2.2”项下方法处理,吸取10 μL,按“2.1”项下色谱条件进样,以militarine为参照峰计算各共有峰的平均相对保留时间和平均相对峰面积RSD值,分别为0.05%、0.27%。
2.2.4 精密度试验 精密称定S14号供试品,按照“2.2.2”项下方法处理,吸取10 μL,按“2.1”项下色谱条件连续进样6次,以militarine为参照峰计算各共有峰的平均相对保留时间和平均相对峰面积RSD值,分别为0.04%、0.13%,说明仪器精密度良好。
2.2.5 稳定性试验 称定S2号供试品,按照“2.2.2”项下方法处理,吸取10 μL,按“2.1”项下色谱条件分别在0、2、4、8、12、24 h进样,以militarine为参照峰计算各共有峰的平均相对保留时间和平均相对峰面积的RSD值,分别为0.07 %、0.33 %,说明供试品溶液在24 h内稳定性良好。
2.3 指纹图谱的建立
2.3.1 指纹图谱的建立和共有峰的指认 采用ChemPatternTM化学指纹图谱分析软件对74批样品进行HPLC指纹图谱分析,见图1。经对比,45批白及样品中共指认出8个共有峰,45批白及样品与29批黄花白及样品共指认出4个共有峰。选取白及饮片中具有代表性的17批饮片的特征峰导入ChemPatternTM软件进行处理,生成白及饮片共有模式特征图谱(图2),结果共提取出19个共有峰。取“2.2.1”项下混合对照品溶液,按照“2.1”项下色谱条件进样所得混合对照品色谱图(图3)。通过与混合对照品色谱图比对,指认出2个共有峰,峰4为天麻素,峰15为militarine。
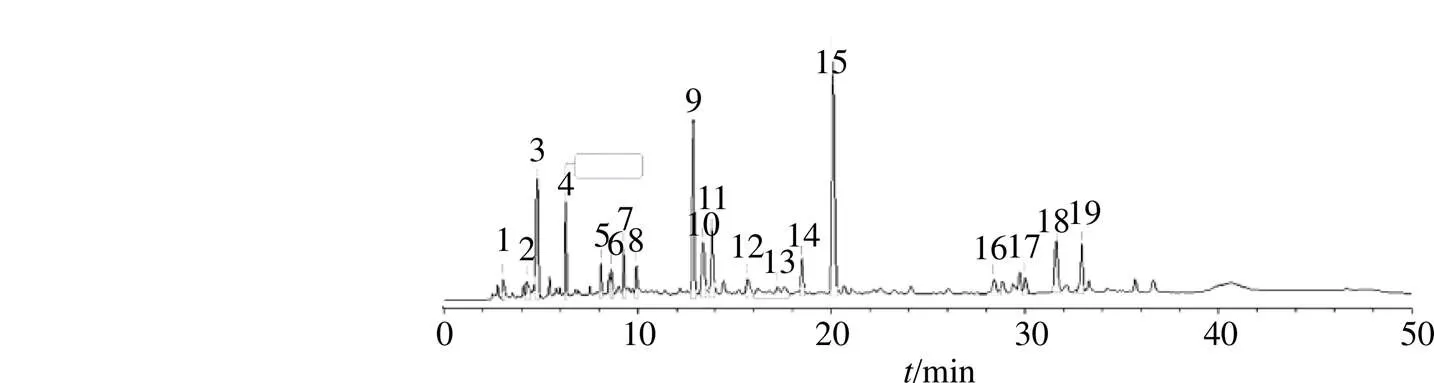
4-天麻素 15-militarine
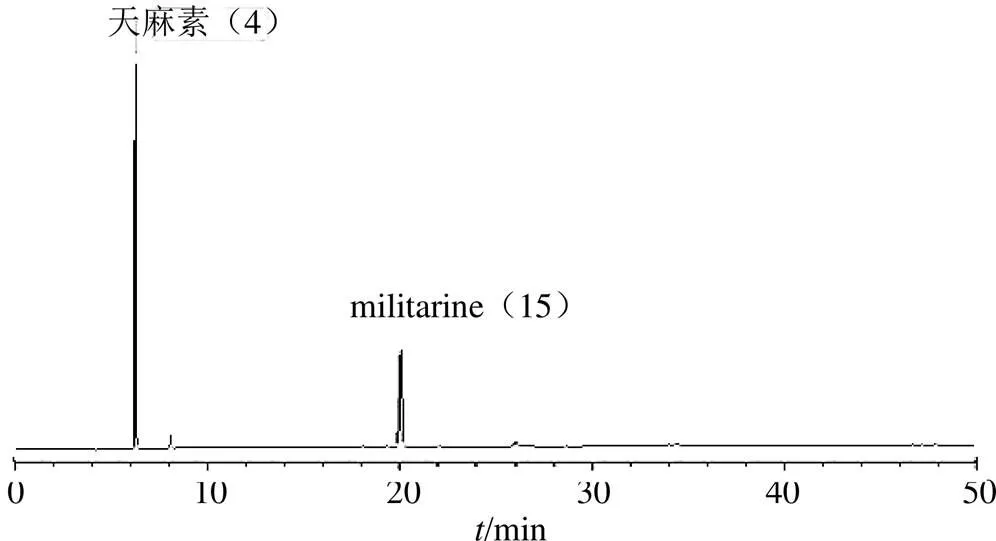
图3 混合对照品指纹图谱
2.3.2 相似度评价 将白及、黄花白及样品的cdf格式指纹图谱数据导入ChemPatternTM软件,采用夹角余弦算法对数据进行处理分析后计算其相似度,利用Origin2022软件将白及和黄花白及相似度结果分别与白及共有模式特征图谱两两比较进行相似度分析,如图4所示。以共有模式特征图谱为参照,从图4中可以直观看到每类样本的相似度分布范围,45批白及与共有模式相似度较高,相似度在0.74~0.97(均值0.89);29批黄花白及的相似度在0.44~0.83(均值0.67),仅个别样品(S61、S62、S63、S70)与白及相似度较高,不易区分。

图4 白及、黄花白及相似度分析散点图
2.4 化学计量学分析
2.4.1 聚类分析(hierarchical clustering analysis,HCA) 以指纹图谱中得到的19个共有峰峰面积为变量,以Euclidean为测度,最长距离为聚类方法,采用夹角余弦算法对白及和黄花白及进行聚类分析,结果见图5。当距离为0.5时,74批样品可聚为2类,35批白及、5批黄花白及(S61、S62、S63、S70、S71)聚为一类,剩余的24批黄花白及与10批白及(S14、S17、S28、S37、S38、S40、S41、S42、S43、S45)聚为一类。对其深入分析发现,10批聚错类白及中的18号峰的平均峰面积显著大于其余36批白及(<0.01),而在变量重要性投影(variable importance projection,VIP)图中,18号峰又是对白及与黄花白及分类影响最大的峰,这可能是其聚错类的原因,聚类分析方法不能将白及与黄花白及区分开。

图5 白及、黄花白及的聚类分析
2.4.2 主成分分析(principal component analysis,PCA) 将74批样品的19个共有峰峰面积经归一化处理后导入到SIMCA14.1软件建立PCA模型,采用等方差法(UV)法进行缩放,提取3个主成分,得到模型解释参数R为0.71,预测能力参数Q为0.40,PCA得分图如图6所示。根据主成分结果分析,对2类样品具有重要鉴别的变量PC1得分50.10%、PC2得分12.60%、PC3得分8.39%,三者之和为71.09%,表明提取的3个主成分可以解释71.09%的原始变量,可解释样品大部分样品信息。虽然模型的预测能力稍低,且白及、黄花白及样品有部分重叠,但大部分样品可基本分为2类,与聚类结果较为一致。

图6 白及、黄花白及的PCA得分图
2.4.3 偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA) 将74批样品的共有峰峰面积经归一化处理后组成19×74阶矩阵导入SIMCA14.1软件进行PLS-DA分析,结果见图7。前三个潜变量可以解释样本57.70%的变异信息,模型参数R为0.85,Q为0.80,均大于0.5,说明模型有较好的稳定性和预测能力[21]。从图7中可以看出,与PCA模型相比,白及、黄花白及样品可以明显分为2类,分类效果显著,表明该方法分类效果较好。为验证该模型是否过度拟合,利用SIMCA14.1软件对其进行了200次置换检验,结果如图8所示,左端随机排列的R、Q均小于右端的原始值,且Q的回归曲线是相交于Y轴的负轴[22],表明模型拟合良好,没有过拟合。PLS-DA模型中的VIP图见图9,VIP值越大表明该峰的差异对白及与黄花白及分类的贡献越高,一般以VIP>1表示对样品质量影响有统计学意义。以VIP>1为阈值,共筛选出了8个共有峰,从图中可以看出,对样品质量影响较大的峰依次是峰18>峰5>峰6>峰4(天麻素)>峰9>峰12>峰15(militarine)>峰3,提示这8个共有峰是引起白及与黄花白及饮片质量差异的主要变量。

图7 白及、黄花白及的PLS-DA分析
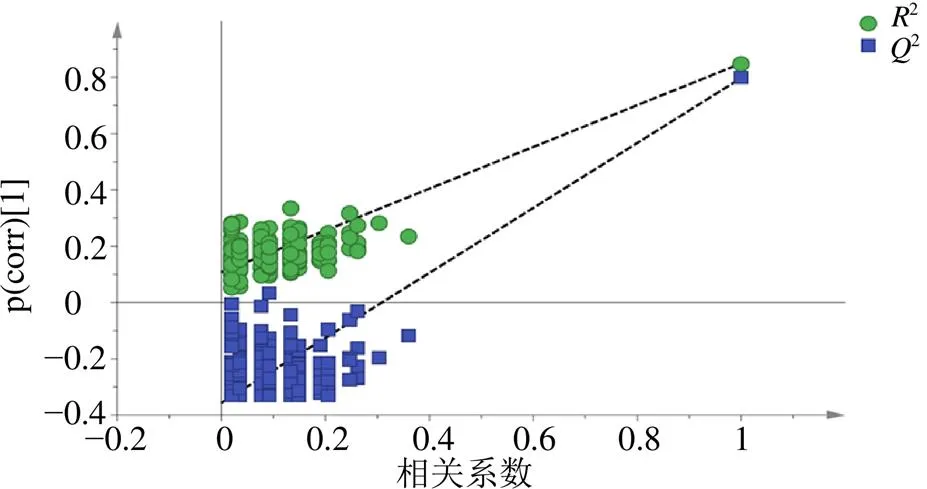
图8 PLS-DA模型的置换检验结果(n=200)

图9 白及、黄花白及19个共有峰的的VIP值图
通过PLA-DA分析结合VIP值筛选出了对白及、黄花白及样品质量影响较大的8个峰,平均峰面积占比69.74%。利用Graphpad软件对这8个共有峰峰面积进行对比分析,结果见图10。发现影响白及与黄花白及饮片质量差异的这8个共有峰,在白及中的平均峰面积均小于黄花白及,二者除了在militarine成分上没有显著性差异外(>0.05),其余7个峰的峰面积均有极显著性差异(<0.01)。在本研究中,白及与黄花白及中的militarine成分没有显著差异,这可能与不同生长环境以及不同栽培方式的化学成分累积的差异有关。野生白及极为稀少,现多为栽培白及,有研究表明栽培白及中的 militarine含量整体低于野生白及(<0.05)[23],这就提醒研究者在人工培育白及时应注意其指标成分含量的变化是否与栽培品有较大差异,在发展人工栽培技术的同时兼顾药材质量,保证白及质量与临床疗效的一致性。

图10 白及、黄花白及8个共有峰峰面积箱形图
3 讨论
3.1 样品的采集
为了深入了解白及目前真实的市场情况,本研究从药材市场、医院、药店等多渠道采集实验样品,包含了白及的道地产区贵州以及主产区云南,确保采集样品的代表性。
3.2 指标成分的选择
相比于《中国药典》2015年版,《中国药典》2020年版新增了1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯(militarine)的含量测定项目,考虑到中药活性成分的复杂多样性,仅单一成分作为测定指标不够全面,因此又增选了白及化学成分研究中常用的成分天麻素[23,24]作为测量指标,探讨其是否可以用于白及与黄花白及的质量评价研究。从PLS-DA分析结果中可以看出,白及与黄花白及中的天麻素具有极显著差异(<0.01),这表明将天麻素用于二者的质量评价研究是可行的。另一方面,天麻素具有抗惊厥、镇痛、降血压及保护神经细胞等作用[25],在白及发挥中枢神经系统药理作用方面起着重要作用,因此建议加大对白及中该成分的研究力度,进一步完善白及的质量控制。
3.3 色谱条件的选择
由于药典中还未收载白及的指纹图谱方法,因此本实验基于文献方法开展了白及的指纹图谱研究:①预实验参照文献报道[23, 26]中白及供试品溶液的制备方法进行了研究,发现以甲醇为溶剂提取的供试品溶液色谱中不含有天麻素成分,以50%乙醇为溶剂制备的供试品溶液色谱中可检测到天麻素[36]成分。②实验针对供试品溶液的进样量进行预试,比较了进样量为2、5、10、20mL时,色谱峰的峰形、峰面积大小以及分离度变化,结果显示进样量10mL时,峰形最优,峰面积适中,分离度较好。③考察了不同流速、不同柱温对色谱峰的影响,发现体积流量为1.0 mL/min、柱温为30 ℃时色谱峰的分离效果较好。④比较了白及液相色谱在紫外检测器220、230、270、280 nm波长下的紫外吸收情况,发现其在280 nm波长下色谱峰的响应值最佳,检出的色谱信息较多,能够较全面地反映样品的图谱特征。
3.4 化学计量学方法特点分析
本研究所采用的化学计量学方法包括无监督的分类模型(HCA、PCA)和有监督的分类模型(PLS-DA)。聚类分析、PCA分析结果大致能将样品区分为2类,个别样品不能区分;PLS-DA分析能明确的将样品区分为白及和黄花白及。其中聚类分析[27]是对数据的初步探索,具有直观、结论形式简明的优点,但当样品量过大时,聚类分析就无法对分类结果的准确性进行预测。PCA是在力求数据信息丢失最少的原则下,对高维的变量进行降维,使大部分数据信息包含在较少的新变量上,新生成的变量相互正交,彼此独立[28]。因此常利用PCA的降维功能,来评估测量的重复性并检测出明显的离群值,发现其潜在的组间区分趋势,为后续的分类或预测的多元统计分析作基础[29]。而PLS-DA分析是一种潜在的变量分类指向,有利于数据模型指导样本分类和寻找组间的差异[30],因而可将样品明确区分。
4 讨论
综上,本研究基于HPLC指纹图谱结合化学计量学方法对白及和黄花白及进行定性辨识研究,建立了白及、黄花白及指纹图谱,对二者进行了相似度评价、HCA、PCA和PLS-DA分析。相似度评价结果与HCA、PCA分析结果较为一致,样品能大致被分为2类,但存在一定偏差;PLS-DA分析能将白及与黄花白及样品完全分开,并筛选了8个影响白及、黄花白及质量差异的共有峰,二者除militarine峰无显著性差异外,其余7个共有峰峰面积均存在极显著差异。本研究建立的白及与黄花白及的定性辨识方法具有较高的可行性,可为白及等易掺伪中药的质量评价方法的建立提供一定的参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 106.
[2] Niu J F, Wang S P, Wang B L,. Structure and anti-tumor activity of a polysaccharide fromschltr [J]., 2020, 154: 1548-1555.
[3] 陈思思, 吴蓓, 谭婷, 等. 白及多糖BSP-1的分离纯化、结构表征及抗肿瘤活性研究 [J]. 中草药, 2019, 50(8): 1921-1926.
[4] 李浩宇, 史珍珍, 舒立峰, 等. 白及多糖抗矽肺大鼠肺纤维化活性研究 [J]. 中药材, 2016, 39(7): 1638-1642.
[5] 刘媛, 陈洁, 孙辉, 等. 中药治疗肺结核的用药规律及其核心药物作用机制的探讨 [J]. 中国防痨杂志, 2022, 44(2): 131-140.
[6] 高俊, 丁兴红, 丁志山, 等. 白及对阿司匹林致大鼠胃溃疡的治疗作用研究 [J]. 浙江中医药大学学报, 2019, 43(2): 182-187.
[7] 蒋俊, 陈红霞, 汤兴利, 等. 基于中医药美白理论的白及研发思考 [J]. 中草药, 2017, 48(11): 2313-2320.
[8] 李萌, 刘方舟, 杜昱, 等. 运用数据挖掘技术分析中医美容外用方剂配伍规律[J]. 新中医, 2022, 54(12): 16-22.
[9] 四川省食品药品监督管理局. 四川省中药材标准: 2010年版 [M]. 成都: 四川科学技术出版社, 2011: 583.
[10] 甘肃省药品监督管理局. 甘肃省中药材标准: 2020年版 [M]. 兰州: 兰州大学出版社, 2021.
[11] 贵州省药品监督管理局. 贵州省中药材、民族药材质量标准: 2003年版 [M]. 贵阳: 贵州科技出版社, 2003: 421.
[12] 陈美君, 李峰庆, 陈鸿平, 等. 中药白及与黄花白及的UPLC指纹图谱研究 [J]. 中药与临床, 2017, 8(5): 8-14.
[13] 杨丽云, 程远辉, 苏泽春, 等. 3种白及属植物化学成分分析 [J]. 安徽农业科学, 2021, 49(19): 173-176.
[14] 陈美君, 李峰庆, 吕蒙, 等. 白及与其混伪品ITS2序列二级结构比较与鉴别 [J]. 中国实验方剂学杂志, 2017, 23(15): 46-52.
[15] 李明华, 程显隆, 李宁新, 等. 白及的质量问题及真伪鉴别方法 [J]. 中国药事, 2018, 32(11): 1490-1499.
[16] 李灿, 曾娟, 龙雨青, 等. HPLC指纹图谱结合多模式化学计量学方法评价枳壳药材质量 [J]. 天然产物研究与开发, 2022, 34(4): 665-676.
[17] 刘天亮, 杨林林, 董诚明, 等. 基于化学模式识别的不同产地金银花HPLC指纹图谱研究 [J]. 中草药, 2022, 53(15): 4833-4843.
[18] 谢苏梦, 季巧遇, 吕尚, 等. 不同产地野菊花HPLC指纹图谱建立及化学模式识别研究 [J]. 中草药, 2021, 52(24): 7616-7623.
[19] 张艳欣, 吴佩颖, 王丹丹. 中药指纹图谱中常用的数理统计方法 [J]. 上海医药, 2019, 40(9): 74-77.
[20] Rebiai A, Hemmami H, Zeghoud S,. Current application of chemometrics analysis in authentication of natural products: A review [J]., 2022, 25(6): 945-972.
[21] 闫凯莉, 尹程程, 刘梦瑶, 等. 芩连润肺汤的HPLC指纹图谱建立、含量测定及多元统计分析[J]. 中国药房, 2021, 32(16): 1956-1963.
[22] 蒋勋, 陶会, 宋杰玉, 等. 不同等级普安红茶的成分差异及其品质特征 [J]. 食品安全质量检测学报, 2022, 13(13): 4235-4241.
[23] 周海婷, 陈志敏, 李文兵, 等. 野生与栽培白及HPLC指纹图谱建立及天麻素与militarine含量测定 [J]. 中药材, 2018, 41(11): 2527-2533.
[24] 秦亚东, 汪荣斌, 方凤满, 等. 化学模式识别分析白及不同采收期次生代谢产物动态变化特征 [J]. 天然产物研究与开发, 2020, 32(1): 11-17.
[25] Wang Y, Wu Z, Liu X,. Gastrodin ameliorates parkinson’s disease by downregulating connexin 43 [J]., 2013, 8(2): 585-590.
[26] 刘刚, 丁志山, 刘育辰, 等. 白及药材的HPLC指纹图谱建立及聚类分析 [J]. 中国药房, 2018, 29(22): 3050-3053.
[27] 孙立丽, 王萌, 任晓亮. 化学模式识别方法在中药质量控制研究中的应用进展 [J]. 中草药, 2017, 48(20): 4339-4345.
[28] 相倩倩, 张云权, 王小花, 等. 化学计量学方法在蜂蜜鉴伪中的应用研究进展 [J]. 江苏农业科学, 2020, 48(8): 32-40.
[29] Se K W, Ghoshal S K, Wahab R A,. A simple approach for rapid detection and quantification of adulterants in stingless bees () honey [J]., 2018, 105: 453-460.
[30] Lennart E, Johan T, Wold S. CV‐ANOVA for significance testing of PLS and OPLS®models [J]., 2008, 22(11/12): 594-600.
Identification ofandby HPLC coupled with chemometrics
FAN Xue-hua1, WANG Yan-li2, HOU Fu-guo1, LI Han1, LI Hai-yang1, YAO Jing2, 3, 5, SHI Jun-han2, 3, 5, GUI Xin-jing1, 2, 5, LIU Rui-xin2, 4, 5
1. Henan University of Chinese Medicine, Zhengzhou 450046, China 2. The First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, China 3. Henan Province Engineering Research Center for Clinical Application, Evaluation and Transformation of Traditional Chinese Medicine, Zhengzhou 450000, China 4. Co-construction Collaborative Innovation Center for Chinese Medicine and Respiratory Diseases by Henan & Education Ministry of China, Henan University of Chinese Medicine, Zhengzhou 450046, China 5. Henan Key Laboratory for Clinical Pharmacy of Traditional Chinese Medicine, Zhengzhou 450000, China
To identificate Baiji ((Thunb.) Reichb. f.)and Huanghuabaiji (Schltr.) by fingerprint combined with chemometrics method.Shim-pack GIST C18-AQ (250 mm´4.6 mm, 5mm) column was used. The mobile phase was 0.1 % phosphoric acid-acetonitrile. The detection wavelength was 280 nm. Flow rate was 1.0 mL/min. Column temperature was 30 °C. Injection volume was 10 μL. ChemPatternTMsoftware was used to analyze the fingerprint data ofand, and the similarity was evaluated. SIMCA14.1 software was used for principal component analysis (PCA) and partial least squares discriminant analysis (PLS-DA ) to study the qualitative identification of the two.In the similarity analysis, the similarity of 45 batches ofwas 0.74—0.97, and the similarity was good. The similarity of 29 batches ofwas 0.44—0.83, and somewere similar to. The results of principal component analysis and cluster analysis were consistent, and most samples could be divided into two categories. The partial least squares discriminant analysis had obvious classification effect, and the model parametersQandRYwere 0.80, 0.85, respectively, which can distinguish the two. Eight common peaks affecting the quality difference ofandwere screened by PLS-DA analysis combined with VIP value, and the eight common peaks were analyzed. Except for the peak area of peak 15 (militarine), there was no significant difference between them (>0.05), the area of seven common peaks ofwas significantly smaller than that of(<0.01 ).HPLC fingerprint combined with chemometrics method can realize the identification ofand, which can provide reference for the quality identification ofdecoction pieces.
(Thunb.) Reichb. f.;Schltr.; fingerprint; chemometrics; militarine ; gastrodine; quality identification
R286.2
A
0253 - 2670(2023)12 - 3990 - 09
10.7501/j.issn.0253-2670.2023.12.025
2022-12-06
国家自然科学基金项目(81773892);国家重点研发计划中医药现代化重点专项(2017YFC1703400);河南省卫生健康委员会国家中医临床研究基地科研专项课题(2021JDZY104);河南省中医药拔尖人才培养项目(重点项目)(2019ZYBJ07);河南省高层次人才特殊支持“中原千人计划”——“中原青年拔尖人才”项目(ZYQR201912158);河南省卫生健康中青年学科带头人专项(HNSWJW-2020014);河南省科技攻关项目(222102310377)
范雪花(1999—),女,河南开封,硕士在读,研究方向为中药质量评价及临床应用研究。E-mail: fan_jingjing@163.com。
通信作者:刘瑞新(1980—),男,主任药师,研究方向为中药饮片临床应用现代化关键技术研究。E-mail: liuruixin7@163.com
桂新景(1991—),男,主管药师,研究方向为中药质量评价及临床应用研究。E-mail: guixinjing1991@126.com
[责任编辑 时圣明]

