西藏高海拔地区人群非心胸外科手术术中低氧血症的危险因素:前瞻性队列研究
段函宇,朱倩梅,次仁德吉,李 艺,苗煦涵,张越伦,刘子嘉,拉巴次仁,申 乐,黄宇光
1西藏自治区人民医院麻醉科,拉萨 850000 中国医学科学院北京协和医院 2麻醉科 3医学科学研究中心,北京 100730
西藏自治区平均海拔在4000 m以上,属于典型的高海拔地区,其呈现为独特的高寒、低氧环境特点,以致长期居住于该地区的居民动脉血氧分压(partial pressure of oxygen,PaO2)和血氧饱和度(saturation of blood oxygen,SpO2)较平原地区居民降低,此类人群在非心胸外科手术中低氧的发生风险更高,并可能对患者预后产生不良影响,但相关研究较匮乏[1-2]。本研究首次分析了西藏高海拔地区人群行全身麻醉非心胸外科手术术中低氧血症的发生率及其危险因素,并简要分析术中低氧血症对患者围术期预后的影响,以期为该类手术患者低氧血症的临床防治提供参考。
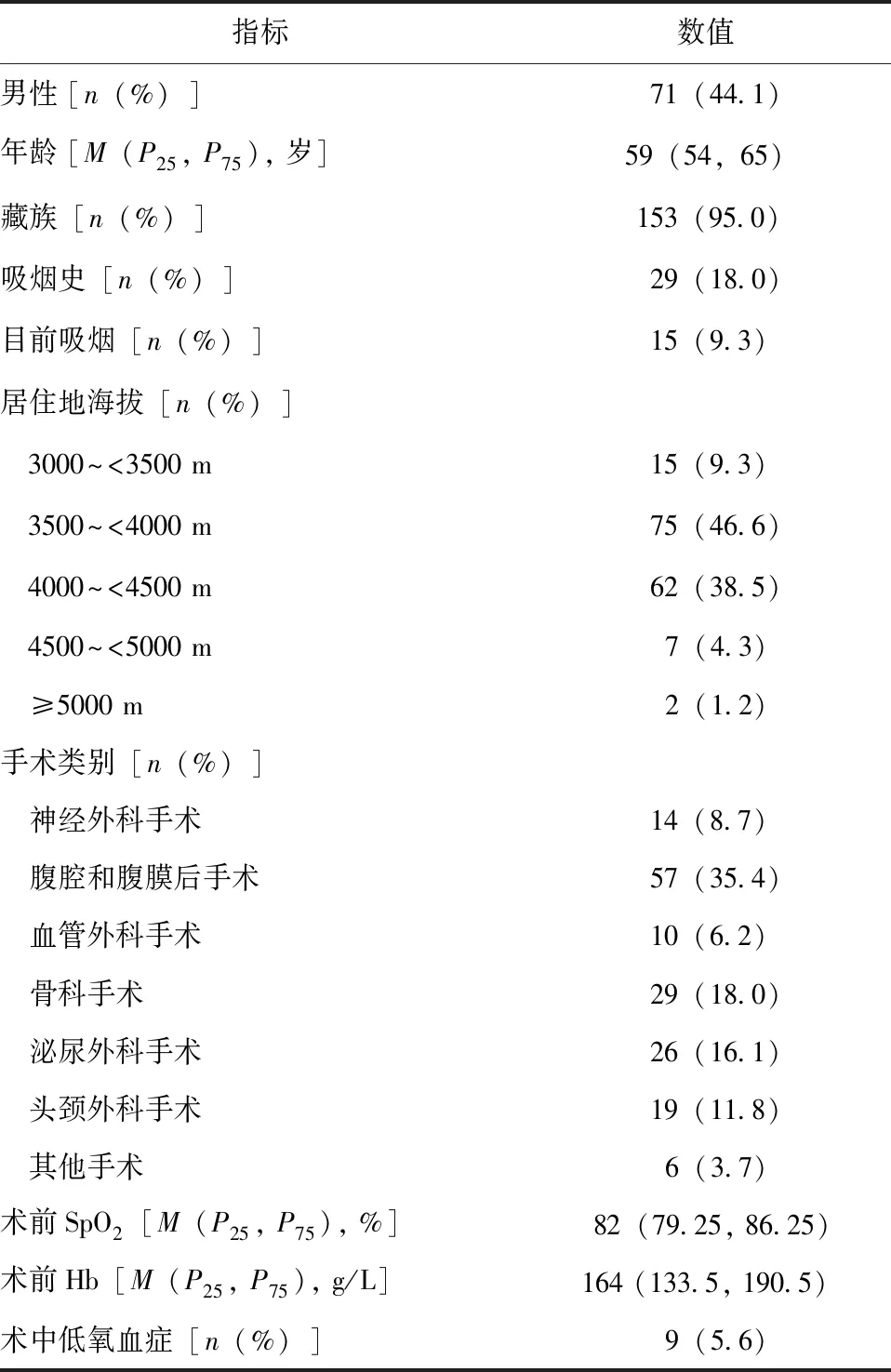
表1 161例行全身麻醉非心胸外科手术患者的临床资料
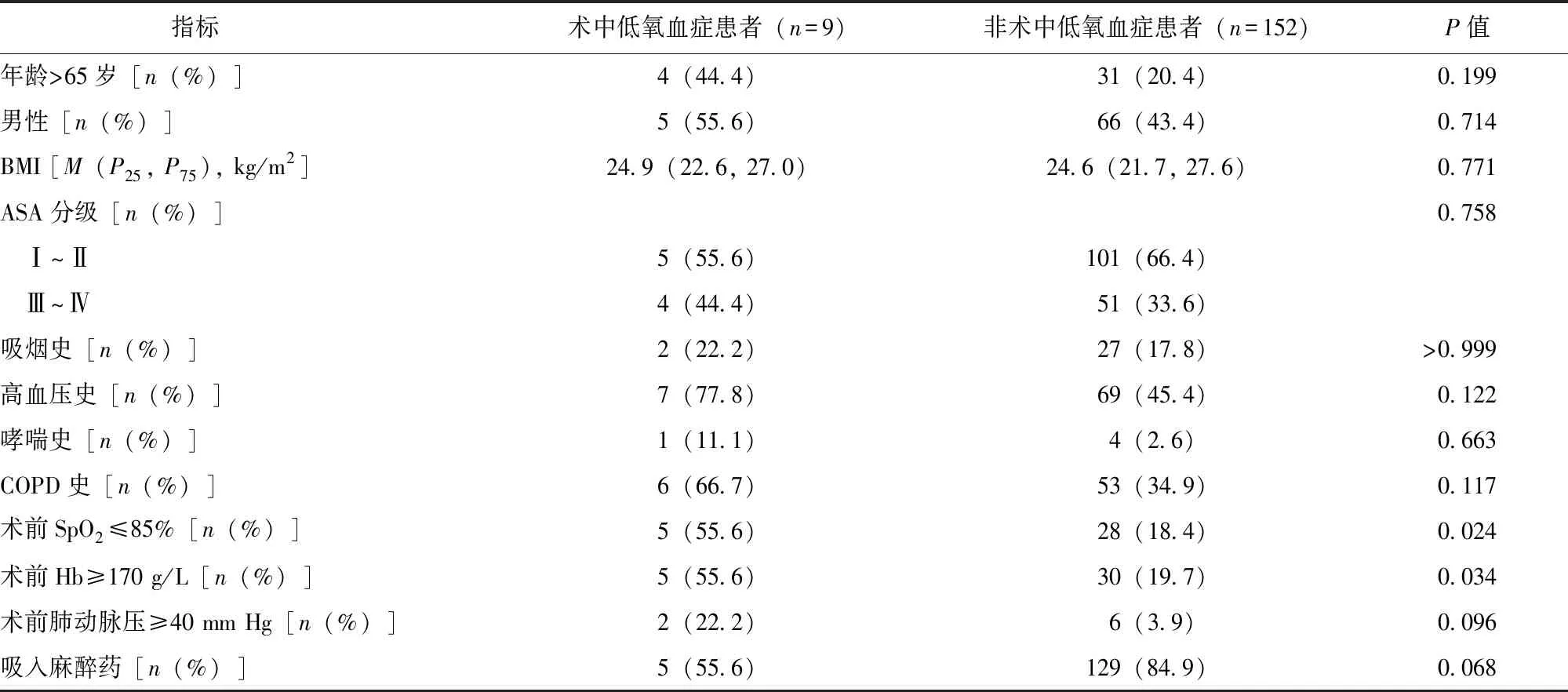
表2 术中低氧血症与非术中低氧血症患者临床资料比较

表3 全身麻醉非心胸外科手术术中低氧血症危险因素的多因素Logistic回归分析结果
1 对象与方法
1.1 研究对象
本研究为单中心前瞻性队列研究。研究对象为2021年6月1日至2022年8月31日西藏自治区人民医院行全身麻醉的非心胸外科手术患者。纳入标准:(1)居住地海拔高于3000 m,持续居住5年以上;(2)年龄≥50岁;(3)全身麻醉手术,手术类别包括腹腔和腹膜后手术(含腹腔镜手术)、血管外科手术、骨科手术、神经外科手术、头颈外科手术等。排除标准:(1)急诊手术;(2)美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级为V级及以上。
本研究已于国际临床试验注册中心(Clinicaltrials.gov)注册(注册号:NCT04819698),并通过西藏自治区人民医院伦理审查委员会审批(审批号:ME-TBHP-20-26),所有患者均签署知情同意书。
1.2 方法
1.2.1 术前评估
所有患者均完善常规术前检查,前瞻性收集患者临床资料,包括一般资料(性别、年龄、民族、吸烟史、居住地等)、既往史[高血压、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)、哮喘等]、体格检查(体质量指数)、术前检查[SpO2、血红蛋白(hemoglobin,Hb)水平、超声心动图等]。
1.2.2 围术期管理
所有患者均无麻醉前用药。入室后建立外周静脉通道,监测SpO2、血压、心率、心电图及呼气末二氧化碳分压。术中监测患者生命体征,维持血流动力学平稳,常规进行体温监测及保护。记录手术类别、ASA分级、麻醉方式(包括静脉麻醉和静吸复合麻醉)。
1.2.3 结局指标定义
(1)主要结局指标:术中低氧血症,其定义为各种原因导致术中PaO2<60 mm Hg(1 mm Hg=0.133 kPa)或SpO2<90%,持续时间大于10 min[3]。术中出现低氧血症后首先进行病因分析,如肺部基础疾病、急性肺水肿、肺栓塞、痰液阻塞气管导管、低血压等,针对病因进行相应处理并适当调节呼吸参数,包括手法肺复张、滴定呼气末正压压力以降低驱动压等保护性通气策略。
(2)次要结局指标:围术期心脏不良事件及术后转归指标。围术期心脏事件包括术中至术后30 d出现的不稳定心绞痛、心肌梗死、充血性心力衰竭、新发心律失常(心动过缓、心动过速、频发室性期前收缩、阵发性室上性心动过速、心房颤动、心房扑动、心室颤动、室性心动过速、二度Ⅱ型及三度房室传导阻滞)、心源性猝死。术后转归指标包括术后是否转入ICU、非心脏术后并发症、术后住院时间及总住院时间。
1.3 样本量估算
根据Kendall样本量粗略估计方法,样本量至少为自变量数目的5~10倍。本研究预期调查12个与术中低氧血症相关的自变量,假设样本量为自变量的5倍,术中低氧血症发生率为30%,经估算所需样本量约为180例。
1.4 统计学处理
采用SPSS 23.0软件进行统计学分析。年龄、体质量指数、术前SpO2等非正态分布的计量资料以中位数(四分位数)表示,其中体质量指数的组间比较采用Mann-WhitneyU检验。为增加分析结果的可解释性,结合文献报道、临床意义及实践[4-5],术中低氧血症危险因素筛选时将年龄、术前SpO2、术前肺动脉压等计量资料转化为二分类变量,组间比较采用卡方检验。性别、ASA分级、吸烟史等计数资料以频数(百分数)表示,组间比较采用卡方检验和Fisher精确概率法。采用多因素Logistic回归法分析术中低氧血症的危险因素。双侧检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 一般临床资料
共入选符合纳入与排除标准的全身麻醉非心胸外科手术患者161例(受限于病例数,未达到预期样本量)。其中男性71例(44.1%),女性90例(55.9%);年龄59(54,65)岁(范围:50~91岁);藏族居民153例(95.0%);146例(90.7%)居住地海拔大于3500 m;9例(5.6%)发生术中低氧血症。161例患者的临床资料见表1。
2.2 术中低氧血症危险因素的单因素分析
单因素分析结果显示,术中低氧血症患者术前SpO2≤85%(P=0.024)、Hb≥170 g/L(P=0.034)的比例均高于非术中低氧血症患者,见表2。
2.3 术中低氧血症危险因素的多因素分析
鉴于目前临床尚无针对术中低氧血症危险因素的公认意见,本研究将单因素分析中P<0.2的指标作为自变量,是否发生术中低氧血症为因变量,纳入多因素Logistic回归分析模型,以进一步筛选行全身麻醉非心胸外科手术患者发生术中低氧血症的危险因素。由于自变量均为二分类变量,分别赋值为0或1,自变量的筛选方式为向前选择法。多因素Logistic回归分析结果显示,术前SpO2≤85%、术前Hb≥170 g/L、术前肺动脉压≥40 mm Hg是高海拔地区人群行全身麻醉非心胸外科手术出现术中低氧血症的独立危险因素(表3)。
2.4 术中低氧血症对患者预后的影响
161例患者中,共28例发生围术期心脏并发症,其中18例为术中发生,8例为术后发生,2例为术中与术后均发生。3例发生非心脏术后并发症(均为非术中低氧血症患者),包括术后出血行二次手术2例,术后脑梗死1例。术中低氧血症患者围术期心脏不良事件发生率较非术中低氧血症患者显著增加(P=0.002),见表4。

表4 术中低氧血症与非术中低氧血症患者预后指标比较
3 讨论
本研究基于前瞻性收集的161例患者临床资料,探究了西藏高海拔地区全身麻醉非心胸外科手术术中低氧血症发生现况及其可能的危险因素,并对术中低氧血症与围术期预后的相关性进行了初步分析。结果显示,行全身麻醉非心胸外科手术人群术中低氧血症发生率为5.6%(9/161),术前SpO2≤85%、术前Hb≥170 g/L、术前肺动脉压≥40 mm Hg是其独立危险因素;相较于非术中低氧血症者,术中低氧血症人群围术期心脏不良事件发生率显著升高(55.6%比15.1%,P=0.002)。
3.1 术中低氧血症的危险因素
由于手术创伤的缘故,心胸外科手术患者术中发生低氧血症较常见;对于非心胸外科手术患者而言,由于术中心肺功能降低,以及受手术体位、麻醉因素、患者年龄等因素的影响,亦可发生术中低氧血症。对于高海拔地区人群,由于长期居住环境中氧分压降低,导致其合并不同程度的慢性低氧血症,故术中低氧血症的发生风险更高,但目前尚缺乏高海拔地区患者术中低氧血症发生现况及其危险因素的相关研究。本研究结果显示,161例行全身麻醉非心胸外科手术高海拔地区居民的术中低氧血症发生率为5.6%,较平原地区人群增高(超过5 min的术中低氧血症发生率为1.01%~1.95%)[6]。
本研究多因素Logistic回归分析显示,术前SpO2≤85%、Hb≥170 g/L以及肺动脉压≥40 mm Hg是高海拔地区人群行全身麻醉非心胸外科手术出现术中低氧血症的独立危险因素。术前SpO2≤85%提示患者已处于低氧或缺氧状态,若得不到及时有效的通气管理,术中低氧血症发生率明显增高。虽然红细胞生成增多可在一定程度上增加血液携氧能力,以适应高海拔地区低氧分压的环境特征,但红细胞过度增多亦可能导致慢性高原病等适应不良综合征[7]。文献显示,长期高原低氧环境所致的红细胞增多症或高血红蛋白血症与心脏及代谢相关不良事件风险增加相关,进而可能诱发术中低氧血症[8-10]。高海拔地区人群因长期处于低氧环境,多存在因缺氧性肺血管收缩导致的肺动脉高压、右心后负荷增加,甚至右心结构和功能发生改变,肺动脉高压一方面可降低患者术中对低氧的耐受性,诱发低氧血症;另一方面术中低氧血症可引起肺动脉压进一步升高,进而形成不良循环,以致术中低氧血症风险增加。
3.2 术中低氧血症对患者预后的影响
除影响术后伤口愈合外[11],术中持续性低氧血症可造成代谢紊乱,以致全身多脏器损伤[12],尤以对循环系统的影响最为显著。轻度缺氧时即可引起心率增快、心肌收缩力增强、心脏做功增加,严重缺氧则可直接抑制心脏活动,造成心肌缺血性损伤。对于长期生活在高海拔地区的人群,存在慢性缺氧和肺小动脉收缩的生理基础,术中低氧血症诱发的肺动脉压升高可进一步加重右心室负荷,进而增加围术期心脏并发症及其他不良事件发生风险[13]。一项评估高海拔地区常住居民低氧血症程度与心脏代谢风险之间关系的队列研究显示,静息SpO2每降低5%,心脏代谢异常的风险可增加数倍[14]。本研究结果显示,非术中低氧血症患者围术期心脏不良事件发生率为15.1%,而在术中低氧血症人群中此数据高达55.6%,进一步验证了术中低氧血症患者更易发生围术期心脏不良事件的结论。
对于存在术中低氧血症高风险的高海拔地区人群,术前积极改善基础疾病并适当纠正低氧血症具有重要临床意义。全军麻醉与复苏学专业委员会联合中华医学会麻醉学分会制定的《高原环境战创伤麻醉共识(2019)》建议高海拔地区人群在术前、术后充分吸氧(6~8 h/d),以提供富氧条件,减少低氧血症发生[15]。此外,高流量鼻导管氧疗是临床改善低氧血症非常有效的简易措施[16-19]。术前SpO2≤85%的高海拔地区人群予以高流量鼻导管氧疗,可能有助于改善围术期低氧血症,进而降低围术期心脏不良事件发生率并改善患者预后。对于久居高原地区的人群,Hb增高为一种代偿机制,术前不宜对Hb水平进行特殊干预,但可通过健康宣教的方式鼓励其进行日常生活方式的调整,如戒烟、适当运动等,以改善心肺功能,优化基础Hb水平[20]。对于术前存在肺动脉压≥40 mm Hg的择期或限期手术患者,应进行充分的术前评估,必要时先进行肺动脉高压的相关治疗,以提高患者围术期心肺储备功能。
本研究局限性:(1)观察指标受限,可能存在其他影响术中低氧血症发生风险的参数未纳入分析;(2)术中低氧血症与患者预后相关性的确切结论尚需多因素分析排除混杂因素的影响;(3)出现低氧血症的病例数较少(仅9例),导致统计分析效能降低,未来需开展大样本多中心研究以探索术中低氧血症的影响因素。虽然存在多方面不足,但本研究结果亦可在一定程度上为临床医生优化围术期氧合提供证据支撑。
综上,术前低氧、高血红蛋白血症以及肺动脉高压是高海拔地区居民行全身麻醉非心胸手术术中出现低氧血症的独立危险因素,应充分完善术前检查,并积极纠正术中低氧血症的危险因素,以改善患者预后。
作者贡献:段函宇、次仁德吉、苗煦涵负责数据收集;朱倩梅、李艺、张越伦、刘子嘉负责数据处理与统计分析、论文撰写;段函宇、刘子嘉、拉巴次仁、申乐、黄宇光负责研究设计及论文修订。
利益冲突:所有作者均声明不存在利益冲突

