胃内球囊用于减重的临床研究进展
康军仁,徐 强,李海龙,魏 薇
中国医学科学院北京协和医院 1临床营养科 2基本外科,北京 100730
肥胖症已成为全球性的公共卫生问题,我国肥胖症现状亦不容乐观[1],2016年Lancet报道我国肥胖人数已位列世界首位[2]。《中国居民营养与慢性病状况报告(2020年)》发现,我国成年居民超重/肥胖发生率>50%[3]。作为一种代谢综合征,肥胖症可增加糖尿病、高血压、高脂血症、脂肪肝等慢性疾病风险,给个人、家庭和社会带来沉重的经济负担[3]。常见的肥胖症治疗策略包括饮食/生活方式干预、药物干预和手术治疗[1-2]等,其中饮食和生活方式干预是基础治疗,而减重手术则是中重度肥胖症患者的有效治疗选择[4-5]。然而作为有创操作,减重手术不仅花费高,且可能存在手术并发症[6],因此临床仍需更安全、无创的治疗手段。
近年来,胃内球囊作为一种单纯容量限制型减重策略,受到临床广泛关注。其通过在胃内放置特殊材料制成的充有液体或气体的球囊,以占据胃内空间,减少胃内有效容积,延缓胃排空并增加饱胀感,从而实现减重目的[7]。胃内球囊可用于单纯通过饮食和运动未能成功减重的肥胖患者,也可用于减重手术术前先期减重的过渡性治疗[8],其减重疗效和安全性已在国际多项临床试验中得到验证[9-10]。目前,我国尚未批准该装置进入临床,胃内球囊的设计和适应证均是基于西方人群,因此我国亟需开展相关循证医学研究。本文通过回顾最新文献,从胃内球囊的适应证、禁忌证、减重效果及相关并发症等方面进行综述,以期为我国临床研究及诊疗提供参考。
1 历史沿革
胃内球囊并非新兴减重装置,其用于临床已有近40年的历史。1985年,由Garren-Edwards发明且命名为“Garren-Edwards gastric bubble”的球囊被美国食品药品监督管理局(Food and Drug Administration,FDA)批准用于减重,该球囊内充满200 mL空气,但后因减重效果差且严重并发症多,于1992年退市[11]。1987年,在美国佛罗里达召开的国际专家共识会议提出,理想的球囊应为盐水填充、表面光滑、X线无法穿透、400~500 mL大小的硅胶制品。其后,随着材料和工艺的进步,多种球囊在欧洲和南美洲获得临床应用,直至2015年,美国FDA才再次批准胃内球囊应用于临床。至今,美国FDA已批准Orbera、Obalon和ReShape Duo 3种球囊装置应用于临床[8];欧盟已批准Orbera、Obalon、ReShape Duo、Elipse、Spatz3、Heliosphere bag等多种球囊应用于临床[7]。
2 胃内球囊适应证和禁忌证
2.1 适用年龄
美国FDA批准的3种胃内球囊适用于22~60岁的肥胖人群[12]。目前多数临床研究纳入对象的年龄为18~65岁[13-14]。年龄<18岁的肥胖症患者能否常规接受胃内球囊治疗而实现临床获益,目前尚存争议。巴西临床实践指南提出胃内球囊适用于12岁以上肥胖人群,且无年龄上限[15]。但一项纳入12名青少年的小样本队列研究结果显示,留置胃内球囊6个月时受试者平均减重5%,但随访2年后减重和代谢获益未能维持[16]。因此,是否推荐青少年使用胃内球囊尚需更多研究加以验证。
2.2 适用体质量指数范围
胃内球囊适用的体质量指数(body mass index,BMI)切点值并无统一的临床标准,不同国家/地区、不同人种之间存在较大差异。大多数西方临床研究中胃内球囊适用的BMI范围如下:(1)30~40 kg/m2,经严格饮食生活方式或药物干预无效;(2)≥40 kg/m2,拒绝手术或有手术禁忌证;(3)≥50 kg/m2,减重手术术前进行先期诱导性减重治疗[7,17-18]。巴西临床实践指南建议,BMI>25 kg/m2的难治性肥胖者即可接受胃内球囊治疗[15]。欧洲将BMI>27 kg/m2作为Obalon球囊置入的适应证[19]。亚洲的一项小样本研究中,纳入胃内球囊治疗的患者BMI>25 kg/m2[20],但BMI<30 kg/m2的临床获益与风险尚需更多研究加以验证。
2.3 禁忌证
胃内球囊常见的绝对禁忌证包括:胃部手术史,食道裂孔疝,消化道出血,胃肠畸形,胃肠动力障碍,胃轻瘫,慢性腹痛,凝血障碍,严重肝硬化,怀孕或哺乳,酒精或药物滥用,激素或基因相关肥胖,置入期间不能按照规定服用质子泵抑制剂,尚未治愈的幽门螺杆菌感染,球囊过敏等;相对禁忌证包括:腹部手术史,炎性肠病,非甾体抗炎药使用期间,食管炎,精神障碍等[7,13-15]。
3 胃内球囊减重机制
3.1 减少胃内游离容积
置入球囊后,机械性地限制了胃内容积,客观上受试者每餐摄入的食物可能减少,从而减少了能量摄入[21]。
3.2 延长胃排空时间
一项纳入29例肥胖症患者的单中心随机对照研究发现,与空白对照相比,置入胃内球囊后,患者的胃排空延迟,且在移除球囊后恢复正常;同时,胃排空延迟时间越长,减重效果越好,提示改变胃动力是球囊减重的重要机制[22]。
3.3 降低胃饥饿素水平
胃内球囊可扩充和拉伸胃壁,在能量摄入减少的基础上降低胃饥饿素水平,增加饱胀感。一项基于健康成年人的研究发现,球囊扩张能够激活疼痛反应区域和失活外部感觉,不进食不影响胃饥饿素分泌;而在营养摄入的过程中,中脑被激活,胃饥饿素水平降低[23]。
4 常见胃内球囊减重效果及其并发症
基于已有的胃内球囊特征,根据球囊内容物不同可分为水囊或气囊;根据球囊数目多少可分为单球囊、双球囊和三球囊;根据放置方式不同可分为胃镜置入球囊和经口吞咽球囊;根据放置后可否调节分为可调节球囊和不可调节球囊(表1)。
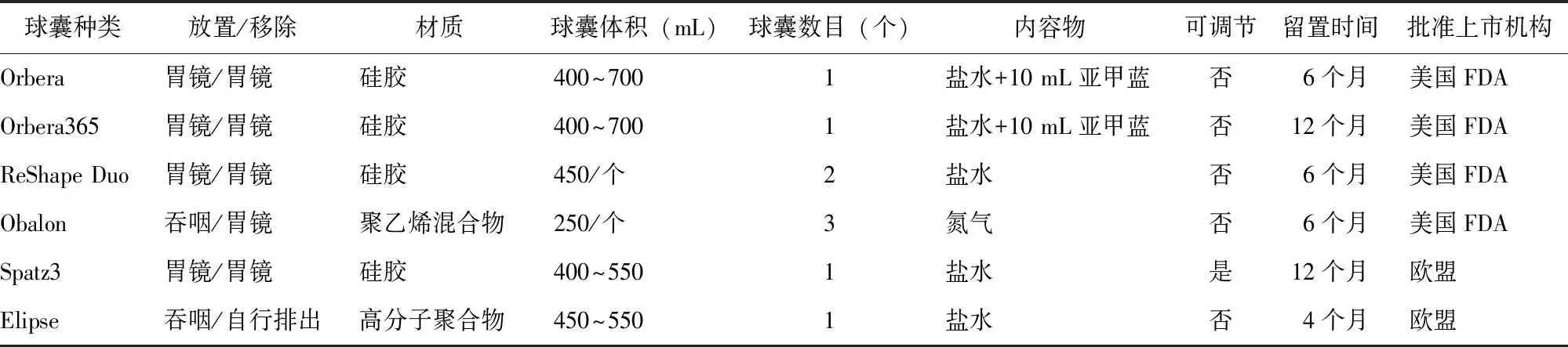
表1 常见胃内球囊及其特征
评价胃内球囊减重效果的常用指标包括:体质量下降(初始体质量-当前体质量),总体质量减少百分比[(初始体质量-当前体质量)/初始体质量]和额外体质量减少百分比[(初始体质量-当前体质量)/(初始体质量-标准体质量)]。文献报道,不同胃内球囊在取出后,总体质量减少6.8%~13.2%,额外体质量减少25.1%~67%;常见并发症以胃肠道症状为主(91%),如恶心、呕吐、反酸、打嗝和腹痛等[9];球囊相关器械并发症包括破裂和移位(0.6%~15%),严重并发症包括移位后引起的胃肠道梗阻(0.15%~2.9%)[24-25],压迫胃壁或胰腺出现胃溃疡(2.9%~3.33%)[24,26]、消化道穿孔(0.05%~1.7%)[25,27-29]或胰腺炎(2.1%)[30],甚至死亡(0.08%)[27,31](表2)。
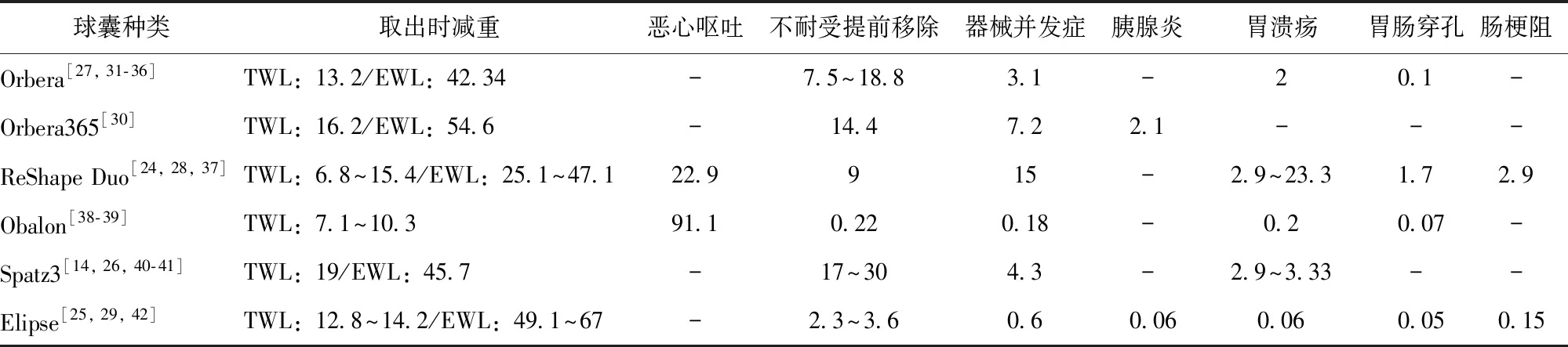
表2 常见胃内球囊减重效果及其并发症发生率(%)
4.1 Orbera球囊
Orbera球囊(Apollo Endosurgery,Austin,TX,United States)是目前国际上应用最广泛的单个球囊,由1991年的BIB球囊(Inamed Corporation,Santa Barbara,CA,United States)[31]演变而来,内部注入400~700 mL生理盐水及10 mL亚甲蓝,放置和取出均需在胃镜下进行。通常在胃内留置6个月,最新的Orbera365球囊可在胃内留置12个月[30]。
一项Meta分析纳入5549例肥胖症患者,置入Orbera球囊后6个月减重13.2%[32]。日本的一项研究发现,接受Orbera球囊治疗的399例肥胖症患者,额外体质量减轻46.6%,总体质量减轻11.5%[33]。在一项长期随访研究中,肥胖症患者Orbera球囊取出后继续随访12个月,额外体质量减轻27.7%,随访5年后,额外体质量减轻13.0%[34]。另一项纳入17项研究的Meta分析发现,置入Orbera球囊6个月时取出,随访12个月后额外体质量减轻25.4%,总体质量减轻11.3%[27]。该研究报道的不良反应包括腹痛、恶心、早期移除、胃溃疡、球囊移位和胃穿孔[27]。
早期文献报道了BIB球囊相关死亡病例[35]。一项2003—2006年的小样本前瞻性研究结果显示,26例肥胖症患者置入BIB球囊,其中1例48岁患者在球囊置入后1d死于误吸导致的心脏骤停[36]。近年来,美国FDA网站上仍有液体球囊死亡的病例报道,常见原因为消化道穿孔。虽然死亡率较低,但球囊置入应严格把控适应证和禁忌证,同时做好监测工作。
由于Orbera365球囊在胃内时间长于普通球囊,其减重效果可能优于常规Orbera 球囊。一项前瞻性研究发现,Orbera365放置12个月后,总体质量减轻16.2 %,额外体质量减轻54.6%[30]。并发症包括不耐受移除、球囊破裂渗漏和胰腺炎[30]。
4.2 ReShape Duo球囊
ReShape Duo球囊(ReShape Duo® Integrated Dual Balloon System)包含两个独立的球囊,二者并不相通,通过柔软的硅胶轴连接,其设计思路在于即便单独球囊破裂后,双球囊结构可降低球囊在肠道移位导致的肠梗阻风险。每个球囊最多可填充450 mL 生理盐水。ReShape Duo球囊可在胃内留置6个月,置入和取出均需在胃镜下进行[31]。
一项随机对照研究发现,187例肥胖症患者置入ReShape Duo球囊后,额外体质量减轻25.1%,高于单纯饮食控制(P=0.004)[37],并发症包括球囊萎缩、不耐受提前移除、胃溃疡和器械相关并发症[37]。另一项研究中,置入ReShape Duo球囊6个月后,患者平均减重16.6 kg,总体质量减轻15.4%,额外体质量减轻47.1%[28],并发症包括不耐受移除、球囊萎缩、胃穿孔和胃溃疡[28]。
4.3 Obalon球囊
Obalon球囊(Obalon Therapeutics Inc,Carlsbad,CA,United States)是美国FDA批准的可吞咽气囊,包含3个不连通的球囊,这种聚乙烯混合物可放在食用明胶制成的胶囊中直接吞入胃内,再由连接的导管(直径3Fr)充气,每个气囊最大容积为250 mL,球囊充气后导管可脱落取出,3个气囊可每个月依次放置1个。Obalon球囊可在胃内留置6个月,取出需在胃镜下进行[31]。
一项多中心随机对照研究显示,387例肥胖症患者置入Obalon球囊6个月后,总体质量减轻7.1%,12个月后球囊组仍有88.5%的患者实现减重维持,总体质量减轻6.9%,严重并发症包括出血性溃疡1例和球囊破裂1例[38]。一项回顾性研究中,1343例肥胖症患者置入Obalon气囊6个月后,平均减重9.7 kg,总体质量减轻10.0%,常见并发症包括腹痛、恶心、呕吐和腹胀,严重并发症包括球囊移位1例和胃穿孔1例[39]。
4.4 Spatz3球囊
Spatz球囊(Spatz FGIA,Great Neck,NY,United States)是一种可调节球囊,球囊连接一个硅胶填充管,通过留置的导管注入盐水,可调整球囊容积大小。Spatz3 是第三代Spatz球囊,可在胃内留置12个月,置入和取出均需在胃镜下进行。Spatz3球囊初始置入体积为400~550 mL,其优势在于当初始容积球囊不耐受时可适当缩小容积,增加患者耐受性;当减重效果不理想时,又可增加容积,以提高减重效果[14]。
一项英国临床研究中,70例肥胖症患者置入Spatz球囊后随访12个月,平均减重21.6 kg,总体质量减少19%,额外体质量减少45.7%。该研究中30%(21例)提前移除球囊,包括4例不耐受、3例球囊破裂和14例减重满意后移除,严重并发症包括导管嵌顿、需手术取出[40]。一项多中心随机对照研究纳入288例成人肥胖症患者,随机2∶1分为球囊干预组和对照组,同时联合饮食生活方式干预。球囊放置时间为8个月,总体质量减轻15%,明显优于对照组。球囊组80%因减重效果不满意或不耐受而进行了球囊调整,17%因不耐受而提前移除球囊[14]。Spatz3球囊的严重并发症还包括胃穿孔、需手术治疗和死亡[41]。
4.5 Ellipse球囊
Ellipse球囊(Allurion Technologies,Wellesley,MA,USA)是一种可直接吞咽并无需胃镜移除的球囊。其由可自行降解的聚合物薄膜制成,封闭在一个可吞咽的胶囊中,同时连接一个长约75 cm的细导管。胶囊吞入胃内后自然分解,球囊被释放,通过连接导管可注入550 mL左右的盐水或蒸馏水。球囊在人体内4个月后可自行降解,通过胃肠道排出体外[31]。Ellipse球囊降低了放置/取出成本及相关风险,适用于不耐受胃镜检查或有麻醉风险的肥胖症患者;但同时,因无需行胃镜检查,可能会忽略已存在的胃溃疡或解剖异常。
一项Meta分析显示,2013例肥胖症患者在接受Ellipse球囊治疗4个月后,总体质量减轻12.8%,随访至12个月,总体质量减轻10.9%,并发症包括早期移除、小肠梗阻和胃穿孔[25]。另一项Meta分析发现,肥胖症患者接受Ellipse球囊治疗后,总体质量减轻12%,额外体质量减轻49.1%[42]。
5 挑战与未来研究方向
5.1 胃内球囊长期减重效果尚不明确
大多数胃内球囊的留置时间为4~6个月,部分为12个月,球囊留置期间减重效果一般较好,但球囊取出后的长期减重效果目前仍不明确[7]。一项Orbera球囊研究中,随访12个月时肥胖症患者额外体质量减轻27.7 %;195例患者随访至5年,额外体质量减轻13.0%[34]。体质量减轻一般会伴随能量消耗下降[43],但身体同时也会启动反馈调节机制,如食欲刺激素和抑胃肽等分泌增加[44]。有研究发现,减重维持时间越长,随着脂肪细胞直径逐步增大,体质量越容易反弹[45]。
手术的减重疗效更为显著,然而并非所有患者均愿意或可接受减重手术,针对不愿意接受减重手术的肥胖症患者,有研究设计了多次放置胃内球囊以探索其长期减重效果。该研究共纳入83例患者,平均BMI为43.7 kg/m2,第一次球囊取出后,BMI减至35.9 kg/m2,18个月后BMI反弹至37.9 kg/m2,随后所有患者均接受二次球囊放置,18例(21.7%)接受三次放置,1例(1.2%)接受四次放置,随访6年,研究终点BMI为37.6 kg/m2,结果发现第二次及以后的球囊放置减重效果远低于首次。该研究纳入的均为不愿接受减重手术的患者,然而在随访过程中,18例(21.7%)最终接受了减重手术[46]。胃内球囊放置虽属于无创操作,但其与减重手术对于肥胖症患者的长期获益比较仍值得深入探讨(表3)。

表3 胃内球囊与减重手术比较
此外,大多数胃内球囊临床研究均联合了饮食生活方式干预,限制了总能量摄入。作为容量限制型减重策略,在球囊取出后,其长期减重效果取决于患者的生活习惯和依从性,同时包括患者的心理健康,尤其是体质量减轻伴随的代谢指标改善,更需要长期随访研究。
5.2 胃内球囊减重效果研究亟需来自中国肥胖人群的证据
5.2.1 BMI切点值
亚洲人群进行的胃内球囊减重研究中,部分采用国际通用的胃内球囊适应证BMI切点值,纳入了BMI>25 kg/m2的患者[20]。但这些研究多为样本量较小的探索性研究,证据级别不高,因此适用球囊治疗的BMI切点值尚需大样本前瞻性研究加以验证。
我国肥胖症类型多为腹型,BMI水平相对较低时即可出现肥胖相关代谢性疾病。以减重手术为例,《中国肥胖及2型糖尿病外科治疗指南(2019版)》将减重手术适应证的BMI切点值下调了2.5 kg/m2[6]。目前胃内球囊在国内尚未批准进入临床,适合中国肥胖人群的球囊BMI适应证目前尚无定论,亟需开展相关研究。
5.2.2 球囊容积
一项Orbera球囊的Meta分析发现,球囊容积增大不易移位,但容积与6个月后减重效果 (P=0.268)、球囊早期移除率(P=0.1)、胃食管反流症状(P=0.64)以及溃疡发生率(P=0.09)均无明显相关性[32]。一项关于Spatz球囊容积的多中心随机对照研究根据患者耐受程度,在胃镜下调整球囊大小以强化减重效果,该研究中,850 mL为实际最大容积[14]。
我国肥胖人群基数大且肥胖类型存在人种差异,因此迫切需要探索适宜中国肥胖人群的球囊容积。
6 小结与展望
同减重手术相比,胃内球囊创伤小、花费低,严重并发症少,为采用长期饮食生活方式减重无效的肥胖症患者提供了新途径。胃内球囊与减重手术适应证的BMI范围存在重叠,一方面,胃内球囊为满足减重手术标准而又不愿接受减重手术治疗的肥胖症患者提供了额外选择;另一方面,对于BMI≥50 kg/m2的人群,胃内球囊可在减重手术前进行先期诱导性减重。
在治疗过程中,胃内球囊减重应联合饮食、运动、心理等干预,采用多学科团队诊疗模式,以强化近期减重及维持长期减重效果。同时,应严格把握胃内球囊置入适应证,定期随诊,监测相关并发症的发生。未来随着材料改进及球囊设计技术的进步,胃内球囊在减重领域的应用前景将更加广阔。
作者贡献:康军仁负责构思、起草、修订论文;徐强、李海龙负责查阅、整理文献资料,修订初稿和写作指导;魏薇负责查阅、整理文献资料及论文修订。
利益冲突:所有作者均声明不存在利益冲突

