贝利尤单抗治疗系统性红斑狼疮出现严重感染风险的系统评价
郑建平,俞惠翻,杨 丽,王立芳,陈锦珊
(联勤保障部队第九〇九医院/厦门大学附属东南医院药剂科, 福建 漳州 363000)
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种复杂的慢性自身免疫性疾病,可累及皮肤、关节、肺、心脏和肾脏等多种器官,主要致病原因是患者自身大量抗体产生和免疫复合物沉积[1]。既往SLE的治疗药物主要包括非甾体抗炎药、糖皮质激素、抗疟药以及免疫抑制剂等,被称为标准治疗(stand of care,SoC)[2]。虽然SoC在临床应用已有60余年,但是存在不良反应大、疾病复发率高和靶向性差等缺点,其中包括严重感染风险[3]。贝利尤单抗是基于B细胞在SLE发病中的重要作用而研发的,美国食品药品监督管理局(FDA)于2011年、欧洲药品管理局(EMA)于2019年批准其为用于治疗SLE的靶向制剂[4-5]。国内相关文献主要涉及贝利尤单抗治疗SLE的疗效研究,现阶段未见对贝利尤单抗治疗SLE是否增加严重感染风险进行系统评价的文献报道。为此,本研究通过对已发表的关于贝利尤单抗治疗SLE的研究中患者出现严重感染风险进行Meta分析,为临床安全用药提供循证证据。
1 资料与方法
1.1 纳入与排除标准
(1)纳入标准:①研究类型为临床随机对照试验(RCT);②研究对象为临床明确诊断为SLE的患者;③干预措施,观察组患者采用SoC联合贝利尤单抗治疗,对照组患者采用SoC联合安慰剂治疗。(2)排除标准:文献中的数据不明确或者不充分。
1.2 文献检索策略
文献检索范围:the Cochrane Library、Ovid Embase、PubMed、中国生物医学文献服务系统、维普数据库、中国知网和万方数据库等;检索时限:建库至2022年7月1日。检索策略为“篇名”和“摘要”相结合,中文检索词为“系统性红斑狼疮”和“贝利尤”,外文检索词为“Lupus Erythematosus,Systemic”和“belimumab”。中文文献检索以中国知网为例,其检索策略为“(篇名=系统性红斑狼疮 或 摘要=系统性红斑狼疮)且(篇名=贝利尤 或 摘要=贝利尤)”;外文文献检索以PubMed为例,其检索策略为“Lupus Erythematosus,Systemic[Title/Abstract] and belimumab[Title/Abstract]”。
1.3 文献筛选及资料提取
文献筛选方法:由2名研究员对初步检索到的文献的文题、摘要以及全文进行阅读,符合本研究制定的纳入与排除标准即可采纳,再交叉核对进一步确认无误。对采纳的文献需要提取以下数据:(1)第一作者、发表年份;(2)随机分组方法、施盲情况等;(3)治疗方案、总病例数和严重感染病例数;(4)以风险率作为评估指标进行分析,风险率=严重感染病例数/总病例数×100%。
1.4 文献质量评价
参照Cochrane系统评价手册中有关RCT的质量评价标准,由2名研究人员先各自对纳入的文献进行质量评价,其标准内容包括随机方法、盲法及分配隐藏、失访或退出。若以上内容描述完全清楚,则评为A级;若以上内容描述不完全清楚,则评为B级;若以上内容描述不明确,则评为C级。若评价结果出现分歧,可通过讨论方式解决。
1.5 统计学方法
采用RevMan 5.3统计软件进行数据分析。根据异质性指数I2及其对应P值来判断异质性大小,若各研究间无异质性(P≥0.1,I2<50%),采用固定效应模型分析;若各研究间存在异质性(P<0.1,I2≥50%),采用随机效应模型分析。分析结果采用风险差异(RD)和95%CI表示。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果与纳入文献的基本信息
检索得到456篇文献,阅读文题及摘要进行初步筛选获得20篇文献,阅读全文后排除11篇文献,最终纳入9篇文献[6-14],共5 174例患者。纳入文献的基本信息见表1。

表1 纳入文献的基本信息Tab 1 Basic information of the enrolled studies
2.2 纳入研究的质量评价
纳入的9篇文献均为RCT研究,其中4项研究[6,11,13-14]提及随机分组方法、盲法以及分配隐藏,2项研究[10,12]提及随机分组方法、盲法,1项研究[7]提及盲法及分配隐藏,1项研究[8]提及盲法。评分结果:8项研究[6-8,10-14]评为B级,1项研究[9]评为C级。纳入研究的偏倚风险见图1—2。
图1 纳入研究的偏倚风险总图Fig 1 General diagram of risk of bias of the enrolled studies

图2 纳入的各研究的偏倚风险Fig 2 Risk of bias of the enrolled studies
2.3 严重感染风险分析
对所纳入的9项研究中治疗后患者出现严重感染的情况进行数据分析。各研究间无统计学异质性(P=0.62,I2=0%),故采用固定效应模型进行分析。结果显示,贝利尤单抗联合SoC组与安慰剂联合SoC组患者出现严重感染的风险比较,差异无统计学意义(RD=-0.00,95%CI=-0.01~0.01,P=0.89),提示在SoC的基础上联合应用贝利尤单抗并未增加严重感染的风险,见图3。

图3 贝利尤单抗联合SoC对比安慰剂联合SoC治疗SLE出现严重感染风险的Meta分析森林图Fig 3 Meta-analysis of comparison of risks of severe infection in SLE patients treated with belimumab combined with SoC and placebo combined with SoC
2.4 发表偏倚分析
对所纳入的9项研究进行发表偏倚分析,结果显示,漏斗图呈现为完整等边三角形,多数研究集中于顶部且对称性良好,表明出现发表偏倚的可能性极低,可信度高,见图4。
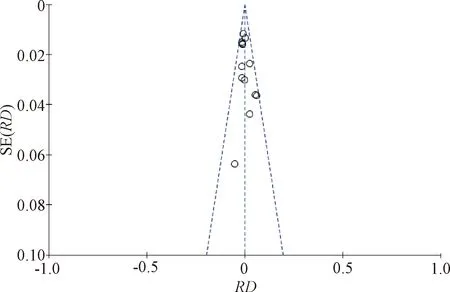
图4 所纳入研究发表偏倚分析的漏斗图Fig 4 Funnel plot of publication bias analysis of the enrolled studies
3 讨论
2019年,欧洲抗风湿病联盟系统性红斑狼疮管理指南提出,在SoC疗效不佳,即出现疾病控制不稳定、治疗期间不能耐受糖皮质激素减量和(或)频繁复发时,推荐生物制剂(如贝利尤单抗或利妥昔单抗)联合SoC治疗[15]。FDA和EMA批准贝利尤单抗为用于治疗SLE的生物制剂[5]。基于上述依据,本研究的对比设计为观察组患者采用贝利尤单抗联合SoC治疗,对照组患者采用安慰剂联合SoC治疗。
研究结果表明,SLE患者外周血中B细胞活化因子(BAFF)的表达水平高于正常健康人,增加的BAFF促进B细胞活化,并最终导致体液免疫反应增强从而致病[16-17]。相关体外研究结果提示,在SLE动物模型中,阻断实验小鼠BAFF后,小鼠外周血中BAFF表达水平降低,B细胞减少,治疗15周后小鼠的蛋白尿减少,肾脏病理损伤减轻[18];同时,在敲除BAFF基因的小鼠中也观察到类似结果[19]。贝利尤单抗作为一种完全人源的抗BAFF生物制剂,主要通过与可溶性BAFF结合从而阻断其生物作用,实现选择性减少幼稚B细胞数量和阻止B细胞的过度活化[20]。本研究结果显示,比较,贝利尤单抗联合SoC组与安慰剂联合SoC组患者出现严重感染的风险比较,差异无统计学意义(P=0.89),该结果主要归究于贝利尤单抗选择性杀伤致病B细胞的作用。B细胞是介导体液免疫应答的重要细胞,能实现清除抗原、抑制炎症反应等作用[21]。因此,对SLE患者进行选择性杀伤致病B细胞的治疗,避免了不必要的B细胞杀伤,从而降低了出现严重感染的风险。同时,本研究分析得出的RD值近乎为0(RD=-0.00),表明在SoC的基础上联合应用贝利尤单抗并未增加严重感染的风险,合理的SoC方案与降低严重感染风险的关联性较大。
综上所述,本研究具有一定的意义。然而,本研究存在局限性,现有的文献均为欧洲国家的相关研究,未见包括我国在内的东北亚国家相关研究报道,所纳入的研究质量等级评价以B级为主,无A级的研究纳入。因此,本研究的结论仍需更多高质量临床资料进行分析和验证,为SLE临床治疗决策提供更充分的循证依据。

