生物化学教材中氨基酸分类与理化性质的辨析
张海涛 伍俊 汪宗桂


摘 要:生物化学教学中关于蛋白质组成的氨基酸种类和分类及其理化性质是本科教学重要内容,目前生物化学教材中有关氨基酸的阐述存在错误或不足,该文根据文献资料补充和更新一些新知识,提出一些修正意见和补充说明,并解释具有三个解离基团氨基酸的等电点(isoelectric point, pI)计算的方法和原理。
关键词:氨基酸;本科教学;水溶性;等电点;生物化学
Abstract: In biochemistry teaching, the amino acid species and classification of protein composition and its physical and chemical properties are important contents of undergraduate teaching. At present, there are some errors or deficiencies in the description of amino acids in biochemistry textbooks. This paper supplements and updates some new knowledge according to the literature, puts forward some correction suggestions and supplementary explanations, and explains the method and principle of calculating isoelectric point (pI) of amino acids with three dissociating groups.
Keywords: amino acid; undergraduate teaching; water solubility; isoelectric point; biochemistry
生物化学与分子生物学是发展和更新较快的前沿学科之一,其主要任务是在分子水平上研究和阐述生物大分子物质的结构与功能,物质代谢途径、规律及调节机制,遗传信息的传递与表达,细胞信号的转导等,是高等医学院校医学专业及相关专业学生的必修课,并为学习其他基础医学和临床医学课程、在分子水平上认识病因和发病机理、诊断和防治疾病奠定扎实的基础。教材中的每一个概念都十分严谨,也十分重要,其严谨性不仅影响到这门学科的科学性,甚至会影响到整个生命科学的科学性。对于那些比较权威及应用比较广泛的统编教材,在生命科学领域更是地位显著,其影响也更加深远[1]。生物化学教学中关于蛋白质组成的氨基酸种类和分类及其理化性质是本科教学重要内容,但现行的生物化学教材对上述内容的阐述尚存在一些不足和遗漏,并且存在一些错误的解释。我们根据教学经验和汇总各方客观资料,提出一些修正意见和补充说明,以供从事生物化学教学的同行分析和商榷,从而保证生物化学教学的科学性和完整性。
一 细胞内合成蛋白质的氨基酸种类
现行的生物化学教材大多介绍组成蛋白质氨基酸种类是20种,其实20世纪80年代[2]和21世纪初[3]已经发现细胞内实际有22种氨基酸由遗传密码对应编码,但大多数教科书一直没有更新这方面的知识。目前已经确定核糖体中合成的多肽(蛋白质)可由22种氨基酸组成,其中20种氨基酸是与61种遗传密码对应的基本氨基酸,而硒代半胱氨酸(selenocysteine,Sec,单字母缩写 U)(或称硒氨酸)[2]和吡咯赖氨酸(pyrrolysine,Pyl,单字母缩写O)[3]是尚未列入教材的两种参与细胞内一些重要蛋白质合成的氨基酸。硒氨酸和吡咯赖氨酸与在多肽链水平上修饰的氨基酸(如羟赖氨酸、羟脯氨酸)是不一样的,硒氨酸和吡咯赖氨酸均有相应的遗传密码对应编码,羟赖氨酸和羟脯氨酸是赖氨酸和脯氨酸羟化修饰后的产物,并不是直接通过密码子翻译而来。两种氨基酸的发现,以及其对应遗传密码的阅读方式均与20种基本氨基酸有很大的不同,这提示生命的进化及遗传密码的阅读可塑性比我们想象的要复杂得多。建议新编教材补充列入这些新知识。
硒氨酸的结构和半胱氨酸或丝氨酸类似,这三种氨基酸侧链基团的氧、硫、硒为同族元素(图1)。硒氨酸的侧链含有-SeH,该基团的pKR=5.73, 在生理条件下,硒氨酸中的硒离子化,可作为一种极其有效的生物催化剂。
硒氨酸对应的密码子是UGA,这个密码子原本是作为终止密码子使用,但在一些特殊的mRNA序列中UGA编码硒氨酸。mRNA上终止密码子UGA后存在一个特殊的信号序列(SECIS),該序列具有引导把UGA解码为Sec的功能。在真核生物的31个硒蛋白基因的3′非翻译区均发现1或2个可能的SECIS结构,大约60个核苷酸的长度,采用茎环结构的RNA元件,它们都含有3段保守碱基AUGA-A(G/U)AA-GA[4]。
目前细胞内没发现存在游离的硒氨酸,也不存在硒氨酰tRNA合成酶,因此细胞内无法直接将游离硒氨酸连接到tRNASec。在细胞内, tRNASec在特殊的丝氨酰-tRNASec合成酶催化下,先与细胞内的丝氨酸(Ser)合成Ser-tRNASec,然后再将Ser-tRNASec携带的Ser修饰为Sec[4]。硒元素由硒代磷酸盐提供。
真核细胞和细菌催化Ser-tRNASec转变为Sec-tRNASec的方式不同。在真核细胞内,首先由磷酸丝氨酰-tRNASec激酶(O-phosphoseryl-tRNASec kinase,PSTK)催化Ser-tRNASec生成磷酸丝氨酰-Ser-tRNASec(Sep-tRNASec)。Sep-tRNASec在Sep-tRNASec:Sec-tRNASec合酶(Sep-tRNASec:Sec-tRNASec synthase,SepSecS)的催化下,接受磷酸硒的硒元素生成终产物Sec-tRNASec(图2)[5]。磷酸硒是人体内主要的硒供体,由磷酸硒合成酶2(selenophosphate synthetase2,SPS2) 利用硒蛋白/硒氨酸降解、硒化物和三磷酸腺苷(ATP)为反应底物催化产生。最后,Sec-tRNASec通过一个专门的延伸因子EFsec转运到核糖体。在脊椎动物中,SECIS结合蛋白2(SECIS-binding protein 2,SBP2)是解码硒氨酸UGA密码子所必需的辅助蛋白因子。
在细菌中,硒氨酸合成酶直接催化Ser-tRNASec去除丝氨酰基团中的羟基形成中间体[6]。随后,中间体接受磷酸硒盐的硒元素最终产生Ser-tRNASec。
现发现硒氨酸是细胞内25种重要的含硒酶(尤其是抗氧化酶)活性中心,如谷胱甘肽过氧化酶、硫氧还蛋白还原酶、甲状腺素-5′-脱碘酶、甘氨酸还原酶、甲酸脱氢酶等,含硒半胱氨酸残基的蛋白质一般称为硒蛋白。硒氨酸在体外表现出一定的细胞毒性,而且从硒氨酸参与合成细胞内硒蛋白的机制分析[5],服用硒氨酸可能对合成硒蛋白无直接促进作用,适当地维持细胞内硒元素的平衡才有助于硒蛋白合成。
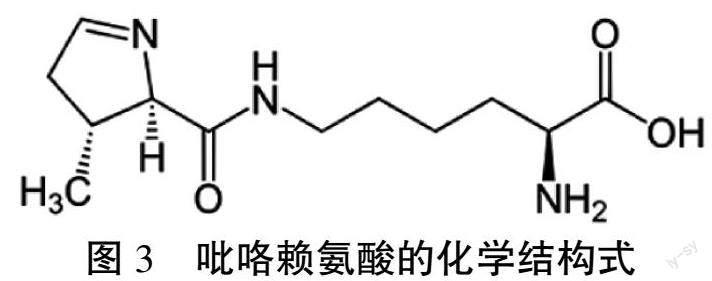
吡咯赖氨酸(N6-[(2R,3R)-3-甲基-3,4-二氢-2-氢吡咯-2-甲酰]-L-赖氨酸)是赖氨酸的侧链氨基被(4R,5R)4-吡咯啉-5-羧基酰胺化。2002年,Krzycki的研究小组在产甲烷菌的古细菌-巴氏甲烷八叠球菌的甲胺甲基转移酶中发现吡咯赖氨酸[7],人体蛋白暂时没发现有吡咯赖氨酸构成的蛋白质。
从吡咯赖氨酸的化学结构式分析(图3),Pyl的侧链含有酰胺键,吡咯环中的=N-也可与水相互作用,形成=N-H+,也就意味Pyl的侧链的性质是极性,且可能在pH7时带正电荷。
吡咯赖氨酸由终止密码子UAG有义编码形成,由相应的吡咯赖氨酰-tRNA合成酶催化生成吡咯赖氨酰基化-tRNA(Pyl-tRNAPyl)。Pyl-tRNAPyl在核糖体中解读mRNA上的UAG密码子,将吡咯赖氨酸写入合成的多肽链。Pyl-tRNAPyl的合成方式有两种:吡咯赖氨酰-tRNA合成酶直接催化Pyl和tRNAPyl合成Pyl-tRNAPyl;先催化赖氨酸与tRNAPyl合成Lys-tRNAPyl,然后将Lys修饰成Pyl。细胞将mRNA终止密码子UAG解读成Pyl密码子同样依赖于UAG后存在一个特殊的核酸信号序列。
二 氨基酸分类和侧链与水溶性的关系
生物化学教材一般根据氨基酸侧链R基团的结构和理化性质不同,可将主要的20种氨基酸分成4类:非极性疏水性氨基酸、极性中性氨基酸、酸性氨基酸和碱性氨基酸[8-10]。
许多教材都有“非极性疏水性氨基酸的水溶性低”“极性中性氨基酸较非极性疏水性氨基酸的水溶性大”的总结性阐述[8-10],但这是一个不科学的阐述,甚至可以说是因氨基酸分类名称而产生的一种错误描述。从20种氨基酸所测得的实际理化参数来看,极性侧链的氨基酸的水溶性不比非极性疏水性氨基酸水溶性大。表1是20种基本氨基酸的水溶性,从表中可知非极性疏水性氨基酸中的脯氨酸水溶性最大,而极性中性氨基酸的酪氨酸的水溶性最小。另外,两个侧链是极性的酸性氨基酸(天冬氨酸和谷氨酸)水溶性也不高。可见,氨基酸的水溶性与其侧链名称无直接联系,但是氨基酸在组成蛋白质后,非极性疏水性氨基酸的非极性侧链可促进蛋白质的疏水区域形成,使得蛋白质在水中的溶解度变小,而极性中性氨基酸由于含有具有一定极性的R基团,其极性侧链常常参与组成蛋白质亲水区域形成,增加蛋白质水溶性。
此外,对于一些氨基酸的分属归类也存在着值得商榷的地方。如,甘氨酸是唯一不含手性碳的氨基酸,侧链只有一个氢原子,而C-H是极性键,严格来说其不应该归类在非极性疏水性氨基酸,实际上该氨基酸水溶性属于易溶,建议单列该氨基酸为非手性碳氨基酸。
对于甲硫氨酸是属于非极性疏水性氨基酸,还是属于极性中性氨基酸,以往不同的教材有差异。鉴于甲硫氨酸的侧链含有碳硫共价键,理论上甲硫氨酸属于极性中性氨基酸,但由于甲硫氨酸的两个碳硫共价键属于双键性质,并且对称直线分布,属于典型的极性键非极性侧链性质,因此目前将甲硫氨酸归在非极性疏水性氨基酸更合理些。
硒氨酸的侧链含有C-Se键,属于极性键,又由于该基团的pKR=5.73, 在生理条件下,可释放质子,导致硒离子化,因此硒氨酸理论上归于酸性氨基酸。半胱氨酸侧链含-SH,-SH的pKR=8.18,在生理条件下,-SH理论上会部分解离,实际上半胱氨酸水溶液呈酸性,pH在3%时为1.2,1%时为1.7,0.1%时为2.4。因此半胱氨酸归于弱酸性氨基酸似乎更合理些。丝氨酸侧链含-OH,pKR=13.6,在生理条件下,-OH解离程度不高,故归于极性中性氨基酸。
吡咯赖氨酸的归属侧链的性质是极性,且可能在pH7时带正电荷,理论上归于碱性氨基酸。
三 氨基酸等电点计算
氨基酸的pI是由氨基酸分子内的可解离基团的解离常数负对数pKa决定的。甘氨酸、天冬酰胺、谷氨酰胺、色氨酸和非极性侧链氨基酸的R侧链无可解离基团,因此这些氨基酸的pI由α-COOH和α-NH3+的解离常数的负对数pK1和pK2决定的。pI的计算方法为:pI=1/2(pK1+pK2)。如亮氨酸的pK-COOH=2.36,pK-NH2=9.60,故pI=1/2(2.36+9.60)=5.98。
如果一個氨基酸中有三个可解离基团,其等电点由α-COOH、α-NH3+和R基团的解离状态共同确定,按照溶液pH从低到高增加,各解离基团释放质子的次序,选择使得氨基酸分子处于净电荷为零的两个相邻的pKa的平均值。例如谷氨酸的三个解离基团:α-COOH(pK1=2.19)、γ-COOH(pKR=4.25)和α-NH3+(pK2=9.67)。该氨基酸分子可解离基团释放质子的次序是α-COOH、γ-COOH和α-NH3+。当pK1
半胱氨酸也含三个解离基团:α-羧基(pK1=1.96)、-SH(pKR=8.18)和α-氨基(pK2=10.28)。pKR
总之,教材是学生学习专业知识的第一手参考资料,教材的编写在保证科学性的基础上,需要详略得当,及时更新知识[11],并且在教材中一些容易混淆的知识点上教师与学生都会有更高的要求,一定要明晰,一些难点问题一定要解析透彻,这样才能让初学的学生更容易理解并掌握学习的知识。本文提供补充一些原生物化学教材有误或不足的内容,以供同行参考。
参考文献:
[1] 杜秀红,崔节虎,刘隽,等.高等院校生物化学教材某些概念科学性探讨[J].医学争鸣,2017,8(4):66-69.
[2] CHAMBERS I, FRAMPTON J, GOLDFARB P, et al. The structure of the mouse glutathione peroxidase gene: the selenocysteine in the active site is encoded by the 'termination' codon, TGA[J]. EMBO J,1986,5(6):1221-1227.
[3] GAYATHRI S,CAREY M J,JOSEPH A K. Pyrrolysine encoded by UAG in Archaea: charging of a UAG-decoding specialized tRNA[J].SCIENCE,2002,296(5572):1459-1462.
[4] COMMANS S, BCK A. Selenocysteine inserting tRNAs: an overview[J]. FEMS MICROBIOL REV,1999,23(3):335-351.
[5] RACHEL S ,MILJAN S. Synthesis and decoding of selenocysteine and human health[J].CROAT MED J,2012,53(6):535-550.
[6] BCK A, FORCHHAMMER K, HEIDER J, et al. Selenocysteine: the 21st amino acid[J]. MOL MICROBIOL,1991,5(3):515-520.
[7] BING H, WEIMIN G, TSUNEO K F, et al. A new UAG-encoded residue in the structure of a methanogen methyltransferase[J].SCIENCE,2002,296(5572):1462-1466.
[8] 周春燕,药立波.生物化学与分子生物学[M].9版.北京:人民卫生出版社,2018.
[9] 刘新光,罗德生.生物化学与分子生物学[M].3版.北京:科学出版社,2021.
[10] 赵炜明,宋高臣.生物化学与分子生物学[M].1版.北京:人民卫生出版社,2020.
[11] 姚青,吕勇刚,王廷,等.甲状腺疾病的教与学——兼論教材纠错[J].西北医学教育,2012,20(2):419-421.

