1例儿童肝豆状核变性并发肝损害的药物治疗分析和药学监护
简璐,刘娉,纪刚剑,张文婷
(1.华中科技大学同济医学院附属同济医院药学部,武汉 430030;2.湖北省孝感市妇幼保健院药学部,孝感 432100;3.郑州大学附属郑州中心医院,郑州市中心医院药学部,郑州 450000;4.武汉市第三医院药学部,武汉 430060)
肝豆状核变性(hepatolenticular degeneration,HLD)也称Wilson病(Wilson's disease,WD),是因铜转运ATP酶β(ATP7B)基因突变,导致细胞铜转运障碍的常染色体隐性遗传病。WD分布于世界各地,据世界卫生组织(WHO)估计,WD的全球患病率为1/10 000~1/30 000[1],我国的患病率为1.96/10 000~5.87/10 000[2]。该病可在任何年龄发病,儿童、青少年多见[3]。男性和女性的患病率相当。由于大量铜蓄积于肝、脑、肾、骨关节、角膜等组织和脏器,患者出现肝脏损害、神经精神异常表现、肾脏损害、骨关节病及角膜色素环(K-F环)等。儿童WD的临床表现多以肝病为主[4]。笔者在本文分析1例并发肝损害的儿童WD病例的药物治疗,为临床药师参与儿童罕见病治疗提供参考。
1 病史摘要
1.1病例介绍 患儿,女,10岁。因“发现肝功能异常20个月余”入院。20个月前因“肝功能异常”于外院住院28 d,予以护肝后复查肝功能:丙氨酸氨基转移酶(ALT )108 U·L-1(↑),天冬氨酸氨基转移酶(AST) 80 U·L-1(↑),院外继续口服护肝药,2个月前复查肝功能:ALT 143 U·L-1(↑),AST 115 U·L-1(↑),1个月前复查肝功能:ALT 207 U·L-1(↑),AST 158 U·L-1(↑),总蛋白81.5 g·L-1(↑),间接胆红素13.0 μmol·L-1(↑),碱性磷酸酶(ALP)384 U·L-1(↑),γ-谷氨酰转肽酶48 U·L-1,总胆固醇5.87 mmol·L-1(↑),乳酸脱氡酶356 U·L-1(↑);肝脏彩超提示脂肪肝,第一肝门处多个淋巴结肿大。铜蓝蛋白0.074 g·L-1(↓),尿铜浓度0.363 μg·mL-1,24 h尿铜108.9 μg。颅脑CT平扫无异常。为求进一步诊治至同济医院门诊就诊。否认家族遗传代谢病史,否认食物、药物过敏史,否认乙型肝炎(乙肝)、结核病史,其母亲有乙肝病史。整个病程中无发热,无呕吐,无腹痛腹泻。
体格检查:体温36.5 ℃;脉搏88次·min-1;呼吸率21次·min-1;体质量38.8 kg。实验室及其他辅助检查:白细胞计数(WBC)6×109·L-1,中性粒细胞2.57×109·L-1,血小板计数298×109·L-1。ALT 108 U·L-1(↑),AST 71 U·L-1(↑),ALP 317 U·L-1(↑),白蛋白39.1 g·L-1。铜蓝蛋白0.085 g·L-1(↓),B型钠尿肽(BNP)80 pg·mL-1,肌酐34 μmol·L-1(↓),甲胎蛋白2.91 ng·mL-1,凝血酶原时间13.1 s。全外显子测序提示检查2个匹配受检者临床表型的致病性/可能致病性的基因变异,铜离子转运ATP酶β肽(ATP7B)(G 3982Ap.1328T,exon4-5del)复合杂合突变。入院诊断:肝豆状核变性。
1.2治疗过程 第1天完善相关辅助检查,给予异甘草酸镁、还原型谷胱甘肽护肝治疗。第3天患儿给予青霉胺驱铜治疗,葡萄糖酸锌减少铜吸收;维生素补充营养。第4天肝纤维化全套提示血清Ⅲ型前胶原肽(PⅢP测定)45.12(↑),血清Ⅳ型胶原测定43.06(↑);肝脏彩超提示肝稍大,加用促肝细胞生长素护肝治疗。第6天复查血常规,白细胞、中性粒细胞、血小板计数均在正常范围。第8天复查肝功能:ALT 73 U·L-1(↑),AST 47 U·L-1(↑),ALP 359 U·L-1(↑),复查尿铜浓度0.202 μg·mL-1,24 h尿铜121.2 μg。患儿病情好转出院。住院期间主要治疗药物见表1。
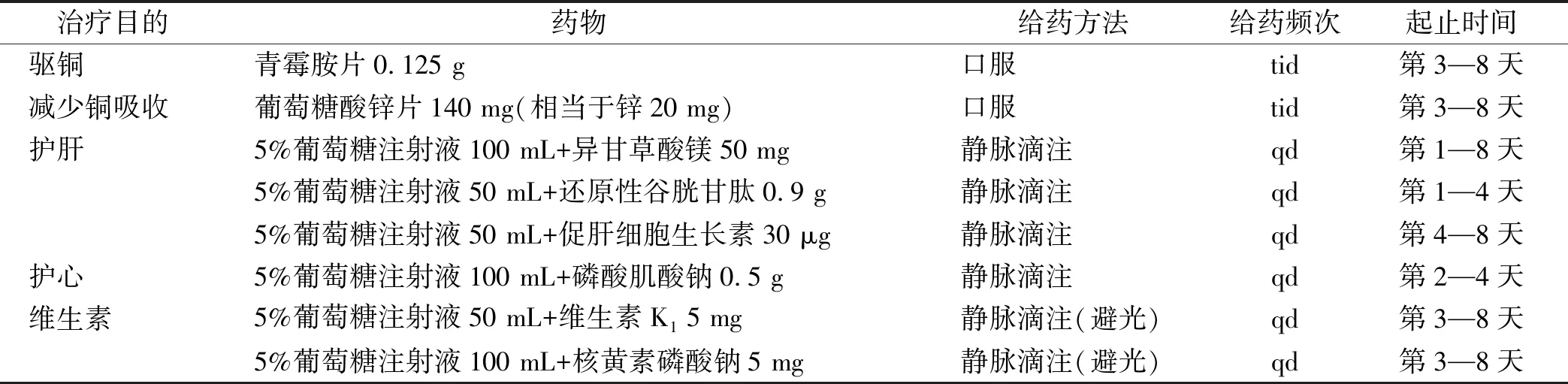
表1 住院期间主要治疗药物
出院诊断:肝豆状核变性(肝型)。出院带药:青霉胺片0.125 g,po,tid;葡萄糖酸锌片140 mg,po,tid;谷胱甘肽片200 mg,po,tid;多维元素(12)1片,po,tid。
2 药物治疗分析
2.1临床病例特点 该患儿入院前辅助检查:铜蓝蛋白0.074 g·L-1(↓),ALT 207 U·L-1(↑),AST 158 U·L-1(↑),尿铜浓度0.363 μg·mL-1,24 h尿铜108.9 μg,ATP7B(G 3982Ap.1328T,exon4-5del)复合杂合突变,WD诊断明确。WD的治疗分为初始治疗和维持期治疗。该患儿首次确诊,进行初始治疗。治疗药物分为两大类:一是通过使用强效螯合剂来达到清除铜的目的。主要使用的螯合剂为青霉胺,是首选标准疗法。其他螯合剂包括二巯丙磺酸钠、二巯丁二酸、曲恩汀等,可用于治疗青霉胺过敏、不耐受或神经精神症状者。二是减少铜吸收的药物,包括锌制剂、四硫代钼酸铵[1]。
根据轻重程度和病程的长短,累及肝脏的WD临床可表现为无症状、急性肝病、肝衰竭、慢性肝病、肝硬化等多种形式[5-6]。指南指出有急性或慢性肝病、肝硬化代偿期者采取三种药物联合使用:青霉胺、二巯丙磺酸钠或二巯丁二酸胶囊;锌制剂以及护肝治疗[7]。该患儿检查提示,肝稍大、脂肪肝、肝纤维化全套血清Ⅲ型前胶原肽、血清Ⅳ型胶原测定数值有升高,提示该患儿肝脏有损害。临床采用青霉胺+葡萄糖酸锌+护肝治疗的联合治疗方案。
2.2WD治疗药物选择和用法用量 青霉胺是世界上第一个口服治疗WD的药物,是一种带有巯基的强效金属络合剂,可以络合细胞内的铜,使之进入血循环,随尿液排出体外,从而减少铜在体内多个脏器的沉积,减轻对脏器的损害,目前仍是治疗WD的一线药物[6]。但严重神经症状的患者谨慎使用青霉胺,因这类患者在使用青霉胺治疗早期会出现神经症状加重[8]。该患儿住院期间无神经精神症状,首选青霉胺符合治疗推荐。儿童应从小剂量(150~300 mg·d-1)开始增加患者的耐受性,初步增加至20 mg·kg-1·d-1,分2或3次口服。维持剂量为10~20 mg·kg-1·d-1,最大剂量为750~1000 mg·d-1,分2次口服[9]。该患儿从入院至出院带药剂量一直维持在10 mg·kg-1·d-1,每日3次,即375 mg·d-1,初始剂量较大,采用最低维持剂量。药师建议调整青霉胺的剂量:第1周每次半片(即0.062 5 g),每日3次;第2周每次1片,每日3次;第3周每次2片,每日3次。此方法从小剂量加用,可使患儿建立青霉胺的耐受性,也能使患儿达到青霉胺的初始治疗剂量。肝功能好转后改用青霉胺每次1片,每日3次维持治疗。临床医生考虑治疗方便性,选择继续观察再做调整。按照当前治疗患儿未出现不耐受现象。
锌制剂可清除体内储存的铜,还可以诱导肝细胞产生金属硫蛋白,减轻铜的毒性[6]。目前,临床常用锌制剂主要为硫酸锌、醋酸锌、葡萄糖酸锌、甘草锌等。胃肠道刺激是该类制剂主要不良反应。由于硫酸锌胃肠道刺激较明显,故在WD的治疗中常用葡萄糖酸锌或醋酸锌。该患儿10岁,体质量<50 kg,锌剂治疗剂量推荐用量为50~75 mg·d-1(即葡萄糖酸锌350~525 mg·d-1),分3次服用[9]。该患儿每日服用葡萄糖酸锌420 mg(锌含量60 mg),符合推荐日剂量。
2.3护肝药物的选择和磷酸肌酸钠的使用指征 WD的一个重要临床表现为肝细胞损伤。该患儿发现肝功能异常20个月余,ALT、AST持续升高,肝纤维化全套部分指标异常,肝脏彩超显示肝稍大,碱性磷酸酶轻度升高,既往有脂肪肝,第一肝门处多个淋巴结肿大。该患儿使用三联护肝药物治疗,分别为异甘草酸镁、还原型谷胱甘肽和促肝细胞生长素。
异甘草酸镁为肝细胞保护药,具有抗炎、保护肝细胞及改善肝功能的作用,主要用于药物病毒性肝炎、急性药物性肝损伤。该药是在病因基础上的辅助用药,只要存在肝脏炎症表现(即ALT/AST异常)即可应用[10]。该患儿ALT、AST持续升高,使用该药合理。还原型谷胱甘肽是含有巯基(SH)的三肽,主要存在于细胞质中,参与体内三羧酸循环及糖代谢。它能激活体内SH酶等,促进碳水化合物、脂肪及蛋白质的代谢。还可通过巯基与体内的自由基结合,促进易代谢的低毒化合物的形成,因此对部分外源性毒性物质具有减毒作用。促肝细胞生长素是从新鲜乳猪肝脏中提取纯化制成的小分子多肽类活性物质,刺激新生肝细胞的DNA合成,促进肝细胞再生,加速肝脏组织的修复,恢复肝功能,可用于各种重型病毒性肝炎(急性、亚急性、慢性重症肝炎的早期或中期)的辅助治疗。
同时使用的抗炎保肝药物种类不宜过多,通常选用1或2种抗炎保肝药物,一般不超过3种,以免增加肝脏负担;且通常不推荐选用主要成分相同或相似的药物联用[11]。该WD患儿肝脏症状相对较轻,同时使用3种护肝药数量过多,可能会增加肝脏负担,建议减少1种护肝药。又因为该患儿已经使用青霉胺用于清除组织内沉积的铜,与铜结合减轻铜的肝毒性,所以建议在监测肝功能下,可停用肝脏解毒药还原性谷胱甘肽。临床采纳建议。
该患儿BNP、肌酸激酶、乳酸脱氢酶等心肌损害标志物均正常,心电图与心脏彩超未见明显异常,也无胸痛、胸闷、心悸、气促等临床表现,且WD未见报道心脏方面的并发症。所以该病例无磷酸肌酸钠使用指征,建议停用。临床采纳建议。
2.4维生素与微量元素的选择和用法用量 虽然低铜饮食有利于WD患者的治疗,但是此种饮食也会给患者带来困扰。因为日常饮食中的食物大多富含铜元素,剔除这些食物后可供WD患者选择的食物就十分受限,且易导致营养不良或营养失衡[12],所以适量的补充维生素与微量元素有利于WD患者的营养健康。儿童尤其建议适量补充钙剂,因为青霉胺和锌制剂会增加尿钙的排出和影响肠道内钙吸收[13]。多种微量元素(12)中含有包括维生素B6与钙在内的12种儿童生长所需维生素与矿物质。该患儿用量为每日3次,每次1片。超过说明书推荐3~12岁儿童每日1片的用量,建议改为每日1片标准用量。此外,青霉胺可能会影响体内维生素B6的代谢,治疗期间建议加用维生素B610~50 mg·d-1[6-7,14]。多种微量元素(12)中每片含维生素B62 mg,尚低于每日所需补充维生素B6的最低推荐剂量,建议可加用维生素B6片,每日1片(每片含维生素B610 mg)。临床采纳建议。
3 药学监护
3.1疗效监护 该患儿以肝病为主要表现,治疗2~6个月后肝功能常明显好转,完全缓解可能需1年以上[15]。治疗期间定期观察患者的症状、体征,血常规、尿常规、肝肾功能、24 h尿铜变化。①24 h尿铜:初始治疗时常通过每2~4周测24 h尿铜来调整青霉胺剂量。在初始治疗的1个月内,24 h尿铜常可以达峰值[1500~8000 μg·(24 h)-1]。随着储存的铜不断消耗,尿铜排泄的速度下降,6个月到1年可以达到维持期所追求的尿铜水平[200~500 μg·(24 h)-1][16-17]。葡萄糖酸锌维持治疗期应追求尿铜<75 μg·(24 h)-1。该患儿治疗1周,尿铜从108.9 μg·(24 h)-1增至121.2 μg·(24 h)-1,铜排泄量仅有小幅度增加,后续应持续监测24 h尿铜排泄量,观察其能否达到峰值,若1个月后仍不能达到24 h尿铜峰值,可能是青霉胺药效衰减或患者体内铜含量较低,可以增加青霉胺剂量,若24 h尿铜仍然没有增高,提示患者体内铜较低,直接改为青霉胺维持剂量。②血清锌和尿锌:该患儿使用锌制剂,建议监测24 h尿锌和血清锌。血清锌水平和尿锌排泄量应分别维持在1250 μg·L-1和1.5~2 g·d-1以上,较低的水平通常表明患者依从性较差[9]。③肝脏彩超:出院时复查肝功能有明显好转,建议今后每半年查一次肝脏彩超。④K-F环:每年评估一次。
3.2安全性监护 青霉胺:①可能引起过敏,青霉素皮试阴性才可以使用。②可引起多种副作用,可导致约5%患者停止治疗。若患者出现发热、皮疹、淋巴结肿大、关节疼痛、中性粒细胞减少(<2×109·L-1)、血小板减少(<120×109·L-1)等,或者尽管血细胞数值仍高于以上值,但观察到连续3次测量结果呈稳定下降时,应当停止用药。轻者可使用抗过敏治疗,如口服小剂量泼尼松(0.5 mg·kg-1·d-1,持续2~3 d),待症状缓解后再次从小剂量使用青霉胺,逐渐加量,同时激素逐渐减量直至停药[6]。还应该观察患者是否出现神经系统恶化以及肝肾功能的毒性的发生(是否有蛋白尿、血尿的表现)。若不能耐受青霉胺治疗,可考虑静脉滴注二巯丙磺酸钠或口服二巯丁二酸胶囊。二巯丁二酸驱铜作用较青霉胺弱,但有脂溶性可以进入血脑屏障,有助于改善神经精神症状。二巯丙磺酸钠驱铜作用是青霉胺的2.6倍。该患儿住院期间使用青霉胺未出现过敏反应,也没有精神症状的发生,治疗一周复查尿蛋白为阴性,交代家长出院后应该持续观察。
葡萄糖酸锌:不良反应少。若是出现胃肠道的不良反应(轻度恶心、呕吐、便秘)考虑换用另一种锌制剂醋酸锌。
异甘草酸镁可能会出现假性醛固酮症,应注意监测血钾,若血钾过低(表现乏力、肌力低下等),应停药。
3.3经济性监护 WD患者需要终身用药,药物是否经济显得格外重要。曲恩汀价格昂贵,国内未见销售,不推荐使用。青霉胺与葡萄糖酸锌片疗效肯定、价格相对较低、患者易购买,在我国仍然是治疗WD的主要药物。
3.4依从性监护 WD患者一经确诊需要终身服药,且需要每天多次服药,依从性常常较差,尤其对于儿童。为了提高终身治疗的依从性,治疗方案应尽量简单[9]。一项关于WD患者接受药物治疗的170例回顾性研究结果显示,仅74.1%患者在平均随访11.7年间坚持药物治疗[18]。可通过定期测定24 h尿铜与尿锌排泄确定是否存在依从性问题并进行干预。
3.5用药指导与健康教育
3.5.1用药指导 食物影响青霉胺和锌的吸收,应在餐前1 h或餐后2 h服用最佳[6-7]。建议每日餐前1 h服用青霉胺,餐后2 h服葡萄糖酸锌。这样既能避免食物对这2种药物吸收的影响,又能避免螯合剂中和锌剂,还能减轻锌剂使用所带来的胃肠道副作用。青霉胺即使暂停数日,再次用药亦可出现变态反应,需重新做青霉素皮试,皮试阴性才可以使用,且应该从小剂量开始使用,避免造成严重的不良反应。维生素K1与核黄素在静脉滴注时应注意避光。不要用牛奶送服药物。用药期间接种疫苗可能导致疫苗效果降低,还可能增加疫苗引起感染的风险,故应避免疫苗接种。
3.5.2低铜饮食 治疗初始阶段,禁止食用富含铜的食物,尽量少食含铜量较高的食物。建议食用含铜量较低的食物、高氨基酸或高蛋白饮食。不可食用过多可能影响锌的吸收的富含粗纤维及植物酸的食物。勿用铜制的食具及用具。检测天然饮用水的铜含量,或使用合适的过滤器除去微量元素,家中使用铜质水管的患者,在用水烹饪或饮用前放水冲洗管道系统。
3.5.3心理疏导 WD是一种遗传病,患者往往伴有情绪低落、心情紧张、焦虑并对治疗缺乏信心,且该患儿即将进入青春期,往往还要面临学业的压力[19]。药师更应该对患儿进行心理疏导,使患儿和家属了解该病是可治愈疾病,提升患者和家属治疗的信心,提高患者与家属的用药依从性。
4 结束语
WD的治疗原则是尽早治疗、个体化治疗、终身治疗、终身监测。同时还应维持低铜饮食,避免摄入含铜量高的食物。在治疗过程中应注意监测症状、体征及相应的实验室指标。患者的精神、神经系统异常及肝脏异常会随治疗逐渐改善,肝脏生化检查结果通常可恢复正常。除了有晚期疾病的患者和出现快速进展性肝衰竭和溶血的患者以外,其他WD患者的预后均非常好。包括WD在内的罕见病大多需要终身治疗且通常合并多种并发症,为保证药物治疗效果,提高用药安全性,临床药师参与的多学科治疗十分必要。

