不同钙离子浓度下铜对磺胺嘧啶在土壤中的吸附/解吸特征*
吕十全 胡树翔 荣方旭 高心雨 巢 亮 刘爱菊#
(1.山东理工大学农业工程与食品科学学院,山东 淄博 255091;2.山东理工大学资源与环境工程学院,山东 淄博 255091)
磺胺类抗生素是最常用的抗生素之一,其在养殖业的使用量仅次于四环素类抗生素。由于磺胺类抗生素的化学性质,绝大部分会以代谢产物或者动物排泄物的形式排出体外,以不同的方式进入土壤环境[1],这些污染物可能通过作物或地下水进入食物链,危害生态和人类健康。近年来,国内外诸多学者对这些新兴污染物在土壤环境中的残留问题进行了研究[2-5]。
Cu、Zn等微量元素作为生长调节剂也在畜禽养殖业中有着广泛应用,是导致土壤重金属、抗生素复合污染问题的重要原因之一。土壤重金属、抗生素复合污染问题引起国内外环境学者的广泛关注。研究结果表明,许多具有多个可电离功能团的磺胺嘧啶(SDZ)可与Cu2+发生络合,并重点研究了络合作用对其吸附的促进作用[6]773。也有研究表明,Cu2+的存在显著增加了磺胺类抗生素的吸附,形成三元磺胺类抗生素-Cu-土壤配合物,从而加速了土壤对抗生素的吸附作用[7-8]。此外,LIU等[6]776研究表明,土壤的基本特征主要影响磺胺类抗生素在土壤中的吸附和转运行为,在pH<5.0时,由于静电竞争,抑制了对泥炭和土壤的吸附;而在pH>5.0时,由于磺胺类抗生素-Cu-土壤复合物或Cu桥的形成,增加了抗生素的吸附。ZHANG等[9]对农用土壤中的磺胺类药物的吸附量和解吸特性进行了研究,结果表明土壤中溶解性有机物对土壤的影响很大。由于土壤成分和特性的复杂性,导致了多种因素对抗生素的吸附和迁移产生了一定的影响。此外,还发现土壤pH、有机质以及共存阳离子对土壤中抗生素的吸收和迁移具有一定的作用[10-11]。且有学者提出,作为主要土壤交换性阳离子,Ca2+不但可以大量存在于土壤中,而且可以与其他抗生素如土霉素结合,形成新的复合物,从而影响土壤的吸附性能[12]553。Ca2+与Cu2+作为同价离子,且二者均具有与抗生素化合物络合配位能力,因而土壤溶液中Ca2+势必会影响Cu2+与SDZ之间的相互作用机制,进而影响SDZ在土壤中的吸附和迁移行为。
本试验研究了不同Ca2+浓度的土壤背景溶液中,Cu2+共存对SDZ在土壤中的吸附/解吸特征,并结合吉布斯自由能变化量(ΔG),运用傅里叶红外光谱(FTIR)分析揭示了SDZ在土壤中的吸附机制,为土壤中抗生素及重金属综合污染特性的评价提供理论基础。
1 材料与方法
1.1 试验材料与试剂
SDZ,分析纯;甲醇,色谱纯;其他试剂均为分析纯,试验用水均为超纯水。样品取自山东淄博张店区的农田土壤(0~20 cm),经风干、研磨,并过2 mm筛后备用。选用土壤的pH为7.5,有机质为12.5 mg/g,阳离子交换量为20.4 cmol/kg,电导率为111 μS/cm,土壤质地为壤土,Cu为24.12 mg/kg,Zn为81.5 mg/kg,测定方法参照文献[13]。
以超纯水为基础,配制0.01、0.05、0.10 mol/L氯化钙溶液作为土壤背景溶液;以甲醇为原料,制备100 mg/L的SDZ贮备液;用CuCl2·2H2O配制Cu2+为1 000 mg/L的氯化铜贮备液。
1.2 等温吸附/解吸试验
本试验参考 OECD guideline 106批次平衡法[14],精确称取1.000 g土壤于50 mL聚丙烯塑料离心管中,按照水土比20 mL∶1 g,分别在0.01、0.05、0.10 mol/L的氯化钙背景溶液的基础上,加入适量的SDZ贮备液,使土壤悬浊液中SDZ的初始质量浓度梯度为0.5、1.0、2.0、4.0、6.0、8.0、10.0 mg/L。在25 ℃、250 r/min下振荡48 h(经动力学预试验证明,48 h已达到吸附平衡),振荡结束后,在4 000 r/min的离心机中进行5 min的离心,过0.45 μm滤膜后取1.5 mL的上清液,再用高效液相色谱-紫外法(HPLC-UV)检测SDZ的浓度。每一次试验处理重复3次。解吸过程是将上述反应48 h后的土壤试样进行分离,然后将上清液倒出,再加入一定浓度的氯化钙溶液,在25 ℃、250 r/min下,置于振荡器上振荡48 h,将试样在4 000 r/min下离心5 min,用0.45 μm滤膜将上清液过滤,然后取1.5 mL的试样进行检测。
在Cu2+与SDZ共存的吸附试验中,添加一定量的氯化铜储备液,使土壤悬浊液中Cu2+的质量浓度分别为200、500 mg/L,其他条件及吸附过程同上述试验方法。解吸过程是选取上述反应48 h后的土壤样品,超纯水洗涤3次后离心分离,添加与吸附试验相同Cu2+浓度的氯化钙溶液,在25 ℃、250 r/min下振荡48 h,然后离心、过滤、测定溶液中抗生素浓度,每个试验重复处理3次。
1.3 FTIR分析
将土壤悬浮液中SDZ的质量浓度增加到100.0 mg/L,吸附振荡试验同上,达到平衡后进行离心,取离心获得土壤固相组分进行干燥处理。按照FTIR分析的样品预处理要求,将适量干燥后的土壤样品与溴化钾混合研磨后,采用傅里叶变换红外光谱仪(Nicolet5700,Thermo,美国),以空白土壤作为对照,在1 000~4 000 cm-1的扫描范围内,扫描16次,分辨率为4 cm-1。
1.4 数据计算和处理
SDZ吸附量计算见式(1):
Y=V(C0-Ce)/M
(1)
式中:Y为SDZ的吸附量,mg/kg;V为土壤溶液的体积,L;C0和Ce分别为溶液中平衡吸附试验开始和平衡时SDZ的质量浓度,mg/L;M为背景溶液中加入的土壤称重量,kg。
采用Langmuir模型方程[15]对SDZ的吸附过程进行拟合,方程见式(2):
qt=KdQmCe/(1+KdCe)
(2)
式中:qt为时间t时SDZ在土壤中的吸附量,mg/kg;Kd为Langmuir吸附特征常数,L/mg;Qm为土壤对SDZ的饱和吸附容量,mg/kg。
采用Freundlich模型方程[16]对SDZ的吸附过程进行拟合,方程见式(3):
(3)
式中:KF为Freundlich吸附特征常数,mg1-n·Ln/kg;n为非线性系数。
ΔG的计算[17]见式(4):
ΔG=-RTlnKOM
(4)
式中:R为气体常量,8.314 J/(mol·K) ;T为热力学温度,本研究取298 K;KOM为有机质吸附常数。
KOM计算见式(5):
KOM=(KF/WOM)×100%
(5)
式中:WOM是测定土壤有机质质量浓度,mg/kg。
滞后系数(HI)计算见式(6):
HI=nD/nS
(6)
式中:nD为解吸反应的Freundlich拟合参数;nS为吸附反应的Freundlich拟合参数。
用 Origin 9.0、Excel 2010完成数据的分析与绘图。
2 结果与讨论
2.1 不同二元组合下SDZ的等温吸附/解吸
土壤中的离子浓度对土壤吸附SDZ有很大的影响[18]。现有的研究结果显示,阳离子可以与SDZ竞争吸附位点,或形成具有较高亲水性的配合物,从而抑制对SDZ的吸附,或者通过与SDZ的配合,使其更容易被吸收[19-20]。图1(a)、(b)、(c)显示了Cu2+共存条件下在不同Ca2+强度下对土壤吸附SDZ的影响。结果表明,在0.01 mol/L Ca2+背景溶液中,Cu2+的加入显著促进了土壤对SDZ的吸附。分析其原因,Cu2+可以起到土壤和抗生素的“桥”作用,从而提高土壤对抗生素的吸附能力[21-23],也就是说,抗生素可以在Cu2+的位点上吸附,随着累积的吸附作用会促进土壤对抗生素的吸附能力[24]。此外,Cu2+的添加使土壤铁、铝氧化物表面氧原子发生极化,从而使H+被释放,然后使土壤pH下降,进而降低了土壤对SDZ的排斥力,加速土壤对SDZ的吸附[25]。但是Ca2+浓度的提高会减弱Cu2+对SDZ的吸附能力,其原因可能与静电竞争吸附效应有关,与SDZ相比,Ca2+带正电荷易与带负电的土壤结合,并在较高的活性位置上占有较多的吸附位点,从而降低了土壤对 SDZ的吸附[26]。
不同Ca2+浓度下Cu2+共存对SDZ土壤解吸的影响见图1(d)、(e)、(f)。在所有试验处理中,土壤对SDZ的解吸量随SDZ浓度的增加而增加。究其原因,与SDZ在土壤颗粒上的吸附机制及相应位点类型有关。即当SDZ浓度较低时,土壤对SDZ的吸附主要以专性吸附为主,SDZ具有高能的结合位点,其他离子难以取代;当土壤饱和后,其专性吸附位点数下降,且以非专性吸附为主,且对SDZ的吸附能力下降,SDZ在土壤中的稳定性下降,从而容易解吸,解吸量也相应提高[27]。而Cu2+的加入促进了土壤SDZ的解吸,且Cu2+浓度的增加,更显著地促进了SDZ的解吸。原因可能是Cu2+的静电吸附导致土壤活性吸附位点减少,进而使SDZ解吸下来[28]。由此可知,对于土壤中吸附的SDZ,Cu2+的介入可促进抗生素SDZ从土壤中解吸,增加其在土壤的迁移扩散的风险。但是,土壤溶液中Ca2+浓度的增加则抑制了SDZ土壤解吸过程,分析其原因,低离子强度下SDZ在土壤中的吸附量较高,一部分SDZ占据低能位点,导致其更容易从土壤中脱附,而高离子强度下SDZ的吸附量较低,SDZ占据大量高能位点,不易被解吸下来[29]。
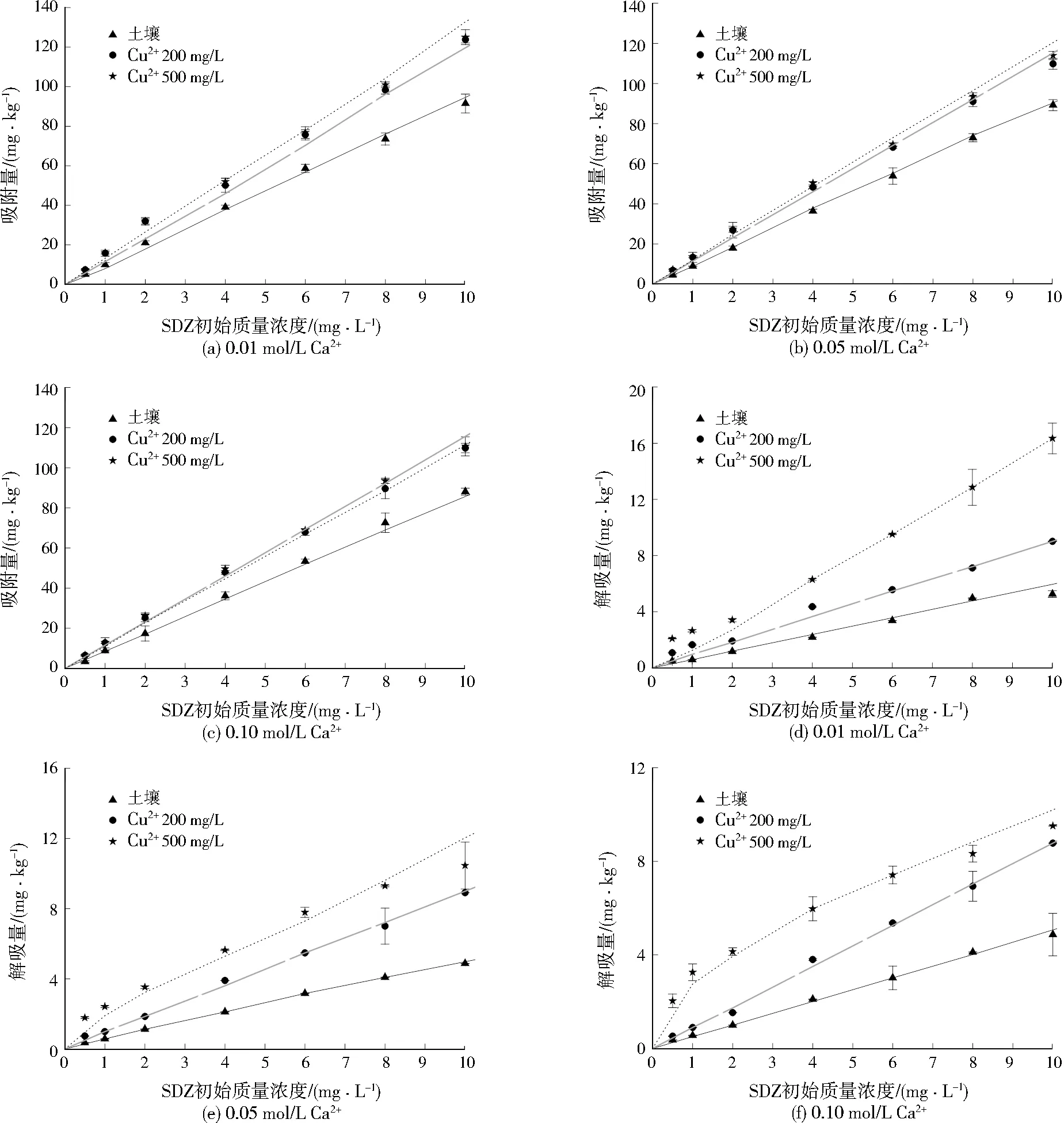
图1 不同二元组合下SDZ的吸附/解吸等温线Fig.1 Adsorption/desorption isotherms of SDZ in different binary combinations
2.2 不同二元组合下SDZ的等温吸附/解吸拟合结果
在不同情况下,两种拟合模型对土壤吸附SDZ的拟合均较好。Freundlich模型和Langmuir模型拟合相关系数(R2)分别>0.95、>0.90,相比之下,Freundlich等温吸附模型拟合效果更好(见表1)。说明两种拟合模型在有无Cu2+存在条件下,都可以很好地描述SDZ在土壤中的吸附,而且这种吸附是由多个分子层的非均匀吸附引起的。此外,n在0.80~0.97,接近于1,表明SDZ在土壤中的吸附接近线性,且其对表面吸附位点的占领是逐步进行的;由n可知,等温吸附线为“L型”,此类型的等温线受溶液中溶质和水分子不同作用的影响[30]4264。Freundlich模型拟合中,KF越大代表土壤对抗生素的吸附能力越强。0.01 mol/L Ca2+条件下,Cu2+为500 mg/L时土壤对SDZ的KF最大;0.10 mol/L Ca2+条件下,无Cu2+添加的试验处理土壤对SDZ的KF最小,这与吸附试验的结果是一致的。而Langmuir模型的Kd的变化趋势与Freundlich模型拟合结果基本一致。进一步证实Cu2+的存在有利于提高土壤对SDZ的固持能力,而Ca2+对SDZ的吸附有明显的抑制作用。
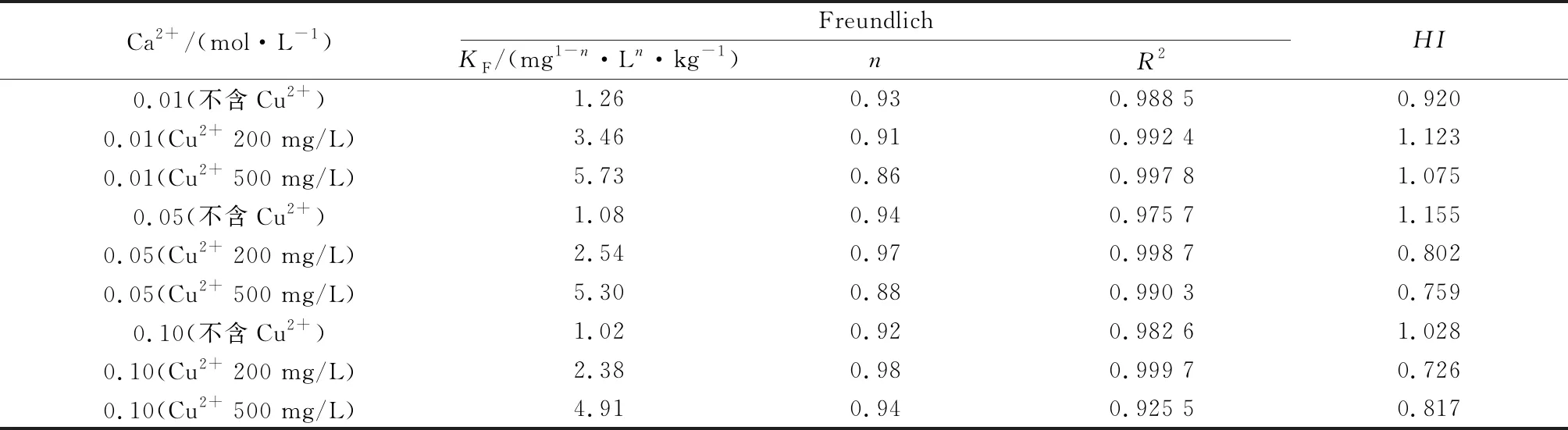
利用 Freundlich模型拟合解吸所得的数据,结果如表2所示。首先,与等温吸附拟合的结果相似,Freundlich模型拟合所得R2较高(>0.92),说明在有无Cu2+存在条件下,该模型均可以很好地描述SDZ在土壤中的解吸特征。所以解吸过程受Cu2+的影响较小。此外,KF随着Ca2+浓度的增加逐渐变小,进一步说明Ca2+的存在抑制了SDZ在土壤的解吸过程。其次,HI可以反映 SDZ与土壤之间的化学键合力的不可逆性[31]。通常,HI=1代表没有滞后现象;在HI<1时为正滞后;当HI>1时为负滞后。当0.7 表1 不同二元组合下SDZ的吸附等温线拟合参数和ΔGTable 1 The adsorption isotherm fitting parameters and ΔG for SDZ in different binary combinations 表2 不同二元组合下SDZ的解吸等温线拟合参数Table 2 The desorption isotherm fitting parameters for SDZ in different binary combinations 从ΔG和FTIR分析的角度,揭示Ca2+和Cu2+共存条件下,土壤对SDZ的吸附机制。吸附质的ΔG是一个很好的指标,可以根据它的变化来推测吸附特性[12]554。|ΔG|<40 kJ/mol,为物理吸附;|ΔG|>40 kJ/mol,为化学吸附。由表1可知,不同Ca2+浓度下,Cu2+共存时SDZ在土壤上吸附的ΔG在-20.051~-17.468 kJ/mol。其中,ΔG<0 kJ/mol,说明土壤对SDZ的吸附属于自发的过程[33-34]。由各试验处理的ΔG变化范围可知,当Cu2+存在时,Ca2+的浓度对SDZ的吸附作用几乎可以忽略不计;同时,所有处理的|ΔG|均小于40 kJ/mol,所以土壤对SDZ的吸附主要是物理吸附。 由不同的作用力吸附热的范围不同(氢键2~40 kJ/mol,范德华力4~10 kJ/mol,离子交换40 kJ/mol,疏水键力5 kJ/mol,偶极力2~29 kJ/mol)可以推断出不同Ca2+浓度下,Cu2+共存时土壤对SDZ的吸附可能存在氢键和偶极键力,进一步说明其吸附机制主要为物理吸附[35]。 FTIR图谱如图2所示。在3 400~3 500 cm-1的条件下,没有吸附SDZ的土壤中,存在分子间氢氧键(—O—H)可伸缩吸收峰,并且在1 600 cm-1附近形成了羧基结构的(—C=O)吸收峰。吸附SDZ的土壤也形成了类似的吸收峰。结果表明,与没有吸附SDZ的土壤相比,土壤在低离子强度下吸附SDZ后,1 600 cm-1附近的羰基结构(—C=O)的吸收峰发生了迁移,从1 645.87 cm-1迁移至1 641.58 cm-1,这种迁移属于红移。与其他处理相比,在SDZ-Cu共吸附处的红移幅度显著增大,说明羰基参与SDZ的吸附。认为 SDZ中羰基、羧基能与金属离子形成络合物,并能在土壤中吸附。同时,1 600 cm-1附近的收缩振动可能是由于氢键作用所致,或者SDZ存在某些中性分子,其苯环结构与苯环、羧基结合,并与π-π共轭结合,由此形成吸附[30]4265;表明土壤对SDZ的吸附可以是氢键作用,也可以是π-π共轭键的结合[36-37]。在3 300~3 500 cm-1时,由于SDZ中—NH键的氢与土壤中的氧原子形成氢键[38],从而使吸收峰从3 413.53 cm-1迁移至3 421.69 cm-1,这种迁移属于蓝移[39]。 图2 不同二元组合下吸附SDZ前后的FTIR图谱Fig.2 FTIR patterns before and after adsorption of SDZ in different binary combinations 与SDZ单一吸附处理相比,土壤在0.01 mol/L Ca2+下吸附SDZ、Cu2+(500 mg/L)时,在1 600 cm-1附近出现红移,在3 400~3 500 cm-1时出现了蓝移。而当土壤在0.05 mol/L Ca2+下吸附SDZ、Cu2+(500 mg/L)时,在1 600 cm-1附近、3 400~3 500 cm-1处吸收峰发生偏移,与0.01 mol/L Ca2+下的吸附特性类似,但偏移程度比较小,这可能是由于离子竞争削弱了Cu2+存在下土壤对SDZ吸附的促进效应。 根据ΔG计算结果和FTIR分析表明,物理吸附是土壤对SDZ的主要吸附方式,伴随着氢键效应和络合作用;Cu2+在土壤存在时,可以通过络合作用形成Cu2+桥,从而加速土壤对SDZ的吸附。 (1) Cu2+共存时通过吸附形成配合物来减少土壤对SDZ的排斥,或通过桥键的方式提高土壤对SDZ的吸附能力。Ca2+与Cu2+的离子竞争,抑制了Cu2+对SDZ在土壤上吸附的促进作用;不同Ca2+浓度下,Cu2+共存时土壤中SDZ的解吸量随着Cu2+浓度的升高而增加,这取决于SDZ在土壤中的吸附机制及位点类型。 (2) Freundlich模型比Langmuir模型能更准确地拟合不同Ca2+浓度下Cu2+共存时土壤对SDZ的吸附过程,这说明该吸附是一种多分子层的非均匀吸附。HI分析表明,不同Ca2+浓度下Cu2+共存时SDZ在土壤上的解吸过程均无明显滞后现象。 (3) ΔG结果显示,土壤对SDZ的吸附主要以物理吸附为主;FTIR分析表明,不同Ca2+浓度下,Cu2+共存时SDZ在土壤中的吸附伴随着氢键效应和络合作用。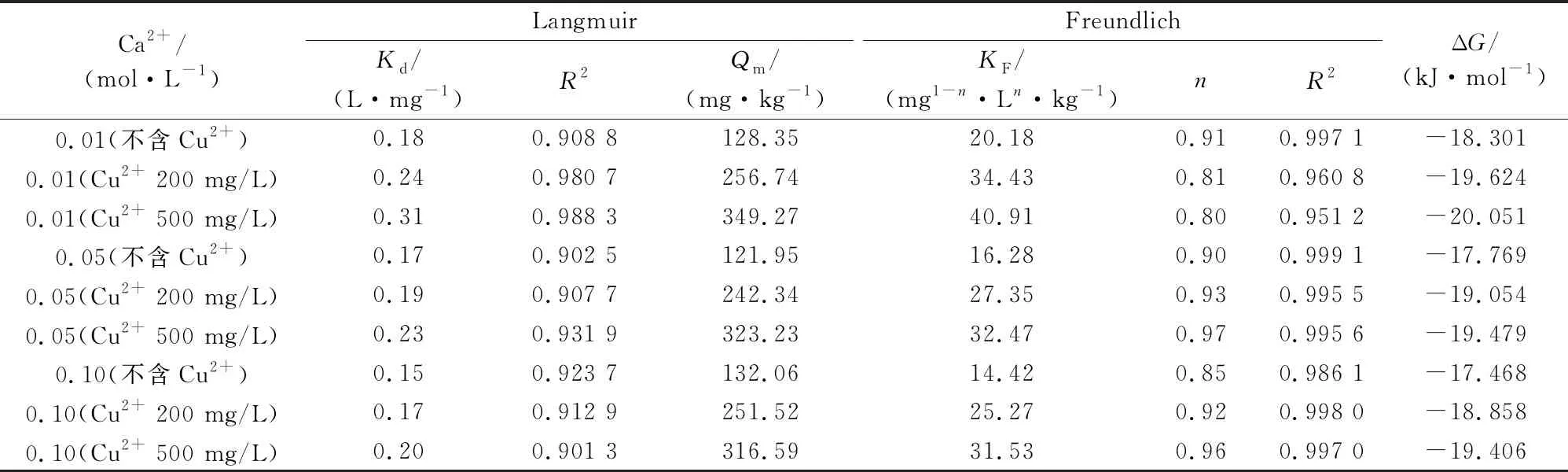
2.3 SDZ在土壤中的吸附机制
3 结 论

