小样本应用贝利尤单抗治疗儿童系统性红斑狼疮的临床疗效观察
王倩涵, 苗永红, 安乐美
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种产生自身抗体、临床表现多样、多脏器受累为特征由免疫介导的多系统疾病[1]。与成人发病的SLE相比,儿童发病更容易出现严重的肾脏、中枢神经系统受累,同时疾病活动高,有更高的激素剂量负担[2]。虽然SLE发病机制不明,但目前认为患者体内B细胞异常激活,使自身抗原反应处于高度活化状态是关键环节,造成机体产生大量自身抗体,从而引发炎症反应[3]。贝利尤单抗是一种能够与B淋巴细胞刺激因子结合的人源化单克隆抗体[4]。贝利尤单抗在儿童SLE治疗中能有效改善疾病的症状,减少疾病的复发率,减少糖皮质激素的剂量[5]。本研究通过回顾性、真实世界临床研究,探讨贝利尤单抗治疗儿童SLE的疗效和安全性,从而为儿童SLE应用贝利尤单抗提供有效的临床借鉴价值。
1 对象与方法
1.1 研究对象 选取2021年1月至2022年8月在河南省人民医院明确诊断的儿童SLE 11例。
1.2 诊断标准 参照SLE国际合作临床组织的分类标准[6]。
1.3 纳入标准 (1)所选病例均接受3个月以上正规SLE治疗,但仍有狼疮活动,大不列颠群岛狼疮评估组(British Isles lupus assessment group,BILAG-2004)指数中新发BILAG A或BILAG B≥1。(2)本研究通过河南省人民医院医学伦理委员会批准(2019伦审第15号),患儿监护人对所做研究均知情同意,并签署知情同意书。
1.4 排除标准 (1)活动性中枢神经系统SLE,患儿在贝利尤单抗基线治疗前60 d内有急性治疗者;(2)严重狼疮肾病或活动性肾炎,患者在贝利尤单抗基线治疗前90 d内有急性治疗者;(3)贝利尤单抗基线治疗时泼尼松剂量≥1.5 mg/(kg·d);(4)既往应用过其他生物制剂者。
1.5 治疗方法 研究对象的基础治疗制定个体化的治疗方案,根据疾病的活动度和受累器官的种类和严重程度进行治疗,包括糖皮质激素联合免疫抑制剂(环磷酰胺、吗替麦考酚酯、环孢素、他克莫司)和抗疟药[7]。贝利尤单抗静脉注射剂量每次10 mg/kg,前3次每2周1次,之后每4周1次。用药前均排除严重感染。
1.6 疗效评估 通过回顾性、真实世界临床研究,比较研究对象治疗前、治疗2周、4周、8周、12周、16周的临床特征,监测血常规、补体C3及C4、抗ds-DNA定量、抗C1q抗体、B淋巴细胞数量、肌酐、24 h尿蛋白定量、尿红细胞变化;观察不同阶段口服激素剂量。疾病活动指数评分采用SLE活动指数(systemic lupus erythematosus disease activity index,SLEDAI-2000)评分[8]、BILAG-2004指数[9]、医师整体评估(physician′s global assessment,PGA)评分[10];16周时监测SLE应答者指数(systemic lupus erythematosus responder index,SRI-4),是否满足以下条件:(1)SLEDAI评分减少≥4分;(2)无新发BILAG A和新发BILAG B≤1个;(3)PGA与基线相比无恶化(增加<0.3分/3分)无临床复发病例[11]。
1.7 安全性评估 评估贝利尤单抗使用后药物不良反应。

2 结果
2.1 临床特征 11例儿童SLE中,男1例,女10例;发病年龄(13.91±1.70)岁;体质量(56.73±10.53)kg;应用贝利尤单抗治疗时中位病程为(8.91±10.41)个月;神经系统受累为主的患儿2例,在贝利尤单抗基线治疗前60 d内没有急性治疗,其中1例合并血栓性血小板减少症。狼疮性肾炎患儿4例,在贝利尤单抗基线治疗前90 d内没有急性治疗,其中1例合并双眼青光眼。基线时全部病例均应用羟氯喹(100%),均应用泼尼松(100%),≤20 mg/d 1例(9.09%),>20~40 mg/d 4例(36.36%),>40 mg/d 6例(54.55%),口服激素剂量(44.32±12.25)mg。6例(54.55%)应用吗替麦考酚酯,2例(18.18%)应用环孢素,2例(18.18%)应用环磷酰胺,2例(18.18%)应用他克莫司。SLEDAI评分为12.00(11.00,15.00),其中≤14分7例(63.64%),≥15分4例(36.36%)。PGA评分以中度活动或重度活动为主,其中0~1分1例(9.09%),1~2.5分5例(45.45%),>2.5分5例(45.45%)。
2.2 治疗不同阶段BILAG器官受累分析 治疗前使用贝利尤单抗前BILAG指数以全身症状、皮肤黏膜、血液系统受累多见,无胃肠道受累病例。与基线相比,治疗4周时全身症状、皮肤黏膜、心血管及呼吸系统、血液系统受累显著改善;与治疗4周相比,治疗8周时皮肤黏膜、神经系统、肌肉骨骼无A或B级BILAG器官受累;与治疗12周相比,治疗16周时肌肉骨骼1例(9.09%),眼部1例(9.09%),肾脏2例(18.18%)仍有B级器官受累,所有器官无新发BILAG A和新发BILAG B。见表1。

表1 治疗不同阶段BILAG器官受累(A或B)分析[n(%)]
2.3 实验室结果分析 与贝利尤单抗治疗前相比,治疗16周白细胞计数较前升高,差异有统计学意义(P<0.05);红细胞较前升高,差异有统计学意义(P<0.05);血红蛋白较前升高,差异有统计学意义(P<0.05);血小板较前升高,差异有统计学意义(P<0.05)。
补体C3于治疗2周升至正常(0.80±0.24)g/L,补体C4于治疗4周升至正常[0.11(0.05,0.12)]g/L,补体C3、C4治疗16周与治疗前相比差异均有统计学意义(P<0.01);抗ds-DNA定量治疗16周未降至正常值,与治疗前相比差异有统计学意义(P<0.05);抗C1q抗体治疗16周接近正常值,与治疗前相比差异统计学意义(P<0.01);B淋巴细胞治疗16周较基线时下降,差异无统计学意义(P>0.05);全部病例基线与治疗不同阶段血清肌酐均正常,差异无统计学意义(P>0.05)。
研究对象中4例有肾脏受累表现,留取不同治疗阶段24 h尿蛋白定量和尿红细胞。治疗8周时24 h尿蛋白定量降至正常(0.48±0.57)g,治疗16周与治疗前相比明显下降,差异无统计学意义(t=2.212,P=0.114);尿红细胞治疗16周与治疗前相比明显下降,差异无统计学意义(Z=1.826,P=0.068)。见表2。
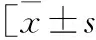
表2 治疗前后实验室结果分析或M(P25,P75)]
2.4 疾病活动度分析 贝利尤单抗治疗16周后与治疗前相比,SLEDAI-2000和PGA评分较基线期下降,差异有统计学意义(P<0.05);泼尼松剂量治疗前后差异有统计学意义(P<0.01);全部病例在第16周获得SRI-4反应,无复发病例。见表3。
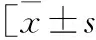
表3 治疗前后疾病活动度及激素剂量分析或M(P25,P75)]
2.5 不良事件 患儿接受贝利尤单抗治疗期间,2例(18.18%)出现不良事件,1例治疗2周出现血红蛋白及血小板下降,期间血红蛋白最低84 g/L,血小板最低64×109/L,治疗12周时恢复正常;1例出现上呼吸道感染,对症治疗后好转。余患儿无贝利尤单抗相关不良反应。
3 讨论
SLE是儿童自身免疫疾病中最常见的一种,全球范围内儿童SLE的患病率为1.9/10万~25.7/10万,儿童时期或青春期发病的儿童约占SLE的20%[12]。SLE传统治疗方案有激素、免疫抑制剂、羟氯喹等,如病情仍持续活动,或激素难以减量,药物副作用明显时需考虑应用生物制剂。贝利尤单抗是目前惟一可用于成人和儿童SLE的生物制剂,是一种完全人源化的单克隆抗体拮抗B细胞活化因子。SLE发病机制尚不明确,目前认为,SLE的发病机制中B细胞的异常激活起到重要作用,B细胞激活因子可以与特异性受体结合,激活与B细胞激活相关的信号通路。贝利尤单抗是抗B细胞激活因子的单克隆抗体,有调查用同源建模构建了贝利尤单抗的结构,通过分子动力学模拟分析B细胞激活因子-belimumab复合物的组合模式,证实了贝利尤单抗的有效性[13]。
儿童SLE使用贝利尤单抗治疗的临床研究较少。2020年一项为期52周随机、双盲、安慰剂对照Ⅲ期临床试验研究静脉注射贝利单抗治疗儿童SLE中的疗效、安全性和药代动力学,研究显示贝利单抗10 mg/kg静脉注射儿童SLE是有益的,与安慰剂组相比,贝利尤单抗组SRI-4应答率高,药物效应动力学、药物代谢动力学和安全性与成人相似[5]。一项纳入53例5~17岁儿童SLE患儿静脉注射贝利尤单抗的随机、双盲、安慰剂对照Ⅱ期试验显示,年龄、性别、疾病活动性和伴随药物治疗对儿童患者应用贝利单抗没有影响,除了10 mg/kg静脉注射剂量外,不需要考虑患者的特征而调整剂量[14]。国内一项回顾性、多中心、真实世界研究对比了贝利尤单抗治疗28周的169例和传统药物治疗的87例SLE患儿,提示贝利尤单抗治疗儿童SLE,能够减少激素和传统免疫抑制药物的用量,与传统药物治疗方案比较,更容易达到低疾病活动度和临床缓解状态,贝利尤单抗治疗对儿童狼疮性肾炎较传统药物治疗方案具有优势,且贝利尤治疗组的感染等不良事件发生率低[15]。
本研究用回顾性、真实世界的研究方法观察贝利尤单抗治疗11例儿童SLE的疗效,发现所有患儿激素均明显减量,研究终点时SLEDAI-2000和PGA评分下降;BILAG器官受累情况好转,所有器官无新发BILAG A和新发BILAG B;全部病例获得SRI-4反应。实验室指标中抗ds-DNA定量、24 h尿蛋白定量有所下降,补体C3、C4水平升高至正常值;有1例患儿应用贝利尤单抗治疗2周时出现血红蛋白及血小板下降,在治疗12周时逐渐升至正常,既往无使用贝利尤单抗引起血红蛋白或血小板下降的相关文献报道,其具体机制需进一步观察研究。贝利尤单抗在临床中多应用于狼疮性肾炎的患者,通过本次16周的真实世界研究发现,除肾炎外,采用贝利尤单抗治疗,各脏器功能损伤都有不同程度的缓解,且应用贝利尤单抗治疗儿童SLE能减少激素和免疫抑制剂的用量,不良反应的发生率低,能更快达到临床缓解。
但由于本研究观察周期短,患儿数量有限,统计结果有一定的偏倚,贝利尤单抗治疗儿童SLE的有效性和安全性仍需进一步长时间的随访,并需要进行大规模、多中心、前瞻性研究来证实贝利尤单抗治疗儿童SLE的有效性。

