血清IL-6、MGP参与慢性肾功能衰竭血液透析患者心血管事件发生的机制
张佳佳
河南省济源市第二人民医院血液净化室 454650
维持性血液透析是慢性肾功能衰竭(Chronic renal failure,CRF)患者生命支持治疗的主要手段,但患者生理方面的改变,包括贫血、炎症、钙磷代谢紊乱等,上述因素之间可相关作用并可作用于心血管系统,促使患者发生一系列心血管疾病,如心律失常、心绞痛等[1]。随着透析治疗技术不断革新,CRF患者行透析治疗后其并发症呈下降趋势,但心血管事件的发生率仍较高。临床已证实,微炎症状态是心血管疾病发生的重要机制,炎症因子可通过黏附、聚集等作用损伤血管内皮细胞,促使粥样硬化斑块形成,而白细胞介素-6(Interleukin-6,IL-6)是较为常用的炎症因子,当CRF患者处于微炎症状态时,IL-6呈高表达[2]。另有研究发现,血管钙化是引起心血管疾病的重要因素[3]。基质Gla蛋白(Matrix Gla protein,MGP)是肾脏疾病患者体内冠状动脉钙化的抑制因子,参与血管钙化的发生发展,且Viegas C等[4]研究发现,炎症因子作为炎症和氧化应激的始动因子,可加速血管钙化进程。故本研究通过观察CRF血液透析患者的IL-6、MGP水平,主要从血管钙化机制上探讨两种指标与心血管事件发生的关系,为临床诊疗血液透析CRF患者心血管事件的发生提供更多依据。
1 资料与方法
1.1 一般资料 本研究经医学伦理委员会审核。前瞻性队列研究,纳入2020年12月—2021年12月于我院血液透析中心的维持性血液透析的CRF患者。纳入标准:(1)CRF符合《内科学(第9版)》[5],标准全球肾脏病预后组织分期为慢性肾脏病(Chronic kidney disease,CKD)[6]5期,肾小球滤过率<15ml/(min·1.73m2);(2)规律血液透析时间≥3个月,透析频率为3次/周,透析时间为4h/次;(3)生命体征相对稳定;(4)预计生存时间>6个月。排除标准:(1)透析前1个月未使用高通量透析治疗、血流灌流等其他血液净化方式治疗;(2)肾脏移植病史;(3)入组前发生心血管疾病;(4)存在严重感染、手术、外伤;(5)存在血液疾病;(6)原发性甲状旁腺功能异常;(7)具有出血倾向。剔除或脱落标准:(1)临床失访;(2)观察期间调整治疗方案;(3)研究期间病死。
1.2 方法
1.2.1 一般资料调查:入组后,于透析治疗前设计基线资料调查表,调查患者性别、年龄、透析龄、合并基础疾病(如糖尿病、高血压)、原发病、吸烟史、肾病家族史等。
1.2.2 实验室相关指标及血清IL-6、MGP检测方法:于透析前,取患者清晨7—9点空腹时间>8h的外周血5ml,常温下3 000r/min,离心15min,取血清,应用日本西门子ADVIA 2400型全自动生化仪检测血钙(Ca)、血磷(P)、白蛋白(Alb)、血肌酐(Scr)、尿素氮(BUN)、甘油三酯(TG)、总胆固醇(TC)水平;甲状旁腺激素(PTH)、血清IL-6采用化学发光法检测;血清MGP采用酶联免疫吸附法检测,试剂盒均购自北京华科泰生物技术。
1.2.3 心血管事件评估:所有患者均于医院继续进行持续性血液透析;每月对患者进行随访(电话、微信或门诊复诊),观察时间为6个月,记录心血管事件发生情况(包括短暂性脑缺血发作、心绞痛、心肌梗死、因心力衰竭或室性心律失常住院等),并根据观察结果分为发生组与未发生组。
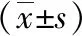
2 结果
2.1 一般资料 共纳入128例患者,失访5例,最终纳入123例。其中男67例,女56例;年龄50~67岁,平均年龄(59.15±3.19)岁;透析龄18~41个月,平均透析龄(28.58±5.19)个月。随访6个月,其中48例发生心血管事件,心血管事件发生率为39.02%。
2.2 发生、未发生心血管事件的血液透析CRF患者一般资料比较 发生组透析龄大于未发生组(P<0.05);两组其他一般资料比较,差异无统计学意义(P>0.05)。见表1。

表1 发生、未发生心血管事件的血液透析CRF患者一般资料比较
2.3 发生、未发生心血管事件的血液透析CRF患者实验室指标比较 发生组血清PTH、IL-6水平高于未发生组,MGP水平低于未发生组,差异有统计学意义(P<0.05);两组其他实验室指标比较,差异无统计学意义(P>0.05)。见表2。

表2 发生、未发生心血管事件的血液透析CRF患者实验室指标比较
2.4 血液透析CRF患者血清IL-6、MGP与临床指标的相关性 血清 IL-6与透析龄呈正相关(P=0.003),与MGP呈负相关(P=0.013);血清MGP与透析龄呈负相关(P=0.004)。血清IL-6、MGP与Ca、P、Alb、Scr、BUN、TG、TC、PTH均无显著相关性(P>0.05)。见图1~3、表3。
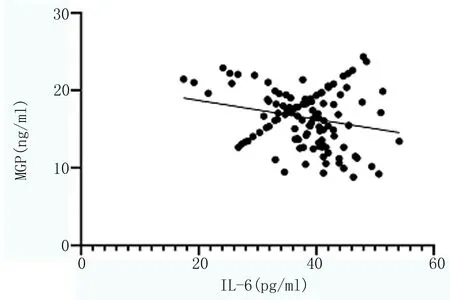
图1 血液透析CRF患者血清IL-6与MGP的相关性

图2 血液透析CRF患者血清IL-6与透析龄的相关性

图3 血液透析CRF患者血清MGP与透析龄的相关性
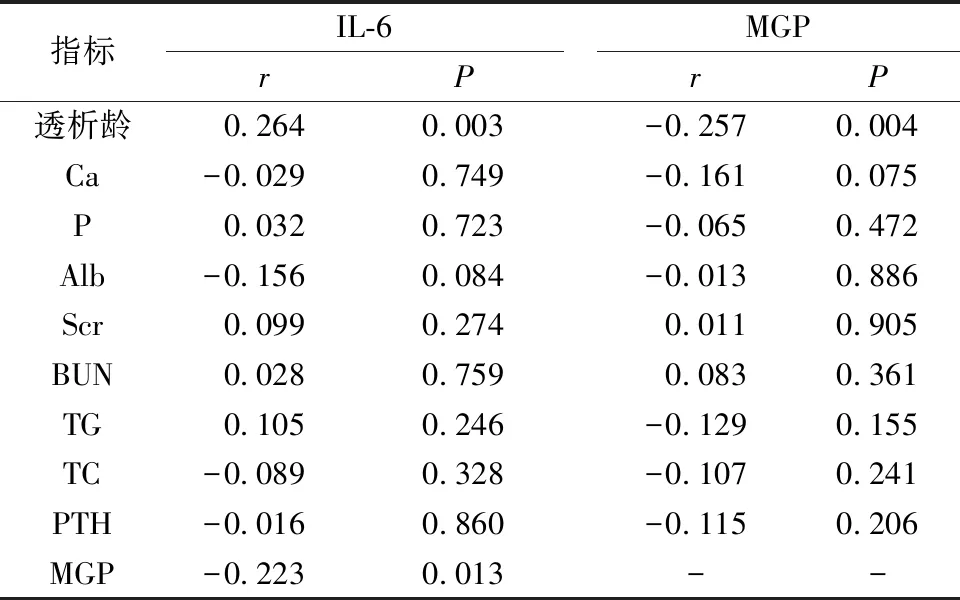
表3 血液透析CRF患者血清IL-6、MGP与临床指标的相关性
2.5 血清IL-6、MGP水平与血液透析CRF患者心血管事件的相关性 采用点二列相关性分析,血清IL-6、MGP水平与血液透析CRF患者心血管事件有关(r=0.379、-0.496,P<0.001)。
2.6 血液透析CRF患者发生心血管事件的多因素Logistic 回归分析 本研究以血液透析CRF心血管事件发生情况作为因变量(1=发生,0=未发生),将表1、2中具有统计学差异的指标(透析龄、PTH、IL-6、MGP)作为自变量(均为连续变量),经Logistic回归分析结果显示,透析龄较大、血清IL-6过表达、MGP低表达与血液透析CRF患者发生心血管事件有关(P<0.05)。见表4。

表4 血液透析CRF患者发生心血管事件的多因素Logistic 回归分析
2.7 血清IL-6、MGP水平预测血液透析CRF患者发生心血管事件的价值 将血清IL-6、MGP水平作为检验变量,将患者心血管事件发生情况作为状态变量(1=发生,0=未发生),绘制ROC曲线(见图4),结果显示,血清IL-6、MGP水平预测血液透析
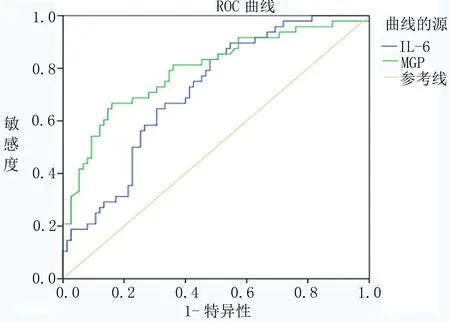
图4 血清IL-6、MGP水平预测血液透析CRF患者发生心血管事件的ROC曲线
CRF患者心血管事件的AUC分别为0.714、0.793,均有一定价值,当血清IL-6、MGP截断值分别取36.905pg/ml、15.325ng/ml时,可获得较高的敏感度、特异度。见表5。
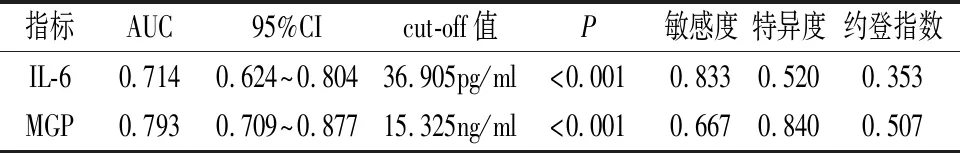
表5 血清IL-6、MGP水平预测血液透析CRF患者发生心血管事件效能
3 讨论
已有的文献报道,与心血管疾病相关的影响因素,如钙磷代谢紊乱、高龄等被证实与慢性肾脏病患者血管钙化密切相关[7]。而冠状动脉粥样硬化处出现钙化,可导致血管出现不同程度狭窄,严重狭窄者可诱发心肌缺血缺氧,增加心绞痛、心肌梗死等风险;且动脉中膜钙化可促使动脉僵硬,导致患者左心室肥厚、心力衰竭。由此可见,血管钙化是引起心血管不良事件的重要因素。本研究主要从血管钙化机制来分析血液透析CRF患者心血管事件发生的病理变化过程。
本研究结果显示,血清IL-6在发生心血管事件的血液透析CRF患者中呈高表达。IL-6是常用来反映CRF患者微炎症状态的临床指标,而微炎症状态是机制在各种毒素、炎症介质等作用下出现的免疫抑制状态,主要表现为多种炎症因子水平升高。临床研究已证实,微炎症与多种心血管事件密切相关[8]。炎症因子及介质可产生大量氧自由基损伤内皮功能,同时在炎症作用下多种细胞因子大量释放可导致内皮功能障碍,进而导致动脉粥样硬化。另有研究发现,微炎症状态与血管钙化的发生密切相关[9]。炎症因子的激活、释放可出现炎症级联反应,损伤动脉壁上的内皮细胞,并启动骨生成程序,可促使平滑肌细胞向成骨样细胞表型转分化,从而加速血管钙化。IL-6在局部炎症早期的作用较为突出,可促进细胞因子和炎症介质释放,T细胞、巨噬细胞向血管壁局部浸润,而T细胞可识别氧化低密度脂蛋白,促使炎症介质及因子含量进一步增加,巨噬细胞吞噬氧化低密度脂蛋白并形成泡沫细胞,进而形成脂质斑块,导致血管钙化,继而并发心血管疾病[10]。虽然本研究中点二列相关性证实了血清IL-6与血液透析CRF患者心血管事件发生有关。但血清IL-6是一种常见的炎症因子,在多种炎症反应中均可出现高表达,其特异性较低,因而IL-6在临床评估血液透析CRF患者心血管事件的价值还需进行深入探讨。
本研究结果显示,MGP在发生心血管事件的血液透析CRF患者中呈低表达。MGP是较为重要的血管钙化抑制因子,在内皮细胞、软骨细胞中均有表达。Barrett H等[11]发现,MGP在血管钙化区的含量明显降低,但具体的调控机制尚不明确。根据临床较多的研究发现,MGP与血管钙化的关系可概括为:(1)钙磷代谢紊乱并不断沉积,导致MGP与骨形态蛋白相结合,抑制矿物质因子沉积,从而抑制钙化病理过程;(2)MGP可直接与胎球蛋白A结合,形成复合物,从而阻断血管钙化进程;(3)MGP可通过结合转化生长因子β超家族成员发挥作用(如骨形态发生蛋白-2),促使转化生长因子β超家族成员的功能(促进平滑肌细胞向成骨样细胞表型转分化,协同诱导和加重血管钙化)丧失作用,阻断平滑肌细胞表型转化为成骨细胞表型,从而抑制血管钙化;(4)MGP可直接作用于平滑肌细胞,促使其凋亡,抑制异位钙化[12-13]。鉴于上述研究背景,MGP在血液透析CRF血管钙化形成过程中有着举足轻重的作用,虽然其具体的作用机制仍不明确,但MGP作为血管钙化抑制因子,临床可考虑将该指标作为治疗的靶点,延缓或抑制血管钙化情况,诱发心绞痛、心肌梗死等。
本研究进一步分析血清IL-6与MGP关系,结果证实两种指标之间存在一定的联系。因微炎症状态与血管钙化的关系已达成共识,本研究不再进行探讨。另外,本研究中分析血清IL-6、MGP与患者临床其他指标的相关性发现,IL-6与透析龄呈正相关,MGP与透析龄呈负相关。可能是因为随着患者透析龄的增加,患者微炎症加重、钙磷沉积,MGP含量降低,增加异位钙化的风险。此外,MGP受多种因素的影响(如钙磷、甲状腺激素水平等),但本研究结果显示,MGP与各指标均无相关系,其具体的原因暂不清楚,需开展分析。
Logistic回归分析发现,血清IL-6过表达、MGP低表达与血液透析CRF患者心血管事件存在一定的联系,证实了上述的研究。且透析龄也是患者心血管事件发生的影响因素,通过校正其他影响因素后,发现患者透析龄每延长1个月,其并发心血管事件的风险升高1.500倍。血液透析作为一种体外循环操作,患者每经历一次透析,血液与透析管道、透析器或透析液接触后,会激活体内的补体和单核系统,产生大量的氧自由基,导致其血管内皮功能障碍,心脏负荷增加,因此,持续性血液透析患者易出现各种心血管疾病[14]。
本研究中预测患者心血管事件的ROC曲线结果显示,血清IL-6、MGP预测患者心血管事件有一定的价值,且MGP预测血液透析CRF患者发生心血管事件的AUC、特异度均高于IL-6,提示MGP有望成为预测血液透析CRF患者发生心血管事件的一项血清学标志物,但具体的应用情况还需探索。
综上所述,血清IL-6、MGP参与行血液透析CRF患者的心血管事件发生机制,血清IL-6过表达、MGP低表达与血液透析CRF患者发生心血管事件有关;通过检测血清IL-6、MGP水平对预测血液透析CRF患者心血管事件发生情况具有一定的价值。但是本研究随访的时间较多,且剔除了心源性猝死的患者,可导致研究结果出现偏倚,本研究仍需进行更长随访时间及考虑心血管事件病死情况,以此证实本次研究结论。且本次研究主要从血管钙化机制探讨IL-6、MGP指标与患者心血管事件的关系,而血管钙化的发生机制较为复杂,还需深入分析。

