D-生物素的高效合成研究
王晨光,杨士伟,束 鑫,3
(1.安徽泰格维生素实业有限公司,安徽蚌埠 233700;2.安徽省药食同源天然资源开发与利用工程实验室(合肥师范学院),安徽合肥 230601;3.安徽丰原药业股份有限公司,安徽合肥 230601)
D-生物素(D-Biotin,又名维生素H、辅酶R)[1-2]是一种水溶性B 族维生素,为无色结晶性粉末。天然D-生物素广泛存在于动物的肾、肝、胰等器官中,以及牛奶、蛋黄、酵母中。它是脂肪和蛋白质正常代谢不可或缺的物质,在医疗、饲料以及生物技术等领域中有广泛应用[3]。
目前,D-生物素几乎都是由化学合成法生产[4-7],顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮是合成D-生物素的关键中间体。现有技术通常采用1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(式II 所示化合物)脱水关环反应合成顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮(式I 所示化合物),反应路线如下:
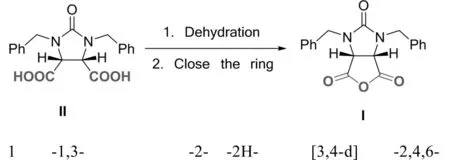
图1 顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮的合成路线
陈芬儿等[8]在上述反应体系中添加乙酸酐催化反应的进行,但1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸与乙酸酐的摩尔比例必须为1∶3 反应才能进行,收率90%,仍有5%~10%的原料未反应完全,难以得到高纯度的产品;且反应后形成大量乙酸酐和乙酸的混合物,二者不易分离套用,并且对反应设备的耐腐蚀性要求高,严重危害环境。陈芬儿等[9]公开了将1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸与酰卤在无溶剂条件下发生脱水、关环反应制得顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮的方法。该方法同样存在产生大量腐蚀性的酸,对反应设备要求高的缺陷。
Sing 等[10]公开了添加催化量的有机酸或无机酸使1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸发生脱水、关环反应制得顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮的方法。该法虽然避免了使用大量具有腐蚀性的酸,但是仍需要添加酸性脱水剂,同样对反应设备的耐腐蚀性要求高,同时也不利于对反应液的回收套用。将1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸在高沸点有机溶剂中回流反应、共沸带水,制得了顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。该方法虽然不需要添加任何脱水剂即可反应完全,但是其反应速率较慢,实验室量级的反应需要至少6 h才能完成,工业生产中则需要15 h左右,能耗高,反应时间长,溶剂损耗大。因此,有待于研究一种反应效率更高、设备腐蚀性更小的合成环酸酐的方法。
本文以二羧酸为原料,叔胺硫酸盐或叔胺硫酸盐与硫酸的混合物为催化剂,分别进行了实验室量级、公斤级顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮合成实验。
1 实验部分
1.1 试剂与仪器
三正丁胺,98.9%,安耐吉试剂有限公司;邻二甲苯,AR,麦克林试剂有限公司;甲苯、二氯甲烷(DCM)、四氢呋喃(THF)、三乙胺(TEA)、氢氧化钠(NaOH)、氢氧化钾(KOH)、氢氧化锂(LiOH)、浓硫酸,AR,国药集团化学试剂有限公司。
Agilent1290 超高压液相色谱仪;AB4000 三重四级杆串联质谱仪(ESI+源);高效液相色谱(HPLC);Nicolet 6700 傅里叶红外光谱仪,赛默飞世尔科技(中国)有限公司;AVⅢ400 MHz 型核磁共振波谱仪(DMSO-d6为溶剂,TMS 为内标),瑞士Bruker 公司。
1.2 实验方法
1.2.1 顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮的合成
将三正丁胺(0.261 5 g,0.001 4 mol)与浓硫酸(折合硫酸0.138 5 g,0.001 4 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三正丁胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和甲苯510 mL,加热至110℃,搅拌回流带水(冷凝管+回流过滤器除水)2 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量甲苯淋洗,干燥后得白色粉末(28.458 8 g),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC(高效液相色谱)检测产物纯度为99.95%,收率为99.95%。m.p.236℃~237℃。 IR(KBr):v=1 805,1 740,1 687,1 227 cm-1。1H NMR(CDCl3):δ=4.21(s,2H,2×CH),4.19,5.10(dd,4H,J=15 Hz,2×CH2C6H5),7.26~7.39(m,10H,2×C6H5)ppm。EI-MS:(m/z,%)=336(M+,13.6),264(15.6),173(5.8),132(10.9),91(100)。
1.2.2 高效液相色谱检测纯度的条件
流动相:55% 乙腈+ 45% 缓冲盐[KH2PO4(1.35 g)+ 85% H3PO4(0.45 mL)+水(500 mL)],用0.45 μm 滤膜过滤,超声脱气;柱型:5 μm,4.6×250 mm,C18;流速:1.0 mL/min;检测波长:210 nm。
2 结果与讨论
2.1 实验室级反应条件考查
当三正丁胺(0.261 5 g,0.001 4 mol)与浓硫酸(折合硫酸0.138 5 g,0.001 4 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三正丁胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和甲苯510 mL,加热至110℃,搅拌回流带水(冷凝管+回流过滤器除水)2 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量甲苯淋洗,干燥后得白色粉末(28.458 8 g),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC(高效液相色谱)检测产物纯度为99.95%,收率为99.95%(表1,序号1)。
当三乙胺(0.203 0 g,0.002 0 mol)与浓硫酸(折合硫酸0.197 0 g,0.002 0 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三乙胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和邻二甲苯510 mL,加热至145℃,搅拌回流带水(冷凝管+回流过滤器除水)2 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量邻二甲苯淋洗,干燥后得白色粉末(28.456 8 g),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC检测产物纯度为99.75%,收率为99.74%(表1,序号2)。
当三辛胺(0.313 3 g,0.000 9 mol)与浓硫酸(折合硫酸0.086 7 g,0.000 9 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三辛胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和乙苯510 mL,加热至135℃,搅拌回流带水(冷凝管+回流过滤器除水)2 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量乙苯淋洗,干燥后得白色粉末(28.460 1 g),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC检测产物纯度为99.65%,收率为99.65%(表1,序号3)。
当三正丁胺(0.185 4 g,0.001 0 mol)与浓硫酸(折合硫酸0.147 1 g,0.001 5 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三正丁胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和对二甲苯750 mL,加热至140℃,搅拌回流带水(冷凝管+回流过滤器除水)4 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量对二甲苯淋洗,干燥后得白色粉末(28.456 2 g),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC检测产物纯度为99.56%,收率为99.55%(表1,序号4)。
将三正丁胺(0.064 9 g,0.000 35 mol)与浓硫酸(折合硫酸0.038 3 g,0.000 39 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三正丁胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和甲苯510 mL,加热至110℃,搅拌回流带水(冷凝管+回流过滤器除水)3 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量甲苯淋洗,干燥后得白色粉末(28.453 4 g),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC检测产物纯度为99.78%,收率为99.76%(表1,序号5)。
将三正丁胺(0.261 5 g,0.001 4 mol)与浓硫酸(折合硫酸0.138 5 g,0.001 4 mol)置于反应瓶中,加热至45℃,搅拌30 min,形成三正丁胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(30.0 g,0.084 7 mol)和甲苯510 mL,加热至110℃,搅拌回流带水(冷凝管+回流过滤器除水)2 h,反应结束后冷却至常温,形成含顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮的悬浮液;向上述悬浮液中加入(S)-1,1-二苯基-1,2-丙二醇(19.38 g,0.085 mol),然后滴加三乙胺(10.1 g,0.054 6 mol),搅拌反应4 h,生成(4S,5R)-1,3-二苯甲基-2-氧代-4,5-咪唑烷二羧酸5-[(S)-2-羟基-1-甲基-2,2-二苯乙基]酯三乙胺,将得到的溶液用10wt%的氢氧化锂水溶液进行处理,过滤,滤饼用纯化水洗涤,真空干燥,得到(4S,5R)-1,3-二苯甲基-2-氧代-4,5-咪唑烷二羧酸5-[(S)-2-羟基-1-甲基-2,2-二苯乙基]酯酸锂46.2 g。经HPLC(高效液相色谱)检测,产物非对映异构纯度为98.5%,总收率为95.5%(表1,序号6)。
当三正丁胺用量为0.001 4 mol,硫酸用量为0.001 0 mol,得到白色粉末产物28.023 6 g,HPLC 检测纯度为98.90%,收率为97.39%(表1,序号7)。当三正丁胺用量为0.001 0 mol,硫酸用量为0.002 0 mol,得到白色粉末产物27.659 8 g,HPLC检测纯度为98.61%,收率为95.84%(表1,序号8)。
当三正丁胺替换为等摩尔量的正丁胺,得到白色粉末产物12.653 1 g,HPLC 检测纯度为88.91%,收率为39.53%(表1,序号9)。当三正丁胺替换为等摩尔量的二正丁胺,得到白色粉末产物12.236 7 g,HPLC 检测纯度为89.60%,收率为38.53%(表1,序号10)。当三正丁胺替换为等摩尔量的三乙胺,HPLC 检测纯度为88.92%,收率为35.21%(表1,序号11)。
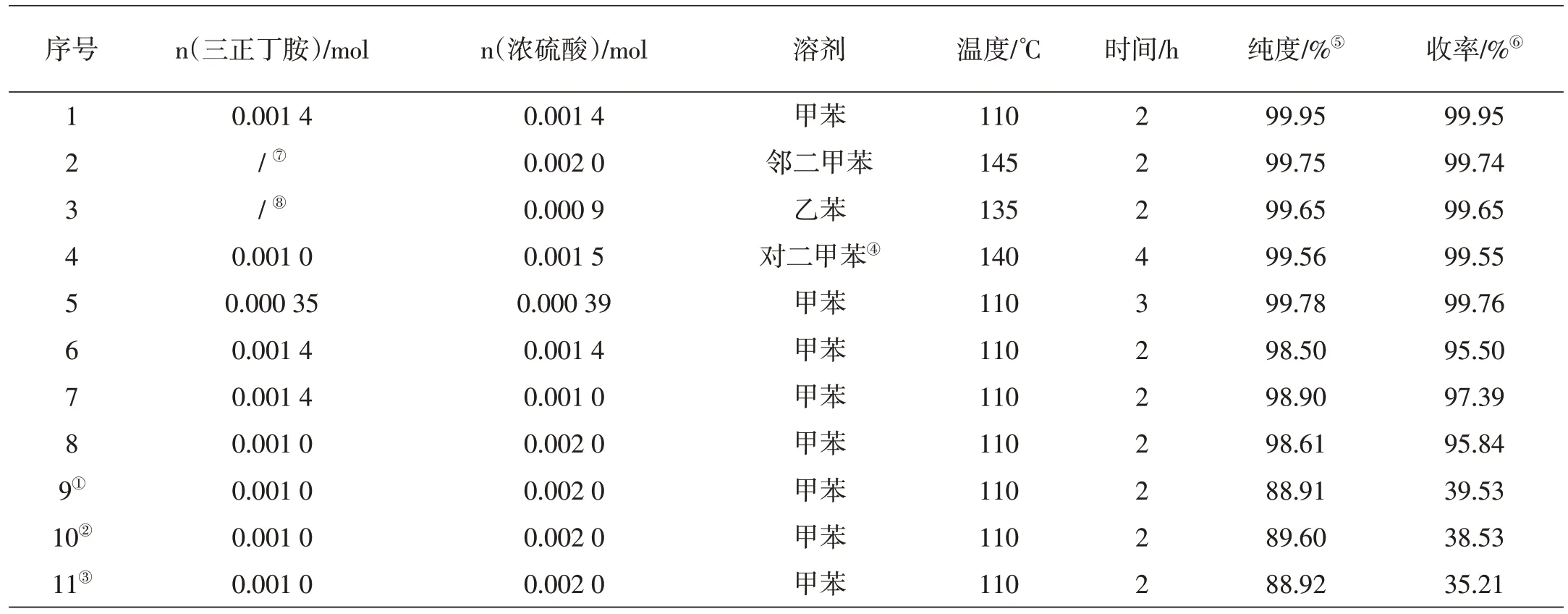
表1 反应条件的优化
2.2 公斤级放大试验
将三正丁胺(4.36 kg,23.6 mol)与浓硫酸(折合硫酸2.31 kg,23.6 mol)置于反应釜中,加热至45℃,搅拌30 min,形成三正丁胺硫酸盐;加入1,3-二苄基咪唑啉-2-酮-顺-4,5-二羧酸(500 kg,1 412.4 mol)和甲苯8 500 L,加热至110℃,搅拌回流带水(冷凝管+回流过滤器除水)8 h,反应结束后冷却至室温,析出固体,过滤,滤饼用少量甲苯淋洗,干燥后得白色粉末(474.55 kg),即为顺-1,3-二苄基咪唑啉-2-酮-2H-呋喃并[3,4-d]咪唑-2,4,6-三酮。HPLC 检测产物纯度为99.92%,收率为99.92%。
3 结论
(1)本文采用的催化剂,实验室级需2 h 可反应完全,公斤级需8 h,比文献报道时间短。
(2)使用的催化剂中叔胺与硫酸的摩尔比过小,硫酸含量过高,导致反应产物被部分氧化,产物纯度和反应速率均明显下降。
(3)本文发现伯胺硫酸盐和叔胺硫酸盐基本没有催化作用,可为工业化生产提供参考。

