阿拉伯木聚糖联合美多芭对帕金森病大鼠炎症因子TNF-α、IL-1β及IFN-γ表达的影响
王功俊,包成政,罗雪莲,王洁,黄晓华,黄小睿,张仕姣,李雪斌,,3
(1. 右江民族医学院,广西 百色 533000;2. 右江民族医学院附属医院,广西 百色 533000;3. 广西高校桂西地区高发病防治研究重点实验室,广西 百色 533000)
帕金森病(Parkinson’s disease,PD)是第二种常见的神经退行性疾病,全球发病率估计为0.1%~0.2%[1]。其典型的病理特征是黑质(SN)中多巴胺能神经元的逐渐丧失,以及α-突触核蛋白(α-synuclein,α-syn)在中枢神经系统(central nervous system,CNS)的异常聚集导致路易小体(lewy body)的形成[2]。近年来关于Toll 样受体/核转录因子-κB(TLR/NF-κB)信号通路与PD相关炎症介质产生的研究越来越多[3]。簇集的α-突触核蛋白与Toll样受体结合并激活小胶质细胞,核因子-κB(NF-κB)活化,启动肿瘤坏死因子α(TNF-α)及白细胞介素1(IL-1β)的表达,促炎细胞因子过度产生和分泌诱导细胞死亡并加速PD发病及病程进展[4]。γ干扰素(IFN-γ)是一种由I型辅助性T细胞产生的促炎细胞因子[5]。目前的治疗方法,如多巴胺能激动剂、抗胆碱能药或单胺氧化酶抑制剂可以缓解PD症状,长期用药副作用较大,急需研发新药物,减缓或停止潜在的神经变性过程。然而,目前的治疗方法不足以根除或限制疾病的发展,它们只有助于症状的改善,且治疗过程中常常出现“开关现象”、“剂末现象”、“晨僵现象”等,影响治疗效果。阿拉伯木聚糖(araboxylan,AX)是一种多糖,由阿拉伯糖、木糖和少量其他碳水化合物组成。AX具有抗氧化抗炎、降血糖、抗肿瘤和肠道益生菌菌群的增殖能力[6]。本研究拟采用鱼藤酮诱导PD大鼠模型,通过AX干预后观察PD大鼠的运动症状改变情况,检测炎性因子(TNF-α、IL-1β、IFN-γ)分泌,了解各组大鼠炎症因子TNF-α、IL-1β及IFN-γ的变化与PD大鼠的神经功能相关性,探讨AX防治PD可能作用机制,为AX用于预防和/或治疗PD临床应用提供实验依据。
1 材料与方法
1.1实验材料
1.1.1实验动物 健康雄性SPF级Sprague-Dawley(SD)大鼠42只,6~8周龄,体重160~180 g,购买于广东维通利华实验动物技术有限公司,许可证号:SCXK(粤)2022-0063。大鼠饲养于右江民族医学院SPF医学实验动物研究中心,大鼠自由摄食,并适应饲养环境1周。实验中涉及的动物操作程序已得到右江民族医学院实验动物伦理委员会批准。
1.1.2主要试剂及仪器 鱼藤酮及葵花油(美国Sigma公司),美多芭(上海罗氏制药有限公司),阿拉伯木聚糖(AX)(赛普瑞特分子生物科技辽宁有限公司),兔抗IL-1β单克隆抗体及兔抗IFN-γ单克隆抗体(英国Abcam生物试剂公司),鼠抗β-actin单克隆抗体(中国武汉Protein公司),山羊抗鼠二抗和山羊抗兔二抗(美国ThermoFisher公司),冰冻切片机(德国LEICA公司),光学显微镜(德国LEICA公司),ELISA试剂盒(中国武汉伊莱瑞特生物科技公司)。
1.2方法
1.2.1动物分组 SD成年雄性大鼠42只,随机选取28只进行PD造模,造模后并分为帕金森模型组(PD组)、美多芭组(M组)和阿拉伯木聚糖组(AX 组)、美多芭+阿拉伯木聚糖组(MX组)4个组,每组7只。其余14只随机分为空白对照组和溶剂对照组,每组7只。
1.2.2造模 采用颈背部皮下注射鱼藤酮法制备PD模型:鱼藤酮(1.5 mg/kg)溶解于葵花油,浓度1.5 mg/mL,给予颈背部皮下注射[7],每连续给药6 d后,停药1次,连续28 d。按照YANG Y等[8]行为学标准评分,PD模型大鼠出现典型的毛色变黄变脏、弓背、拒捕减弱、震颤等表现则视为造模成功。溶剂对照组:连续颈背部皮下注射葵花油1.5 mg/(kg·d) ,每连续给药6 d后,停药1次,连续28 d。
1.2.3给药方法 空白对照组、溶剂对照组及PD组:不予处理,正常饲养。 AX组、M组、MX组模型制备成功后,M组美多芭灌胃(50 mg/kg,每天1次)干预,AX组使用AX灌胃(0.8 g/kg,每天1次)干预,MX组使用AX(0.8 g/kg,每天1次)联合美多芭(50 mg/kg,每天1次)灌胃,各组大鼠在喂养14 d,最后一次灌胃后24 h,应用悬挂试验及爬杆进行行为学研究。
1.2.4行为学检测方法 干预后每只大鼠进行悬挂爬杆和爬杆训练3次,训练完毕对其进行行为学测定。悬挂实验:用于检测大鼠肌张力,将大鼠两前爪悬挂于水平放置的金属丝(直径 2 mm、长约30 cm) 上,金属丝距地面1 m,记录大鼠落地前的时间。对悬挂时间进行评分:0~4 s为0分,5~9 s为1分,10~14 s为2,15~19 s为3分,20~24 s为4分,25~29 s为5分,超过30 s为6分。每只大鼠重复测量3次,每次间隔5 min。爬杆实验:评估大鼠四肢运动的协调性,木杆上顶端放置圆形球,杆(高60 cm、直径0.7 cm)用医用纱布缠好,保证有摩擦力;将大鼠头向下放置在木杆的顶部,使大鼠沿杆自然爬下,观察其下行过程中的行为并计分,每只鼠允许爬杆3次。评分标准如下:四肢并用,一次顺利从杆上爬下为0分;螺旋向下爬行但兼有后肢滑行行为的为0.5分;上杆后间歇停顿数次后爬下,但可抱紧金属杆为1分;滑行后掉落为1.5分;不能抓杆,直接掉落为2.0分。
1.2.5样本提取 所有大鼠进行行为学测试完成后,次日每组随机选取6只大鼠用异氟醚对大鼠进行深度麻醉后,开腹腔腹主动脉采血,常温静置1 h后,于4 ℃离心机1 000 r/min,离心20 min,取上清液,放-80 ℃存冰箱。 每组随机选取6只大鼠,断头取脑,于冰盘上迅速开颅取脑,液氮急速冷冻,放置-80 ℃冰箱保存备用,用于WB检测大鼠黑质纹状体的IFN-γ蛋白表达;另外剩下每组1只大鼠进行心腔内注射生理盐水和4%多聚甲醛进行内固定,迅速取脑,置于4%多聚甲醛室温保存,应用免疫组化检测IL-1β蛋白的表达。
1.2.6实验方法
1.2.6.1ELISA检测大鼠血清TNF-α、IL-1β含量 从-80 ℃冰箱取出血清,静置20 min。按照说明书给样本及标准品稀释,每孔100 μL加样分别加入样品稀释液、不同浓度梯度的标准品、待测样品,封板膜封板,37°孵育,加酶,显色后加入终止液,用酶标仪检测波长在450 nm处吸光度值。
1.2.6.2免疫组化 从4%多聚甲醛取出大脑,按照大鼠脑定位图谱,切到大鼠黑质纹状体层面,常规脱蜡至水,厚度为6 μm,切片用3%柠檬酸修复液高压修复,打开顶阀后修复10 min。将压力锅自然冷却至室温,然后用蒸馏水洗涤5 min。加入3%甲醇过氧化氢20 min,用蒸馏水冲洗5 min,用PBS浸泡1 min,滴5%BSA,室温孵育30 min弃去,滴一抗工作溶液在4 ℃过夜,滴二抗,在37 ℃孵育20 min,封片,显微镜观察、图像采集。
1.2.6.3WB检测 从-80°冰箱取出样本,随机分离出一侧中脑黑质放于离心管中,于研钵中磨碎黑质脑组织,蛋白提取试剂盒提取总蛋白,BCA法测定蛋白浓度,依次进行12.5% SDS-PACE 电泳分离白,电泳至溴酚蓝刚跑出即可终止,转印至 PDDF膜上,快速封闭液封,一抗孵育过夜,TBST洗膜3遍,加入二抗,室温孵育2 h,ECL法发光显影,图片保存,ImageJ软件分析数据,以β-actin为内参,计算相对表达量。
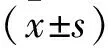
2 结果
2.1行为学结果
2.1.1悬挂实验 PD模型组与空白组、溶剂组悬挂时间明显缩短,差异有统计学意义(P<0.001);AX组、M组与PD模型组比较,悬挂时间延长,差异有统计学意义(P<0.05);MX组与PD模型组比较,悬挂时间延长,差异有统计学意义(P<0.01);而且MX组较AX组、M组悬挂时间延长,差异无统计学意义(P>0.05);说明各组大鼠给予干预后,明显改善了大鼠的肌张力,而且联合干预改善症状更明显。见表1。
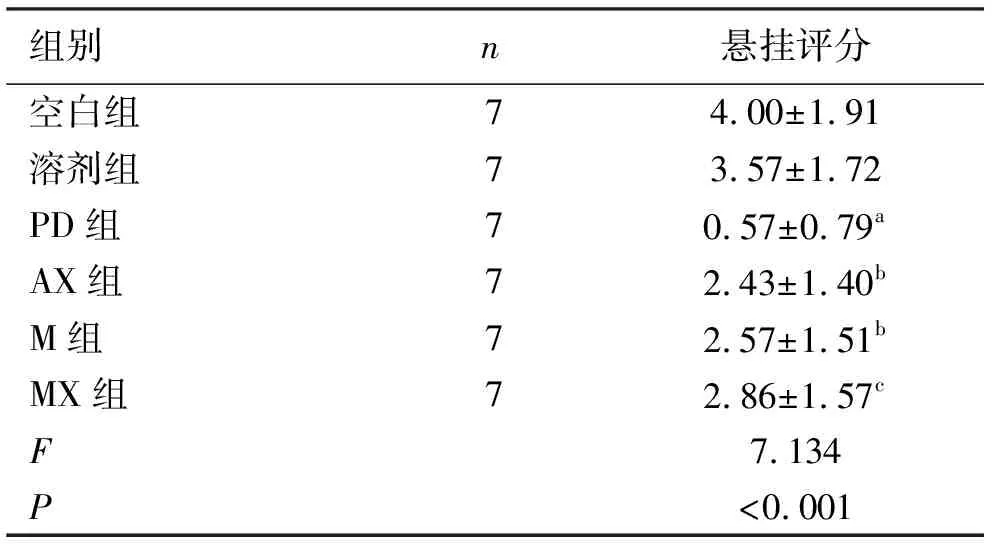
表1 各组大鼠悬挂实验结果
2.1.2爬杆实验 PD模型组与空白组、溶剂组,大鼠四肢协调能力明显减弱,下滑加速,甚至不能抱杆、直接坠落,差异有统计学意义(P<0.001)。AX组、M组大鼠与PD组比较,四肢协调力显著改善,差异有统计学意义(P<0.05)。MX组较PD组明显改善症状,爬杆过程中,四肢并用,动作协调,能一次性爬到杆底,差异有统计学意义(P<0.01);说明各组大鼠给予干预后,明显改善了大鼠的四肢协调力,而且联合干预改善症状更明显。见表2。
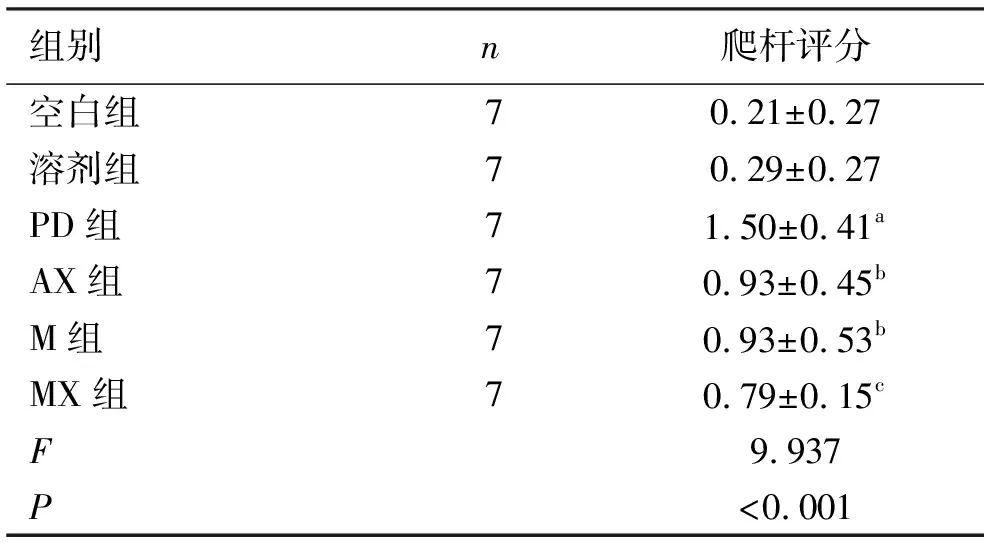
表2 各组大鼠爬杆实验结果
2.2ELISA检验 与空白对照组、溶剂对照组比较,PD模型组血清TNF-α含量增高,差异有显著意义(P<0.001);AX、M组、MX组与PD模型组比较血清TNF-α含量均降低,AX组与PD模型组比较,差异无统计学意义(P>0.05);M组与PD模型组比较,差异有统计学意义P<0.05;MX组与PD模型组比较,差异有显著意义(P<0.001)。MX组与M组比较,差异无统计学意义(P>0.05);MX组与AX组比较,差异有统计学意义(P<0.05)。与空白对照组、溶剂对照组比较,PD模型组血清IL-1β含量增高,差异有显著意义(P<0.001);AX、M组、MX组与PD模型组比较血清IL-1β含量均降低,AX组与PD模型组比较,差异有统计学意义(P<0.05);M组、MX组与PD模型组比较,差异有显著意义(P<0.001)。MX组与M组比较,差异无统计学意义(P>0.05);M组、MX组与AX组比较,差异有统计学意义(P<0.05)。见表3。
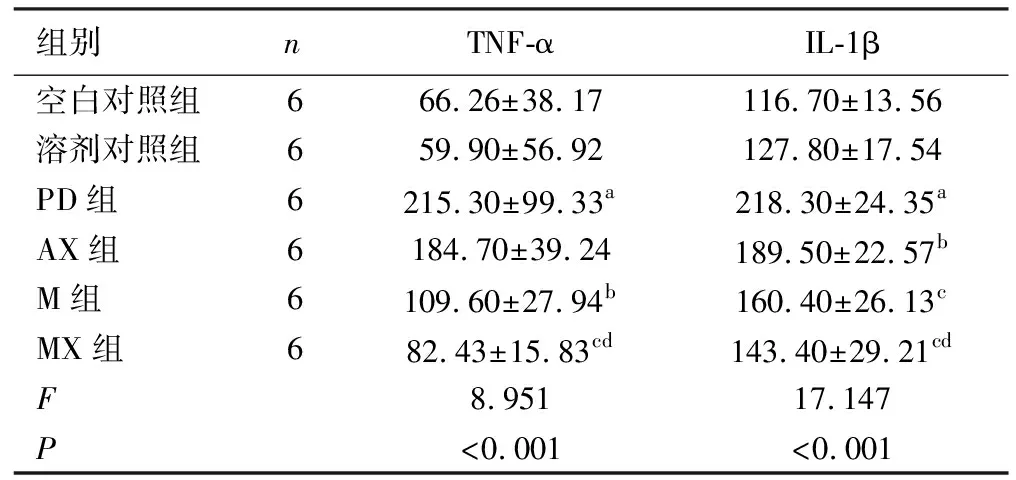
表3 各组大鼠ELISA检测TNF-α、IL-1β结果 单位:μg/μL
2.3WB检测各组大鼠脑黑质纹状体组织中IFN-γ蛋白相对表达量比较 与空白对照组、溶剂对照组比较,PD组黑质纹状体IFN-γ的含量增高,差异有统计学意义(P<0.001);与PD组比较,AX组、M组黑质纹状体IFN-γ的含量降低,差异有统计学意义(P<0.05);与PD组比较,MX组黑质纹状体IFN-γ的含量降低,差异有统计学意义(P<0.001)。与AX组比较,MX组黑质纹状体BDNF蛋白表达增加,差异无统计学意义(P>0.05)。M组与AX组比较,差异无统计学意义(P>0.05)。见图1、图2。
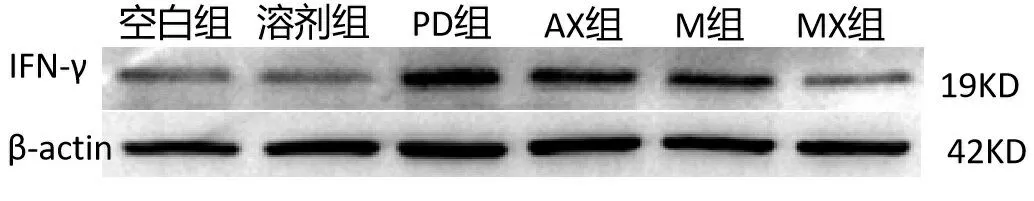
注:IFN-γ(γ干扰素) ;β-actin内参。
2.4免疫组化 与空白对照组、溶剂对照组比较,模型组黑质纹状体IL-1β表达量明显增加;与PD组比较,AX、M组、MX组黑质纹状体IL-1β表达量减少。如图3。
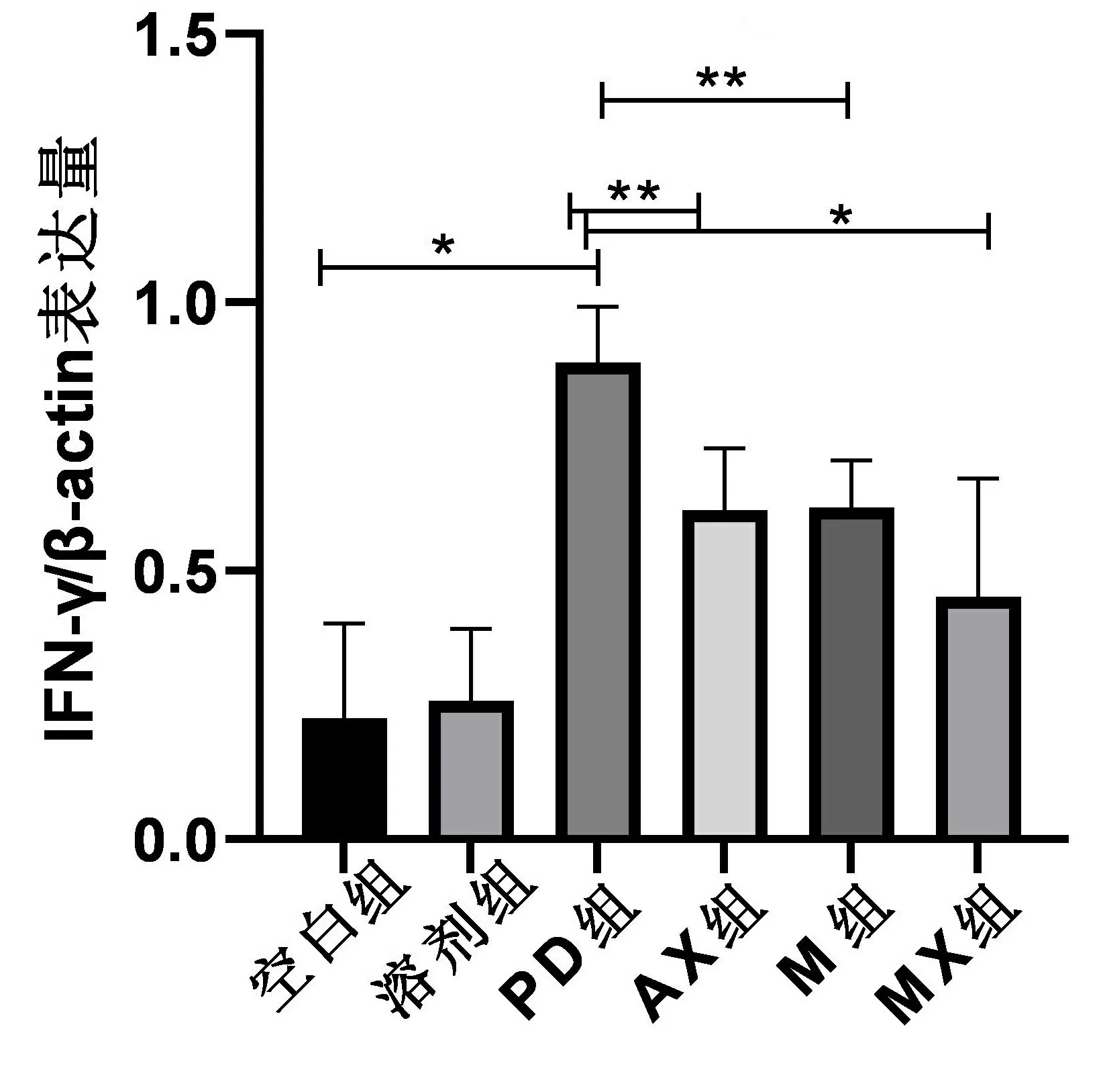
注:IFN-γ(γ干扰素);两组比较,*P<0.001,**P<0.05。
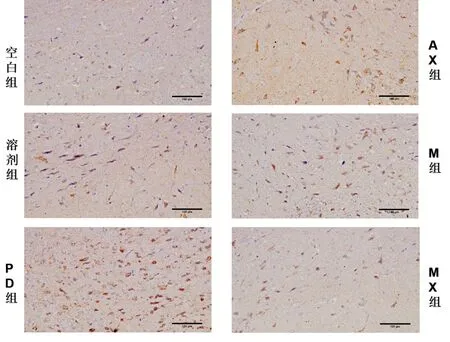
注:细胞核为蓝色,阳性表达为棕黄色。
3 讨论
PD是一种进行性神经退行性疾病,神经炎症反应是导致多巴胺能神经元神经变性的原因之一[9-10]。大量研究结果表明,炎症和氧化应激与PD发病机制之间的联系已被证实,大脑中促炎症细胞因子的水平升高,如TNF-α、IL-1β和IFN-γ,是PD的主要病理特征之一[11]。中枢神经系统的免疫细胞,如小胶质细胞和星形胶质细胞,通过释放因子来调节炎症,以及活性氧的形成[12]。这些因素的释放导致炎症反应,对神经元有毒性作用。因此,过度和不规则的小胶质细胞激活在PD病理中起着重要作用,促炎症细胞因子的释放,导致细胞凋亡,以及多巴胺能神经元的损失[4]。过去数年发表的大量关于炎症在多巴胺能神经元逐渐丧失中的作用的研究证实,神经炎症是PD致病的重要组成部分[13]。在动物模型中,已知农药鱼藤酮能诱导多巴胺能神经元的中度损伤,并再现PD的许多运动和非运动症状,包括周围病变、神经炎症、睡眠障碍,目前已是造PD大鼠模型的经典方法[14]。本研究采用连续颈背部皮下注射鱼藤酮溶剂于葵花油1.5 mg/(kg·d) ,每连续给药6 d后,停药1次,连续28 d,PD模型大鼠出现典型的毛色变黄变脏、弓背、拒捕减弱、震颤等表现则视为造模成功[15]。研究表明,AX是较为有效的免疫调节剂,还具有抗炎、抗氧化、降血糖和抗肿瘤的特性[16-17]。AX干预大鼠后抑制了NF-κB的表达[18-19], NF-κB信号通路与氧化应激和炎症反应密切相关[20],NF-κB可以改变炎症细胞因子如TNF-α和IL-1β的表达[19]。本研究中探讨了AX对PD动物模型脑内神经炎性损伤的保护作用,实验结果表明,神经毒性物质鱼藤酮诱导的PD模型脑内黑质纹状体小胶质细胞和星形胶质细胞的激活,促进血清中炎症因子TNF-α和IL-1β的释放,脑内黑质纹状体IL-1β和IFN-γ表达量增高。AX组、M组、MX组与PD组比较,血清中TNF-α、IL-1β的含量均降低,而且MX组与AX组、M组比较,其降低更为明显;血清中TNF-α在MX组与AX组比较中,差异有统计学意义。大脑内黑质纹状体WB结果显示,AX组、M组、MX组给予干预后IFN-γ蛋白相对的表达量均较低,而且MX组与AX组、M组比较,其降低较为明显;在行为学悬挂实验和爬杆实验中发现各组大鼠给予干预后症状明显改善,结果表明AX能有效地改善PD大鼠的运动症状及抑制炎症因子的释放。
本研究结果表明,AX联合美多芭能有效的抑制炎症因子TNF-α、IL-1β和IFN-γ的释放,减轻PD大鼠黑质纹状体神经元的损失,较好地改善PD的神经功能,为AX联合美多芭用于治疗PD的临床应用提供了新的靶点,同时为临床用药选择提供了新的思路。

