胰腺透明细胞变异型实性-假乳头状肿瘤1例并文献复习
李育刚,罗 艳,许晴晴
胰腺实性-假乳头状肿瘤(solid pseudopapillary neoplasm, SPN)是一种少见的胰腺肿瘤,透明细胞变异型实性-假乳头状肿瘤(clear cell variant of solid pseudopapillary neoplasm, ccSPN)是SPN的罕见变异型,其发病率低,国外文献仅报道10例。本文收集1例经手术切除及病理确诊的ccSPN,结合相关文献探讨其临床病理学特征、诊断、鉴别诊断,旨在提高临床和病理医师对ccSPN的认识水平。
1 材料与方法
1.1 临床资料患者女性,54岁,因腹痛入院。MRI示胰体尾部有一大小27 mm×24 mm结节状混杂信号影,其内见结节状T1WI低信号、T2WI高信号影(图1)。DWI上无明显弥散受限,增强后结节强化,腹膜后未见肿大淋巴结。于2021年1月20日行3D腹腔镜胰体尾肿物切除术。
1.2 方法手术切除标本经10%中性福尔马林固定,脱水,石蜡包埋,切片,HE染色,镜下观察。免疫组化染色采用EnVision两步法,抗体包括CK、vimentin、CD10、β-catenin、CD56、Syn、CgA、E-cadherin、Ki-67,均购自福州迈新公司。
2 结果
2.1 眼观胰腺组织大小5.0 cm×4.0 cm×2.5 cm,切开见一大小2.6 cm×2.5 cm×2 cm质硬肿块,呈暗红色,周围见钙化。
2.2 镜检镜下见肿瘤界尚清,瘤细胞体积小,形态温和,呈巢状或小梁状排列,大部分胞质内含大小不等的空泡或胞质完全空泡化(图2),甚至胞质完全透亮(图3),细胞核圆形或卵圆形,核仁不明显,未见明确核分裂象。瘤组织被透明变的纤维组织分隔,局部黏液样变;未见脉管神经侵犯。
2.3 免疫表型瘤细胞vimentin(图4)、CD10(图5)、β-catenin(图6)、CD56、Syn均阳性,CK、E-cadherin、CgA均阴性,Ki-67增殖指数约2%。
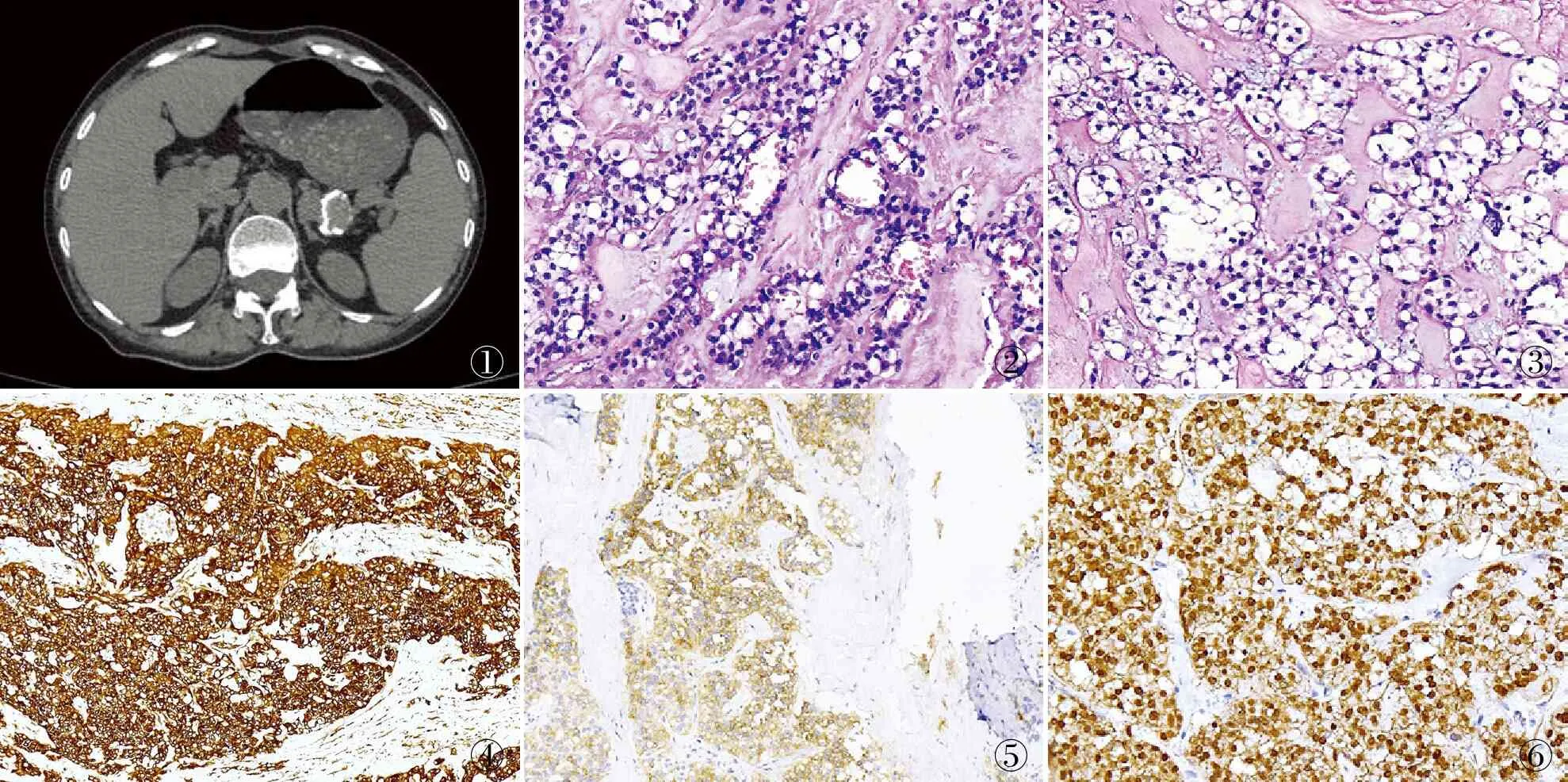
①②③④⑤⑥
2.4 病理诊断(胰体尾部)透明细胞变异型实性-假乳头状肿瘤,未见明确脉管神经侵犯。
2.5 随访患者随访时间1年,恢复良好,未见复发或转移。
3 讨论
SPN是一种少见的胰腺肿瘤[1],呈低度恶性,占胰腺原发肿瘤的1%~2%,可发生于任何年龄,多见于青春期及年轻女性(男女比为1 ∶9),平均年龄30岁。该肿瘤可在胰腺任何部位发生,以胰尾部略多见,其次为胰体尾部,偶可侵犯邻近组织,并可转移至肝、肺、皮肤等部位。临床可无症状或仅有腹部不适,实验室血清检查,如血淀粉酶、降钙素原和肿瘤标志物,如AFP、CEA、CA19-9、CA125等多正常。影像学检查可发现肿块,如MRI特征为肿块呈低密度,囊实混杂,界清,可见钙化。SPN发生机制尚未明确,有研究发现Wnt/β-catenin、Hedgehog、AR信号通路和上皮-间质转换相关基因参与其发生[2]。
SPN组织学显示其由囊性区、实性区、假乳头区[3]按不同比例组成,实性区瘤细胞呈弥漫分布,大小一致,圆形或卵圆形,胞质淡染,核卵圆形,核仁不明显;假乳头区瘤细胞被纤细的纤维血管分隔包绕成特征性的假乳头结构,该结构是重要的形态学诊断证据;囊性区大小不等,瘤细胞呈小梁状或腺泡状排列,常见不同程度的出血、坏死。ccSPN是SPN的罕见变异型,由Albores-Saavedra等[4]于2006年首次提出。该亚型最重要的形态特征是瘤细胞呈小梁状或弥漫分布,部分病例的假乳头结构不是其主要组织学结构,瘤细胞胞质内出现大小不等空泡,甚至胞质完全透亮,这些空泡不含糖原、脂质或黏液。超微病理学示这些空泡可能是滑面内质网和线粒体扩张所致。免疫表型:约50%的SPN中CK阳性,但CK7通常阴性;vimentin、α1-AT、β-catenin(胞核和胞质)、CD10、Cyclin D1常阳性,而E-cadherin胞膜阴性。有研究显示β-catenin编码基因CTNNB 13号外显子突变,导致单一氨基酸改变[5],使β-catenin和Cyclin D1在核内聚集;同时,细胞膜上E-cadherin受体消失[6],使β-catenin和Cyclin D1阳性,而E-cadherin胞膜阴性。CD56、Syn可阳性,一般CgA阴性。TFE3属于转录因子家族成员,在SPN中具有较高敏感性[7],但FISH检测未见染色体易位,其确切机制有待进一步分析。另外,CD200[8]、LEF1[9]、p504S[10]亦可在SPN中表达。国外文献报道10例和本例ccSPN的临床病理特征详见表1[4-5,11-15]。
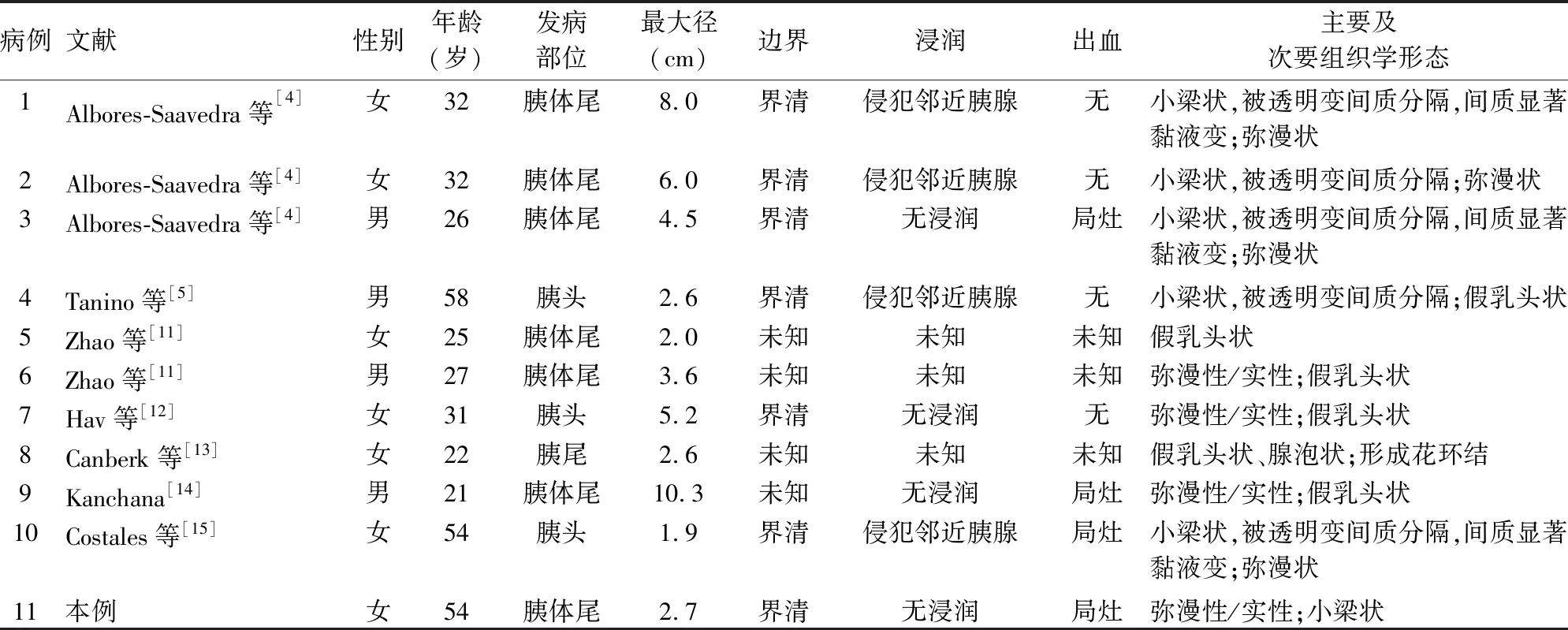
表1 11例胰腺透明细胞变异型实性-假乳头状肿瘤的临床病理特征
外科手术切除是SPN主要治疗手段,尽管多数患者预后尚可[16],但仍有5%~19%患者术后出现复发[17],1%~2%患者出现转移[14]。患者术后5、10年无瘤生存率分别为95.4%和93.7%[18]。多项研究尝试分析SPN复发转移的高危因素,如Kang等[18]研究发现肿瘤最大径超过8 cm、瘤细胞明显异型、脉管神经侵犯、胰周脂肪侵犯和肿瘤临床分期(4期,根据AJCC第8版分期标准)与SPN复发和转移密切相关,但单独一项镜下特征无法预测复发的可能性。Estrella等[19]发现肿瘤侵犯肌型血管、肿瘤分期(5期,根据欧洲内分泌肿瘤分期标准)是独立预后因子。尽管ccSPN病例数较少,但若出现经典型SPN可能的预后危险因素(如脉管神经侵犯、胰周侵犯等),仍需在病理报告中注明,并进行密切的追踪随访。
ccSPN因其独特的形态学特征,其鉴别诊断与经典型SPN有所不同。(1)胰腺透明细胞变异型神经内分泌肿瘤:该肿瘤瘤细胞标志物CgA、Syn、β-catenin均阴性。(2)透明细胞变异型胰腺导管腺癌:瘤细胞明显异型,免疫组化标记CK7阳性,CgA、Syn均阴性[20]。(3)血管周围上皮样细胞肿瘤:肿瘤具有肌源性和黑色素双向分化特点,免疫组化标记SMA、HMB-45、Melan A均阳性,CK、CgA均阴性。(4)转移性肾透明细胞癌:有肾肿瘤病史,免疫组化标记CD10、EMA、PAX-2、RCC均阳性,CgA、Syn均阴性。(5)转移性气球样黑色素瘤:黑色素标志物阳性,如HMB-45、S-100、Melan A、SOX10均阳性。(6)腺泡细胞癌:结节状,界不清,无SPN假乳头结构,核分裂象显著,免疫组化标记β-catenin核阳性、CD56阴性。
综上所述,ccSPN是胰腺SPN的一种罕见变异型,手术切除是主要治疗手段,病理组织学诊断及鉴别诊断与经典型SPN不同,在日常病理诊断工作中应防止误诊。

