酶催化合成L- 茶氨酸的纯化研究进展
许锦雄,杜阳吉,王钰佳
(广东广业清怡食品科技股份有限公司,广东 广州 511400)
L - 茶氨酸属于酰胺类化合物,分子式为C7H14N2O3,是茶叶中独有的游离氨基酸。大量研究结果表明L- 茶氨酸具有多种重要的生理功能,所以在食品、保健品、医药等领域得到广泛的应用。目前市场上茶氨酸来源于化学合成、生物酶发酵,以及从天然茶树中提取[1]。化学合成反应剧烈,合成过程中使用的有毒溶剂,且会产生D - 茶氨酸。从天然茶树中提取L - 茶氨酸的效率最低,价格最贵。生物酶催化合成L - 茶氨酸反应温和,且不会产生D- 茶氨酸。参考国内外有关文献对L- 茶氨酸的酶法合成进行了概括,且重点对酶催化合成L - 茶氨酸的纯化进行综述,以期能对L - 茶氨酸的研究开发和综合利用提供理论依据,为其生物合成工业化生产提供参考[2]。
1 酶催化合成L- 茶氨酸
在茶树中,L - 茶氨酸合成酶(Theanine synthetase,TS) 在ATP 供能的条件下,催化L - 谷氨酸和乙胺合成L- 茶氨酸。Sasaoka 等人对L- 茶氨酸合成酶的研究表明该酶对乙胺具有高亲合力,但易分解且难纯化,L- 茶氨酸的体外合成是不合适的,因而制约了它在L- 茶氨酸的体外合成。
L- 茶氨酸合成酶催化合成L- 茶氨酸见图1。

图1 L- 茶氨酸合成酶催化合成L- 茶氨酸
随着基因工程技术的进步,科研人员对酶促体外合成L- 茶氨酸进行了技术创新。
L- 茶氨酸体外合成见图2。
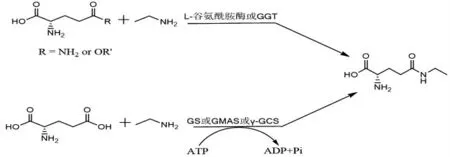
图2 L- 茶氨酸体外合成
1.1 L- 谷酰胺酸酶催化
L- 谷氨酰胺酶是一种酰胺基水解酶,催化L -谷氨酰胺的γ - 酰胺键水解为L- 谷氨酸和游离氨,在原核和真核生物中广泛分布。
L- 谷氨酰胺酶催化见图3。

图3 L- 谷氨酰胺酶催化
孙帅[3]利用L- 谷酰胺酶催化L- 谷氨酰胺,系统以谷氨酰胺作为γ - 谷氨酰基给体,在反应过程中,谷氨酰胺易水解为谷氨酸。因此需要调整反应底物中的谷氨酰胺和乙胺的配比,以确保茶氨酸的产率最大化。研究得到谷氨酰胺酶催化合成茶氨酸的最适反应条件:反应体系(0.3 mol/L 谷氨酰胺,1.8 mol/L乙胺溶液,2 U 粗酶液,1 mmol/L Ca2+溶液,pH 值9.8,浓缩1.3 倍),46 ℃下反应6 h[3-5]。从分析结果看,谷氨酰胺酶法合成茶氨酸的最佳工艺条件产率仅为0.239 g/L,这与茶氨酸的工业化生产的要求有很大差距。
1.2 γ - 谷氨酰转肽酶(GGT) 催化
GGT 是一种能同时催化供体和受体基质的双底物酶,在不同的生物源中具有相似的催化性质和特异性。GGT 的催化机理是通过向受体基质中的γ -谷氨酰基进行传递。在进行催化反应时,常采用2 个步骤进行,第一步用含有γ - 谷氨酰的化合物与对应的谷氨酰基结合,形成酶复合体;第二步,将结合的谷氨酰基转移到对应的受体基质上,如氨基酸、乙胺、水等。
γ - 谷氨酰转肽酶(GGT) 催化见图4。
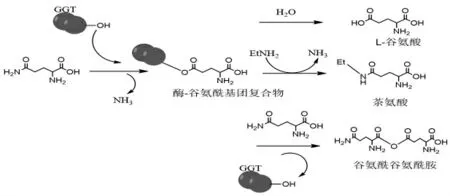
图4 γ - 谷氨酰转肽酶(GGT) 催化
从图4 可以看出,在这一过程中, GGT 对不同的受体底物进行了不同的反应。当以乙胺为受体,产生了转肽,从而生成了茶氨酸;在供体基质L-Gln同时充当受体的情况下,会产生自转肽反应;当催化剂受体为水分子时,最终为水解反应。
刘栓英,傅嘉懿,吕晶晶,李依韦等人,和斐等人,Komera Irene 等人,黄锋等人[6-12]用GGT 催化L- 谷氨酰胺与乙胺合成茶氨酸。在35 ℃,pH 值为10.0,0.2 mol/L L - 谷氨酰胺和2 mol/L 乙胺在酶质量浓度为1.0 U/mL 条件下反应得到茶氨酸38.33 g/L。通过分批加料茶氨酸产量可达58.73 g/L,茶氨酸的产率达60%。该方法可以运用在茶氨酸的工业化生产上,由于副产物较多,后续的纯化分离具有挑战性。
1.3 L- 谷氨酰胺合成酶(GS) 催化合成
GS(L- 谷氨酰胺合成酶) 以L- 谷氨酸盐和游离铵盐为原料催化合成L - 茶氨酸,同时通过三磷酸腺苷(ATP) 水解提供能量辅助反应的进行。从Pseudomonastaetrolens Y-30 中提取的GS 经过纯化后具有生产L - 茶氨酸的能力。编码P.taetrolens Y-30中GS 的基因序列已被测出,该序列能够在大肠杆菌中成功表达。重组的GS 酶与原本GS 酶具有相同特性,但酶产量比原菌高出30 倍[13]。
GS 的催化反应要求持续供给ATP,所以还需要开发一种高效的ATP 再生技术用于L - 茶氨酸的GS 合成。在最佳工艺条件下,GS 催化合成L - 茶氨酸的收率达到28%。该收率较低,不适合工业化生产。
1.4 γ- 谷氨酰甲胺合成酶(GMAS) 催化合成
研究表明,GMAS 显示出了比GS 更高的结合乙胺的能力。M.mays NO.9 来源的GMAS 在ATP 持续供能的条件下,生产L- 茶氨酸产率可达到110 g/L,远超于P.taetrolens Y-30 来源的GS。此外,利用固定化酶的技术将该酶固定化在硅藻土等载体上可以持续进行6 次的高转化率反应生产L- 茶氨酸。
朱新雅[14]利用GMAS 酶在温度32 ℃,pH 值8.0,以L - 谷氨酸和乙胺的加入量均为150 mmol/L 作为反应物,细胞湿重为50 g/L,反应8 h 的条件下合成茶氨酸。此外还需在体系中加入50 mmol/L 硫酸镁,100 mmol/L 六偏磷酸钠,5 mmol/L ATP 用于ATP 循环的再生。最终,L- 茶氨酸的产量为20.68 g/L,转化率为79.24%[15]。该方法虽然要加入ATP,但目前ATP 再生系统工业化应用成熟,加上其茶氨酸转化率高,因此目前产业化生产茶氨酸主要利用该方法。
2 酶催化合成L- 茶氨酸的纯化
为了酶的稳定催化,需要在反应体系中加入大量的磷酸盐、金属阳离子(Mg2+、Ca2+等),以及反应原料乙胺盐酸盐。由此可得,反应液的主要成分为阴阳离子,一部分变性蛋白、茶氨酸、谷氨酸。由于所有的物质均溶于水且不溶于大部分的有机溶剂,所以酶催化合成法比传统的化学合成后续纯化十分困难。根据反应液的组成,可以将纯化过程分为3 步,分别是前处理过滤蛋白、细菌、脱色,除盐工艺,精制茶氨酸。下面根据该3 步进行综述。
2.1 前处理纯化
酶通过工程菌发酵后破壁得到,因此反应液中存在破碎的细胞器、除工程菌外的杂菌以及部分变形蛋白。这些杂质大部分不溶于水,因此可以通过简单的物理分离除去。
2.1.1 离心过滤
离心过滤法是最简单的分离方法,在工业生产上运用成熟。通过离心,可以将大部分不溶性固体分离出来,再进行过滤可以得到清液。该方法分离速度快,且产物无损耗。其缺点也十分明显,无法除去杂菌、色素及部分水溶性蛋白。通常在过滤后还需加入活性炭进行脱色处理,但杂菌仍然无法除干净。
2.1.2 絮凝法
絮凝法用于除菌十分成熟,在谷氨酸的生产用十分常见,运用也十分成熟。通过加入化学絮凝剂,使得细菌等杂质被絮凝剂捕获,经过过滤后可除去。然而絮凝法操作起来比较繁琐,有时会产生毒性物质。而色素也无法通过该步骤完全除去[16]。
2.1.3 膜过滤
随着材料学的不断发展,诞生了膜过滤这一方法。微滤膜具高效分离0.1~10.0 μm 粒度的优点,操作简单、绿色环保,适合用于L - 茶氨酸发酵液的菌体分离。超滤法也能用于分离分子量大于5 kDa的物质[17]。L- 茶氨酸发酵液大部分通过微滤膜和超滤膜组合进行初步分离提取。
膜通量是衡量膜性能的一个重要指标,即单位时间内通过单位膜面积的滤过液体积。由于膜孔直径较小,在连续运行过程中容易出现堵塞,导致膜通量降低。影响膜通量的因素有许多,包括膜本身的性质。
发酵液体最大的特性就是黏度高,随着黏度的增加,薄膜的渗透能力逐渐降低。随着温度的升高,其黏度也随之下降;但温度太高,微滤膜就会变得不稳定,细菌和其他不稳定的蛋白质会堵塞过滤膜,导致膜通量降低。
一般情况下,微滤膜的分离压力为0.03~0.03 MPa。在过滤开始后,在滤膜的表面会逐渐形成少量的胶体,如果压力差太小,过膜的动力就会减弱,从而使膜通量下降;如果压差太大,凝胶层会变厚,密度增大,不仅直接堵塞过滤膜,还抵消外部的压力,导致膜通量下降。
膜过滤的原料易得,且更换率低,虽仍然无法去除色素,但在众多初级分离方法中分离效率最高。
2.2 除盐纯化
为了酶的催化效率,反应体系中加入了大量的辅助盐,所以体系中杂质最多、最难除去的就是盐,除盐步骤对于分离纯化至关重要。由于茶氨酸溶于水且难溶于有机溶剂,因此简单萃取不能进行除盐。目前的除盐方法主要分2 种,一是衍生法,即对茶氨酸进行化学修饰来改变其性状使得溶于某种溶剂或不溶于水,以此达到除盐的目的;二是物理方法,即通过离子交换树脂、大孔树脂、C18反向色谱柱、电渗析等方法,分离盐和茶氨酸。
2.2.1 沉淀法除盐
利用特殊的有机试剂,按不同氨基酸的性质进行沉淀,实现与其他杂质的分离。在酶催化合成体系也适用,袁华等人[18]通过往加热反应液至70 ℃,调节pH 值至中性,加入碱式碳酸铜得到紫色沉淀物,沉淀物用1 mol/L H2SO4溶解得到茶氨酸、碳酸铜混合液,通入H2S 气体除去铜离子,加入适量氢氧化钡沉淀硫酸根离子后得到茶氨酸[19]。
朱新雅[14]根据反应液的组成,计算后加入适量氯化铵,生成鸟粪石(Mg(NH4)PO4·6H2O),除去反应液中的磷酸根离子、镁离子。再通过重结晶得到茶氨酸纯品。
2.2.2 离子交换树脂除盐
工业中常用的氨基酸分离方法是离子交换树脂法。茶氨酸的等电点是5.6 左右,因此可以根据要除去杂质的酸碱性选择合适的离子交换树脂及洗脱液,纯化过程中不需要用到化学溶剂,绿色环保。
(1) 阳离子交换树脂。茶氨酸是典型的两性电解质,在pH 值低于5.6 的溶液中带正电荷,从而能与阳离子树脂上的交换基团结合。当pH 值大于5.6,茶氨酸失去正电荷从树脂交换基团上脱落,达到除盐目的[20-22]。
对D301、D380、724、732 这4 种常用的树脂进行了静态吸附试验。724、732 型树脂的再生性能比D301、D380 型要好,4 种树脂中732 型树脂吸附容量最大,同时吸附率也最高。
不同离子交换树脂的交换特性见表1。

表1 不同离子交换树脂的交换特性
使用阳离子交换树脂需注意,溶液pH 值过高会导致阳离子树脂出现渗漏情况,但L- 茶氨酸在pH值低于3.0 的溶液中很容易分解。上样流速过高时,树脂出现了渗漏,且洗脱液中L - 茶氨酸的浓度较低。洗脱液的氨水浓度太低时,洗脱曲线出峰滞后,峰宽较大,峰值也较小。
(2) 阴离子交换树脂。阴离子交换树脂纯化原理与阳离子交换树脂类似,当pH 值大于其等电点时,氨基酸带负电荷,并与树脂上的交换基团相结合吸附,当pH 值下降时,氨基酸的负离子键作用会减弱,从而被洗脱。
使用阴离子交换树脂需注意,当pH 值>8 时,吸附力明显增加;pH 值8.5 时吸附最大;之后随着pH 值的进一步增加,交换容量有所降低。
离子交换的一个重要参数是固液两相的接触时间,如果上样液流速过快,来不及与树脂交换,就会导致交换区高度拉长,发生渗漏现象。实际操作中流速控制为0.5 BV/h 比较适宜[23-27]。
(3) 离子交换树脂结语。离子交换树脂除盐是最常用的手段,工业化应用十分成熟。一般反应液中包含盐的种类较多,需要同时使用阴阳交换树脂进行除盐,可以将2 个系统进行串联,即能完成除盐。
但是需要注意离子交换树脂的吸附量,一旦纯化产品浓度大大超出,则无法进行纯化。若需进行除盐则需要对样品进行稀释,而稀释会导致浓缩样品的蒸汽用量增加。所以离子交换树脂除盐只适合盐含量不高的样品,否则缺乏经济性。
2.2.3 大孔吸附树脂除盐
大孔树脂不含离子交换基,但其微珠具有与被分离物体的分子大小相符的吸收位置和扩散通路,常呈白色球形,按其分子结构可划分为无极性和极性2 种类型。高聚霞[31]发明了一种利用特制弱极性的大孔树脂(JAD-1000) 吸附柱层析分离茶氨酸,用pH 值3.0 的洗脱液洗脱[28]。
D401 型螯合树脂是一种氨基羧酸树脂,含有亚氨基二乙酸基,能够与二价金属离子形成稳定的络合结构,与金属结合能力强,吸附能力强,操作简单[29]。刘步云等人[28]利用该树脂除去反应液中的Cu2+。在试验考查的pH 值范围内,树脂对Cu2+的吸附量相差不大,且对茶氨酸的吸附量均很小,表明该树脂在较宽的pH 值范围内对Cu2+均具有很好的吸附选择性[29]。
由于大孔树脂并不能像离子交换树脂定向吸附,因此其除盐效果十分局限。体现在除盐种类的局限性,除盐效率低。因此利用大孔树脂吸附除盐后还需要再进一步纯化,达不到产业化的要求。
2.2.4 电渗析除盐
电渗析法是一种将阴离子交换膜和阳离子交换膜交替放置在正、负离子交换膜间,由专用的隔板分隔,构成脱盐淡化和浓缩两套体系。在直流电场的作用下,通过电位差作为驱动力,通过离子交换膜的选择性渗透,使溶液与溶液分离,达到浓缩、淡化、精制和精制的目的。
当氨基酸溶液的pH 值在其等电点时,氨基酸溶液呈电中性,在直流电场中不发生移动;当溶液的pH 值小于等电点时,氨基酸呈电正性,在直流电场中可通过阳离子交换膜(C) 向阴极移动;当氨基酸溶液的pH 值大于等电点时,氨基酸呈电负性,在直流电场中可通过阴离子交换膜向阳极移动。因此可以采用电渗析技术对氨基酸溶液进行分离提纯。
陈希书等人[30]利用电渗析技术对茶氨酸发酵液进行精制,具有较好的脱盐效果。集中不同初始电导率情况下脱盐时,脱盐率都能达到85%左右,脱盐效果比较明显;在流量不同的情况下,脱盐率也能达到要求,且脱盐效果比较明显,均具有一定的可行性。因此茶氨酸的电渗析脱盐过程整体是可行的。
电渗析技术原理与离子交换树脂相类似,但没有离子交换树脂的吸附容量的局限性,对含盐量高的样品也能进行纯化,且不需要加入洗脱剂。分离过程利用电能作为动力,绿色环保。它还能通过多增加加滤膜,可以达到浓缩、脱色的效果。电渗析虽然会损失部分样品,但对比其他除盐方式,其纯化效率也很高。
2.2.5 C18反相色谱柱
反相色谱(RPC) 是指以非极性的反相介质为固定相,极性有机溶剂的水溶液为流动相,利用溶质极性(疏水性) 差异对溶质分离纯化。C18色谱柱常用在氨基酸的检测上,利用水作流动相,能够将茶氨酸与其他的盐分离出来。
高聚霞[31]制备耐中压的钢化玻璃结构层析柱(40 mm×800 mm),填料是粒度30 μm 左右的C18。利用该层析柱,对样品进行除盐,得到茶氨酸质量分数98.2%,回收率72.5%。目前,已有企业利用C18反相色谱柱技术进行茶氨酸的工业化生产。
C18反相色谱柱技术目前主要用在HPLC 上,国外也有不少企业利用该技术进行分离。其对含盐量要求不高,不需要额外加入溶剂,利用柱塞泵提供分离动力,绿色环保。该填料可以通过有机溶剂进行活化,活化后可重复利用,使用寿命长,维护成本低。虽然其前期投入成本很高,但纯化过程产品无损耗,纯化效率最高。
2.3 精制茶氨酸
通过除盐后的茶氨酸含量大多达到98%左右,因此需要对其进一步的精制才能达标。精制步骤则主要是为了将水溶液的茶氨酸取出,因此大多数通过改变溶液极性,或浓缩得到产品。
2.3.1 有机溶剂沉析
因为茶氨酸在有机溶剂中溶解度低,加入乙醇、甲醇、丙酮、乙酸乙酯改变溶剂极性后,茶氨酸会析出,再经过滤,烘干即可得到及格产品。
该方法虽然十分简单,但由于有机溶剂的残留问题,通常使用乙醇进行沉析。
2.3.2 重结晶
重结晶原理与上一种方法类似,一般只能用乙醇、甲醇进行重结晶。重结晶使用的溶剂十分巨大,不具有经济性。但重结晶得到的产品是晶体,是所有方法中堆积密度最高、不易起尘的。因此,重结晶得到的产品售价更高。
2.3.3 冻干
冷冻干燥是指先对溶液进行降温冻结成固体,在真空的条件下使固态水直接升华分离,而物质本身留在冻结时的冰架中,因此它干燥后体积不变。该方法得到的产品不会因为加热过高引起产品变黄、炭化的问题。
3 结语
由于高效、节能、环境友好等优点,酶催化合成L - 茶氨酸日益受到青睐,目前占具25%的市场份额。
在传统发酵工业中,分离纯化的投入占据整个工厂投资的60%,而基因重组的工程菌发酵过程,分离纯化部分的投入占据整个投资的80%~90%。因此,分离纯化技术成为茶氨酸能否进行工业化生产的关键点。目前,茶氨酸工业化生产并不采用单一的分离纯化技术,而是多种分离纯化技术的结合,随着分离纯化技术的不断发展,茶氨酸的分离越来越高效。
工业化纯化茶氨酸举例见图5。

图5 工业化纯化茶氨酸举例

