外泌体在青光眼诊疗中的作用研究进展
酆欣婷 综述 张旭 审校
南昌大学附属眼科医院 南昌大学眼视光学院,南昌 330006
外泌体是目前发现最小的一种细胞外囊泡,广泛分布于人体血液、唾液、脑脊液、尿液等各种体液中[1]。由于外泌体在人生理状态和疾病中的重要作用,以及在疾病诊疗中潜在的临床应用价值,近年来对其研究越来越多。青光眼是全球首位不可逆性致盲眼病,其特征是视网膜神经节细胞(retinal ganglion cells,RGCs)及其轴突进行性丧失,并伴随视野缺损[2]。原发性青光眼早期症状隐匿,不易被发现,在我国一半以上的患者被诊断为青光眼时即有严重视野缺损[3],错失了最佳治疗时机,这提示早期诊断对于降低视力损害的风险至关重要。研究表明,外泌体是参与青光眼发病及进展的重要介质,同时可能作为青光眼早期诊断的潜在标志物及治疗载体。此类纳米级细胞外囊泡可以穿过生物屏障,直接靶向目标受体细胞,递送治疗分子,可能为青光眼视神经退行性病变的治疗提供新思路。本文就外泌体在青光眼发生和诊疗中的研究进展进行综述。
1 外泌体概述
1.1 外泌体的基本特征
外泌体是一类直径为40~160 nm(平均100 nm)的细胞外囊泡[4],内含DNA、RNA、蛋白质、脂质、细胞质等多种细胞成分。人体绝大多数细胞都可产生外泌体,其广泛存在于各种体液中[1]。外泌体起源于细胞膜内陷形成的早期内体,而后成熟为晚期内体并转化为多泡小体(multivesicular bodies,MVBs),后者含有腔内囊泡(即未来的外泌体),最终MVBs与细胞膜融合并通过胞吐作用释放外泌体[4]。
外泌体的生物发生途径包括转运必需内体分选复合物(endosomal sorting complexes required for transport,ESCRT)依赖途径和非ESCRT依赖途径,以实现外泌体内容物的特定分选[5]。外泌体在分泌后,可以通过与靶细胞膜融合,将其内容物整合到靶细胞中;或通过受体介导的内吞作用、巨胞饮作用、吞噬作用等多种形式的内吞作用将其携带的各种信息传递给靶细胞(受体细胞);也可以直接与靶细胞通过受体-配体相互作用传递信号,以实现细胞间通讯[6](图1)。此外,外泌体的组成、生物发生可以反映分泌细胞的状态,亦可调节细胞内外环境[7]。
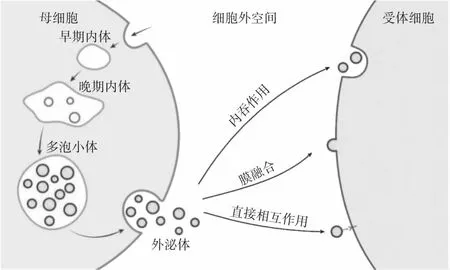
图1 外泌体的产生和摄取过程
1.2 外泌体的生物学功能
外泌体具有多种生物学功能,因细胞来源不同而功能各异,包括:(1)信号转导 信号转导是外泌体最基本且重要的生物学功能。外泌体作为细胞通讯的载体,可将其内容物运输到邻近或远处细胞,从而调节各种生理和病理过程[7]。(2)炎症调节 外泌体可促进/抑制炎症小体活化[8],干细胞源性外泌体抑制炎症小体活化,然而免疫细胞源性外泌体则引发炎症小体的激活,提示外泌体可作为炎症反应相关疾病的治疗工具。(3)免疫调节 免疫细胞源性外泌体可促进/减弱免疫反应,取决于外泌体组成、诱导产生的细胞环境,使外泌体在免疫应答、免疫赦免等方面发挥重要作用[9]。(4)修复再生 外泌体参与神经血管再生,促进轴突生长[10],有利于神经再生及功能恢复。(5)自噬调节 不同来源的外泌体可促进/抑制自噬[11]。Rong等[12]研究表明,在脊髓损伤的大鼠模型中,神经干细胞衍生的外泌体通过促进自噬减少神经元凋亡,抑制神经炎症。此外,外泌体还可作为疾病的生物标志物及治疗载体。
1.3 外泌体与眼部组织的免疫调节
外泌体可调节免疫反应,而眼部被视为类似胎盘和中枢神经系统的免疫赦免组织结构,血-视网膜屏障释放的外泌体可能在调节眼的免疫赦免中发挥重要作用[13]。廖志雄等[14]研究表明,兔房水中外泌体能够明显抑制T淋巴细胞增生、免疫抑制分子肿瘤坏死因子β(tumor necrosis factor-β,TNF-β)表达,故推测外泌体很可能参与了眼球免疫耐受的维持。另一项研究中,Knickelbein等[15]证实人视网膜色素上皮细胞衍生的外泌体可根据炎症环境调节单核细胞表型,在炎症因子的刺激下可抑制单核细胞的免疫活性,从而减少潜在的免疫反应损害。免疫炎症与青光眼发病有关,外泌体的免疫作用广泛,但在眼部组织中多表现为负向免疫调节作用,有利于减少免疫炎症攻击对眼部组织造成的损害。但阐明外泌体如何在生理和病理状态下调节眼的免疫功能仍需进一步研究。
2 外泌体与青光眼的发病机制
2.1 外泌体与小梁网细胞调节
目前,青光眼确切的发病机制尚未阐明,但病理性眼压升高是其发病的主要危险因素[16]。外泌体可通过运输青光眼相关蛋白、调节Wnt信号通路、影响细胞外基质(extracellular matrix,ECM)周转等参与调节小梁网细胞功能及房水动力学,进而影响眼压[17]。(1)运输青光眼相关蛋白 Myocilin是一种青光眼相关分泌蛋白,其突变导致眼压升高[18]。Stamer等[19]在小梁网细胞衍生的外泌体中检测到myocilin,且与外泌体结合排出细胞。Myocilin通过外泌体释放途径调节眼压,参与青光眼发病机制,提示外泌体在眼压控制中的作用。(2)调节Wnt信号通路 Tabak等[20]研究发现,无色素睫状上皮细胞(non-pigment ciliary epithelial cells,NPCE)衍生的外泌体在小梁网细胞中干扰Wnt信号传导,通过使GSK3β磷酸化减弱和β-catenin的表达水平降低来影响小梁网钙黏蛋白,导致房水流出阻力增加和眼压升高,且只有在低浓度外泌体的刺激下才能产生这种效应。此外,Lerner等[17]证明NPCE外泌体中富含Wnt信号转导的负调节剂微小RNA-29b(microRNA-29b,miR-29b)。(3)影响ECM周转 研究表明,小梁网通过侵袭性伪足结构周转ECM并维持房水流动的通道,而外泌体定位于侵袭性伪足结构中[21],提示外泌体在介导细胞-ECM相互作用中发挥重要作用。以上研究表明外泌体可从不同途径影响小梁网细胞功能,从而参与青光眼的发生和发展,进一步探讨外泌体信号通路有助于发现针对房水引流系统的青光眼治疗新靶点。
2.2 外泌体与视网膜神经炎症
炎症已被证明在青光眼的发病中起重要作用[22]。小胶质细胞作为视网膜的免疫活性细胞,在青光眼发病中的作用也进行了一些研究。Aires等[23]证明反应性小胶质细胞介导的慢性神经炎症在青光眼病理学中起作用,暴露于高静水压的小胶质细胞产生的外泌体促进炎症细胞因子的产生。将上述过程中产生的外泌体注射到C57BL/6J小鼠的玻璃体腔中,观察到视网膜小胶质细胞的持续激活,介导细胞死亡,从而减少RGCs数量,但来自对照组小胶质细胞的外泌体却无法诱发视网膜炎症和细胞死亡。提示小胶质细胞的外泌体在眼压升高的情况下可传递炎症信号,导致青光眼疾病条件下的视网膜变性。这提示通过外泌体阻碍小胶质细胞通讯可发挥神经保护作用,阻止疾病进展的可能性。未来可通过外泌体将抗炎药物输送到小胶质细胞中,抑制神经炎症反应。
青光眼与中枢神经系统神经退行性疾病的一个共同特征是慢性神经炎症[22]。与在青光眼模型中的发现类似,大脑受到有害刺激后,小胶质细胞会释放与其他小胶质细胞相互作用的外泌体,导致神经炎症环境的扩大[24]。病理性tau蛋白的沉积是阿尔茨海默病的主要标志,该现象也在青光眼患者的视网膜中被发现[25]。研究表明,小胶质细胞可通过释放外泌体传播病理性tau蛋白,而抑制外泌体生成可显著降低病理性tau蛋白的传播,从而减少在健康细胞中的沉积[26]。以上研究提示,由小胶质细胞衍生的外泌体可能通过介导慢性神经炎症参与神经退行性疾病的发生。
3 外泌体与青光眼的诊断
3.1 泪液中的外泌体
外泌体在泪液、房水、玻璃体、血液中含量丰富[1]。近年来,随着研究的不断深入,有研究者认为外泌体可作为预测疾病理想的低侵袭性生物学诊断标志物[27]。泪液是反映眼部健康或疾病相关的重要体液,其成分变化受青光眼影响,视网膜损伤后3 d即检测到小鼠泪腺基因表达的改变[28],提示泪液可在早期反映青光眼的病理变化。而泪液中外泌体含量丰富并稳定存在[7],泪液外泌体研究可显著提高泪液生物标志物检测的敏感性[29]。鉴于其简单且无创的采样过程,未来可找出泪液外泌体中差异性表达的物质,作为青光眼早期诊断的候选生物标志物,从而早期诊断青光眼,有利于改善患者预后并减轻医疗负担。
3.2 房水中的外泌体
眼内房水处于动态循环中,其成分与眼球局部生理病理环境密切相关,房水中外泌体主要来自于眼内组织[30],这提高了利用房水诊断眼病的可行性。房水由睫状体产生,主要经过小梁网流出,外泌体在两者之间的通讯中发挥作用[31]。Dismuke等[31]首次证明外泌体是房水的重要成分之一,房水中含有特征性外泌体RNA,这为开发用于疾病诊断的外泌体提供了重要信息。Sacc等[32]对青光眼和非青光眼患者的房水进行蛋白质组学分析,发现青光眼患者房水中有13种蛋白质表达水平显著升高,其中热休克蛋白90可介导外泌体的释放[33]。以上研究提示,房水中的外泌体及其RNA载荷或蛋白质可用作青光眼的诊断生物标志物。在此基础上,Hsu等[30]提供了一种基于微流控芯片的新型诊断技术,可以简化从房水中分离外泌体的程序,节省大量时间,这项技术的普及应用将有助于进行更多的房水分析研究,进而完善眼科检查。
3.3 玻璃体中的外泌体
一项对从人类获得的视网膜和玻璃体液样本进行蛋白质组学分析的研究发现,与年龄相当的非青光眼对照组相比,青光眼样本检测到差异调节的蛋白质,经典的补体途径相关蛋白被激活;另有蛋白通路分析表明,线粒体氧化磷酸化机制存在缺陷,这些蛋白质改变与炎症反应和线粒体功能障碍相关[34]。Zhao等[35]在人类玻璃体中检测到含有视网膜蛋白的外泌体,且发现玻璃体中外泌体含量丰富。这些研究支持了玻璃体作为青光眼诊断生物标志物的组织来源的可行性。未来,可能从玻璃体中分离出青光眼特异性外泌体,从而有助于疾病的诊断,也为玻璃体腔注射外泌体达到青光眼临床治疗效果提供了可能。
3.4 血液中的外泌体
血液是一种可到达全身的体液,相比于其他液体成分更为复杂。池在龙等[36]对231例原发性青光眼患者和120例对照者的血浆外泌体进行分析,发现6种miRNA在原发性青光眼患者血液分离出的外泌体中表达上调,其表达水平与青光眼的发生和发展相关。与上述miRNA发现相似的是,池在龙等[37]还在青光眼患者的血浆外泌体中发现长链非编码RNA TRAM2的差异表达。他们认为以上标志物对青光眼均有一定的诊断价值,且特异性和灵敏度高,适用于大规模的筛查。但由于血液受到全身各组织结构的影响,而眼是一个很小的器官,若能从血浆中分离纯化特定细胞来源(眼源性)的外泌体,将提高血浆外泌体用于诊断青光眼的说服力。
4 外泌体与青光眼的治疗
4.1 外泌体的神经保护作用
多项研究已证明天然干细胞源性外泌体对青光眼的治疗作用,可作为一种有效的神经保护疗法。Mead等[38]将骨髓间充质干细胞源性外泌体注射到视神经挤压模型大鼠的玻璃体中,发现外泌体在整个视网膜中迅速扩散,促进RGCs的存活及轴突再生,并有助于保留RGCs功能。他们还证明,外泌体产生的神经保护作用是通过miRNA依赖机制来实现的。外泌体将miRNA输送到RGCs中表达,导致新的蛋白质翻译,在敲除miRNA关键的效应分子Argonaute-2后,外泌体的治疗效果减弱。Liu等[39]研究表明,在阿尔茨海默病小鼠模型中,骨髓间充质干细胞源性外泌体可通过抑制小胶质细胞活化及其相关的神经炎症、上调突触相关蛋白和脑源性神经营养因子蛋白表达,发挥神经保护作用。除了显著的神经保护作用外,干细胞源性外泌体还可选择性下调炎性T细胞的信号通路,而不影响调节性T细胞的扩增和免疫抑制特性;且干细胞源性外泌体的神经保护作用可被TNF-α强化[40-41]。以上研究表明,干细胞源性外泌体不仅在免疫调节中发挥作用,而且在抑制炎症损害中起作用。
此外,Mathew等[42]研究表明,玻璃体腔注射干细胞源性外泌体后可迅速到达RGCs,为其提供神经营养蛋白,且外泌体在玻璃体内保留4周,以剂量依赖性和可饱和的方式与玻璃体结合。但Mead等[43]研究显示,外泌体只能防止RGCs功能的早期损害,而在青光眼病程的后期则不能防止RGCs功能损害[43]。以上外泌体神经保护作用的研究为临床给药提供了一定的依据。有趣的是,Mead等[44]发现,神经保护作用仅在接受骨髓间充质干细胞源性外泌体注射的动物中被观察到,而成纤维细胞衍生的外泌体无治疗效应,表明干细胞源性外泌体在RGCs存活和青光眼治疗中有特定的潜力。另外,脐带间充质干细胞、人类胚胎干细胞衍生的外泌体也展现出神经保护作用[45-46]。以上研究表明,外泌体在视神经保护和再生治疗中具有一定的潜力,且为外泌体的临床应用提供了许多有用的信息。
4.2 外泌体的递送作用
外泌体可跨越生物屏障,天然外泌体及工程化外泌体都可作为药物递送囊泡[7],且与游离药物相比,载药外泌体具有更好的疗效和更高的生物利用度[47],为眼部疾病药物治疗提供了新的思路。Mead等[38]研究发现,天然干细胞源性外泌体在大鼠玻璃体腔注射后1 h即可成功地将神经营养因子输送到受伤的RGCs,展现出外泌体作为治疗分子运载体的能力。而工程化外泌体作为极具应用前景的新一代药物递送囊泡,可以进一步提高外泌体的治疗效率、特异性及安全性[48]。工程化外泌体的修饰策略主要包括内容修饰和外膜修饰[49]。通过工程化外泌体,将外源性治疗药物,如小分子或核酸药物整合到外泌体中,然后递送到特定类型的细胞或组织中,可实现靶向药物递送,从而促进靶细胞的功能。综上,以上研究提示外泌体可成为治疗青光眼更有效的新工具,开辟无细胞疗法治疗青光眼的新时代。
5 外泌体在眼科的应用难点与优势
目前,外泌体在眼科领域中的临床研究仍较少,主要集中在基础研究方面。结合现有的研究结果,外泌体应用到临床还需克服以下问题:(1)动物实验结果表明,外泌体每周或每月注射才有治疗作用,其治疗作用是暂时的且依赖于重复注射[44]。(2)目前缺乏稳定的分离纯化方法[50]。(3)外泌体具有显著的异质性[4],质量控制是亟需解决的难题。外泌体用于青光眼治疗的优势:(1)外泌体对视网膜无毒性作用[51]。(2)外泌体是天然的细胞外囊泡,生物膜稳定性高,免疫原性低[6],可降低药物的清除率。(3)外泌体易于穿过生物屏障,给药方式灵活。将外泌体应用到眼科临床还需更多的实验验证,但外泌体表面蛋白使之具有靶向性,未来或可通过修饰外泌体使其靶向定位于视网膜神经元,实现高浓度冲击治疗,挽救视功能。
6 总结与展望
外泌体的多种生物学功能使其在复杂的青光眼病理变化中发挥重要作用,可将外泌体作为潜在的风险预测因子以补充现有的青光眼诊断策略及协助判断青光眼患者预后。此外,通过靶向修饰打造的工程化外泌体有望成为一种高效且安全的递送载体,有助于提高其诊断潜力和治疗效率。随着研究的深入,外泌体在青光眼中的应用及靶向治疗也将不断趋于成熟。今后外泌体在青光眼领域的研究也可围绕以下几个方面开展:将其作为青光眼早期诊断的标志物,助力青光眼的早期诊断、靶向治疗及改善预后;将外泌体作为转染载体,从而精密地调控目标蛋白的表达;对外泌体进行人工修饰,以锚定特定类型的靶细胞,精确地调节其功能。在精准医疗的时代,外泌体具有良好的眼科应用前景,有望成为青光眼诊治的新选择。
利益冲突所有作者均声明不存在利益冲突
志谢感谢南昌大学眼视光学院彭振对本文的指导

