黔产大青化学成分及其抗菌活性研究
霍晓敏, 李丽君, 冉坚强, 薛 站, 刘丽娜, 谭承建*
( 1. 贵州民族大学 民族医药学院, 贵阳 550025; 2. 贵州民族大学 化学工程学院, 贵阳 550025; 3. 贵州医科大学 生物与工程学院, 贵阳 550025 )
奶牛乳房炎是我国奶牛养殖业的常见疾病,主要是由金黄色葡萄球菌、链球菌、无乳链球菌等引起的炎症(王丽芳等,2020)。目前,奶牛乳房炎的防治主要依靠抗生素,但抗生素的长期滥用会引起耐药菌的产生,威胁公共卫生安全(徐鸿润等,2021)。临床上,中草药被广泛用于细菌感染、炎症消除等疾病的防治,因其毒副作用较小,且不易产生耐药性(张晓东等,2021),为抗奶牛乳房炎药物的研究提供了新思路。研究表明,中草药的天然有效成分可以直接抑制致病菌的生长繁殖,减弱其致病性,雪白睡莲花、蒲公英、连翘、金银花等提取物均对奶牛乳房炎的致病菌如金黄色葡萄球菌、大肠杆菌有明显的抑制作用(钟华晨等,2020;刘丹丹等,2021);中草药中皂苷类、黄酮类等天然活性成分可以通过影响炎症因子的分泌,增强免疫能力,抵御致病菌的入侵进而降低奶牛乳房炎的发病率(候昆等,2019)。
大青(Clerodendrumcyrtophyllum)又称路边青、山大青,为马鞭草科大青属植物,主要分布于我国华东、中南、西南(四川除外)各省区(裴鉴和陈守良,1982)。《本草纲目》中记载大青味苦性寒,有清热解毒的功效。在贵州省黔东南苗族地区,大青是一味常用的民族药物,苗医用大青的水煎液内服来治疗小儿感冒发烧,疱疹病毒感染如口疮、带状疱疹等疾病(陆科闵和王福荣,2006)。大青提取物具有一定的抗菌活性(白云霄等,2013),但其中的活性成分未被阐明。因此,为深入探究大青中抗菌活性成分,拟为大青抗奶牛乳房炎药物的研发提供基础研究数据。本研究以黔产大青为研究对象,依托民族医药研究平台,采用现代色谱分离手段、现代波谱学技术和现代药理学方法,拟探讨以下问题:(1)黔产大青乙醇提取物的化学成分;(2)分离得到的部分化合物的抗菌活性。
1 材料与方法
1.1 材料、仪器和试剂
1.1.1 材料 大青药材采自于贵州省贵定县云雾镇,经贵阳中医学院孙庆文教授鉴定为马鞭草科大青属植物大青(Clerodendrumcyrtophyllum)。凭证标本(GZQSY2015D45)存放于贵州民族大学天然药物化学实验室。乳房链球菌(Streptococcusuberis)、无乳链球菌(S.agalactiae)由广东省农业科学院提供。
1.1.2 仪器和试剂 Avance NEO400型核磁共振波谱仪(德国 BruKer 公司);Xevo G2-S QTof型质谱仪(美国 Waters 公司);UltiMate 3000型高效液相色谱仪(赛默飞世尔科技有限公司);XBridge BEH C18半制备型色谱柱(10 mm×250 mm,5 μm,美国 Waters 公司);Rotavapor R-3型数显旋转蒸发仪(瑞士步琦有限公司);LiChroperp RP-18(40~63 μm,德国 Merck 公司);Sephedex LH-20(瑞典 Pharmacia 公司);柱色谱硅胶(青岛海洋化工厂公司产品);ZF-6型三用紫外分析仪(上海嘉鹏科技有限公司);HZT-A1000型电子天平(福州闽衡电子仪器有限公司);DB-1型电热板(常州国华电器有限公司);全波长酶标仪(芬兰 Thermo 公司);全自动酶标仪(美国 BioTek 公司);MTT噻唑蓝(北京 Solarbio 生物科技有限公司);PBS磷酸缓冲液(北京 Solarbio 生物科技有限公司);SDS十二烷基硫酸钠(分析纯,美国 Sigma 公司);甲醇、二氯甲烷、石油醚、乙酸乙酯、正丁醇等分析纯试剂(成都科隆化学品有限公司);甲醇、乙腈等色谱纯试剂(上海星可高纯溶剂有限公司);显色剂为5%硫酸乙醇溶液。
1.2 方法
1.2.1 提取与分离 将25 kg干燥的大青(地上部分)粉碎,用95%乙醇热回流提取3次,每次2 h,提取液合并,经减压浓缩后得到粗浸膏1 136 g。粗浸膏用水混悬,得到悬浮液,然后依次用等体积的石油醚、二氯甲烷、正丁醇进行萃取,之后分别对其进行减压浓缩得到石油醚部位172 g,二氯甲烷部位41 g,正丁醇部位429 g,水部位373 g。
取石油醚部位103 g,经硅胶柱(石油醚∶乙酸乙酯=200∶1、100∶1、50∶1、20∶1、5∶1、1∶1)梯度洗脱,得到13个不同流分,石油醚∶乙酸乙酯=200∶1洗脱得到流分Fr.a,石油醚∶乙酸乙酯=100∶1洗脱得到流分Fr.b1-2,石油醚∶乙酸乙酯=50∶1洗脱得到流分Fr.c1-2,石油醚∶乙酸乙酯=20∶1洗脱得到流分Fr.d1-3,石油醚∶乙酸乙酯=5∶1洗脱得到流分Fr.e1-3,石油醚∶乙酸乙酯=1∶1洗脱得到流分Fr.f1-2。Fr.b1经反复重结晶得到化合物1(589.5 mg);Fr.b2经硅胶柱(石油醚∶乙酸乙酯=50∶1)、Sephadex LH-20 柱(二氯甲烷∶甲醇=1∶1)洗脱得到化合物2(8.4 mg)、3(10.2 mg)。Fr.d1经反复重结晶得到化合物4(114.2 mg);Fr.d2经硅胶柱(石油醚∶乙酸乙酯=30∶1)、Sephadex LH-20 柱(二氯甲烷∶甲醇=1∶1)洗脱得到化合物5(7.2 mg);Fr.d3经硅胶柱(石油醚∶乙酸乙酯=20∶1)洗脱得到化合物6(9.1 mg)。Fr.e2经硅胶柱(石油醚∶乙酸乙酯=10∶1)洗脱得到化合物7(9.8 mg)。Fr.f1经硅胶柱(二氯甲烷∶甲醇=30∶1)、2次Sephadex LH-20 柱(二氯甲烷∶甲醇=1∶1)洗脱得到化合物8(18.3 mg);Fr.f2经硅胶柱(二氯甲烷∶甲醇=30∶1)洗脱得到化合物9(52.1 mg)。
取正丁醇部位397 g,经大孔树脂D101柱以乙醇(30%、50%、70%、90%、100%)梯度洗脱,得到11个不同流分,30%乙醇洗脱流分Fr.A;50%乙醇洗脱流分Fr.B1-3;70%乙醇洗脱流分Fr.C1-4;90%乙醇洗脱流分Fr.D1-2;100%乙醇洗脱流分Fr.E。Fr.B2经反相RP-18柱分离,甲醇-水(35%~100%)梯度洗脱,得到Fr.B2-1~Fr.B2-4。取Fr.B2-3经2次Sephadex LH-20 柱(甲醇)洗脱,得到化合物11(11.7 mg);经半制备高效液相色谱(C18柱,水∶乙腈=78∶22)分离,得到化合物10(19.2 mg)。取Fr.B3经反相RP-18柱分离和甲醇-水(35%~100%)梯度洗脱,得到Fr.B3-1~Fr.B3-3,取Fr.B3-2经Sephadex LH-20 柱(甲醇)分离和硅胶(二氯甲烷∶甲醇=30∶1~1∶1)梯度洗脱,得到化合物12(27.4 mg)。Fr.C1经反相RP-18柱分离和甲醇-水(30%~100%)梯度洗脱,得到Fr.C1-1~Fr.C1-5。取Fr.C1-2经Sephadex LH-20 柱(甲醇)分离和半制备高效液相色谱(乙腈∶0.1%磷酸水溶液=18∶82)纯化后得到化合物13(21.1 mg)、14(15.3 mg)。Fr.C2经反相RP-18柱分离和甲醇-水(30%~100%)洗脱后,得到Fr.C2-1~Fr.C2-4。取Fr.C2-1经2次Sephadex LH-20 柱(二氯甲烷∶甲醇=1∶1)、硅胶柱(二氯甲烷∶甲醇=20∶1)洗脱得到化合物15(37.4 mg);取Fr.C2-2经Sephadex LH-20 柱(二氯甲烷∶甲醇=1∶1)、硅胶柱(二氯甲烷∶甲醇=12∶1)洗脱,反复重结晶得到化合物16(29.5 mg);取Fr.C2-3经两次Sephadex LH-20 柱(二氯甲烷∶甲醇=1∶1)、半制备高效液相色谱(水∶甲醇=56∶44)洗脱,得到化合物17(7.7 mg)。Fr.C3经反相RP-18柱分离和甲醇-水(35%~100%)洗脱后,得到Fr.C3-1~Fr.C3-4。取Fr.C3-3经Sephadex LH-20 柱(甲醇)、硅胶柱(二氯甲烷∶甲醇=20∶1)洗脱,得到化合物18(53.2 mg)。
1.2.2 抗菌活性实验 抗菌活性测定参考课题组前期建立的一种定量检测细菌活菌数的MTT方法(马林玉等,2021),取适量乳房链球菌、无乳链球菌分别接种于肉汤培养基,于37 ℃培养12 h,分别将菌液稀释至106CFU·mL-1,备用。取96孔培养板,每孔加入菌液90 μL,将96孔板划分DMSO阴性对照组、氨苄青霉素阳性对照组和8个浓度的给药组,每组设置3个复孔,取10 μL样品溶液加入给药组各孔。于37 ℃暗培养24 h(无乳链球菌无氧环境)。每孔加入45 μL 0.5 mg·mL-1MTT溶液。空白凋零组加入与MTT等量的PBS,继续避光培养4 h。显色的菌液离心(12 000 r·min-1、4 ℃、10 min),弃上清液,加入125 μL DMSO。向已完全溶解的产物中加入150 μL的SDS,取200 μL混合溶液转移至96孔板中,用全自动酶标仪测定OD570。
2 结果与分析
2.1 结构鉴定
化合物1无色针状结晶,C30H50O,ESI-MSm/z:449.4 [M+Na]+。1H-NMR(400 MHz,CDCl3)δ:1.18(3H,s,H-28),1.05(3H,s,H-27),1.01(3H,s,H-30),1.00(3H,s,H-26),0.95(3H,s,H-29),0.88(3H,d,J= 6.5 Hz,H-23),0.87(3H,s,H-25),0.72(3H,s,H-24);13C-NMR(100 MHz,CDCl3)δ:22.41(C-1),41.65(C-2),213.36(C-3),58.34(C-4),42.27(C-5),41.41(C-6),18.37(C-7),53.22(C-8),37.57(C-9),59.60(C-10),35.47(C-11),30.12(C-12),39.38(C-13),38.42(C-14),32.55(C-15),36.14(C-16),30.63(C-17),42.91(C-18),35.75(C-19),28.30(C-20),32.90(C-21),39.82(C-22),6.96(C-23),14.79(C-24),18.08(C-25),18.80(C-26),20.39(C-27),32.22(C-28),35.16(C-29),31.92(C-30)。以上数据与文献(Toshihiro et al.,1992)一致,故鉴定化合物1为木栓酮。
化合物2白色油状物,C46H80O2,ESI-MSm/z:687.4 [M+Na]+。1H-NMR(400 MHz,CDCl3)δ:5.12(1H,t,J= 3.6 Hz,H-12),4.51(1H,m,H-3),2.29(1H,m,H-2′),1.07(3H,s,H-27),1.01(3H,s,H-25),0.98(3H,s,H-26),0.92(3H,d,J= 7.2 Hz,H-30),0.91(3H,s,H-23),0.89(3H,s,H-24),0.89(3H,d,J= 6.7 Hz,H-29),0.80(3H,s,H-28);13C-NMR(100 MHz,CDCl3)δ:38.59(C-1),23.79(C-2),80.75(C-3),37.90(C-4),55.41(C-5),18.40(C-6),33.02(C-7),40.18(C-8),47.78(C-9),36.95(C-10),23.52(C-11),124.48(C-12),139.78(C-13),42.22(C-14),28.81(C-15),26.76(C-16),33.90(C-17),59.21(C-18),39.76(C-19),39.80(C-20),31.40(C-21),41.69(C-22),28.24(C-23),17.01(C-24),15.88(C-25),16.97(C-26),23.39(C-27),28.24(C-28),17.66(C-29),21.55(C-30);173.88(C-1′),35.02(C-2′),34.58-22.85(C-3′-15′),14.28(C-16′)。以上数据与文献(Fatma et al.,2016)一致,故鉴定化合物2为α-amyrin palmitate。
化合物3无定形白色粉末,C46H80O2,ESI-MSm/z:687.6 [M+Na]+。1H-NMR(400 MHz,CDCl3)δ:4.69(1H,s,H-29),4.57(1H,s,H-29),4.47(1H,dd,J= 10.6,5.7 Hz,H-3),2.30(2H,t,J= 7.5 Hz,H-2′),1.68(3H,s,H-30),1.03(3H,s,H-27),0.94(3H,s,H-24),0.86(3H,s,H-23),0.79(3H,s,H-16′);13C-NMR(100 MHz,CDCl3)δ:37.98(C-1),23.89(C-2),80.78(C-3),38.51(C-4),55.52(C-5),18.14(C-6),34.35(C-7),40.99(C-8),50.48(C-9),38.19(C-10),21.09(C-11),25.32(C-12),37.23(C-13),42.97(C-14),27.58(C-15),35.71(C-16),43.14(C-17),48.43(C-18),48.15(C-19),151.10(C-20),29.85(C-21),40.14(C-22),28.11(C-23),16.12(C-24),16.72(C-25),16.31(C-26),14.66(C-27),18.35(C-28),109.50(C-29),19.43(C-30);173.89(C-1′),35.01(C-2′),25.24(C-3′),29.32-29.97(C-4′-13′),32.08(C-14′),22.84(C-15′),14.27(C-16′)。以上数据与文献(Lin & Tome,1988)一致,故鉴定化合物3为sambuculin A。
化合物4无色针状结晶,C29H46O,ESI-MSm/z:433.3 [M+Na]+。1H-NMR(400 MHz,CDCl3)δ:5.35(1H,d,J= 3.5 Hz,H-6),5.24(1H,dd,J= 15.3,7.9 Hz,H-22),5.21(1H,dd,J= 12.7,7.5 Hz,H-23),4.69(2H,m,H-27),3.93(1H,m,H-3),1.25(3H,s,H-19),1.65(3H,s,H-26),1.02(3H,d,J= 4.7 Hz,H-21),0.83(3H,t,J= 7.6 Hz,H-29),0.69(3H,s,H-18);13C-NMR(100 MHz,CDCl3)δ:37.33(C-1),31.72(C-2),71.92(C-3),42.34(C-4),140.82(C-5),121.80(C-6),31.98(C-7),32.02(C-8),50.23(C-9),36.60(C-10),21.15(C-11),39.76(C-12),42.35(C-13),56.93(C-14),24.40(C-15),29.79(C-16),55.96(C-17),12.14(C-18),19.48(C-19),40.28(C-20),20.88(C-21),137.29(C-22),130.12(C-23),52.08(C-24),148.71(C-25),20.31(C-26),109.60(C-27),25.79(C-28),12.23(C-29)。以上数据与文献(Kitajima & Tanaka,1993)一致,故鉴定化合物4为22-dehydroclerosterol。
化合物5无色油状物,C20H28O3,ESI-MSm/z:339.2 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ:6.12(1H,m,H-3′),5.76(1H,s,H-9),2.38-2.44(2H,m,H-2),2.07(3H,s,H-13),1.98(3H,d,J= 1.5 Hz,H-5′),1.89(3H,s,H-4′),1.87(3H,s,H-12),1.04(3H,s,H-14),1.02(3H,d,J= 6.8 Hz,H-15);13C-NMR(100 MHz,CD3OD)δ:31.46(C-1),29.70(C-2),73.27(C-3),46.28(C-4),42.23(C-5),40.77(C-6),127.79(C-7),192.36(C-8),125.67(C-9),167.43(C-10),144.29(C-11),20.96 (C-12),21.46(C-13),16.16(C-14),9.80(C-15);167.58(C-1′),126.93(C-2′),137.56(C-3′),14.57(C-4′),19.36(C-5′)。以上数据与文献(Wang et al.,2014)一致,故鉴定化合物5为isopetasin。
化合物6无色针状结晶,C46H80O2,ESI-MSm/z:703.6 [M+K]+。1H-NMR(400 MHz,CDCl3)δ:4.64(2H,d,J= 7.1 Hz,H-30),4.48(1H,dd,J= 10.7,5.6 Hz,H-3),1.04(3H,s,H-27),1.03(3H,s,H-26),1.00(3H,s,H-25),0.99(3H,s,H-28),0.90(3H,s,H-23),0.88(3H,s,H-24),0.87(3H,d,J= 6.0 Hz,H-29),0.84(3H,s,H-16′);13C-NMR(100 MHz,CDCl3)δ:38.44(C-1),23.71(C-2),80.55(C-3),37.85(C-4),55.47(C-5),18.17(C-6),33.98(C-7),40.95(C-8),49.94(C-9),37.02(C-10),21.40(C-11),25.18(C-12),38.75(C-13),42.33(C-14),25.87(C-15),40.01(C-16),35.28(C-17),47.65(C-18),38.54(C-19),153.66(C-20),25.04(C-21),39.02(C-22),27.97(C-23),16.57(C-24),15.89(C-25),16.36(C-26),14.14(C-27),26.30(C-28),19.25(C-29),107.40(C-30);173.75(C-1′),34.05(C-2′),25.18(C-3′),29.69(C-4′-C-13′),31.94(C-14′),22.71(C-15′),18.10(C-16′)。以上数据与文献(Patra et al.,1981)一致,故鉴定化合物6为taraxasteryl palmitate。
化合物7白色针状结晶,C29H48O,ESI-MSm/z:451.4 [M+K]+。1H-NMR(400 MHz,CDCl3)δ:5.35(1H,d,J= 5.1 Hz,H-6),5.15(1H,dd,J= 15.2,8.6 Hz,H-22),5.02(1H,dd,J= 15.2,8.6 Hz,H-23),3.53(1H,m,H-3),1.01(3H,s,H-19),0.92(3H,d,J= 6.5 Hz,H-21),0.85(3H,d,J= 3.5 Hz,H-27),0.83(3H,d,J= 1.7 Hz,H-26),0.81(3H,d,J= 4.5 Hz,H-29),0.68(3H,s,H-18);13C-NMR(100 MHz,CDCl3)δ:37.39(C-1),29.29(C-2),71.96(C-3),42.46(C-4),140.89(C-5),121.87(C-6),32.04(C-7),32.04(C-8),50.27(C-9),36.65(C-10),21.23(C-11),39.82(C-12),42.42(C-13),56.91(C-14),24.45(C-15),29.07(C-16),56.19(C-17),12.00(C-18),19.54(C-19),40.64(C-20),21.23(C-21),138.46(C-22),129.41(C-23),51.38(C-24),31.78(C-25),21.36(C-26),19.17(C-27),25.55(C-28),12.12(C-29)。以上数据与文献(贾瑞芳等,2021)一致,故鉴定化合物7为豆甾醇。
化合物8无色油状物,C52H88O7,ESI-MSm/z:847.6 [M+Na]+。1H-NMR(400 MHz,CDCl3)δ:5.35(1H,d,J= 3.3 Hz,H-6),5.23(1H,dd,J= 15.2,7.8 Hz,H-22),5.17(1H,dd,J= 15.2,7.1 Hz,H-23),4.70(2H,m,H-27),4.37(1H,d,J= 7.6 Hz,H-1′),1.99(3H,s,H-26),1.02(3H,s,H-19),1.01(3H,d,J= 6.6 Hz,H-21),0.99(3H,s,H-18),0.81(3H,s,H-29),0.69(3H,s,H-17″);13C-NMR(100 MHz,CDCl3)δ:37.30(C-1),31.95(C-2),79.72(C-3),39.70(C-4),140.36(C-5),122.06(C-6),34.29(C-7),31.88(C-8),50.19(C-9),36.72(C-10),21.08(C-11),38.93(C-12),42.27(C-13),56.87(C-14),25.00(C-15),28.72(C-16),55.92(C-17),12.06(C-18),19.38(C-19),40.23(C-20),20.85(C-21),137.16(C-22),130.12(C-23),52.01(C-24),148.55(C-25),20.22(C-26),109.55(C-27),25.71(C-28),12.14(C-29);101.26(C-1′),76.18(C-2′),73.77(C-3′),73.42(C-4′),70.38(C-5′),63.57(C-6′);174.33(C-1″),34.29(C-2″),31.88(C-3″),29.70(C-4″-C-14″),24.33(C-15″),22.71(C-16″),14.13(C-17″)。以上数据与文献(Xu et al.,2013)一致,故鉴定化合物8为22-dehydroclerosterol-3-O-β-D-(6′-O-margaroyl)-glucopyranoside。
化合物9白色无定形粉末,C35H56O6,ESI-MSm/z:595.4 [M+Na]+。1H-NMR(400 MHz,DMSO)δ:5.33(1H,s,H-6),5.22(1H,dd,J= 12.6,4.8 Hz,H-22),5.19(1H,dd,J= 12.2,5.1 Hz,H-23),4.68(2H,s,H-27),4.22(1H,d,J= 7.8 Hz,H-1′),1.61(3H,s,H-26),0.98(3H,d,J= 6.7 Hz,H-21),0.96(3H,s,H-19),0.79(3H,t,J= 7.3 Hz,H-29),0.67(3H,s,H-18);13C-NMR(100 MHz,DMSO)δ:36.85(C-1),31.43(C-2),76.95(C-3),38.34(C-4),140.48(C-5),121.21(C-6),29.29(C-7),31.43(C-8),49.65(C-9),36.25(C-10),21.49(C-11),38.34(C-12),41.80(C-13),56.26(C-14),23.88(C-15),28.31(C-16),55.30(C-17),11.88(C-18),19.12(C-19),40.44(C-20),19.94(C-21),136.84(C-22),129.59(C-23),51.31(C-24),147.70(C-25),20.71(C-26),109.98(C-27),25.23(C-28),12.02(C-29);100.81(C-1′),73.49(C-2′),76.78(C-3′),70.11(C-4′),76.95(C-5′),61.11(C-6′)。以上数据与文献(Saeedan et al.,1997)一致,故鉴定化合物9为3-O-β-D-galactopyranosyl-(24β)-ethylcholesta-5,22,25-trien。
化合物10淡黄色粉末,C31H40O15,ESI-MSm/z:675.3 [M+Na]+。1H-NMR(400 MHz,DMSO)δ:7.56(1H,d,J= 15.8 Hz,H-7′),7.29(1H,d,J= 1.7 Hz,H-2′),6.82(1H,d,J= 8.0 Hz,H-5′),6.40(1H,d,J= 15.8 Hz,H-8′),5.06(1H,s,H-1‴),4.38(1H,d,J= 7.8 Hz,H-1″),3.82(3H,s,3-OCH3),3.79(3H,s,3′-OCH3),2.76(2H,m,H-7),1.12(3H,d,J= 6.1 Hz,H-6‴);13C-NMR(100 MHz,DMSO)δ:132.80(C-1),112.70(C-2),147.90(C-3),147.42(C-4),117.34(C-5),121.25(C-6),36.68(C-7),72.22(C-8),56.41(3-OCH3);127.05(C-1′),117.96(C-2′),151.54(C-3′),149.77(C-4′),115.56(C-5′),124.99(C-6′),147.80(C-7′),113.98(C-8′),167.65(C-9′),57.33(3′-OCH3);104.03(C-1″),76.21(C-2″),80.95(C-3″),70.51(C-4″),76.24(C-5″),62.43(C-6″);102.97(C-1‴),72.07(C-2‴),71.87(C-3‴),73.37(C-4‴),70.83(C-5‴),19.79(C-6‴)。以上数据与文献(高映等,2017)一致,故鉴定化合物10为肉苁蓉苷D。
化合物11淡黄色粉末,C26H30O11,ESI-MSm/z:541.2 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ:9.57(1H,d,J= 7.9 Hz,H-9′),7.61(1H,d,J= 15.7 Hz,H-7′),7.00(1H,d,J= 1.8 Hz,H-2),6.86(1H,dd,J= 8.2,1.9 Hz,H-6),6.78(1H,d,J= 8.1 Hz,H-5),6.74(1H,dd,J= 8.0,16.0 Hz,H-8′),4.37(1H,d,J= 7.8 Hz,H-1″),3.91(3H,s,3-OCH3),3.83(3H,s,3′-OCH3);13C-NMR(100 MHz,CD3OD)δ:133.52(C-1),110.82(C-2),149.12(C-3),147.83(C-4),116.17(C-5),119.96(C-6),90.18(C-7),52.17(C-8),71.95(C-9),56.44(3-OCH3);129.67(C-1′),114.39(C-2′),145.92(C-3′),152.75(C-4′),131.33(C-5′),120.29(C-6′),156.26(C-7′),127.14(C-8′),196.28(C-9′),56.76(3′-OCH3);104.34(C-1″),75.14(C-2″),78.03(C-3″),71.56(C-4″),78.17(C-5″),62.69(C-6″)。以上数据与文献(孟永海,2007)一致,故鉴定化合物11为 tortoside F。
化合物12淡黄色粉末,C20H20O6,ESI-MSm/z:379.1 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ:9.58(1H,d,J= 7.8 Hz,H-9′),7.62(1H,d,J= 15.8Hz,H-7′),7.29(1H,s,H-6′),7.23(1H,d,J= 1.3 Hz,H-2′),6.95(1H,d,J= 1.8 Hz,H-2),6.83(1H,dd,J= 8.2,1.8 Hz,H-6),6.78(1H,d,J= 8.1 Hz,H-5),6.69(1H,dd,J= 15.7,7.8 Hz,H-8′),5.61(1H,d,J= 6.4 Hz,H-7),3.91(3H,s,3′-OCH3),3.82(3H,s,3-OCH3);13C-NMR(100 MHz,CD3OD)δ:133.91(C-1),110.55(C-2),149.19(C-3),147.83(C-4),131.25(C-5),119.99(C-6),90.10(C-7),54.65(C-8),64.54(C-9),56.78(3-OCH3);129.62(C-1′),114.21(C-2′),146.02(C-3′),152.94(C-4′),130.85(C-5′),119.80(C-6′),156.16(C-7′),127.09(C-8′),196.19(C-9′),56.37(3′-OCH3)。以上数据与文献(Li et al.,2017)一致,故鉴定化合物12为balanophonin。
化合物13黄色粉末,C21H20O11,ESI-MSm/z:471.1 [M+Na]+。1H-NMR(400 MHz,DMSO)δ:12.99(1H,s,5-OH),7.44(1H,d,J=8.3,2.2Hz,H-6′),7.42(1H,d,J= 2.1 Hz,H-2′),6.90(1H,d,J= 8.3 Hz,H-5′),6.78(1H,d,J= 2.1 Hz,H-8),6.75(1H,s,H-3),6.44(1H,d,J= 2.1 Hz,H-6),5.08(1H,d,J= 7.4 Hz,H-1″);13C-NMR(100 MHz,DMSO)δ:164.50(C-2),103.20(C-3),181.94(C-4),161.16(C-5),99.56(C-6),162.97(C-7),94.74(C-8),156.98(C-9),105.37(C-10);121.39(C-1′),113.60(C-2′),145.82(C-3′),149.98(C-4′),116.02(C-5′),119.21(C-6′);99.88(C-1″),73.15(C-2″),77.19(C-3″),69.56(C-4″),76.42(C-5″),60.63(C-6″)。以上数据与文献(周志强,2013)一致,故鉴定化合物13为木犀草苷。
化合物14黄色粉末,C29H36O15,ESI-MSm/z:647.2 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ:7.56(1H,d,J= 12.8 Hz,H-7′),7.03(1H,d,J= 1.4 Hz,H-2′),6.92(1H,dd,J= 8.0,1.4 Hz,H-6′),6.75(1H,d,J= 6.6 Hz,H-5′),6.67(1H,d,J= 1.4 Hz,H-2),6.65(1H,d,J= 6.4 Hz,H-5),6.52(1H,dd,J= 1.4,7.8 Hz,H-6),6. 25(1H,d,J= 12.7 Hz,H-8′),5.16(1H,s,H-1‴),4.34(1H,d,J= 6.3 Hz,H-1″),1.06(3H,d,J= 4.9 Hz,H-6‴);13C-NMR(100 MHz,CD3OD)δ:131.39(C-1),117.07(C-2),145.94(C-3),144.49(C-4),114.55(C-5),121.26(C-6),36.41(C-7),70.33(C-8);127.53(C-1′),116.28(C-2′),146.66(C-3′),149.65(C-4′),116.48(C-5′),123.25(C-6′),148.01(C-7′),115.17(C-8′),168.31(C-9′);104.00(C-1″),76.04(C-2″),81.65(C-3″),71.91(C-4″),75.78(C-5″),62.19(C-6″);102.94(C-1‴),72.18(C-2‴),72.21(C-3‴),73.66(C-4‴),70.42(C-5‴),18.40(C-6‴)。以上数据与文献(高燕萍等,2016)一致,故鉴定化合物14为类叶升麻苷。
化合物15黄色粉末,C15H10O6,ESI-MSm/z:309.0 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ:12.96(1H,s,5-OH),10.81(1H,s,7-OH),9.91(1H,s,3′-OH),9.39(1H,s,4′-OH),7.40(1H,dd,J= 8.3,2.3 Hz,H-6′),7.38(1H,d,J= 2.2 Hz,H-2′),6.88(1H,d,J= 8.3 Hz,H-5′),6.66(1H,s,H-3),6.43(1H,d,J= 2.1 Hz,H-8),6.18(1H,d,J= 2.0 Hz,H-6);13C-NMR(100 MHz,CD3OD)δ:164.76(C-2),102.48(C-3),182.49(C-4),161.85(C-5),98.78(C-6),164.97(C-7),93.65(C-8),158.05(C-9),103.91(C-10);122.32(C-1′),112.78(C-2′),145.68(C-3′),149.64(C-4′),115.41(C-5′),118.92(C-6′)。以上数据与文献(李勇军等,2005)一致,故鉴定化合物15为木犀草素。
化合物16白色结晶,C17H24O8,ESI-MSm/z:379.1 [M+Na]+。1H-NMR(400 MHz,DMSO)δ:6.68(2H,s,H-3,5),6.33(1H,d,J= 16.3 Hz,H-7),6.24(1H,m,H-8),4.89(1H,d,J= 7.3 Hz,H-1′),3.76(6H,s,2-OCH3,6-OCH3),1.83(3H,d,J= 5.8 Hz,H-9);13C-NMR(100 MHz,DMSO)δ:134.07(C-1),153.16(C-2,6),104.54(C-3,5),133.62(C-4),131.21(C-7),125.34(C-8),18.61(C-9),56.81(2-OCH3,6-OCH3);103.09(C-1′),74.64(C-2′),77.66(C-3′),70.40(C-4′),77.00(C-5′),61.37(C-6′)。以上数据与文献(刘燕等,2015)一致,故鉴定化合物16为 acantrifoside E。
化合物17白色胶状,C32H50O13,ESI-MSm/z:665.3 [M+Na]+。1H-NMR(400 MHz,CD3OD)δ:6.47(1H,s,H-14),4.44(1H,d,J= 7.9 Hz,H-1′),4.33(1H,d,J= 7.8 Hz,H-1″),3.22(1H,d,J= 7.9 Hz,H-3),1.20(3H,s,H-20),1.19(3H,d,J= 6.8 Hz,H-17),1.17(3H,d,J= 6.9 Hz,H-16),1.01(3H,s,H-18),0.86(3H,s,H-19);13C-NMR(100 MHz,CD3OD)δ:34.59(C-1),26.53(C-2),88.10(C-3),39.41(C-4),52.72(C-5),18.87(C-6),33.12(C-7),133.52(C-8),132.28(C-9),38.87(C-10),147.54(C-11),141.10(C-12),139.48(C-13),116.46(C-14),25.24(C-15),22.51(C-16),22.80(C-17),27.84(C-18),16.92(C-19),19.55(C-20);106.62(C-1′),73.83(C-2′),76.86(C-3′),70.31(C-4′),76.74(C-5′),61.44(C-6′);103.96(C-1″),74.08(C-2″),79.07(C-3″),69.66(C-4″),76.65(C-5″),60.90(C-6″)。以上数据与文献(Hu et al.,2018)一致,故鉴定化合物17为 trichotomside B。
化合物18淡黄色粉末,C30H38O15,ESI-MSm/z:637 [M-H]-。1H-NMR(400 MHz,CD3OD)δ:7.59(1H,d,J= 15.8 Hz,H-7′),7.07(1H,s,H-2′),6.95(1H,d,J= 8.3 Hz,H-6′),6.80(1H,d,J= 3.2 Hz,H-5′),6.78(1H,d,J =3.2 Hz,H-2),6.73(1H,d,J= 1.8 Hz,H-5),6.66(1H,d,J= 1.8 Hz,H-6),6.28(1H,d,J= 15.9 Hz,H-8′),5.19(1H,s,H-1‴),4.37(1H,d,J= 7.9 Hz,H-1″),3.80(3H,s,3-OCH3),2.80(2H,t,J= 6.8 Hz,H-7),1.09(3H,d,J= 6.2 Hz,H-6‴);13C-NMR(100 MHz,CD3OD)δ:132.71(C-1),116.97(C-2),147.12(C-3),146.66(C-4),112.69(C-5),121.14(C-6),36.40(C-7),72.22(C-8),56.40(3-OCH3);127.53(C-1′),115.18(C-2′),147.37(C-3′),149.63(C-4′),116.48(C-5′),123.23(C-6′),147.97(C-7′),114.57(C-8′),168.27(C-9′);104.02(C-1″),76.03(C-2″),81.63(C-3″),71.93(C-4″),75.80(C-5″),62.22(C-6″),102.93(C-1‴),70.43(C-2‴),72.02(C-3‴),73.67(C-4‴),70.32(C-5‴),18.42(C-6‴)。以上数据与文献(李友宾等,2005)一致,故鉴定化合物18为肉苁蓉苷 C。
2.2 抗菌活性结果
采用MTT法测试大青粗提物对乳房链球菌、无乳链球菌的抗菌活性。结果显示,正丁醇部位Fr.B3、Fr.C1、Fr.D2组分对乳房链球菌有抗菌活性, IC50分别为7.02、0.89、6.79 mg·mL-1; Fr.B3、Fr.C1、Fr.C3、Fr.C4、Fr.D2 5份粗提物对无乳链球菌有抗菌活性,IC50分别为2.38、0.72、1.31、4.63、0.98 mg·mL-1。这表明Fr.C1部位具有一定的抗菌活性。
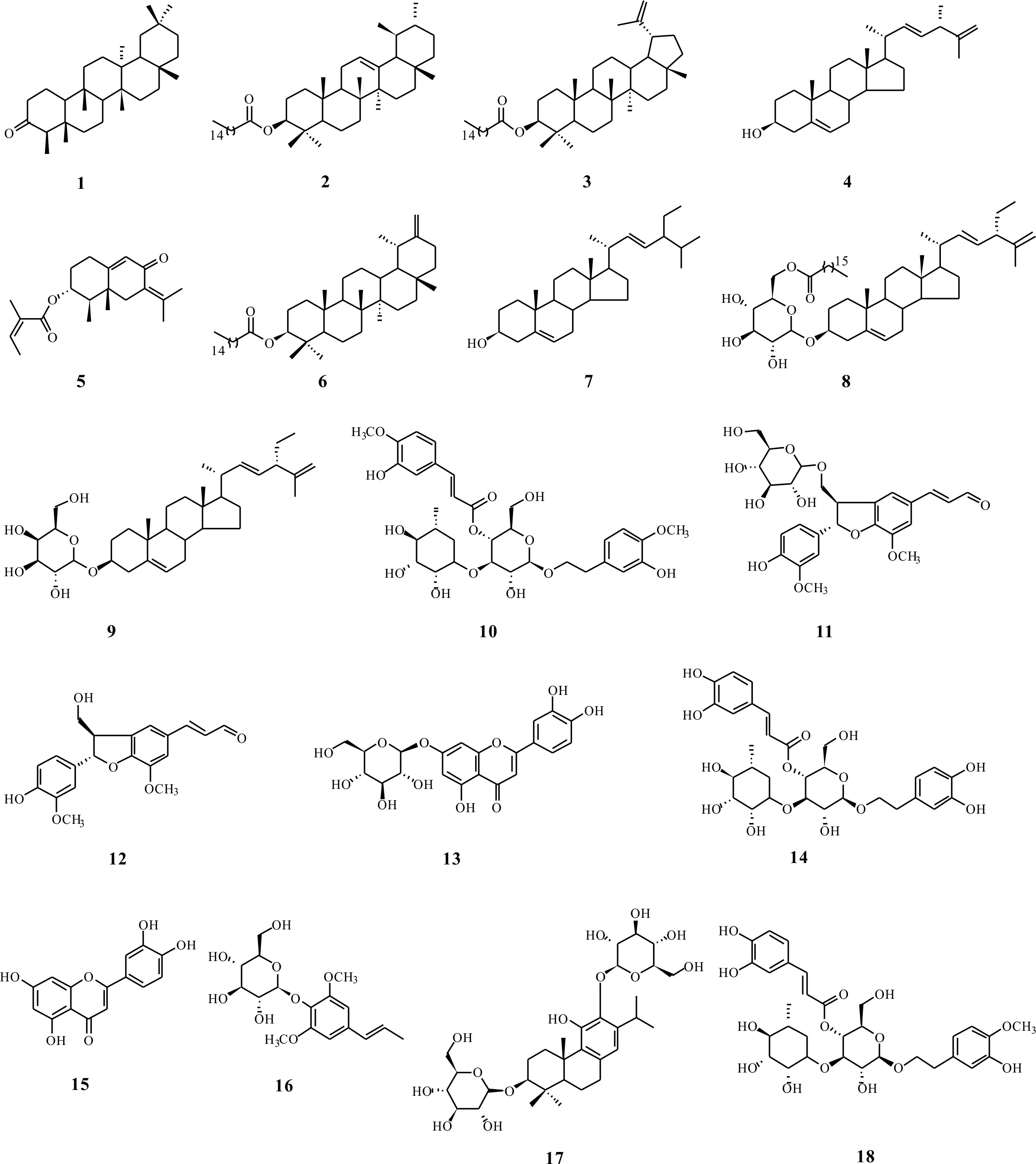
图 1 化合物1-18结构式Fig. 1 Structures of compounds 1-18
采用同样的方法对经过粗筛活性较好的部位Fr.C1分离得到的2个单体化合物进行抗菌活性测试,测定结果为化合物13对乳房链球菌有一定的抑制活性,MIC为0.18 mg·mL-1,对无乳链球菌无明显抑制活性;化合物14对乳房链球菌和无乳链球菌均无明显抑制活性。
3 讨论与结论
本研究对黔产大青乙醇提取物中化学成分进行分离鉴定,从中共得到了18个化合物。经查阅相关文献,化合物2、3、5、6、8-13、16-18均为首次从大青中分离得到。部分化合物的抗菌活性试验结果表明,化合物13对乳房链球菌有一定的抑制活性。
木犀草苷(13)是木犀草素(15)7-OH配糖化后的一种苷,研究表明木犀草素(15)能通过破坏细菌细胞壁和细胞膜结构完整性和抑制DNA拓扑异构酶活性发挥抗菌效果(王倩和谢明杰,2010),木犀草苷(13)对乳房链球菌的抑制作用是否也通过上述机制得以实现,还有待进一步深入研究。本次实验中虽然类叶升麻苷(14)未表现出抗菌活性,但该化合物具有较强抗氧化活性(杨建华等,2009),可以对抗因炎症反应而产生的过氧化物,进而修复炎症组织。奶牛乳房炎是由多种因素引起的炎症反应,主要是病原微生物的感染,常见致病菌有无乳链球菌、乳房链球菌、金黄色葡萄球菌等(张晓东等,2021)。此外,奶牛乳房组织新陈代谢旺盛,体内自由基含量过高引起氧化应激,亦可损伤奶牛乳房细胞进而诱发乳房炎(郭咏梅和闫素梅,2021)。如果将具有抗奶牛乳房炎致病菌作用的木犀草苷(13)与对抗炎症反应的类叶升麻苷(14)联用,是否能显著增强对奶牛乳房炎的防治效果,还需进一步探究。本研究丰富了大青化学成分的物质基础,初步探讨了其抗菌活性成分,为后续大青抗奶牛乳房炎药物的研发提供了一定参考,拓展了苗族医药在动物疾病防治方面的应用。

