环状RNA circRSF11 结合HuR 促进辐射诱导的肝星状细胞炎性表型
周佩涛,程炳霖,孙一宁,吴德华,陈宇翰
1南方医科大学南方医院放疗科,广东 广州 510515;2南方医科大学第一临床医学院,广东 广州510515
放疗已成为原发性肝癌综合治疗模式中的重要组成部分[1,2]。然而,在给予肝癌根治性放疗剂量的同时,也存在诱发放射性肝病(RILD)的风险[3,4]。作为肝癌放射治疗的常见并发症,RILD组织学早期表现主要是急性放射性肝炎,晚期表现主要是放射性肝纤维化,严重的RILD 可致患者肝功能衰竭死亡[5,6]。因此,降低RILD发生率和减轻RILD程度是临床实践中提高肝癌放疗效果的关注点之一。环状RNA(circRNA)是一类无游离5’端或3’端,核酸分子间以共价键形成单链闭合环状的基因转录产物[7]。许多研究已证实circRNA与肿瘤、内分泌、老化等多种疾病的发生发展密切相关[8-10]。circRNA可通过多种方式发挥作用,诸如参与调控亲本基因表达,调控转录本可变剪切,作为miRNA海绵吸附小RNA(miRNA),直接与RNA结合蛋白(RBP)结合或充当RBP的支架,甚至还可翻译蛋白质等[11,12]。本课题组前期研究发现辐射诱导肝星状细胞(HSC)炎性表型促进RILD 发病[13]。另外,辐射诱导HSC 的circRNA RSF1(hsa_circ_0023706)表达上调,其通过吸附miR-146a-5p促进HSC的炎性表型[14]。此外,课题组前期预测发现circRSF1 与人抗原R(HuR)蛋白有多个结合位点,而HuR 蛋白已被证实参与调控一些炎症相关的mRNA的表达或翻译进而影响炎症免疫应答的发生[15]。但目前尚未见circRSF1结合RBP发挥功能的相关研究报道。本研究揭示circRSF1可通过结合HuR蛋白并阻遏HuR与IκBα结合进而促进NF-κB激活,从而实现对HSC炎性表型的调控,丰富了相关发病调控机制。后续研究将进一步探讨circRSF1结合HuR介导炎症通路激活在小鼠RILD模型中的调控作用,以期为RILD防治靶点的开发提供更多的依据。
1 材料和方法
1.1 细胞培养与照射
人HSC株LX2(广州吉妮欧生物科技有限公司)在含有10%(V/V)胎牛血清(Gibco)的Dulbecco's Modified Eagle's培养基(DMEM;ph7.4)中培养,置于37 ℃、5%CO2的培养箱中培养。按照如下参数进行单次8 Gy照射:6-MV X射线,剂量率300 cGy/min,细胞培养板下方置一块1.5 cm补偿膜,机架角旋转至180°,源皮距设置为100 cm,射野大小依据照射细胞板数而定,一般不超过40 cm×40 cm。
1.2 细胞转染
circRSF1过表达质粒、circRSF1 siRNA和阴性对照(广州吉赛生物),HuR过表达质粒及阴性对照(上海吉凯基因医学科技股份有限公司),HuR siRNA、miR-146a-5p 模拟物和相应阴性对照(广州锐博生物技术有限公司)。参照说明书,使用Lipofectamine 3000(Invitrogen)进行细胞转染,分别将质粒(1 μg)、siRNA或miR-146a-5p 模拟物(终浓度50 nmol/L)转染入24孔板中的细胞。HuR 的特异性siRNA 序列为CAACAAGUCCCACAAAUAAUU,circRSF1 siRNA设计的目标序列为CACAAAGGAACAGAAAGAA。
1.3 qRT-PCR
使用TRIzol reagent(Invitrogen)从细胞中提取RNA,应用Prime Script RT试剂盒(Takara Bio,Shiga)合成cDNA,然后使用SYBR®Premix Ex Taq™(Takara)试剂盒在实时检测系统(QuantStudio 6 Flex)进行qRTPCR 检测。引物序列见表1。使用GAPDH 作为circRNA或mRNA的检测内参,采用2-△△CT法计算基因表达。
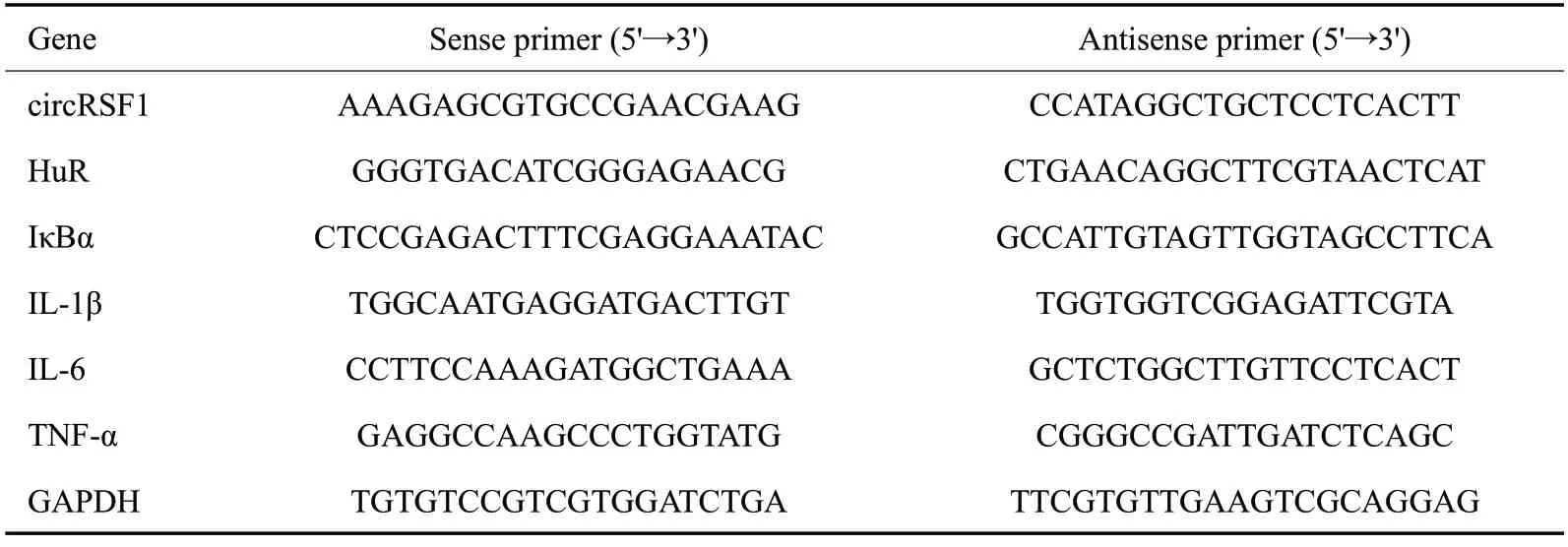
表1 用于qRT-PCR的引物Tab.1 Primers for qRT-PCR
1.4 Western blot
使用含有苯甲基磺酰氟(上海碧云天生物技术有限公司)的RIPA裂解液在冰上裂解提取蛋白。将蛋白质萃取物转移至10%~15%的十二烷基硫酸钠-聚丙烯酰胺凝胶进行电泳分离,然后将凝胶上的蛋白转移至PVDF膜(Millipore)。经过5%脱脂奶粉封闭1 h后,使用相应一抗在4 ℃孵育过夜。本研究中使用的抗体包括anti-HuR(#12582)、anti-IκBα(#4814)、anti-nuclear factor-κB(NF-κB)p65(#8242)、anti-phospho-NF-κB p65(Ser536;#3033)和anti-GAPDH(#2118)均购自Cell Signaling Technology。然后用辣根过氧化物酶偶联二抗(Cell Signaling Technology)在室温下孵育1 h。使用化学发光系统(BLT GelView 6000 Pro,广州博鹭腾生物科技有限公司)对蛋白印迹进行可视化。所有蛋白条带以GAPDH作为检测内参。
1.5 RNApull down
利用Pierce Magnetic RNA-protein Pull-Down 试剂盒(Pierce Biotechnology)进行RNA pull down 检测。参照说明书,将与circRSF1互补的生物素化RNA探针或阴性对照探针与链霉亲和素包被的磁珠在26 ℃下孵育30 min,生成包被的磁珠。将30 μL细胞裂解液用于制备RNA-蛋白结合反应的混合物,部分细胞裂解液作为input。然后将混合物与探针包被的磁珠在4 ℃孵育30 min。将RNA 结合蛋白复合物洗脱后,采用Western blot分析下拉物中的蛋白。
1.6 RNA结合蛋白免疫沉淀(RIP)
采用Magna RIP 试剂盒(Millipore)进行RIP 检测。参照说明书,将磁珠与5 μg抗兔IgG(Millipore)或5 μg抗HuR(#12582,Cell Signaling Technology)抗体混合,然后将细胞裂解液和RIP免疫沉淀缓冲液与磁珠-抗体复合物在4 ℃旋转孵育过夜。经过蛋白酶Κ处理后,从免疫沉淀复合物中洗脱RNA,进一步纯化后进行qRT-PCR检测。
1.7 统计学方法
应用SPSS 16.0 统计软件进行数据分析。数据采用均数±标准差表示,两组间的差异比较采用t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 HuR表达下调促进辐射诱导的HSC炎性表型
给予LX2细胞不同剂量X线照射后检测发现,8 Gy诱导circRSF1表达上调最为显著(P<0.05,图1A)。通过circRNA 研究网站CircInteractome (https://circinteractome.irp.nia.nih.gov/)预测发现,circRSF1与HuR蛋白有多个结合位点。相比非照射组,予8 Gy X线照射后LX2细胞的HuR表达无明显改变(图1B)。为明确HuR表达水平在辐射背景下对HSC功能的影响,本研究分别对LX2细胞敲低或过表达HuR后进行照射。转染HuR siRNA可显著下调HuR和IκBα的表达,促进NF-κB p65磷酸化和促炎因子(IL1-β、IL-6、TNF-α)生成(P<0.05,图1C)。相反,予LX2细胞过表达HuR后可上调HuR和IκBα的表达,抑制NF-κB p65磷酸化和促炎因子(IL1-β、IL-6、TNF-α)生成(P<0.05,图1D)。此外,过表达或敲低HuR对LX2细胞的circRSF1和活化指标α-SMA的表达均无明显影响(图1C、D)。

图1 改变HuR的表达对受照的HSC炎性表型和NF-κB激活的影响Fig.1 Effect of modifying the expression of HuR on inflammatory phenotype and NF-κB activation in irradiated HSCs.A:Expression of circRSF1 in LX2 cells with X ray irradiation at different doses(Gy).B:Expression of HuR in LX2 cells with or without irradiation.C:Effect of HuR knockdown on inflammatory phenotype and NF-κB activation in irradiated LX2 cells.D:Effect of HuR overexpression on inflammatory phenotype and NF-κB activation in irradiated LX2 cells.*P<0.05 vs NIR or negative control (NC).NIR: Nonirradiation;si-NC:siRNAnegative control;OE-NC:Negative control overexpressing plasmid.
2.2 circRSF1过表达阻遏HuR与IκBα结合
为探讨circRSF1是否通过HuR调控IκBα表达,本研究分别将circRSF1过表达质粒或siRNA转染入LX2细胞,发现过表达或敲低circRSF1对HuR表达均无影响(图2A)。RNA pull down 和Western blot 检测发现circRSF1能与HuR蛋白结合,且circRSF1表达上调促进了HuR蛋白与circRSF1结合(图2B)。RIP和qRTPCR检测发现,HuR蛋白能与circRSF1结合,且circRSF1 表达上调,结合在HuR 蛋白的circRSF1 明显增多,而结合在HuR 蛋白的IκBα mRNA 明显减少(P<0.05,图2C)。将circRSF1 过表达质粒和或miR-146a-5p 模拟物转染入LX2 细胞,发现circRSF1 和或miR-146a-5p 表达上调对HuR 蛋白表达无影响,circRSF1过表达可抑制IκBα的表达,而miR-146a-5p则无此效应(图2D)。
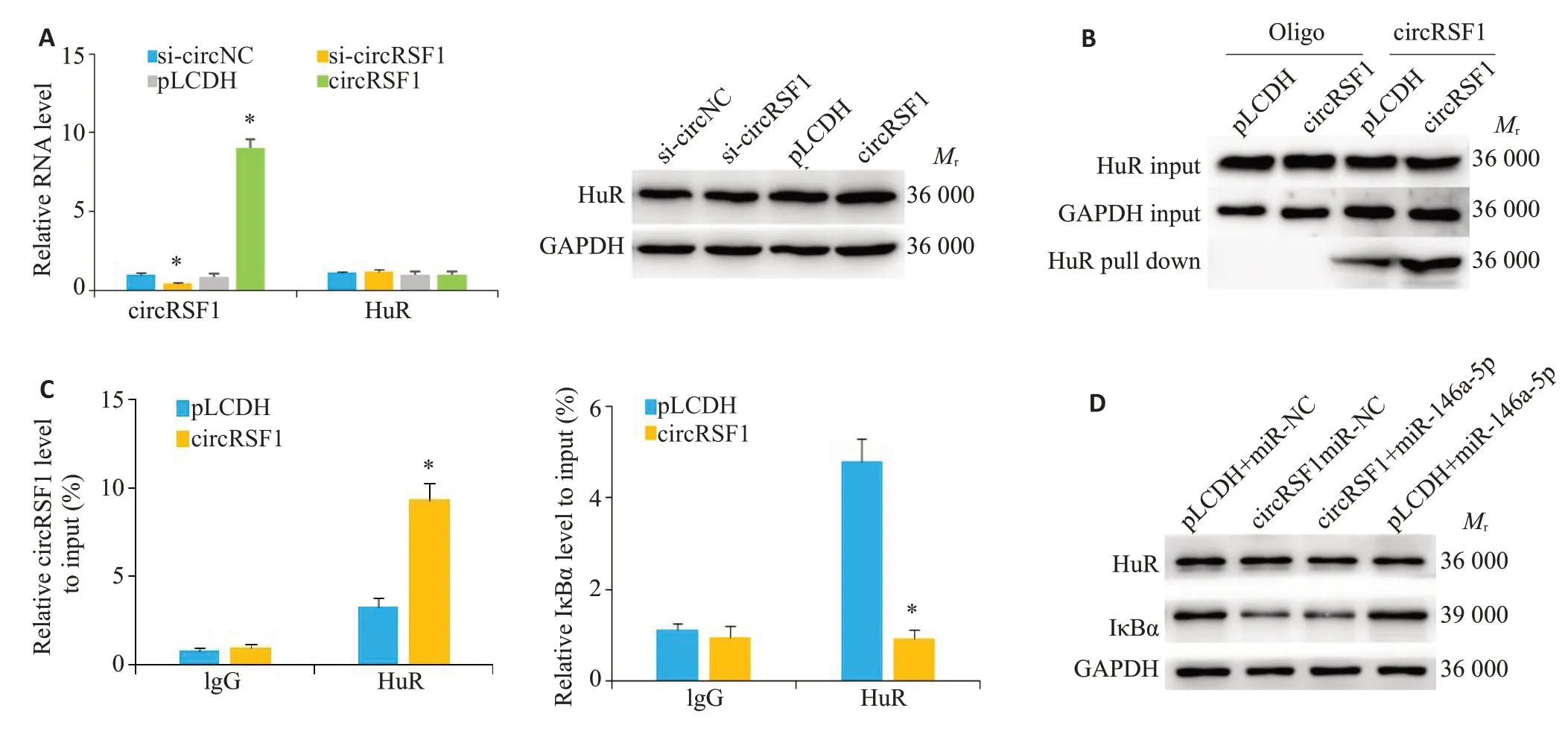
图2 circRSF1与HuR结合的验证Fig.2 Verification of the binding between circRSF1 and HuR.A: Effect of knockdown or overexpression of circRSF1 on HuR expression.B:Interaction between HuR protein and circRSF1 detected by RNA pull-down assay.C:Interaction of HuR protein with circRSF1 and IκBα detected by RIP assay.D: Effect of overexpression of circRSF1 and/or miR-146a-5p on expressions of HuR and IκBα.*P<0.05 vs corresponding negative control.si-circNC:Negative control siRNA for circRSF1;si-circRSF1:Specific siRNAagainst circRSF1;pLCDH:pLCDH-ciR vector.
2.3 抑制circRSF1表达对HSC的抑炎效应可被HuR敲低逆转
将circRSF1 siRNA联合HuR siRNA共转染HSC后予照射,结果显示敲低circRSF1 抑制HSC 生成IL1-β、IL-6、TNF-α,而予联合敲低HuR则可上调HSC的促炎因子(P<0.05,图3A)。敲低circRSF1导致IκBα表达上调和NF-κB p65磷酸化减少,予联合敲低HuR后则可下调IκBα表达和促进NF-κB p65磷酸化(P<0.05,图3B)。
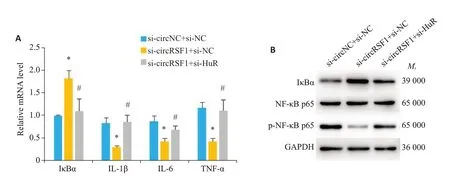
图3 联合敲低circRSF1与HuR的表达对受照的HSC炎性表型和NF-κB激活的影响Fig.3 Effect of knockdown of circRSF1 and HuR on inflammatory phenotype(A)and NF-κB activation(B)in irradiated HSCs.*P<0.05 vs corresponding negative control.#P<0.05 vs si-circRSF1 group.
2.4 上调circRSF1表达对HSC的促炎效应可被HuR过表达逆转
将circRSF1过表达质粒联合HuR过表达质粒共转染HSC后予照射,结果显示circRSF1过表达促进HSC生成IL1-β、IL-6、TNF-α,而予联合过表达HuR则可抑制HSC的促炎因子生成(图4A)。circRSF1过表达抑制IκBα表达和促进NF-κB p65磷酸化,而予联合过表达HuR后则可上调IκBα表达和抑制NF-κB p65磷酸化(P<0.05,图4B)。
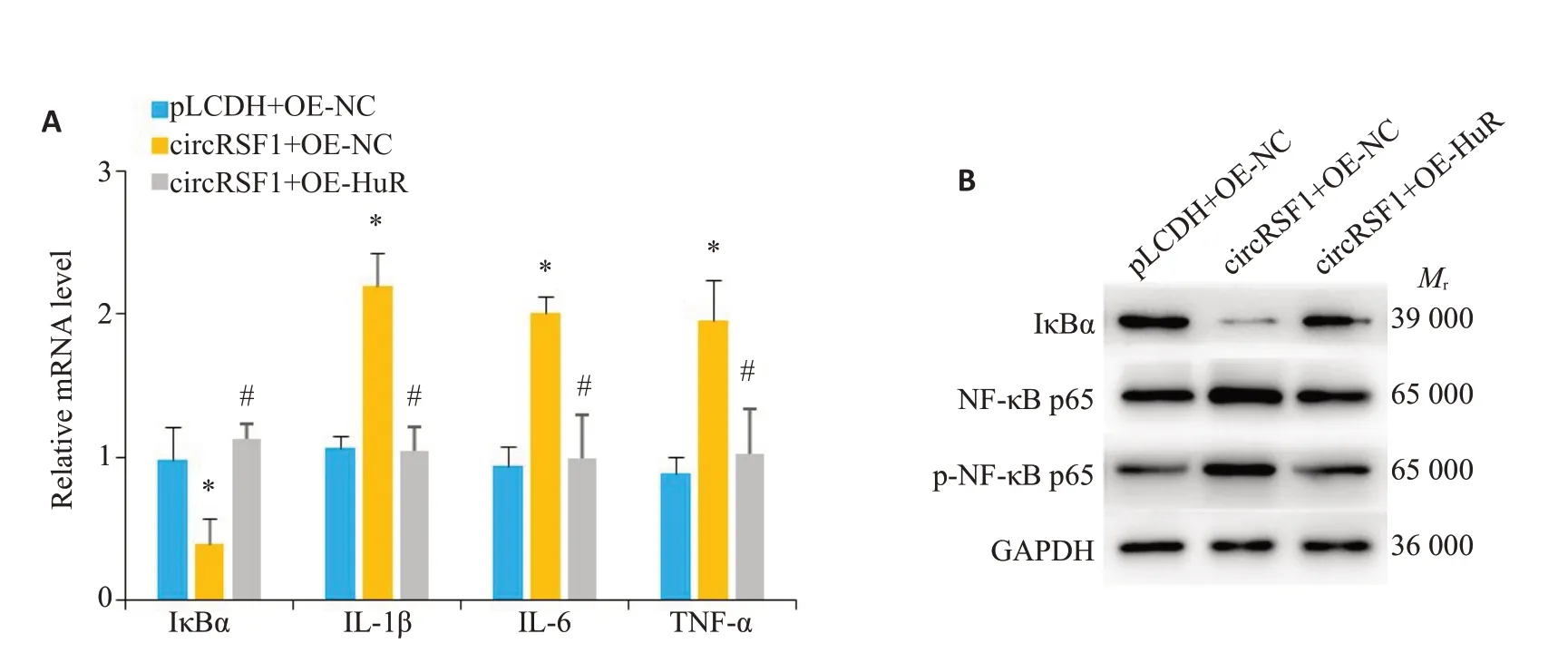
图4 联合过表达circRSF1与HuR对受照的HSC炎性表型和NF-κB激活的影响Fig.4 Effect of overexpression of circRSF1 and HuR on inflammatory phenotype (A) and NF-κB activation(B)in irradiated HSCs.*P<0.05 vs corresponding negative control.#P<0.05 vs circRSF1 group.
3 讨论
circRNA可以与不同的RNA结合蛋白结合形成特定的复合物,随后影响相关蛋白的作用模式[16-18]。本研究通过预测发现circRSF1与HuR蛋白有多个结合位点。HuR,又称类胚胎致死性异常视觉蛋白1,该蛋白可特异性地结合靶mRNA 3'非翻译区(3'UTR)中的AU富集元件,通过提高靶mRNA的稳定性和或翻译效率而上调靶基因在细胞中的表达水平[19]。相反,circRNA则可通过竞争结合HuR导致HuR靶mRNA的稳定性下降和表达下调,例如,circDLC1 可与HuR 结合,减少HuR 与MMP1 mRNA 的相互作用,从而抑制MMP1 mRNA的表达,最终抑制肝癌进展[20]。本研究也发现circRSF1与HuR结合后减少HuR与IκBα mRNA的结合,导致IκBα mRNA 表达下调。部分circRNA 结合HuR后并不影响靶mRNA的表达,但可下调靶mRNA的翻译效率导致靶蛋白生成减少。据报道,circ-PABPN1 与HuR 的结合能阻止HuR 与PABPN1、Atg16l1 mRNA的结合并减少这些mRNA的翻译[21,22]。另有研究显示,circPPM1F 与HuR 的竞争性相互作用导致PPM1F的翻译受阻,从而减轻PPM1F对NF-κB途径的抑制作用[23]。结合本研究结果和既往报道表明,circRNA能够作为HuR蛋白的“海绵”,阻遏HuR与其靶基因的结合进而影响靶基因的表达,参与调控疾病的发生发展。另外,与本研究结果不同的是,也有部分研究报道circRNA可以作为HuR的蛋白支架,协助HuR调控靶基因的表达[24]。如,circTICRR通过结合HuR蛋白进而稳定GLUD1 mRNA并升高GLUD1蛋白的水平,促进宫颈癌增殖[25]。circEIF3H可作为HuR的支架来调节HSPD1,RBM8A和G3BP1的mRNA稳定性,促进三阴性乳腺癌增殖和转移[26]。另有研究报道circStag1 与HuR相互作用并促进HuR易位到细胞质中,高细胞质水平的HuR通过稳定和增强β-连环蛋白表达,导致Wnt信号通路的激活,从而刺激骨髓间充质干细胞的成骨分化[27]。我们推测circRNA与HuR蛋白的互作方式可能与不同的疾病背景有关,在不同条件下,circRNA可充当RBP“海绵”或支架发挥不同的功能。
本研究发现,在辐射背景下,沉默HuR的表达可促进HSC生成炎性因子。相关研究已证实,HuR蛋白通过调控炎症通路相关调节因子的mRNA的稳定性和或翻译进而影响炎症反应的发生。如,HuR 通过提高NΚRF mRNA的稳定性并上调NΚRF的表达,进而抑制NF-κB信号通路,减少退行性髓核细胞中的炎症和胞外基质降解[28]。再有,HuR的表达上调可促进GILZ的翻译,进而抑制NF-κB活化,导致炎症因子生成减少[29]。另一项研究显示HuR 能特异性结合IκBα mRNA 的3'UTR调控IκBα表达;HuR过表达或敲低可分别上调或下调IκBα蛋白表达,进而影响NF-κB的表达[30]。本研究发现circRSF1与HuR结合后使HuR与IκBα mRNA的结合减少,导致IκBα蛋白表达下调进而促进NF-κB活化,增加促炎因子生成,此效应可被HuR过表达逆转,表明circRSF1通过阻遏HuR的功能发挥从而促进炎症通路激活。
综上所述,HuR增强IκBα表达并抑制NF-κB通路激活,减轻HSC受照后的炎性表型,而circRSF1通过结合HuR降低IκBα表达,促进HSC受照后的炎性表型。本研究在前期阐明circRSF1能够作为miRNA海绵的基础上进一步揭示circRSF1能够结合RBP发挥调控功能,丰富了circRNA在RILD发病过程中的调控机制。然而,体外细胞实验无法模拟体内复杂的微环境,因而后续研究需要在动物体内和临床实践中进一步验证。体外实验初步探索的机制和靶点为后续开展体内实验提供了研究方向和转化目的。如何实现HSC的靶向给药以及防止核酸类药物的体内降解等问题均是我们后续开展在体研究和临床转化的重要关注点。

