N乙酰L缬氨酸的合成与分析





摘要:建立高效液相色谱紫外检测分离测定L缬氨酸和N乙酰L缬氨酸的方法,以此为手段对N乙酰L缬氨酸的制备过程进行监控。研究了以L缬氨酸为原料,乙酸酐为乙酰化试剂制备N乙酰L缬氨酸的工艺。确定了乙酰化反应条件、中和结晶条件等,获得的优化工艺条件为:100 gL缬氨酸,500 mL水,90 mL乙酸酐,温度35 ℃,pH 8.0,反应时间2 h。随后用37%浓盐酸中和至pH 1.5,旋转蒸发,冷却结晶12 h,得N乙酰L缬氨酸产品。母液浓缩回收利用。产品总收率为122%,通过FTIR,HNMR和HPLC对其结构进行了确证,质量达到行业标准。
关键词:N乙酰L缬氨酸;乙酰化;L缬氨酸L缬氨酸是组成蛋白质的20种氨基酸之一,属于支链氨基酸,也是人体必需的8种氨基酸和生糖氨基酸,与异亮氨酸和亮氨酸一起作用可以促进身体正常生长,修复组织,调节血糖,并提供机体所需要的能量[1]。N乙酰L缬氨酸为重要的精细有机化工中间体,广泛应用于医药、农药、化学工业等领域[2]。氨基酸均有一个aNH2,可以与适当的乙酰化试剂反应,常用的乙酰化试剂有乙酸、乙酰氯和乙酸酐。使用乙酸进行乙酰化需在高温下反应,易导致氨基酸消旋;乙酰氯的反应活性过强,容易水解,不宜在水溶液中进行反应。因此最常用的乙酰化试剂是乙酸酐,在微碱性的水溶液中与氨基酸反应生成乙酰氨基酸[35]。
已有N乙酰L酪氨酸、N乙酰L半胱氨酸、N乙酰L亮氨酸、N乙酰L谷氨酸、N乙酰L苏氨酸等乙酰氨基酸制备的报道[611]。基本工艺是:将氨基酸溶解在弱碱性水溶液中,加入乙酸酐进行乙酰化反应,再从反应液中分离提取目标产物。由于各种氨基酸的侧链基团不同,物理、化学性质有很大差异,因此制备各种乙酰氨基酸的工艺方法和工艺参数都有所不同。尚未报道N乙酰L缬氨酸的制备。
高效液相色谱结合紫外检测已被用于酪氨酸等氨基酸的分离测定[1214],也被用于某些乙酰氨基酸的分离测定,如乙酰半胱氨酸,乙酰酪氨酸等[1520]。但未见分离测定L缬氨酸和N乙酰L缬氨酸的报道。
本文首先建立了一种高效液相色谱紫外检测分离测定L缬氨酸和N乙酰L缬氨酸的方法。以此为手段对制备N乙酰L缬氨酸的工艺过程进行监控,研究了乙酸酐用量、反应温度、反应时间等对乙酰化反应的影响,研究了产品的优化结晶条件,由此确定优化的制备工艺参数。
1实验部分
1.1仪器与试剂
LabTECH高效液相色谱仪:北京莱伯泰科仪器有限公司,配备紫外检测器;旋转蒸发器(RE-301E):上海互佳仪器设备有限公司);酸度计(PHS-25):杭州雷磁分析仪器厂;集热式恒温加热磁力搅拌器(DF-10S):天津华鑫仪器有限公司;蠕动泵(BT-100):重庆杰恒蠕动泵有限公司;循环水式多用真空泵(SHZ-D140)、傅里叶变换红外光谱仪(Nicolet iS50):赛默飞世尔科技(中国)有限公司;500 MHz核磁共振谱仪:AVANCE,美国布鲁克科技有限公司。
L缬氨酸:工业级,江苏汉菱生物工程有限公司提供;L缬氨酸标准品:采用工业级L缬氨酸精制;N乙酰L缬氨酸标准品:自制N乙酰L缬氨酸再精制;乙酸酐: 分析纯;氢氧化钠:工业级片碱,重庆天原化工公司;浓盐酸:37%,分析纯;甲醇为色谱纯试剂。其他试剂为分析纯以上。
1.2实验方法
1.2.1高效液相色谱分离测定L缬氨酸和N乙酰L缬氨酸1.2.1.1标准对照液的制备
分别称取0.250 g L缬氨酸、N乙酰L缬氨酸标准品,混合后加水溶解,转入250 mL容量瓶中以水定容,得质量浓度为1.00 g/L的L缬氨酸、N乙酰L缬氨酸混合标准溶液。试验时根据需要,准确移取适量混合标准溶液,稀释至一定体积,制备一定质量浓度的标准对照液。
1.2.1.2供试液的制备方法
准确移取或称取适量的样品,用水溶解后转入100 mL容量瓶中定容。
1.2.1.3色谱条件
色谱柱(C18,5 μm,250×4.6 mm id),流速0.8 mL/min,柱温35 ℃,进样体积20 μL,检测波长210 nm。
流动相:40/60甲醇/10 mmol/L磷酸盐,pH 3.0。其中10 mmol/L磷酸盐溶液:称取1.36 g磷酸二氢钾,加水约900 mL溶解,用10%稀磷酸调pH至3.0,再加水至1 000 mL。
1.2.2N乙酰L缬氨酸的制备方法
1.2.2.1L缬氨酸的乙酰化
将250 mL三口瓶置于磁力搅拌恒温水浴锅中,加入10 g L缬氨酸、100 mL水,将酸度计的pH电极插入瓶中监控物料pH。调节水浴锅温度至规定值,滴加30%NaOH至规定的pH。此时为乙酸酐加入零点,开始滴加规定量乙酸酐,同时滴加30%NaOH维持在规定的pH,滴加乙酸酐总耗时2 h,滴加完乙酸酐后再反应0.5 h。
1.2.2.2中和结晶
加37%浓盐酸中和至pH 1.5。旋转蒸发至70 mL,降温,搅拌结晶,12 h后抽滤,用水洗3次,80 ℃烘干得N乙酰L缬氨酸精品。母液另行处理。
1.2.2.3回收母液中N乙酰L缬氨酸
母液与洗水合并,旋转蒸发至出现结晶,缓缓降温,搅拌结晶,12 h后抽滤,得N乙酰L缬氨酸粗品,可用于下一批乙酰化时配料。
2结果与讨论
2.1分析方法的建立
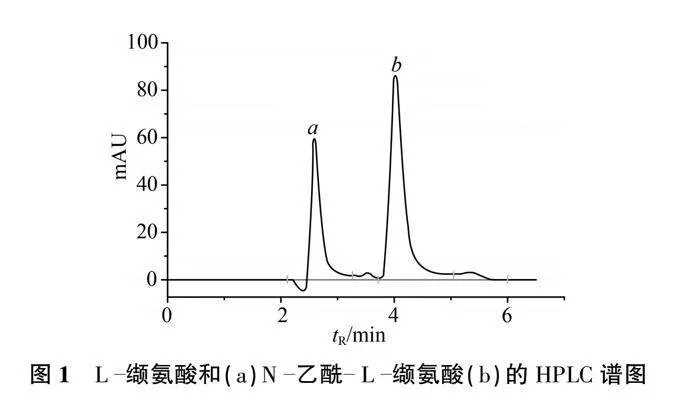
通过实验研究,建立了高效液相色谱分离测定L缬氨酸和N乙酰L缬氨酸的方法。典型色谱图见图1。
2.2乙酰化反应的影响因素
乙酸酐是氨基进行乙酰化的常用试剂,其反应活性适中,反应条件易控制。可在水溶液中与氨基酸的氨基反应生成N乙酰氨基酸。本研究选择乙酸酐对L缬氨酸进行乙酰化,反应式见图2。
在水溶液中,乙酸酐还会发生水解副反应,导致参与主反应的乙酸酐减少,需要增加乙酸酐用量。在乙酰化反应和乙酸酐水解过程中都会生成大量乙酸,为维持反应体系的pH,需加碱中和反应中产生的乙酸。
2.2.1乙酸酐用量对乙酰化反应的影响
采用1.2.2.1的方法,控制乙酰化反应pH在8.0左右,水浴温度为35 ℃,在滴加乙酸酐反应阶段,每滴加一定量乙酸酐,暂停滴加乙酸酐,但继续滴加30%NaOH维持pH,至pH不再降低为止。按1.2.1的方法对反应液取样,进行液相色谱分析,测定其中L缬氨酸和N乙酰L缬氨酸的含量,根据测定结果及取样时物料总质量,计算L缬氨酸和N乙酰L缬氨酸在反应液中的质量。结果见图3。
实验中发现,反应初期,溶液中的L缬氨酸与滴入的乙酸酐反应,导致其质量逐渐降低;生成N乙酰L缬氨酸的质量逐渐升高。直至乙酸酐用量达到9 mL以后N乙酰L缬氨酸曲线逐渐走平,残留在反应液中的L缬氨酸趋近于0 g。
表明L缬氨酸已被全部乙酰化,不再有新的N乙酰L缬氨酸生成。
理论上10 g L缬氨酸(0.085 4 mol)乙酰化需消耗乙酸酐8.1 mL。实验表明,当乙酸酐加入量为9 mL,即理论加入量的111%时, 溶液中已无L缬氨酸存在。为保证L缬氨酸反应完全,本研究选择乙酸酐加入量为9 mL。
2.2.2反应pH对乙酰化反应的影响
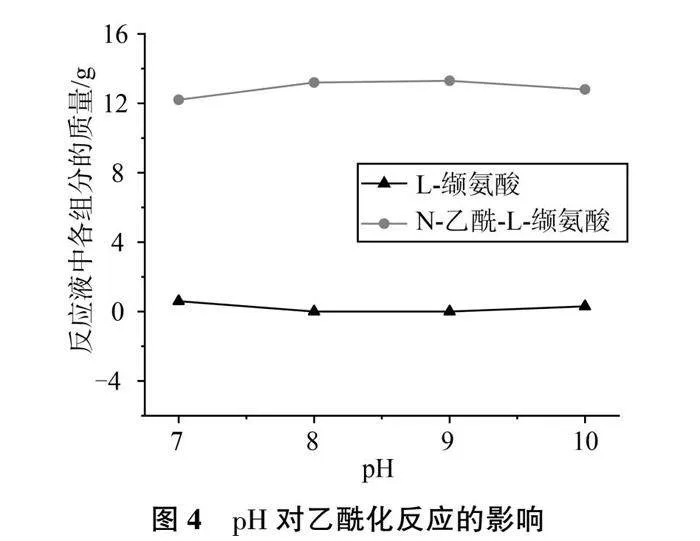
乙酸酐对氨基酸乙酰化一般宜在微碱性水溶液中进行,为考察反应pH对乙酰化反应的影响,按1.2.2.1的方法,控制乙酰化反应pH为不同值,水浴温度为35 ℃,均滴加9 mL乙酸酐,反应终止后取样分析,计算反应液中L缬氨酸和N乙酰L缬氨酸的质量,结果见图4。
实验发现,在pH 8~9的条件下乙酰化,都可以将L缬氨酸全部转化为N乙酰L缬氨酸;在pH 7的条件下乙酰化,会有少量L缬氨酸残留;在pH 10的条件下乙酰化,也有少量L缬氨酸残留。后面两种情况下如果继续滴加乙酸酐,仍然可以将所有L缬氨酸全部乙酰化,总的效果就是增大了乙酸酐的消耗量。本研究选择在pH 8.0的条件下进行乙酰化反应。
2.2.3反应温度对乙酰化反应的影响
为考察反应温度对乙酰化反应的影响,按1.2.2.1的方法,控制乙酰化反应pH为8.0,控制水浴温度为规定值,均滴加9 mL乙酸酐,反应终止后取样分析,计算反应液中L缬氨酸和N乙酰L缬氨酸的质量。
实验发现, 在25~55 ℃范围内,反应温度对乙酰化反应没有明显的影响,在55 ℃下乙酰化,反应液中残留少量L缬氨酸,仅占总量的1%左右。25~45 ℃条件下乙酰化,所有L缬氨酸全部乙酰化。本研究选择在35 ℃下进行乙酰化反应。
2.2.4反应时间对乙酰化反应的影响
由于可能存在乙酸酐水解的副反应,因此在乙酰化反应过程中,采用滴加乙酸酐的方式,而不是一次性加入全部乙酸酐。滴加乙酸酐的速度可能影响乙酰化反应。实验发现,乙酰化反应速度较快,滴加速度对乙酰化反应没有太大的影响,1 h滴完与3 h滴完乙酸酐,测定反应液中各组分质量,发现乙酰化反映的情况没有明显区别。考虑到滴入的乙酸酐在溶液中的搅拌分散情况,以及乙酸酐水解影响,滴入乙酸酐不应太快。本研究选择在2 h内滴完乙酸酐。
2.3N乙酰L缬氨酸的中和结晶
水解后的反应液中含有目标产物N乙酰L缬氨酸,还含有高质量浓度的乙酸钠及少量其他副产物。需将目标产物从反应液中结晶分离出来。
N乙酰L缬氨酸有一个游离羧基,其酸碱性质类似于乙酸,在较高pH下部分离解生成带负电荷的离子。只有在较低的pH条件下才会以不带净电荷的中性分子形式存在,此时其溶解度最低。因此实验中加入盐酸中和至pH 1.5。
由于N乙酰L缬氨酸在溶液中的溶解度较大,需将中和液旋转蒸发至70 mL,取下冷却结晶,20 ℃条件下过滤分离,洗涤,干燥得到N乙酰L缬氨酸精品10.6 g。得母液52 mL, 其中N乙酰L缬氨酸质量浓度为19 g/L,质量为0.98 g。洗水30 mL,其中N乙酰L缬氨酸质量浓度为50.5 g/L,质量为1.52 g。
经检测,N乙酰L缬氨酸产品质量符合行业标准(见表1)。
2.4母液处理
产品结晶母液及洗水中还含有一定量的N乙酰L缬氨酸,如果能部分回收,则产品收率可进一步提高。此母液中还含有高浓度的乙酸钠和氯化钠。实验发现,N乙酰L缬氨酸在纯水中的溶解度较大,在含有乙酸钠和氯化钠的溶液中溶解度较小。在饱和盐溶液中溶解度最小。因此,将结晶母液及洗水合并,再旋蒸至盐结晶刚刚出现,冷却,使N乙酰L缬氨酸结晶析出,过滤,不洗,可得N乙酰L缬氨酸粗品2.3 g(干重),经HPLC测定其中含N乙酰L缬氨酸70%,总量为1.6 g。此粗品在下一批次乙酰化时加入反应液中。
2.5原料消耗定额及产品收率
按照本研究选定的工艺条件进行放大实验,每次固定投料量为100 g L缬氨酸,并投入上一批次母液中回收的N乙酰L缬氨酸粗品,连续运行4批。得到制备N乙酰L缬氨酸工艺的原料消耗定额和产品收率,结果见表2。
3产物结构表征
3.1FTIR
主要官能团的吸收频率为:υ(O—H),3 303 cm-1,υ(N—H),3 101 cm-1,2 968 cm-1,υas(COO),1 604 cm-1,υs(COO),1 396 cm-1,υ(C—O),1 205 cm-1,由此可以确定该谱图为N乙酰L缬氨酸的红外吸收光谱图(见图5)。
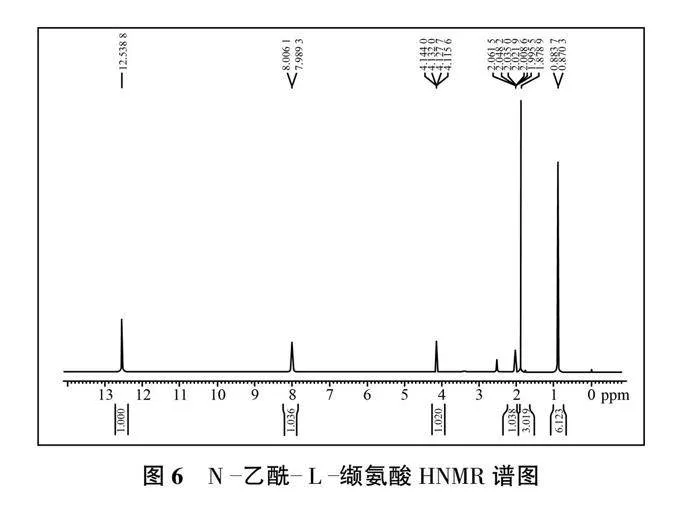
3.2HNMR
图6为产物HNMR。由图6可见:d=12.50处为—COOH中氢原子的共振峰,是受氨基吸电子效应影响的氢。d=8.00处为QSChNa中氢原子的共振峰;d=4.13处为—NH中氢原子的共振峰;d=1.87~2.06处为—CH2中氢原子的共振峰;d=0.87处为产物以甲基封端的—CH3的氢原子共振峰。
综合FT-IR和HNMR表征结果,证明产品为N乙酰L缬氨酸。
4结论
在微碱性水溶液中,用乙酸酐乙酰化L缬氨酸可制备N乙酰L缬氨酸。工艺条件温和,操作简便。优化工艺条件为:
(1) 乙酰化:100 g L缬氨酸,1 000 mL水,35 ℃,滴加90 mL乙酸酐,滴加30%NaOH保持pH 8.0。滴加乙酸酐时间2 h。
(2) 中和结晶:加37%浓盐酸中和至pH 1.5。旋转蒸发至溶液体积700 mL,冷却结晶12 h,抽滤,洗涤,80 ℃烘干得N乙酰L缬氨酸精品。
(3) 母液处理:旋转蒸发至出现结晶,冷却结晶12 h,抽滤,得N乙酰L缬氨酸粗品,可用于下一批乙酰化时配料。产品总收率为122%,产品质量符合行业标准。
参考文献:
[1]徐衡,张群,孔学军.N乙酰L半胱氨酸合成新方法[J].精细化工,2000(4):205207.
[2]徐衡,张群,孔学军.N乙酰L半胱氨酸合成新工艺[J].氨基酸和生物资源,2000(1):2326.
[3]张小林,杨期勇,孙曰圣.N乙酰L谷氨酸的制备[J].化学世界,2002(7):363365.
[4]王伟,李华,杨开伦.N乙酰苏氨酸合成的初探[J].化学工业与工程,2007(6):476479.
[5]史黎黎,秦凡.正交设计优化N乙酰L亮氨酸的合成研究[J].江汉大学学报(自然科学版),2007(2):4446.
[6]吴传隆. 高纯度N乙酰D,L缬氨酸的高效生产方法:中国,103408474A[P].
[7]徐红岩,孙雪峰,颜行,等.一种(2S)2(乙酰氨基)4(甲基亚磺酸酰基)丁酸的合成方法:中国,109053504A[P].
[8]李援朝,薛志杰.一种合成多卡巴胺的方法. 中国,1470506[P].
[9]新沂市汉菱生物工程有限公司. 一种N乙酰L酪氨酸的生产方法:中国, 102827018A[P].
[10]陈士安. 一种生产乙酰酪氨酸的方法:中国,106748870A[P].
[11]刘爱福. N乙酰L酪氨酸的制备方法:中国,1594283A[P].
[12]周桂友,侯艳芳,董新吉.柱前衍生反相高效液相色谱法测定氨基酸[J].理化检验(化学分册),2011,47(8):889893.
[13]陈恭铭. 高效液相色谱法测定复方氨基酸注射液中的酪氨酸和色氨酸含量[J].海峡药学,2014,26(4):8283.
[14]田丽萍,杨绪庆,卜晓萍. 高效液相色谱法联合测定新生儿血中苯丙氨酸和酪氨酸的应用[J]. 现代预防医学,2012,39(11):28142816.
[15]陈宇堃,梁蔚阳. HPLC法测定小儿复方氨基酸注射液(19AAⅠ)中乙酰酪氨酸含量[J].中国生化药物杂志,2015,35(5):166168.
[16]纪宇. RP-HPLC 法测定17 种复方氨基酸注射液中的N乙酰L半胱氨酸和N乙酰L酪氨酸[ J].药物分析杂志,2002,22(3):240241.
[17]吴小曼,纪宇. 反相高效液相色谱法测定复方氨基酸注射液中的乙酰半胱氨酸和乙酰酪氨酸[J].中国生化药物杂志,2003(4):194195.
[18]陈永波,饶斌,沈艳芬,等. 高效液相色谱法测定17AA氨基酸注射液中N乙酰L半胱氨酸和N乙酰L酪氨酸[J].氨基酸和生物资源,2002(4):6770.
[19]高春,纪宏,高恒莹,等. 复合氨基酸注射液(17AA)中N乙酰L酪氨酸及N乙酰L半胱氨酸的HPLC测定[J].中国医药工业杂志,2001(2):1718.
[20]高春,周淑平,李群,等. 18种复合氨基酸注射液中N乙酰L酪氨酸及L色氨酸含量测定方法的研究[J].中国生化药物杂志,1998(3):144145.

