秦岭特色药用植物桃儿七内生真菌代谢产物的分离鉴定及生物活性研究
李 婷,赵 祥,潘会宾,王 懿,高吉仁
(商洛职业技术学院公共课教学部,陕西 商洛726000)
桃儿七[Sinopodophyllumhexandrum(Royle) Ying]是小檗科鬼臼亚科桃儿七属植物,主要分布在我国西北和西南地区[1]。作为传统中药材,桃儿七对血病、胎盘滞留及中风等疾病具有显著疗效[2]。研究发现,桃儿七根和茎中糖苷衍生物在睾丸癌、淋巴癌、白血病和小细胞肺癌治疗中发挥着重要作用[3-4],且其有效成分鬼臼毒素是合成抗癌药物的前体物质[5]。近年来,随着医学的发展及抗癌药物需求量的增加,桃儿七的需求量也随之增加,但桃儿七已被列入珍稀濒危植物,因此,合理开发其潜在的药用价值具有重要意义。
植物内生真菌[6]在植物生长过程中具有促生、抗逆等积极作用,可帮助寄主植物合成次级代谢产物或完成代谢物的生物转化[7]。内生真菌长期与寄主植物共存,可产生与宿主植物相同或相近的具有生物活性的次级代谢产物,这些代谢产物具有抗菌、抗肿瘤及抗氧化等作用,是筛选活性物质的潜在资源[8]。研究者[9-10]已从桃儿七根和茎中分离到了可产鬼臼毒素的内生真菌,但真菌代谢产生的生物活性物质不能达到工业生产要求,不利于菌种的扩大筛选[11]。由于桃儿七植物不同产地、不同营养器官中生物活性物质的含量差异较大[12],作者以秦岭桃儿七内生烟色拟盘多毛孢菌为研究对象,采用萃取法从菌丝中分离活性代谢产物,对其结构进行鉴定,并对其生物活性进行初步分析,为桃儿七内生真菌活性药用成分的开发利用提供理论依据。
1 实验
1.1 材料、试剂与仪器
桃儿七,采自陕西秦岭山,海拔高度377.12 m。采样时挑选无病害健康植株,取材部位为植物根、茎、叶。
马铃薯葡萄糖琼脂(PDA)固体培养基:200 g土豆,20 g葡萄糖,20 g琼脂,1 000 mL水。PDA液体培养基不加琼脂。
葡萄糖(分析纯)、冰醋酸(色谱纯)、丙酮(色谱纯)、石油醚(色谱纯),国药集团化学试剂有限公司;琼脂、乙酸乙酯(色谱纯),美国Sigma公司;甲醇(色谱纯),上海科旺化学试剂有限公司;Sephadex LH-20羟丙基葡聚糖凝胶,Pharmacia公司;薄层色谱用硅胶,西安道生化工科技有限公司;200~300目色谱柱硅胶,青岛海洋化工厂;(R)-(-)-α-甲氧基-α-(三氟甲基)苯乙酰氯[(R)-MTPA],Alfa Aesar 公司。
AM-400型核磁共振波谱仪,德国Bruker公司;Auto-Spec3000型质谱仪,英国VG公司;RP-18反相硅胶色谱柱,美国Merck公司;手提式不锈钢压力蒸汽灭菌器,上海三申医疗器械有限公司;SW-CJ-2D型垂直流超净工作台,苏州净化设备有限公司;真空泵,巩义予华仪器有限责任公司;iMark型酶标仪,日本Bio-Rad Laboratories公司。
1.2 内生真菌的分离及代谢产物提取
对桃儿七根、茎、叶表面消毒后,置于PDA固体培养基上,以组织块法分离出内生真菌,经纯化后得到烟色拟盘多毛孢菌。
将烟色拟盘多毛孢菌活化后接入PDA液体培养基中,于28 ℃振荡培养12 d,抽滤;菌丝用乙酸乙酯-甲醇-冰醋酸(80∶15∶5,体积比)浸提3次,合并提取液,经乙酸乙酯萃取后得浸膏。以RP-18反相硅胶色谱柱处理浸膏,采用水及体积分数30%、50%、70%、100%丙酮梯度洗脱,采用薄层色谱法(TLC)和反复硅胶柱色谱(洗脱剂为石油醚-乙酸乙酯)分离得到10个单体化合物,分别标记为1-1、1-2、1-3、1-4、1-5、1-6、1-7、1-8、1-9、1-10。
1.3 化合物的Mosher酯制备及表征
分别将化合物1-1、1-2、1-3和1-4分为 2 部分,用无水吡啶溶解后加入10 μL 的(R)-MTPA,于30 ℃下搅拌12 h,蒸干有机溶剂,以Sephadex LH-20凝胶柱纯化产物,通过氘代甲醇(CD3OD)核磁共振(NMR)和异核单量子关系(HSQC)确定仲醇羟基的β-、γ-和δ-位的各个质子的化学位移变化,确定化合物的绝对构型[13]。
1.4 化合物的细胞毒活性检测
以依托泊苷为阳性对照,参照El-Sayed等[14]方法,采用3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT) 比色法检测化合物1-1~1-10对人非小细胞肺癌细胞A549、人宫颈癌细胞HeLa和人肝癌细胞HepG2的细胞毒活性。将对数生长期的A549、HeLa和HepG2细胞悬液分别接种于96孔板中,37 ℃下培养1 d,加入经二甲基亚砜(DMSO)稀释的化合物溶液,每个化合物做3个复孔,置于培养箱中培养36 h,取出,加入MTT培养4 h,弃上清,每孔加入DMSO 150 μL,测定570 nm处吸光度,按式(1)计算细胞抑制率(R,%):
(1)
式中:Ae为实验组的吸光度;Ab为空白组的吸光度;Ac为对照组的吸光度。
1.5 乙酰胆碱酯酶抑制活性检测
参照dos Santos等[15]方法,采用Ellman光度法检测乙酰胆碱酯酶抑制活性。将150 μL浓度为0.1 mol·L-1的磷酸盐缓冲液(pH值8.04)加入96孔板中,依次加入30 μL化合物溶液、50 μL 5,5′-二硫代双(2-硝基苯甲酸)(756 μmol·L-1)、20 μL稀释后的乙酰胆碱酯酶溶液(0.54 U·mL-1);以加兰他敏作为阳性对照,以磷酸盐缓冲液作为阴性对照。混匀后置于37 ℃培养箱孵育5 min,加入50 μL底物碘化硫代乙酰胆碱(3 mmol·L-1),用酶标仪在405 nm处检测动力学速率,按式(2)计算抑制率(R,%):
(2)
式中:Ke、Kp、Kn分别为实验组、阳性对照组、阴性对照组的动力学速率。
由于抑制率与浓度之间存在一定的线性关系,通过回归方程计算IC50值,并依据IC50值评价乙酰胆碱酯酶的抑制活性。
1.6 α-葡萄糖苷酶抑制活性检测
参照文献[16]方法并作适当修改。将99 μL浓度为 67 mmol·L-1的磷酸盐缓冲液(pH值 6.8)加入96孔板中,加入DMSO稀释的不同浓度(1.0 mmol·L-1、0.5 mmol·L-1、0.25 mmol·L-1和0.1 mmol·L-1)化合物溶液1 μL,然后加入25 μL α-葡萄糖苷酶(0.4 U·mL-1),置于37 ℃培养箱孵育10 min;取出,加入25 μL底物对硝基苯酚、α-D-吡喃葡萄糖苷(p-NPG)(5.0 mmol·L-1),置于37 ℃培养箱孵育10 min;加入50 μL Na2CO3溶液(0.2 mol·L-1)终止反应,测定405 nm处吸光度,重复测定3次,结果取平均值,并计算半抑制浓度(IC50)。以阿卡波糖作为阳性对照,反应体系总体积为200 μL。
1.7 数据统计处理
2 结果与讨论
2.1 化合物结构鉴定

表1 化合物1-1的1HNMR和13CNMR数据(CD3OD)Tab.1 1HNMR and 13CNMR data of compound 1-1 in CD3OD
化合物1-1的分子式为C17H22O6(计算值为345.130 8;不饱和度为7),综合分析13CNMR、DEPT和HSQC图谱信息,表明化合物1-1含有4个甲基[δH2.10(3H,s,OAc-17),1.47(3H,s,CH3-13),1.32(3H,s,CH3-14),0.97(3H,d,J=7.1 Hz,CH3-15);δC20.61(q,C-17),11.20(q,CH3-13),22.46(q,CH3-14),10.30(q,CH3-15)];2个亚甲基[δH3.79(1H,d,J=9.8 Hz,H-12),3.71(1H,dd,J=9.3 Hz、4.7 Hz,H-12a),2.25(1H,d,J=13.2 Hz,H-6),1.52(1H,d,J=13.2 Hz,H-6a);δC71.18(t,C-12),34.96(t,C-6)];5个次甲基[δH6.38(1H,s,H-9),5.14(1H,t,J=5.2 Hz,H-3),3.72(1H,dd,J=9.3 Hz、4.7 Hz,H-2),3.63(1H,d,J=3.8 Hz,H-1),1.80(1H,dd,J=7.0 Hz、5.7 Hz,H-4);δC125.29(d,C-9),72.84(d,C-3),54.83(d,C-2),58.97(d,C-1),45.41(d,C-4)];1个羰基碳[δC172.35(s,C-16)];5个脂肪族季碳[δC146.94(s,C-10),101.92(s,C-8),70.49(s,C-7),63.34(s,C-11),41.38(s,C-5)]。结合1H与1H-COSY的相关关系H-2/H-3、H-3/H-4、H-4/H-15及1H与HMBC的相关关系H-1/C-5,9、H-2/C-4,10、H-3/C-5,16、H-4/C-6,10,14、H-6/C-4,10,14、H-9/C-5,7、H-12/C-7,8、H-13/C-7,12、H-14/C-4,10、H-15/C-3,5,分析化合物1-1与已知化合物eremofortin C-1的13CNMR数据发现,两个化合物的13CNMR数据基本接近。与文献[17]数据比对发现,化合物1-1与已知化合物eremofortin C-1的结构相似,化合物1-1中δC101.92(C-8)与化合物eremofortin C-1中δC102.41(C-8)之间仅相差0.49 ppm;分析HR-ESI-MS数据发现,两个化合物的分子离子峰之间仅相差14,由此初步确定为失去了一个亚甲基的碎片,再根据化合物1-1的IR光谱在2 939 cm-1处出现一个宽的吸收谱带,可以确定连接在eremofortin C-1的C-8位上是一个甲氧基,而连接在化合物1-1的C-8位上是一个羟基。通过SciFinder数据库搜索,最终确定化合物1-1是一个新的艾里莫芬烷型倍半萜类化合物,命名为pestalotiopnoid A。化合物1-1的相对构型通过NOESY数据推理得到,以圆二色谱(CD)计算确定其绝对构型(图1)。
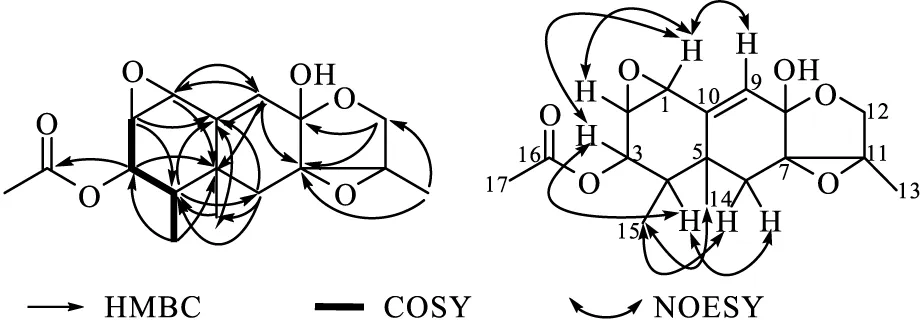
图1 化合物1-1的关键HMBC、COSY和NOESYFig.1 Key HMBC,COSY,and NOESY of compound 1-1
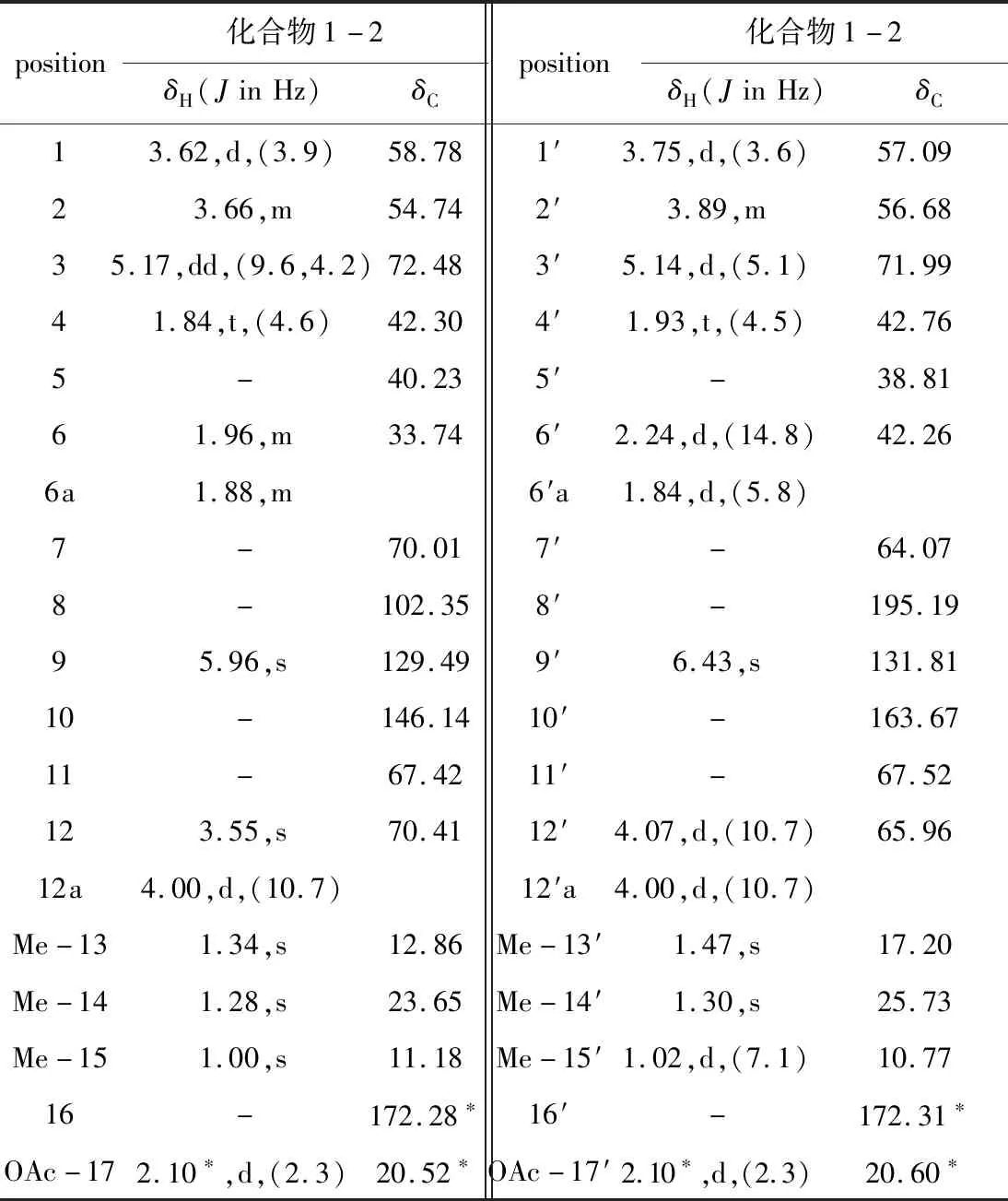
表2 化合物1-2的1HNMR和13CNMR数据(CD3OD)Tab.2 1HNMR and 13CNMR data of compound 1-2 in CD3OD
化合物1-2的分子式为C34H42O11(计算值为649.261 9;不饱和度为14),综合分析13CNMR、DEPT和HSQC图谱信息,表明化合物1-2含有8个甲基[δH2.10*(6H,d,J=2.3 Hz,OAc-17,17′),1.34(3H,s,CH3-13),1.47(3H,s,CH3-13′),1.28(3H,s,CH3-14),1.30(3H,s,CH3-14′),1.00(3H,s,CH3-15),1.02(3H,d,J=7.1 Hz,CH3-15′);δC25.73(q,CH3-14′),23.65(q,CH3-14),20.60*(q,C-17′),20.52*(q,C-17),17.20(q,CH3-13′),12.86(q,CH3-13),11.18(q,CH3-15),10.77(q,CH3-15′)];4个亚甲基[δH4.07(1H,d,J=10.7 Hz,H-12′),4.00(2H,d,J=10.7 Hz,H-12′a,12a),3.55(1H,s,H-12),2.24(1H,d,J=14.8 Hz,H-6′),1.84(1H,d,J=5.8 Hz,H-6′a),1.96(1H,m,H-6),1.88(1H,m,H-6a);δC70.41(t,C-12),65.96(t,C-12′),42.26(t,C-6′),33.74(t,C-6)];10个次甲基[δH5.96(1H,s,H-9),6.43(1H,s,H-9′),5.17(1H,dd,J=9.6 Hz、4.2 Hz,H-3),5.14(1H,d,J=5.1 Hz,H-3′),3.62(1H,d,J=3.9 Hz,H-1),3.75(1H,d,J=3.6 Hz,H-1′),3.66(1H,m,H-2),3.89(1H,m,H-2′),1.84(1H,t,J=4.6 Hz,H-4),1.93(1H,t,J=4.5 Hz,H-4′);δC131.81(d,C-9′),129.49(d,C-9),72.48(d,C-3),71.99(d,C-3′),58.78(d,C-1),57.09(d,C-1′),56.68(d,C-2′),54.74(d,C-2),42.76(d,C-4′),42.30(d,C-4)];3个羰基碳[δC195.19(s,C-8′),172.31*(s,C-16′),172.28*(s,C-16)];9个脂肪族季碳[δC163.67(s,C-10′),146.14(s,C-10),102.35(s,C-8),70.01(s,C-7),67.52(s,C-11′),67.42(s,C-11),64.07(s,C-7′),40.23(s,C-5),38.81(s,C-5′)]。结合1H与1H-COSY的相关关系H-1/H-2、H-2/H-3、H-3/H-4、H-4/H-15、H-1′/H-2′、H-2′/H-3′、H-3′/H-4′、H-4′/H-15′及1H与HMBC的相关关系H-1/C-5,9、H-2/C-4,10、H-3/C-5,15,16、H-4/C-2,6,10,14、H-6/C-4,8,13,14、H-9/C-1,5,7、H-12/C-7,13、H-13/C-7,12、H-14/C-4,6,10、H-15/C-3,5、H-1′/C-5′,9′、H-2′/C-4′,10′、H-3′/C-5′,15′,16′、H-4′/C-2′,6′,10′,14′、H-6′/C-4′,8′,13′,14′、H-9′/C-1′,5′,7′、H-12′/C-7′,8′,13′、H-13′/C-7′,12′、H-14′/C-4′,6′,10′、H-15′/C-3′,5′,通过HR-ESI-MS数据和C-8(δC102.35)、C-12(δC70.41)及H-12′/C-8之间的长程耦合关系,可以确定化合物1-2中存在一个由C-11′/C-12′/O/C-8组成的醚键,且化合物1-2是由具有高氧化度的化合物PR-toxin和化合物1-1之间脱去一分子水成醚缩合而成。通过SciFinder数据库搜索和相关文献[18]调研,确定化合物1-2是一个新的艾里莫芬烷型倍半萜类化合物,命名为pestalotiopnoid B,通过NOESY数据推理得到其相对构型。对已知化合物eremofortin C-1进行单晶培养并结合相关文献调研,利用X-射线单晶衍射证实了化合物1-2的平面结构并确定其绝对构型(图2)。
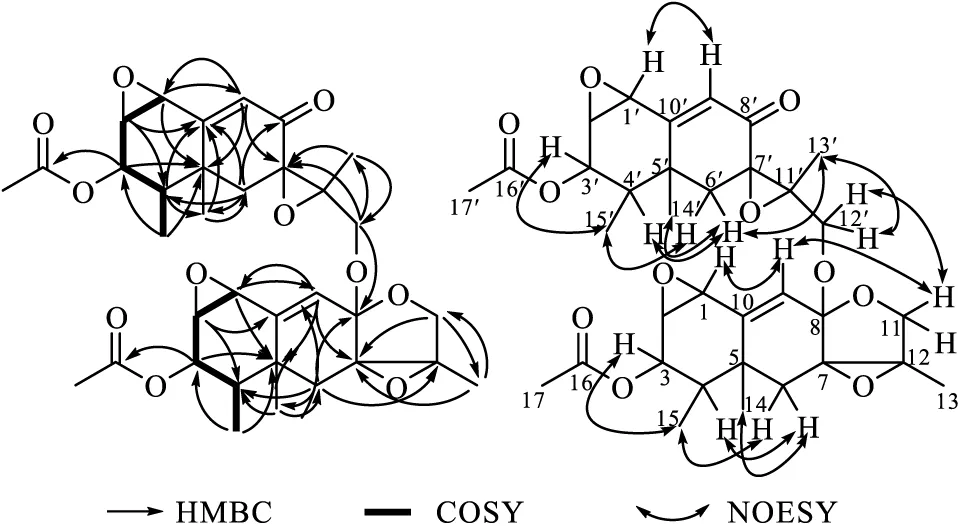
图2 化合物1-2的关键HMBC、COSY和NOESYFig.2 Key HMBC,COSY,and NOESY of compound 1-2
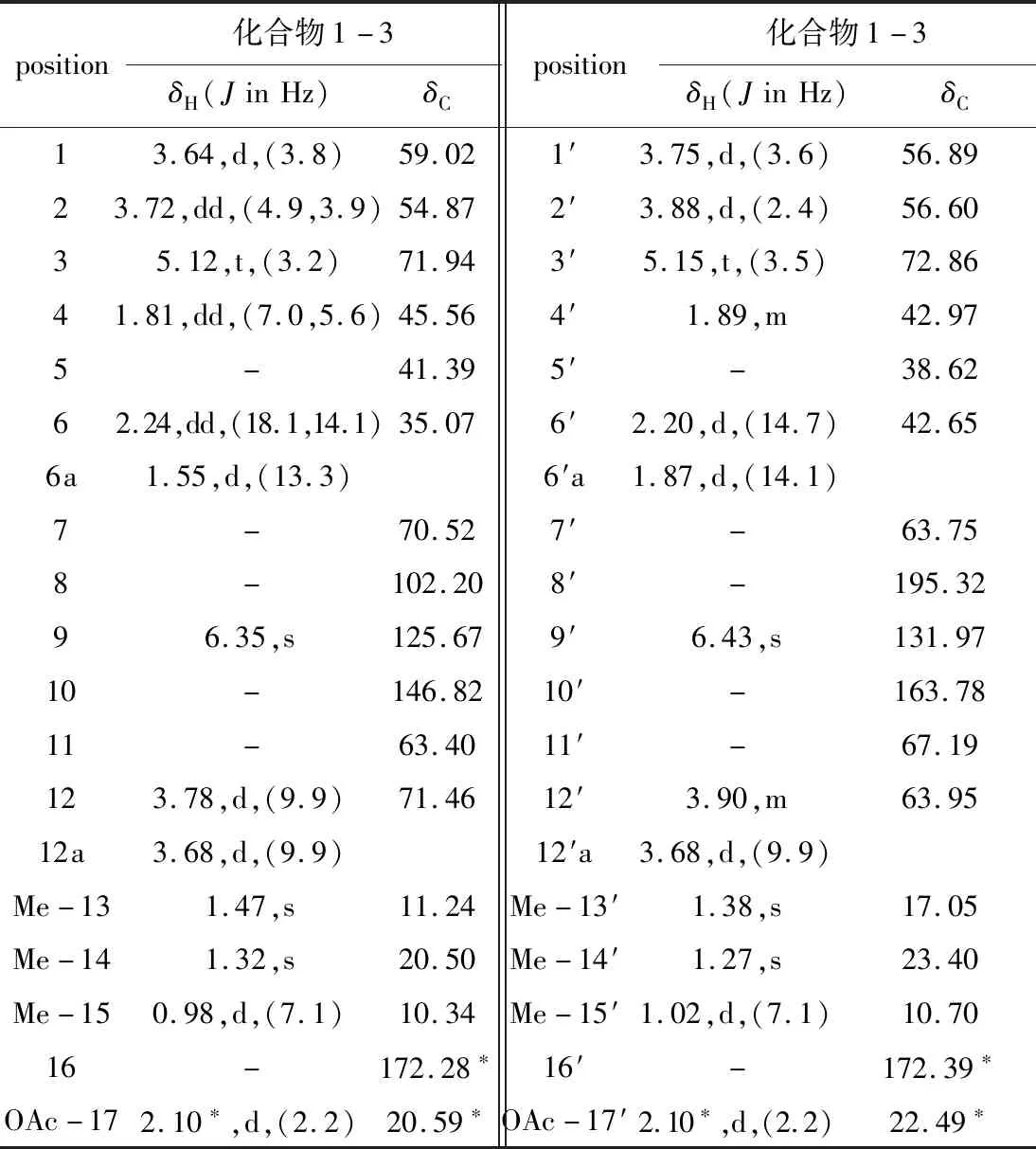
表3 化合物1-3的1HNMR和13CNMR数据(CD3OD)Tab.3 1HNMR and 13CNMR data of compound 1-3 in CD3OD
化合物1-3的分子式为C34H42O11(计算值为649.261 9;不饱和度为14),综合分析13CNMR、DEPT和HSQC图谱信息,表明化合物1-3中含有8个甲基[δH2.10*(6H,d,OAc-17,17′),1.38(3H,s,CH3-13′),1.47(3H,s,CH3-13),1.27(3H,s,CH3-14′),1.32(3H,s,CH3-14),0.98(3H,d,J=7.1 Hz,CH3-15),1.02(3H,d,J=7.1 Hz,CH3-15′);δC23.40(q,CH3-14′),22.49*(q,C-17′),20.59*(q,C-17),20.50(q,CH3-14),17.05(q,CH3-13′),11.24(q,CH3-13),10.70(q,CH3-15′),10.34(q,CH3-15)];4个亚甲基[δH3.78(1H,d,J=9.9 Hz,H-12),3.90(1H,m,H-12′),3.68(1H,d,J=9.9 Hz,H-12a),1.55(1H,d,J=13.3 Hz,H-6a),2.24(1H,dd,J=18.1 Hz、14.1 Hz,H-6),1.87(1H,d,J=14.1 Hz,H-6′a),2.20(1H,d,J=14.7 Hz,H-6′);δC71.46(t,C-12),63.95(t,C-12′),42.65(t,C-6′),35.07(t,C-6)];10个次甲基[δH6.35(1H,s,H-9),6.43(1H,s,H-9′),5.15(1H,t,J=3.5 Hz,H-3′),5.12(1H,t,J=3.2 Hz,H-3),3.64(1H,d,J=3.8 Hz,H-1),3.75(1H,d,J=3.6 Hz,H-1′),3.72(1H,dd,J=4.9 Hz、3.9 Hz,H-2),3.88(1H,d,J=2.4 Hz,H-2′),1.81(1H,dd,J=7.0 Hz、5.6 Hz,H-4),1.89(1H,m,H-4′);δC131.97(d,C-9′),125.67(d,C-9),72.86(d,C-3′),71.94(d,C-3),59.02(d,C-1),56.89(d,C-1′),56.60(d,C-2′),54.87(d,C-2),45.56(d,C-4),42.97(d,C-4′)];3个羰基碳[δC195.32(s,C-8′),172.39*(s,C-16′),172.28*(s,C-16)];9个脂肪族季碳[δC163.78(s,C-10′),146.82(s,C-10),102.20(s,C-8),70.52(s,C-7),67.19(s,C-11′),63.40(s,C-11),63.75(s,C-7′),41.39(s,C-5),38.62(s,C-5′)]。结合1H与1H-COSY的相关关系H-1/H-2、H-2/H-3、H-3/H-4、H-4/H-15、H-1′/H-2′、H-2′/H-3′、H-3′/H-4′、H-4′/H-15′及1H与HMBC的相关关系H-1/C-5,9、H-2/C-4,10、H-3/C-5,15,16、H-4/C-2,6,10,14、H-6/C-4,8,13,14、H-9/C-1,5,7、H-12/C-7,13、H-13/C-7,12、H-14/C-4,6,10、H-15/C-3,5、H-1′/C-5′,9′、H-2′/C-4′,10′、H-3′/C-5′,15′,16′、H-4′/C-2′,6′,10′,14′、H-6′/C-4′,8′,13′,14′、H-9′/C-1′,5′,7′、H-12′/C-7′,8′,13′、H-13′/C-7′,12′、H-14′/C-4′,6′,10′、H-15′/C-3′,5′,通过HR-ESI-MS数据和相关NMR数据,可以确定化合物1-3与化合物1-2结构相同,造成13CNMR数据不同的原因可能是化合物1-3与1-2的构型不同,因此,化合物1-3命名为pestalotiopnoid C。化合物1-3的相对构型通过NOESY数据推理得到,以CD计算确定其绝对构型(图3)。
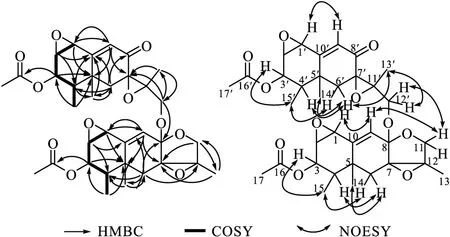
图3 化合物1-3的关键HMBC、COSY和NOESYFig.3 Key HMBC,COSY,and NOESY of compound 1-3

表4 化合物1-4的1HNMR和13CNMR数据(CDCl3)Tab.4 1HNMR and 13CNMR data of compound 1-4 in CDCl3
化合物1-4的分子式为C18H28O6(计算值为363.177 8;不饱和度为5),综合分析13CNMR、DEPT和HSQC图谱信息,表明化合物1-4中含有4个甲基[δH2.02(3H,s,CH3-15),1.59(3H,s,CH3-16),1.16(3H,s,CH3-13),1.03(3H,s,CH3-12);δC27.16(q,CH3-12),24.07(q,CH3-13),21.56(q,C-15),19.06(q,CH3-16)];3个亚甲基[δH4.34(1H,d,J=11.3 Hz,H-18),3.95(1H,d,J=11.0 Hz,H-18a),2.29(1H,dd,J=11.8 Hz、4.1 Hz,H-8),1.56(1H,d,J=11.6 Hz,H-8a),1.92(1H,dd,J=12.9 Hz、6.3 Hz,H-11),1.74(1H,dd,J=12.9 Hz、10.9 Hz,H-11a);δC64.70(t,C-18),38.87(t,C-8),32.85(t,C-11)];5个次甲基[δH5.88(1H,d,J=2.5 Hz,H-4),5.24(1H,dd,J=11.5 Hz、4.1 Hz,H-9),3.78(1H,dd,J=9.2 Hz、2.0 Hz,H-5),3.24(1H,dd,J=10.7 Hz、6.3 Hz,H-2),2.89(1H,d,J=9.2 Hz,H-6);δC138.95(d,C-4),75.60(d,C-5),74.67(d,C-9),65.58(d,C-6),41.43(d,C-2)];5个脂肪族季碳[δC170.44(s,C-14),137.91(s,C-3),79.24(s,C-1),56.78(s,C-7),43.07(s,C-10)];1个甲氧基[δH3.42(3H,s,OCH3-17);δC57.69(OCH3-17)]。结合1H与1H-COSY的相关关系H-2/H-11、H-4/H-5、H-5/H-6、H-8/H-9及1H与HMBC的相关关系H-2/C-10,18、H-4/C-2、H-5/C-7,17、H-6/C-8,16、H-8/C-1,16、H-9/C-2,14、H-11/C-1,3,12,13、H-12/C-1,13、H-13/C-1,11,12、H-16/C-6,8、OCH3-17/C-5、H-18/C-2,4,通过HR-ESI-MS和C-6(δC65.58)、C-7(δC56.78)等数据,可以确定化合物1-4含有一个由C-6/O/C-7组成的环氧结构。通过SciFinder数据库搜索和相关文献[19]调研,确定化合物1-4是一个新的石竹烯型倍半萜类化合物,命名为pestalotiopsin K,通过NOESY数据推理得到其相对构型。对该化合物进行单晶培养,再利用X-射线单晶衍射证实其平面结构并确定其绝对构型(图4)。通过单晶结果及相关数据可知,化合物1-4的OH-1与OH-18之间形成氢键,在空间上构成4/6/9三环网状骨架(图5)。
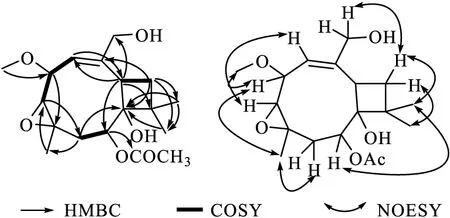
图4 化合物1-4的关键HMBC、COSY和NOESYFig.4 Key HMBC,COSY,and NOESY of compound 1-4
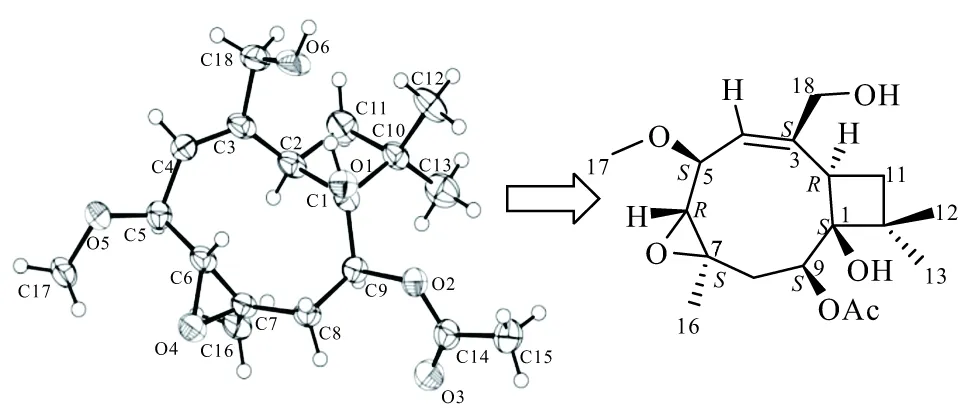
图5 化合物1-4的X-射线单晶衍射ORTEP图Fig.5 XRD ORTEP diagram of compound 1-4
化合物1-5:无色油状液体;HR-ESI-MS,m/z:393.130 8([M+Na]+,C21H22O6Na+;计算值:393.131 4);1HNMR(400 MHz,CD3OD),δ:6.58(1H,dd,J=2.3 Hz、0.8 Hz,H-6),6.57(1H,d,J=2.2 Hz,H-8),6.08(1H,dd,J=5.7 Hz、2.5 Hz,H-13),5.99(1H,dd,J=5.7 Hz、1.8 Hz,H-14),5.68(1H,d,J=2.3 Hz,H-18),5.66(1H,d,J=2.2 Hz,H-19),4.78(1H,m,H-17),3.77(1H,d,J=5.8 Hz,H-16),3.57(1H,d,J=1.6 Hz,H-11),2.93(1H,m,H-12),2.61(3H,s,CH3-21),1.63(3H,s,CH3-20),1.24(3H,d,J=7.2 Hz,CH3-22);13CNMR(100 MHz,CD3OD),δ:168.78(C-2),163.38(C-4),162.53(C-9),158.98(C-7),143.83(C-13),139.44(C-5),131.16(C-18),129.85(C-14),128.47(C-19),116.36(C-6),111.62(C-15),105.84(C-10),104.37(C-3),101.50(C-8),78.18(C-16),67.82(C-17),52.23(C-11),47.35(C-12),21.73(CH3-21),21.42(CH3-22),13.54(CH3-20)。通过与文献[11]NMR数据对比,确定化合物1-5为pestalustaine B(图6a)。

图6 化合物1-5(a)和1-6(b)的结构式Fig.6 Structural formulas of compounds 1-5(a) and 1-6(b)
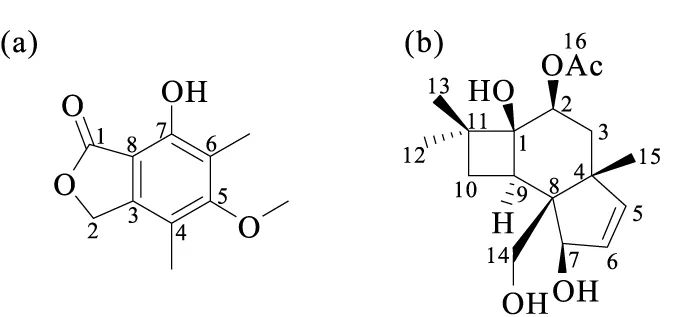
图7 化合物1-7(a)和1-8(b)的结构式Fig.7 Structural formulas of compounds 1-7(a) and 1-8(b)
化合物1-8:白色无定形固体;HR-ESI-MS,m/z:333.167 6([M+Na]+,C17H26O5Na+;计算值:333.167 2);1HNMR(400 MHz,CDCl3),δ:5.73(1H,dd,J=5.9 Hz、2.6 Hz,H-6),5.67(1H,d,J=5.9 Hz,H-5),5.32(1H,dd,J=10.5 Hz、5.7 Hz,H-2),4.16(1H,d,J=2.9 Hz,H-7),3.71(1H,d,J=11.7 Hz,H-14a),2.54(1H,dd,J=12.7 Hz、8.0 Hz,H-9),2.10(1H,dd,J=12.7 Hz、9.2 Hz,H-10a),1.58(1H,dd,J=9.0 Hz、8.1 Hz,H-10b),1.78(2H,s,H-3),2.02(3H,s,CH3-17),1.08(3H,s,CH3-12),1.12(3H,s,CH3-13),1.06(3H,s,CH3-15);13CNMR(100 MHz,CDCl3),δ:170.44(C-16),141.64(C-5),129.58(C-6),87.34(C-7),79.92(C-1),72.48(C-2),62.10(C-14),54.94(C-8),50.40(C-4),47.06(C-9),42.31(C-11),36.42(C-3),35.06(C-10),23.54(CH3-15),23.39(CH3-12),23.33(CH3-13),21.40(CH3-17)。通过与文献[19]NMR数据对比,确定化合物1-8为punctaporonin L(图7b)。
化合物1-9:淡黄色油状液体;HR-ESI-MS,m/z:333.167 8([M+Na]+,C17H26O5Na+;计算值:333.167 8);1HNMR(400 MHz,CDCl3),δ:5.95(1H,s,H-5),5.94(1H,s,H-7),5.67(1H,d,J=13.6 Hz,H-6),4.86(1H,t,J=5.3 Hz,H-2),4.16(2H,d,J=11.5 Hz,H-14),3.48(1H,m,H-9),2.91(1H,d,J=5.9 Hz,H-3a),1.55(1H,d,J=16.6 Hz,H-3b),2.20(1H,t,J=11.9 Hz,H-10a),1.63(1H,d,J=9.8 Hz,H-10b),2.09(3H,s,CH3-17),1.21(3H,s,CH3-15),1.14(3H,s,CH3-12),1.12(3H,s,CH3-13);13CNMR(100 MHz,CDCl3),δ:172.31(C-16),143.68(C-5),137.43(C-8),128.63(C-7),123.88(C-6),81.22(C-1),75.79(C-2),72.56(C-4),65.06(C-14),44.78(C-3),40.36(C-11),39.23(C-9),33.64(C-10),31.20(CH3-15),24.23(CH3-12),23.37(CH3-13),21.45(CH3-17)。通过与文献[23]NMR数据对比,确定化合物1-9为punctaporonin H(图8a)。

图8 化合物1-9(a)和1-10(b)的结构式Fig.8 Structural formulas of compounds 1-9(a) and 1-10(b)
化合物1-10:白色粉末状固体;HR-ESI-MS,m/z:275.162 3([M+Na]+,C15H24O3Na+;计算值:275.162 3);1HNMR(400 MHz,CD3OD),δ:5.74(1H,dd,J=5.9 Hz、2.4 Hz,H-6),5.71(1H,d,J=5.9 Hz,H-7),4.14(1H,d,J=2.4 Hz,H-5),3.66(1H,d,J=11.2 Hz,H-14a),2.49(1H,dd,J=12.8 Hz、7.8 Hz,H-9),2.05(1H,m,H-10a),1.55(1H,m,H-10b),1.99(1H,m,H-2a),1.33(1H,dt,J=12.3 Hz、5.5 Hz,H-2b),1.84(1H,dd,J=9.2 Hz、3.8 Hz,H-3),1.13(3H,s,CH3-12),1.06(3H,s,CH3-13),1.02(3H,s,CH3-15);13CNMR(100 MHz,CD3OD),δ:142.94(C-7),130.80(C-6),89.36(C-5),80.35(C-1),62.89(C-14),56.59(C-8),49.13(C-9),47.00(C-4),43.64(C-11),36.31(C-10),32.40(C-2),31.88(C-3),24.92(CH3-15),24.01(CH3-12),23.58(CH3-13)。通过与文献[24-25]NMR数据对比,确定化合物1-10为punctaporonin A(图8b)。
2.2 细胞毒活性
对化合物1-3、1-4、1-8进行细胞毒活性评价,结果见图9。

*表示P<0.05,与依托泊苷相比具有统计学差异;**表示P<0.01,与依托泊苷相比具有显著性差异图9 不同化合物细胞毒活性比较Fig.9 Comparison of cytotoxic activities of different compounds
由图9可知,化合物1-3对A549细胞的IC50值为(32.27±4.26) μmol·L-1,与依托泊苷相比,无统计学差异(P>0.05);对HeLa和HepG2细胞的IC50值分别为(9.71±0.61) μmol·L-1和(12.63±0.47) μmol·L-1,均显著低于依托泊苷(P<0.01),表明化合物1-3对A549、HeLa和HepG2细胞均表现出明显的细胞毒活性。化合物1-4和1-8对A549细胞的IC50值,与依托泊苷相比,均具有统计学差异(P<0.05);对HeLa和HepG2细胞的IC50值均显著高于依托泊苷(P<0.01)。
2.3 乙酰胆碱酯酶抑制活性
乙酰胆碱酯酶抑制剂是治疗阿尔茨海默病最有效的手段[26],目前报道的高效乙酰胆碱酯酶抑制剂均来源于药用植物[27-28]。化合物1-1和1-3对乙酰胆碱酯酶的IC50值分别为31.0 μmol·L-1和16.1 μmol·L-1,化合物1-1的IC50值明显高于加兰他敏(P<0.05),化合物1-3的IC50值与加兰他敏相比无统计学差异(P>0.05)。其它化合物在浓度为1 μmol·L-1时,对乙酰胆碱酯酶均未表现出明显的抑制活性。
2.4 α-葡萄糖苷酶抑制活性(图10)

图10 不同化合物α-葡萄糖苷酶抑制活性比较Fig.10 Comparison of α-glucosidase inhibitory activities of different compounds
由图10可知,化合物1-1、1-2、1-3和1-4对α-葡萄糖苷酶均未表现出明显的抑制活性。
3 结论
从桃儿七内生烟色拟盘多毛孢菌代谢产物中分离并鉴定了10个萜类化合物,其中化合物1-1、1-2、1-3和1-4为新化合物,对其细胞毒活性、乙酰胆碱酯酶抑制活性及α-葡萄糖苷酶抑制活性进行了分析。结果表明,化合物1-3、1-4和1-8对A549、HeLa和HepG2细胞均表现出明显的细胞毒活性,表明化合物1-3、1-4和1-8具有潜在的抗肿瘤活性,但其抗肿瘤活性与化合物结构之间的关系还需进一步研究分析。化合物1-3对乙酰胆碱酯酶表现出较强的抑制活性,但其对乙酰胆碱酯酶活性抑制具体机制尚不清楚,还有待进一步研究。基于桃儿七内生烟色拟盘多毛孢菌分离出具有抗肿瘤活性和抑制乙酰胆碱酯酶活性的萜类化合物,为桃儿七内生真菌抗肿瘤及治疗阿尔茨海默病新药开发提供了新思路。

