蝉花菌质在饲料中应用安全性初探
纪伟, 刘晓梅, 苏文英, 孙长胜, 闫文娟, 柴文波, 任立凯*
(1.连云港市农业科学院,江苏 连云港 22200; 2.浙江泛亚生物医药股份有限公司,浙江 嘉兴 314200)
蝉花(IsariacicadaeMiquel)在《本草纲目》《图经本草》和《经史证类备急本草》等古代经典医学论著均有记载,具有丰富的营养价值[1-5]。别称金蝉花、胡蝉、蝉蛹草等,是麦角菌科真菌蝉棒束孢寄生在蝉科竹蝉、蝼蛄、山蝉及黑蚱等的若虫[6-7],气候环境适宜时,吸收虫体的营养转化成菌丝体,顶端分枝“发芽”,形似花冠,故而称为蝉花[4,8-9]。蝉花菌质是将蝉花子实体采收后剩余的培养基,在发酵过程中,培养基大部被分解转化,里面含有部分蝉花虫草菌丝体,故命名为蝉花菌质[5]。根据文献记载,蝉花经人工培育,其菌丝体不仅含有腺苷、多糖等活性成分,还含有丰富的氨基酸、微量元素、D-甘露醇和核苷类、维生素类、蕈糖和硬脂酸等物质[3,10]。开发应用这部分资源,不仅为蝉花子实体收获后的培养基解决了出路问题,而且变废为宝,大大提高了蝉花培养物的附加值[11]。依据《新食品原料安全性审查管理办法》和《食品安全法》的规定,蝉花子实体(人工培植)已通过国家食品安全风险评估中心专家评审委员会技术审查,并于2021年1月7日被国家卫生健康委员会批准为“新食品原料”,成为我国100余种新食品原料的新晋成员[12-13]。所使用的蝉花菌株和蝉花子实体(人工培植)的安全性已得到认可,关于蝉花菌质的安全性研究还未有公开报道。本研究通过蝉花菌质小鼠经口急性毒性试验、雌性小鼠和雄性小鼠的小鼠骨髓细胞微核试验和小鼠的精子畸形试验开展蝉花菌质的安全性评价工作,为蝉花菌质纳入饲料原料目录和应用于饲料行业提供科学理论依据。
1 材料与方法
1.1 蝉花菌质
蝉花菌质为蝉花人工培育完成后,采收完蝉花子实体的小麦培养基。在发酵过程中,小麦培养基大部分被分解转化,里面含有部分蝉花虫草菌丝体,该样品为浙江泛亚生物医药股份有限公司制备提供。
1.2 供试材料
小鼠经口急性毒性试验:SPF级ICR小鼠购买50只,雌雄各半,分2次购入,试验动物为5~6周龄,体重18~22 g;小鼠骨髓细胞微核试验:SPF级ICR小鼠100只,雌雄各半,试验动物为7~12周龄,体重25~30 g;小鼠精子畸形试验:SPF级雄性ICR小鼠50只,试验动物为6~8周龄,体重25~35 g。以上试验动物均购自北京为通利华动物科技有限公司,试验动物合格证号为SCXK(京)2016-0011。
1.3 主要试剂和仪器
环磷酰胺(Beijing Giant-Carrier Co.Ltd);吐温-80(国药集团化学试剂有限公司);磷酸二氢钾(国药集团化学试剂有限公司);磷酸氢二钠(国药集团化学试剂有限公司);小牛血清(兰州民海生物工程有限公司);甲醇(国药集团化学试剂有限公司);羧甲基纤维素钠(北京化学试剂公司);丙三醇(国药集团化学试剂有限公司);吉姆萨染料(北京华博源科技开发中心);伊红(曙Y,北京化学试剂公司);香柏油(国药集团化学试剂有限公司);中性树脂胶(国药集团化学试剂有限公司)。隔水式恒温培养箱(上海一恒科技有限公司);数显恒温水浴锅(金坛医疗仪器厂);生物显微镜(日本Olympus公司);酸度计(意大利HANN公司)。
1.4 试验方法
1.4.1 小鼠经口急性毒性试验
预试验:设置高剂量组为5 000 mg·kg-1体重,以3.125倍递减设置高、中、低3个剂量组,即分别以5 000、1 600、512 mg·kg-1为高、中、低剂量组开展预试验,以期找到0/4致死剂量和4/4致死剂量。预试验各剂量组的小鼠数量均为4只(雌雄各半),按灌胃体积为0.02 mL·g-1体重,将受试物用1%的羧甲基纤维素钠配置成混悬液,依次将高、中、低剂量组经口灌胃染毒。染毒后观察小鼠的情况,包括一般表现、中毒症状和死亡情况,观察周期为1~2周,并对死亡小鼠剖检处理,做好试验记录。根据预试验的结果发现,预试验各剂量组小鼠(雌雄各半)均未出现死亡情况。
正式试验:依据预试验的结果,将染毒剂量确定为5 000 mg·kg-1体重作为正式试验的染毒剂量。将30只试验用小鼠随机分成3组,每组10只(雌雄各半),将受试物用1%的羧甲基纤维素钠配置成混悬液,经口灌胃染毒。染毒后观察小鼠的情况,包括小鼠的一般表现中毒症状和死亡情况,连续观察7 d,若4 d后继续有死亡的情况,观察时间需要14 d,必要时可以延长至28 d,并对死亡的小鼠剖检处理,做好详细记录。如果所有试验小鼠均未出现死亡情况,则需要在试验结束时每组随机挑选2只小鼠进行大体剖检并做好详细记录[14]。
1.4.2 小鼠骨髓细胞微核试验
染毒剂量与分组。依据农业部公告第1247号-12兽药小鼠精子畸形试验指导原则,在受试物LD50大于5 000 mg·kg-1体重时,试验组高剂量设为5 000 mg·kg-1体重,将2 500和1 250 mg·kg-1体重设为中剂量组和低剂量组,另设1个阴性(溶剂)对照组和1个阳性对照组。阳性对照物选用环磷酰胺,按40 mg·kg-1体重剂量给予。分别将小鼠按每组20只(雌雄各半),分为5组进行试验[15]。
受试物的配制与染毒。将受试物按各测试浓度用1%羧甲基纤维素钠配制成混悬液,染毒方式采用经口灌胃法,用1%羧甲基纤维素钠对阴性对照组进行灌胃;按2 mg·mL-1浓度配制对阳性对照组小鼠进行经口灌胃染毒,小鼠灌胃体积为每克体重0.02 mL。每日1次,连续2 d给药。
标本制备。选取在第二次给予受试物6小时后的小鼠,随机选取雌性和雄性小鼠各5只,使用颈椎脱臼法随机处死,将每只小鼠的两侧股骨取下,剔除肌肉,去除表面血污,将股骨两端剪去。用移液枪吸取小牛血清0.2 mL冲洗骨髓腔数次,在相应编号的载玻片上滴上冲洗物;将骨髓腔冲洗物在玻片上涂匀后,推片,每只小鼠2张,快速干燥;将干燥的涂片固定于甲醇中,10 min后取出晾干;吉姆萨应用液20 min染色后,使用蒸馏水冲洗,晾干,待查;阅片。用双盲法镜阅片,选择着色浓淡适中区域分散均匀、完整的细胞,用油镜观察。每只小鼠涂片计数1 000个以上嗜多染红细胞(PCE)数,观察并计数其中有核的PCE数。同时在同一视野下观察计数成熟红细胞(RBC)数,并记录每只小鼠RBC数、含微核PCE细胞数、PCE检查数[16]。
1.4.3 小鼠精子畸形试验
染毒剂量与分组。依据农业部公告第1247号-11兽药小鼠精子畸形试验指导原则,当受试物半数致死量(LD50)>5 000 mg·kg-1时,试验组高剂量设为5 000 mg·kg-1,将2 500和1 250 mg·kg-1体重设为中和低剂量组,另设1个阴性(溶剂)对照组和1个阳性对照组。选用环磷酰胺作为阳性对照组,按40 mg·kg-1体重剂量给予。将雄性ICR小鼠随机分组,每组10只,分为5组进行试验。
受试物的配制与染毒方法。将受试物按各测试浓度用1%羧甲基纤维素钠配制成混悬液,染毒方式采用经口灌胃法,用1%羧甲基纤维素钠对阴性对照组进行灌胃;按2 mg·mL-1浓度配制对阳性对照组小鼠进行经口灌胃染毒,小鼠灌胃体积为每克体重0.02 mL。每日1次,连续5 d给药。
采样和制片。每个剂量组选取5只小鼠采样、制片,一般选择在第一次染毒后35 d后的小鼠。处死小鼠的方法采用颈椎脱臼法,剪开腹腔,将摘取的两侧附睾放入盛有2 mL生理盐水的平皿中;将附睾纵向剪1刀,用吸管吸取其中的生理盐水吹打数次,净置5 min;使用4层擦镜纸过滤,除去组织碎片,在载玻片上滴滤液2滴,推片,样片制片4张/只小鼠;采用自然干燥后,用甲醇固定10 min,干燥;使用2%的伊红染色50 min,用水冲洗染液,自然晾干。
阅片。先在低倍镜下找到精子重叠较少、背景清晰的区域,再在高倍镜下观察精子形态。精子明显是人为剪碎、头部与其他精子及碎片重叠或有头无尾(轮廓不清)者均不计数。每个剂量组分别检查精子1 000条,对在同一视野中的畸形精子进行分类计数,包括双尾、尾折叠、分无钩、胖头、香蕉形、双头、无定形,做好详细记录。
2 结果与分析
2.1 小鼠经口急性毒性试验结果
正式试验中所有受试ICR小鼠在试验观察期内均未出现中毒症状,亦未见死亡,且试验结束后大体剖检小鼠的肾脏、肺脏、脾脏、肝脏、胃肠道、心脏等组织器官,均未发现异常变化。
经口染毒剂量按5 000 mg·kg-1体重,经重复试验3次,在试验观察期内ICR小鼠死亡率详见表1,结果均为0,可判定蝉花菌质对ICR小鼠经口急性毒性试验的LD50大于每公斤体重5 000 mg。
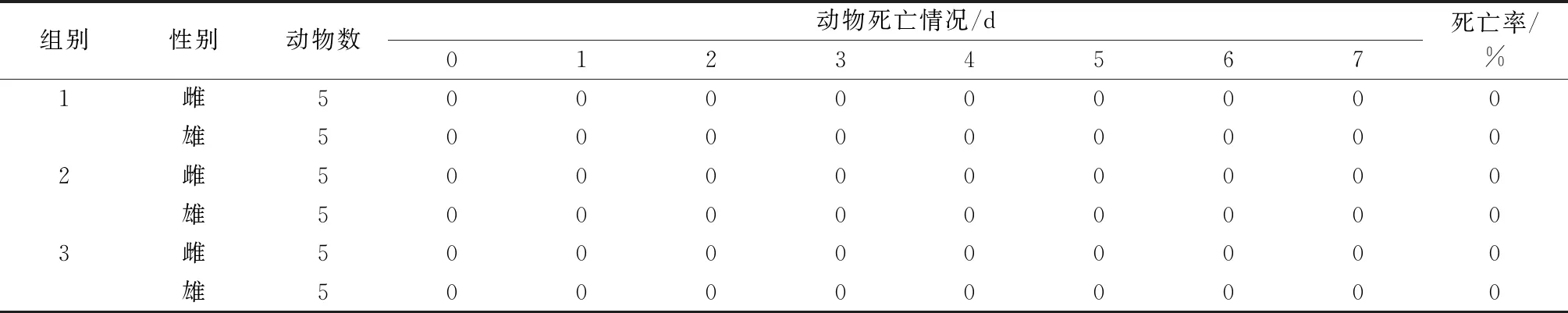
表1 动物死亡结果
2.2 小鼠骨髓细胞微核试验结果
根据表2、3可知,阳性对照组2种性别小鼠骨髓细胞中含微核嗜多染红细胞率显著高于阴性对照组相应性别,而蝉花菌质各剂量组雌、雄小鼠骨髓含微核嗜多染红细胞率与阴性对照组之间比较无显著性差异,且各试验组嗜多染红细胞(PCE)与成熟红细胞(RBC)比值(PCE/RBC)在正常范围内,表明蝉花菌质在1 250~5 000 mg·kg-1体重剂量对雌、雄小鼠骨髓中嗜多染红细胞(PCE)的微核率无显著影响,可判定蝉花菌质的小鼠骨髓细胞微核试验结果为阴性。
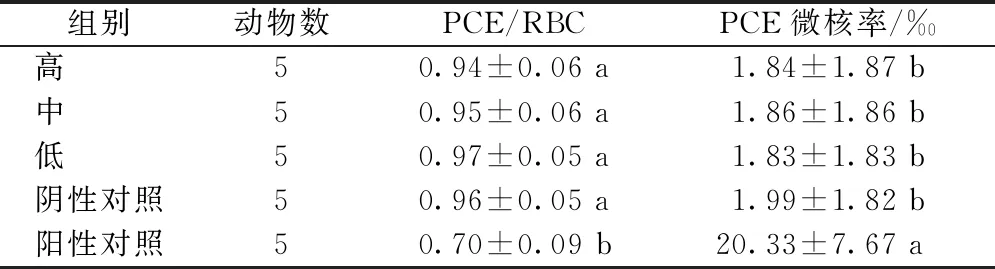
表2 蝉花菌质小鼠骨髓细胞微核试验结果(雌性小鼠)
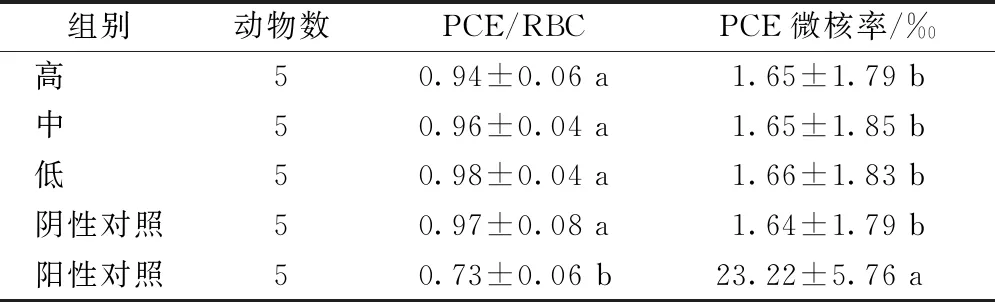
表3 蝉花菌质小鼠骨髓细胞微核试验结果(雄性小鼠)
2.3 小鼠精子畸形试验结果
从表4可以看出,阳性对照组精子畸形率极显著高于阴性对照组,蝉花菌质在1 250~5 000 mg·kg-1体重剂量范围内小鼠精子畸形率与阴性对照组比较无显著性差异,可判定蝉花菌质小鼠精子畸形
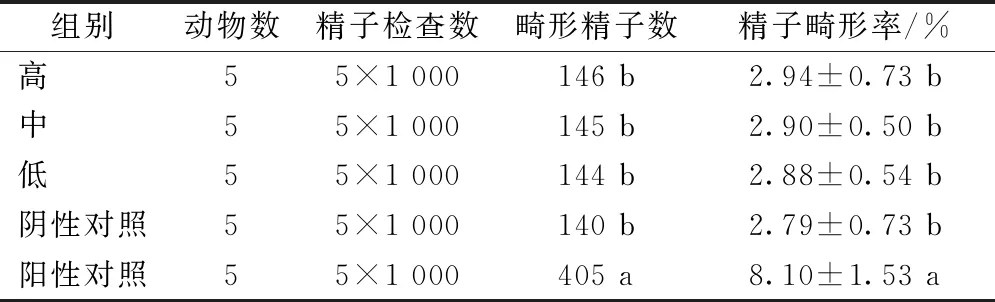
表4 蝉花菌质小鼠精子畸形情况
试验结果为阴性。从表5可以看出,蝉花菌质在1 250~5 000 mg·kg-1体重剂量小鼠各类精子畸形百分率中“无钩”占百分比最高,其次是“无定形”,各类畸形精子百分率中“双尾”占百分比最低。
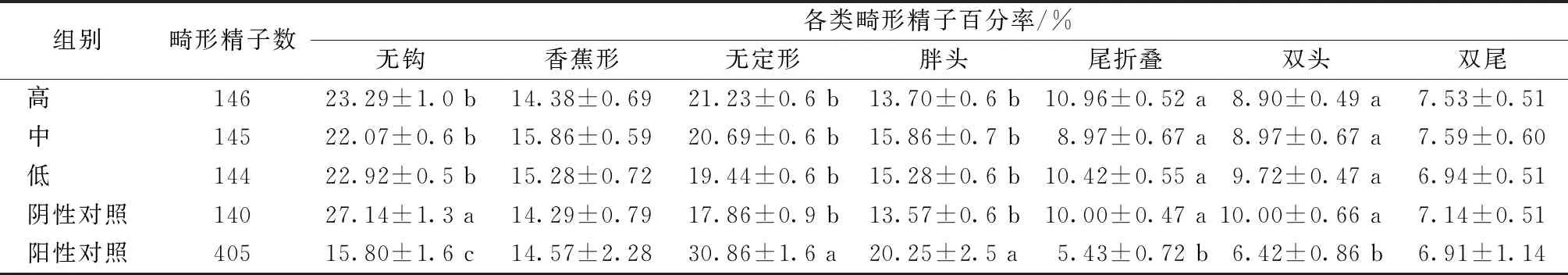
表5 蝉花菌质小鼠精子畸形比例
3 讨论
本研究包括蝉花菌质小鼠经口急性毒性试验(LD50测定)、雌性小鼠和雄性小鼠的小鼠骨髓细胞微核试验和小鼠的精子畸形试验,以期通过以上试验开展蝉花菌质在饲料中应用的安全性评价工作。研究结果表明,受试的所有ICR小鼠在试验观察期内均未见中毒症状和死亡情况,在试验结束后大体剖检小鼠的肾脏、肺脏、脾脏、肝脏、胃肠道、心脏等组织器官,均未发现异常变化。根据本试验判定,蝉花菌质对ICR小鼠经口急性毒性试验的LD50大于5 000 mg·kg-1体重。蝉花菌质在1 250~5 000 mg·kg-1体重剂量经口染毒后,各小鼠骨髓细胞中含微核嗜多染红细胞(PCE)率和小鼠精子畸形率与阴性对照组比较均无显著性差异,说明小鼠骨髓细胞微核试验结果和小鼠精畸形试验结果均为阴性。以上试验表明,蝉花菌质具有很好的安全性,为蝉花菌质应用于饲料工业等领域提供科学理论依据。

