肺炎支原体感染致塑型性支气管炎患儿的临床研究
朱云芳,刘亚辉,梁 宽,贾永飞,杨桃妮
1.陕西省宝鸡市人民医院儿科,陕西宝鸡 721000;2.陕西省宝鸡市高新医院儿科,陕西宝鸡 721000
塑型性支气管炎(PB)是指因气管支气管被树样管型或内生异物堵塞,进而诱发肺通气功能障碍和肺不张的一种疾病,可诱发呼吸窘迫急症[1]。目前国内外已有报道称PB通常发生于先天性心脏病患儿术后,但国内报道的PB多为病毒或细菌感染病例,且发病特点和发病率均不明[2-3]。目前临床中尚未明确PB的发病机制,多数学者认为其发生与变态反应相关,呼吸道黏膜在各种致病因子的刺激下血管通透性增加,导致机体渗出大量纤维蛋白,促进气道内黏液分泌量增多,细胞浸润于管腔内,在支气管内酸碱度变化和组织凝血酶的作用下发生蛋白沉淀,最终形成树样管型,容易堵塞气道而造成换气和通气功能障碍,严重者会诱发呼吸功能不全,若患儿得不到及时有效的诊断和治疗,则会因塑型性物质而堵塞气道,危及生命[4-5]。近年来随着支气管镜技术在临床中的推广和应用,PB患儿的数量逐渐增多,已有研究指出肺炎支原体(MP)感染在PB中也有重要地位[6],临床中应积极提高医生对MP感染所致PB的认识,以采取积极有效的措施改善MP感染所致PB患儿的预后,现分析报道如下。
1 资料与方法
1.1一般资料 回顾性分析2019年6月至2021年6月宝鸡市人民医院收治的318例MP感染患儿的临床资料。其中男214例,女104例,年龄1~6岁,平均(3.38±0.89)岁。根据患儿是否出现PB分为PB组(52例)和非PB组(266例)。诊断标准:(1)肺炎,符合《儿童社区获得性肺炎诊疗规范(2019年版)》[7]中相关标准,且伴有呼吸道症状,胸部X线片显示大片肺实质或肺不张。(2)MP感染,外周血MP-免疫球蛋白(Ig)M阳性或鼻咽深部抽吸MP-DNA>108 copy/L(荧光实时定量聚合酶链反应检测)。纳入标准:(1)经临床诊断为MP感染的患儿;(2)年龄≤13岁的患儿;(3)于本院顺利完成治疗出院的患儿;(4)各项临床资料及随访资料均完整的患儿。排除标准:(1)非感染因素所致PB的患儿;(2)除MP或细菌外存在其他感染的患儿;(3)既往有支气管扩张症或哮喘病史的患儿;(4)中途转院的患儿。
1.2方法 查阅既往资料和相关文献,确定并采用调查法收集MP感染患儿的相关资料,查阅院内所记录的患儿入院时的一般资料和临床资料,分析并展开对比研究。
1.3观察指标
1.3.1临床特征 包括发热、热峰、热程、咳嗽、喘息、肺部体征(湿啰音、干啰音、呼吸音减弱)、X线片/CT结果(合并大叶性病变、合并胸腔积液、合并肺不张)。
1.3.2一般资料 包括性别、年龄、起病至呼吸困难时间、喘息史、过敏史、过敏性体质家族史、发病季节。
1.3.3临床资料,包括天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、C反应蛋白(CRP)、CD3+、CD3+CD4+、CD3+CD8+、CD4+/CD8+、CD3-CD19+、CD3-CD(16±56)+、CD19+CD23+、D-二聚体(D-D)、红细胞沉降率(ESR)、纤维蛋白原(FIB)、IgA、IgG、IgM、IgE、乳酸脱氢酶(LDH)、中性粒细胞计数(N)、白细胞计数(WBC)、机械通气治疗、住院时间。

2 结 果
2.1两组患儿临床特征比较 MP感染患儿的临床症状以发热、咳嗽、肺部湿啰音和呼吸音减弱为主,且多数合并大叶性病变、胸腔积液。其中PB组患儿发热、呼吸音减弱、合并胸腔积液的发生率及热峰高于非PB组,差异有统计学有意义(P<0.05)。见表1。

表1 两组患儿临床特征比较[n(%)或
2.2两组患儿一般资料比较 PB组患儿有过敏史患儿比例高于非PB组,差异有统计学有意义(P<0.05)。见表2。

表2 两组患儿一般资料比较[n(%)或
2.3两组患儿临床资料比较 PB组患儿的AST、ALT、CRP、CD3-CD(16±56)+、D-D、ESR、IgA、IgE、LDH、N水平,以及机械通气治疗≥3 d发生率均高于非PB组,住院时间长于非PB组,IgG水平低于非PB组,差异均有统计学有意义(P<0.05)。见表3。
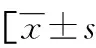
表3 两组患儿临床资料比较或n(%)]
2.4MP患儿发生PB的危险因素分析 有过敏史、CRP≥15 mg/L、D-D≥750 μg/L为MP患儿发生PB的危险因素(P<0.05)。见表4。

表4 MP患儿发生PB的危险因素分析
3 讨 论
PB是以气管内形成支气管树样管型为特征的疾病,发病后可造成支气管通气障碍,预后较差,若无法及时诊断和治疗,则会增大临床治疗难度,且随着病情的加重甚至诱发呼吸衰竭和通气障碍,留下严重后遗症,甚至死亡[8]。近年来已有大量学者对PB的病因、发病机制、诊断、治疗和预后等展开研究,有学者指出MP可直接损伤机体免疫功能,其在难治性、坏死性和重症肺炎的发生中均有重要作用,且MP诱发PB的情况也逐渐增多,逐渐成为临床研究的热点之一[9]。本文回顾性分析MP感染所致PB患儿的临床特征,并分析MP患儿发生PB的危险因素,为今后临床诊治提供参考。
本文研究结果显示,MP感染患儿的临床症状以发热、咳嗽、肺部湿啰音和呼吸音减弱为主,且多数合并大叶性病变、胸腔积液。MP患儿的临床表现无明显特异性,无论是何种病原体感染均以发热和咳嗽为主要临床表现。其中PB组患儿发热、呼吸音减弱、合并胸腔积液的发生率高于非PB组,且PB组患儿热峰高于非PB组,可能是由于MP感染患儿发生PB后机体免疫炎症反应导致大量中性粒细胞聚集和降解,形成高黏滞性物质,同时嗜酸性粒细胞聚集,支气管上皮细胞脱落,对支气管黏膜纤毛清除功能造成影响,进而影响肺部功能,因此患儿发热、呼吸音减弱及胸腔积液的发生率升高。而本文中MP感染所致PB患儿以左下肺大叶性病变为主,为临床诊断提供了参考,当然这一结果也可能与本研究所选取患儿存在地域性限制相关,为确保结果的准确性,今后应扩大研究对象的纳入范围,进一步开展相关研究。进一步探究发现,合并过敏史、CRP≥15 mg/L、D-D≥750 μg/L为MP患儿发生PB的危险因素(P<0.05)。有学者指出,过敏性体质可增加MP感染导致的难治性MPP的发生率,是由于通过细胞因子作用,过敏因素会促进难治性MPP的发生,因此过敏可能会增强MP的严重程度,进而促进了塑型性物质的形成,但其具体作用机制仍需进一步探究[10]。CRP为临床常用的炎症反应指标,其水平高低可帮助识别重症MP患儿,本研究CRP≥15 mg/L为PB发生的危险因素,可能是由于CRP水平升高提示机体存在严重免疫炎症反应,强烈的器官黏膜炎症反应会促进塑型性物质的形成[11]。D-D为机体监测纤溶亢进和高凝状态的分子标志物,其水平与血管内皮损伤相关,D-D≥750 μg/L时患儿病情危重,MP感染可诱发肺部毛细血管网损伤,与既往学者指出的PB塑型性物质形成机制相关[12]。
综上所述,MP感染致PB患儿多表现出发热、呼吸音减弱、肺大叶性病变、胸腔积液的特征,合并过敏史、CRP≥15 mg/L、D-D≥750 μg/L为MP患儿发生PB的危险因素,应对高危MP患儿给予积极干预,以降低PB发生率。

