基于GC-MS鉴别活体太平洋牡蛎不同流通阶段气味特征变化
林恒宗,梁志源,秦小明,高加龙,范秀萍,黄艳平,常向阳,邓 杰,吴炜俊
(广东海洋大学食品科技学院,国家贝类加工技术研发分中心(湛江),广东省水产品加工与安全重点实验室,水产品深加工广东普通高校重点实验室,广东 湛江 524088)
牡蛎为我国重要的经济贝类,2020年总产量约为542万 t,约占贝类总产量的1/3[1]。鲜活牡蛎由于其肉质爽滑、味道鲜甜,且富含蛋白质、牛磺酸、糖原及微量元素等营养物质而深受消费者青睐,因此在我国牡蛎主要以鲜销生食为主[2-3]。牡蛎采捕离水后需历经运输、净化、保活、销售等商业流通环节,然而牡蛎在各流通环节均会受到环境胁迫应激如:缺氧、干露、振荡、饥饿、温度波动等,随着流通时间的延长,机体组织脏器受到不同程度的损伤,存活质量也受到显著影响[4],因此如何将高品质鲜活牡蛎运输至内地市场已经成为行业研究热点。近年来,国内外针对活体牡蛎运输的研究取得了一定的经济和社会效益,如:香港牡蛎(Crassostrea hongkongensis)[5]在生态冰温条件下保活9 d,其存活率高达90%。但产业实际中判断牡蛎活力及品质劣变的方法仅能依靠开壳、敲击、嗅闻等传统经验手段,难以全面反映牡蛎流通过程中活力及整体品质。
活体牡蛎具有独特的海洋鲜香气味,在流通过程中香气会随着时间的延长、环境的改变而发生变化,因此风味降解是鉴别牡蛎活力品质变化的关键途径。近年来,气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)联用技术被广泛应用于食品挥发性风味成分分析[6-8],目前该技术在活体贝类净化及保活流通中已有相关报道,如:冉云等[9]采用GC-MS技术,明确了缢蛏(Sinonovacula constricta)暂养净化8 h可明显降低其不良气味;张思嘉等[10]采用相同方法探究净化对美洲帘蛤(Mercenaria mercenaria)风味成分的影响也得出类似结果;傅润泽等[11]研究表明,虾夷扇贝(Patinopecten yessonensis)在保活运输后其挥发性风味物质与采捕后相比具有明显差异;然而鲜见该技术应用于活体牡蛎商业流通过程中风味品质监控的研究。因此,本研究模拟当前国内活体太平洋牡蛎流通模式,采用GC-MS联用法以鉴定活体太平洋牡蛎中挥发性风味物质种类及含量,分析流通各环节风味物质变化规律,探明各流通环节间内在联系,以期建立一种鉴别活体太平洋牡蛎品质状态的方法。
1 材料与方法
1.1 材料与试剂
活体太平洋牡蛎于2021年10月购自山东威海灯塔水母海洋科技有限公司,规格为(129.51±2.81)g/个,壳长(127.62±2.07)mm,壳宽(64.11±3.57)mm,壳高(31.98±2.47)mm。牡蛎采捕后保留外壳附着物,每50 kg分装于铺有海水冰的泡沫箱内,经专用冷链运输车低温运输48 h抵达广东海洋大学保活流通实验室,剔除活力弱或死亡的个体,立即用灭菌人工海水清洗表面泥污后进行暂养净化,以消除捕捞或运输操作时应激胁迫。
海水晶 江西盐通科技有限公司;2,4,6-三甲基吡啶(2,4,6-trimethylpyridine,TMP) 上海安谱有限公司;其余试剂均为国产分析纯。
1.2 仪器与设备
贝类暂养净化系统 广州创岭水产有限公司;YC-800低温恒温层析柜 北京亚星仪科公司;SPX-250B生化培养箱 上海博迅公司;PR224ZH精密天平美国OHAUS公司;5810R冷冻离心机 德国Eppendorf公司;8-2T恒温磁力搅拌器 上海梅颖浦有限公司;PB-10 pH计、57330-U固相微萃取装置、50/30 μm-57348-U型-DVB/CAR/PDMS固相微萃取针 德国Supelco公司;7890A-5975C GC-MS联用仪、HP-5MS色谱柱(60 m×0.25 mm,0.25 μm) 美国Agilent公司。
1.3 方法
1.3.1 牡蛎净化
净化流程及方法参照SC/T 3013—2002《贝类净化技术规范》,在贝类净化系统中按太平洋牡蛎养殖海域盐度((31±0.5)‰)配制人工海水,开启增氧设备持续曝气24 h,以流速2.5 m3/h通过紫外灯管循环灭菌制冷至25 ℃,通臭氧至海水臭氧质量浓度0.15 mg/L,将清洗后的牡蛎分装于塑料筐(600 mm×420 mm×315 mm),置于预冷的循环人工海水中净化24 h,暂养期间不投喂饵料,保持水体溶解氧不小于8 mg/L,净化完成后挑选富有活力的个体进行下一步实验。
1.3.2 诱导休眠及生态冰温保活
参照本团队前期实验方法[4],将暂养净化后的牡蛎采用聚氯乙烯热收缩膜逐个包裹,包装完成后将牡蛎分装于塑料周转筐中(600 mm×420 mm×315 mm),转移至低温恒温层析柜诱导休眠处理,处理方式为调节恒温层析柜,从(25±0.5)℃开始,以5 ℃/h的速率降至生态冰温休眠温度0 ℃,温度每下降5 ℃停留90 min,避免温度急剧下降造成应激损伤。诱导休眠结束后,迅速将牡蛎分装于套有内膜袋的泡沫箱(450 mm×250 mm×200 mm)中,装箱前在箱底平铺一层无菌海水制备而成的冰袋,逐层覆盖浸足灭菌海水的海绵保湿处理,加盖后放置在温度设定为0 ℃的层析柜中进行无水保活。
1.3.3 样品采集与制备
实验分别在净化前、净化后、休眠后、保活3 d、保活6 d、保活9 d取样,每组随机取活体牡蛎60 只,迅速开壳刨取牡蛎全脏器,用预冷质量分数为0.86%生理盐水漂洗,吸水纸拭干表面水分,冰浴高速混合匀浆成肉糜状,立即使用或液氮速冻后置于-80 ℃冻存。
1.3.4 挥发性气味成分分析
1.3.4.1 萃取方法
参照Van Houcke等[8]萃取方法并加以改进,精确称取5.000 g牡蛎匀浆肉糜置于20 mL顶空瓶内,顶空瓶内注入10 μL质量浓度为50 μg/mL的TMP作为内标物,密封,置于85 ℃水浴中磁力搅拌(转速500 r/min)平衡20 min,萃取针在GC进样口250 ℃活化20 min后插入顶空瓶内萃取30 min。
1.3.4.2 GC-MS条件
GC条件:采用不分流进样模式,HP-5MS色谱柱(60 m×0.25 mm,0.25 μm);初始温度50 ℃,保持3 min;随后分别以5、4 ℃/min和4 ℃/min的速率升温至100、140、180 ℃,并在终温处分别保持2、1 min和2 min,最后以5 ℃/min升至250 ℃,保留5 min;高纯度氦气作为载气;流速1.5 mL/min;进样口温度250 ℃。
MS条件:采用电子电离模式;电子能量70 eV;离子源温度230 ℃;四极杆温度150 ℃;接口温度250 ℃;全扫描m/z35~550。
1.3.4.3 定性分析
根据GC-MS得出的太平洋牡蛎挥发性香气化合物的质谱信息,与NIST和Wiley谱库对比,辅助人工图谱解析,选择正反向匹配值均大于800的化合物进行定性分析,各化合物峰面积由仪器软件计算。
1.3.4.4 定量分析
采用内标法进行半定量分析[12],根据已知浓度的TMP峰面积计算出不同实验组牡蛎组织样品中各挥发性风味物质的含量,按式(1)计算:

式中:Ci为目标化合物的含量/(ng/g);Ax为目标化合物的峰面积;Ai为内标化合物TMP的峰面积;Cx为内标化合物的含量/(ng/g)。
1.3.4.5 关键挥发性风味物质的分析
参照Feng Yunzi等[13]方法及相关文献挥发性风味物质的阈值,以香气活性值(odor activity value,OAV)对样品中起关键作用的挥发性物质进行确定,按式(2)计算OAV:

式中:Ci为目标化合物的质量含量/(ng/g);Ct为该物质的感觉阈值/(ng/g)。
1.4 数据处理与分析
2 结果与分析
2.1 太平洋牡蛎流通过程中挥发性风味物质组成分析
采用顶空固相萃取结合GC-MS测定,通过NIST/Wiley数据库匹配,鲜活太平洋牡蛎共鉴定出7大类、49 种挥发性风味化合物(表1、图1),其中醛类15 种、酯类14 种、烷烃类5 种、杂环化合物4 种、酮类4 种、醇类3 种、芳香族化合物2 种以及其他化合物2 种。可见,醛、酯类化合物为活体太平洋牡蛎中含量最丰富的挥发性风味物质,在葡萄牙牡蛎(Crassostrea angulata)[14]、欧洲扁牡蛎(Ostrea edulis)[8]中也发现类似结果。由图1可知,太平洋牡蛎采捕离水后在不同流通阶段挥发性风味物质的种类和含量均发生不同的变化。净化前牡蛎共鉴定出31 种挥发性风味物质,醛类15 种,含量为700.86 ng/g;酯类6 种,含量为726.74 ng/g;酮类3 种,含量为91.8 ng/g。复水净化后,醛、脂类化合物各减少1 种,含量分别下降了64.25%、46.73%;酮类化合物减少1 种,含量下降了36.49%。诱导休眠至保活流通终期挥发性风味物质种类及含量大体呈上升趋势,保活9 d后,酯类化合物较净化前增加了8 种,含量为净化前的4.56 倍;醛酮类化合物减少各减少2 种,其中醛类化合物增加了19.9%,酮类化合物则下降了39.9%;同时杂环及烃类物质分别增加1~2 种。以上结果显示,活体太平洋牡蛎采捕后不同流通阶段挥发性风味化合物差异明显,但要确定各阶段风味物质具体含量变化仍需进一步分析。
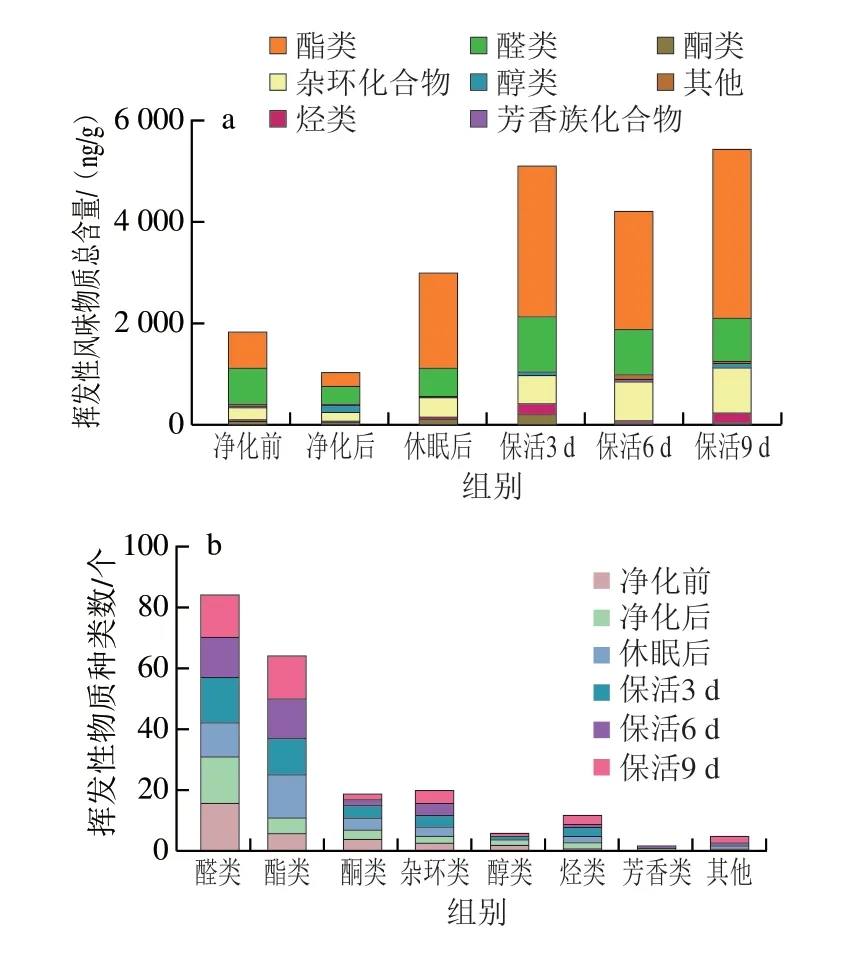
图1 太平洋牡蛎不同流通阶段挥发性风味物质含量(a)、种类个数(b)变化Fig.1 Changes in contents (a) and types of flavor substances (b) of C.gigas during different circulation stages
2.2 太平洋牡蛎不同流通阶段挥发性风味物质的变化
为解析太平洋牡蛎在不同流通阶段挥发性风味成分变化,首先将化合物按官能团分类,并通过相关文献对其气味特征进行描述(表1)。大量研究表明,挥发性醛类化合物为鲜活太平洋牡蛎主要香气来源[15],本研究同样发现醛类物质在活体太平洋牡蛎中占主导地位,这可能与牡蛎生长环境及摄食密切相关。暂养净化期间庚醛、壬醛、月桂醛、己醛、十三醛、十一醛、苯甲醛、癸醛等直链饱和醛的含量与净化前相比有所下降,但无显著差异(P>0.05),这些醛类化合物是脂质氧化的降解产物,其中壬醛是油酸和亚油酸氧化的产物,多具有塑料味、鱼腥味[14];己醛、癸醛、庚醛会产生刺鼻的油脂氧化气味[14];苯甲醛具有苦味和焦糖类似味,被认为是苯丙氨酸Strecker反应降解的产物。冉云等[9]研究表明,缢蛏体内泥土味、腥臭味、粪便味等不良风味主要来源于直链饱和醛,这也证实了牡蛎通过暂养净化能缓解捕捞或运输操作时应激胁迫导致的脂质氧化损伤,保留其独特风味的同时可降低其不良气味使牡蛎更加适口。(E)-2-壬烯醛、(E)-2-辛烯醛、(E,E)-2,4-壬二烯醛等不饱和醛类较净化前同样有所下降,其中(E)-2-壬烯醛降幅更为明显(P<0.05),Aruna等[16]研究发现,这些产物多为脂肪酸氧化降解产物,推测太平洋牡蛎采捕后长时间暴露于空气中体内多不饱和脂肪酸氧化速率加快,复水后其胁迫解除,活力恢复,缓解了脂质氧化进一步加剧,体内挥发性气味物质得以再次积累,呈现出浓烈的清香气味。牡蛎在诱导休眠后醛类化合物含量呈明显上升趋势;之后随着保活时间的延长,含量变化与保活时间呈正相关。推测牡蛎长时处于低温胁迫状态,导致肌肉细胞内生物大分子氧化损伤,肌肉脂质、游离脂肪酸发生初始氧化损伤,其降解产物为醛类化合物,同时也是贝类鲜甜香气的主要来源[17]。保活9 d后,活体牡蛎组织中庚醛、壬醛、苯甲醛等14 种醛类明显高于净化后水平(P<0.05),可见无水保活有利于提升牡蛎整体风味。

表1 太平洋牡蛎流通过程中挥发性风味物质含量变化Table 1 Changes of volatile flavor substances in C.gigas during circulation stages
酯类香气化合物主要呈奶油香、水果香、花香、甜味、青草味等愉悦性气味[18],鲜活太平洋牡蛎检测出肉豆蔻酸甲酯、棕榈酸甲酯、壬烯酸甲酯、十七酸甲酯等14 种酯类,其中棕榈酸甲酯在保活第9天其含量高达1264.76 ng/g。这些酯类大多为牡蛎组织中未经甲酯化处理的脂肪酸与不饱和脂肪酸,其不仅可以作为能源抵御不良环境变化,同时也是牡蛎中鲜、香气味的主要来源[19]。牡蛎在复水净化后肉豆蔻酸甲酯、十五碳酸甲酯、十六烯酸甲酯、棕榈酸甲酯较净化前明显下降(P<0.05),可见牡蛎采捕离水后,干露、缺氧胁迫致使脂质发生了初级氧化,复水净化后牡蛎活力恢复,缓解了脂肪氧化进一步加剧,同时牡蛎处于饥饿胁迫状态需消耗脂肪酸以维持的正常生命代谢活动。诱导休眠至保活流通终期,肉豆蔻酸甲酯、棕榈酸甲酯、十六烯酸甲酯、亚油酸甲酯、二十碳五烯酸甲酯等酯类物质随运输时间的延长呈上升趋势(P<0.05),提示低温运输胁迫导致牡蛎肌肉组织脂质氧化加剧,然而这些化合物多为牡蛎中的不饱和脂肪酸,其赋予牡蛎独特脂肪清香气味,保活9 d后活体牡蛎组织中仍检测出二十碳五烯酸等人体所需的酯类化合物大量存在,可见牡蛎在长时无水流通过程中整体风味及营养物质未发生改变。在已有的研究中,吴梓宣等[20]研究表明,虾夷扇贝在暂养净化过程中,随着净化时间的延长其多不饱和脂肪酸呈下降趋势。Fan Xiuping等[21]研究发现,珍珠龙胆石斑鱼(♀Epinephelus fuscoguttatus×♂E.lanceolatus)在无水保活过程中二十碳五烯酸甲酯呈下降趋势,与本研究结果相似。
烷烃类、酚类、含硫等杂环类挥发性风味物质在各不同流通阶段的牡蛎中检出较少,烷烃类物质的产生主要来源于脂肪酸烷氧自由基断裂,含氮含硫及杂环化合物主要由蛋白质在微生物和酶的作用下分解产生,酚类物质则可能来自环境中的污染物[22]。在本研究中,活体牡蛎鉴定出十六烷、2-乙基呋喃、2-戊基呋喃、二甲基硫醚等活贝中具有代表性的关键气味物质,其中2-乙基呋喃、2-戊基呋喃具有很强的肉香味;二甲基硫醚则由氨基酸降解产生,是牡蛎中最重要的香气挥发物[11,23]。牡蛎在暂养净化后十六烷、2-乙基呋喃较净化前有所提升,研究表明,采捕后未经净化的活贝肠道中含有大量未排出的粪便、泥沙等杂质,这些残留物通常被认为是不良口感及腥臭味的主要来源[9],可见通过暂养净化牡蛎愉悦性风味得到明显改善。随着保活时间的延长,2-乙基呋喃、2-戊基呋喃、二甲基硫醚较净化后显著提升(P<0.05),同时吲哚类化合物缓慢增加,牡蛎组织整体香气含量呈积聚趋势,这一现象在活体虾夷扇贝[11]流通过程中也有报道,提示在长时低温流通过程中牡蛎生理状态变差,风味品质也受到一定的影响,但由于这几类化合物阈值较高,对牡蛎气味作用不显著。
酮类化合物在牡蛎等海洋贝类中主要贡献青草香、脂肪香、花香、果香风味,是脂肪氧化及氨基酸降解产物,本研究中活体牡蛎鉴定出2-壬酮、3,5-辛二烯-2-酮、3-辛酮、(E)-3,5-辛二烯-2-酮4 种化合物;其中2-壬酮已被鉴定为活体牡蛎中主要呈鲜味化合物[24]。酮类化合物含量变化与醛类物质呈负相关,在流通过程中整体呈波动下降趋势,其中3,5-辛二烯-2-酮、3-辛酮与净化后相比具有明显差异(P<0.05),这可能是流通过程中微生物快速增长,代谢活动需分解羟基类化合物,从而导致风味品质逐渐下降。醇类化合物主要由脂肪氧合酶和氢过氧化酶降解亚油酸产生,其风味阈值远高于醛酮类化合物,对牡蛎整体风味贡献较小,但一些不饱和醇的阈值较低,对牡蛎的整体风味有一定贡献。如:十六烷醇、7-十四烷醇、1-戊烯-3-醇,这几类物质通常具有植物芳香气味,在净化前后均能检出,但随着流通时间的延长,脂质氧化作用导致这些化合物发生明显的积聚。
2.3 太平洋牡蛎不同流通阶段挥发性风味物质聚类热图分析
为直观区分太平洋牡蛎在不同流通阶段挥发性香气物质的差异,将各流通阶段香气化合物含量进行热图聚类分析,结果如图2所示。49 种化合物可聚类为4 类,其中香气化合物A类>B类>C类>D类,活体太平洋牡蛎不同流通阶段香气化合物差异最为显著的是A、B类化合物,包括十六烯酸甲酯、棕榈酸甲酯、己醛、3-辛酮、2-乙基呋喃等醛、酯物质。由样品聚类分析结果可以看出,净化前与净化后组牡蛎在最小距离水平首先发生聚类,表明牡蛎在净化前与净化后挥发性物质组成与含量相似性较高,这说明太平洋牡蛎在采捕离水后通过暂养净化机体呈现出明显的恢复性,对其风味具有明显改善作用;在保活流通阶段,休眠组与保活第6天首先发生聚类,随着欧式距离的增加与保活第3、9天聚为另一大类;表明随着保活时间的延长,牡蛎体内挥发性物质含量发生明显改变。鲜活牡蛎鉴定出挥发性风味化合物种类较多,为明确牡蛎各流通阶段关键风味物质及含量变化仍需采用OAV进行筛选分析。

图2 太平洋牡蛎不同流通阶段挥发性风味物质含量变化热图Fig.2 Heatmap of changes in volatile flavor substances of C.gigas during circulation stages
2.4 太平洋牡蛎不同流通阶段关键风味化合物的确定
为进一步明确各不同流通阶段太平洋牡蛎关键风味物质及其含量变化,依据牡蛎风味化合物的组成及其阈值,采用OAV评价方法以客观反映每种挥发性化合物对牡蛎总香气的贡献。一般认为,OAV不小于1的物质是影响样品关键风味化合物,且OAV越大则对样品香气贡献程度越高[25]。由表2可知,挥发性香气化合物以醛酮类为主,因而确定醛酮类化合物为活体太平洋牡蛎中关键香气成分;太平洋牡蛎在各不同流通阶段OAV不大于1的物质共有5 种,分别为苯甲醛、(E)-3,5-辛二烯-2-酮、3,5-辛二烯-2-酮、2-乙基呋喃、1-戊烯-3-醇,说明其对牡蛎总体风味具有修饰作用;OAV不小于1的物质有13 种,分别为己醛、庚醛、十一醛、(E)-2-壬烯醛、4-乙基苯甲醛、壬醛、(E)-2-癸烯醛、(E,E)-2,4-壬二烯醛、癸醛、(E)-2-辛烯醛、2-戊基呋喃、3-辛酮、2-壬酮,表明这些挥发性化合物为活体牡蛎流通过程中起主要贡献的风味物质,其中己醛(青香味)、癸醛(脂味、海味)、(E,E)-2,4-壬二烯醛(脂香味)、(E)-2-辛烯醛(油脂味)、(E)-2-壬烯醛(肉香味)、2-戊基呋喃(青草香味)是牡蛎独有的主要挥发性物质,与已有相关文献[24-26]报道一致。将OAV进行热图可视化处理(图3),净化前、净化后组聚集,说明其挥发性物质含量相似度较高;保活6 d和保活3、9 d分别在2 个不同大类分支上,表明牡蛎在流通阶段挥发性风味物质含量具有差异。暂养净化后醛酮类化合物OAV较净化前明显下降,提示牡蛎脂肪氧化得到明显缓解,愉悦性风味成分得到改善;诱导休眠至保活流通阶段,牡蛎体内挥发性风味化合物较净化前明显上升,醛酮类化合物随着保活时间的延长明显积聚,提示脂质氧化进一步加剧,其中戊醛、己醛、E-2-庚醛等醛类化合物是油酸和亚油酸的氧化降解产物[25],赋予牡蛎清香、脂肪香、花香、新鲜气味。Zhang Zuoming等[27]研究发现,腐败变质的牡蛎组织中三甲胺、二甲硫化合物占主导地位,而本研究在各流通阶段均检出以上物质,可见牡蛎仍保留较高的鲜香气味。

表2 太平洋牡蛎不同流通阶段挥发性风味物质OAVTable 2 OAVs of volatile flavor substances in C.gigas during different circulation stages
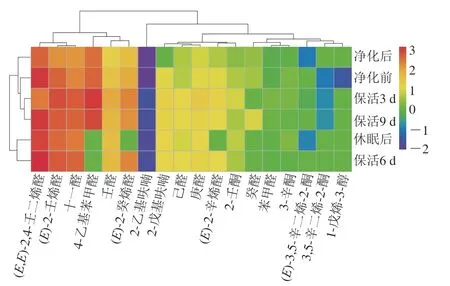
图3 太平洋牡蛎不同流通阶段挥发性风味物质OAV变化热图Fig.3 Heatmap of changes in OAVs of volatile flavor substances in C.gigas during different circulation stages
2.5 太平洋牡蛎不同流通阶段挥发性风味物质PCA
为了更直观体现活体太平洋牡蛎不同流通阶段气味特征差异,依据OAV筛选结果,选取关键香气成分进行PCA。如图4所示,箭头代表各挥发性风味物质组成分二维和三维空间的投影,箭尖距离原点越远,表示该变量被主成分解释的程度越高[28]。由图4a可知,不同流通阶段牡蛎样品整体区分度较高,净化前组牡蛎处于第2象限,对PC2有正响应值;净化后组与诱导休眠组牡蛎处于第3象限,对PC1、PC2均具有负响应值;保活第3天处于第4象限,对PC1有正响应值;保活第6、9天处于第1象限,对PC1、PC2均具有正响应值,可见,牡蛎在不同流通阶段有明显的区分度。由图4b可知,PC1、PC2、PC3表示太平洋牡蛎样品的三维分析图,PC的贡献率分别为59.4%(PC1)、15.8%(PC2)和10.4%(PC3),累计贡献率为85.6%,同样表明PC1、PC2和PC3能够较好地反映太平洋牡蛎中大部分挥发性风味化合物的信息,同时也进一步说明了活体牡蛎体内挥发性风味化合物在长时保活流通过程中随着时间的延长而发生了明显的变化。

图4 太平洋牡蛎不同流通阶段挥发性风味物质PCA二维图(a)、三维图(b)Fig.4 Two-(a) and three-(b) dimensional PCA plots of volatile flavor substances in C.gigas at different circulation stages
3 结论
采用GC-MS技术分析活体太平洋牡蛎不同流通阶段挥发性风味物质组成与含量变化情况,共鉴定出49 种挥发性风味化合物,确定醛、酮、酯类化合物为活体牡蛎主要风味物质,其含量变化可作为反映生理状态的参考;牡蛎采捕离水后,应激胁迫对其挥发性风味物质影响较大;通过24 h暂养净化,牡蛎愉悦性风味化合物明显提升,刺激性气味化合物明显降低,脂质氧化得到明显的缓解;诱导休眠至保活流通阶段,牡蛎脂质氧化随着保活流通时间的延长加剧,挥发性风味物质呈缓慢下降趋势。太平洋牡蛎采捕后通过暂养净化24 h,机体活力品质与风味物质达到新的水平,更有利于后期长时低温无水保活;同时挥发性成分分析可以作为活体贝类流通过程中活力品质鉴定的一种方法。

