肺癌胸腔镜术后病人肺部并发症列线图预测模型的构建
梁冬燕,王 慧,邱玲动,高 娜,任艳华,张艳芬,公丕欣*
1.山东第一医科大学(山东省医学科学院),山东 271000;2.山东第一医科大学第二附属医院
肺癌是全球癌症死亡的主要原因之一,对人类的健康和经济构成威胁[1]。手术切除和淋巴结清扫术仍是早期肺癌病人的最佳治疗方法[2]。尽管胸腔镜手术作为微创术式已逐渐取代传统开胸手术成为我国治疗肺癌的首选方式,但由于肺容积减少、呼吸肌力量减弱和咳嗽效率降低等原因,术后肺部并发症(postoperative pulmonary complications,PPCs)的发生率并不低[3]。术后肺部并发症不仅严重影响病人心肺功能的恢复,而且延长了住院时间,增加了住院成本,是术后病人死亡和治疗失败的重要原因之一[4]。随着胸腔镜在肺癌病人中的普及应用,我国对胸腔镜肺癌病人的相关研究逐年增加,多数研究针对单一并发症,忽略了不同并发症在病人术后不同阶段发生甚至同时发生的情况。因此,本研究根据欧洲联合工作组发布的术后肺部并发症定义指南[5],对多种术后肺部并发症进行预测因子的模型构建及验证,旨在为早期识别高危病人,实施外科护理提供依据。
1 对象与方法
1.1 研究对象 选取2021 年1 月—2022 年4 月在山东省某三级甲等医院胸外科行胸腔镜根治术的肺癌病人作为研究对象。纳入标准:①经病理组织学、纤维支气管镜、增强CT 扫描以及常规胸部平扫等检查确诊为肺癌;②病人接受胸腔镜手术治疗,无中转开胸手术;③符合欧洲围术期临床结局(European perioperative clinical outcome,EPCO)中的术后肺部并发症诊断标准;④合并糖尿病、高血压、高血脂等基础疾病的病人相关指标在围术期控制在手术指征范围内;⑤具有完整的临床资料。排除标准:①临床资料不完整或自动出院病人;②中转开胸病人;③本次住院同期行其他手术的病人;④既往曾行胸部手术的病人;⑤术前行新辅助放化疗或分子靶向治疗者;⑥术前存在肺部感染等术后肺部并发症诊断指标者。本研究已获得医院伦理委员会审核批准(批准号:2022-082)。因本研究为回顾性研究,故获批免签署知情同意书。
1.2 术后肺部并发症的定义 根据欧洲麻醉学学会(European Society of Anaesthesiology,ESA)和欧洲重症监护医学学会(European Society of Intensive Care Medicine,ESICM)的联合工作组发布的EPCO 定义指南[5],将呼吸道感染、呼吸衰竭、胸腔积液、肺不张、气胸、支气管痉挛和吸入性肺炎作为确定术后肺部并发症的综合指标,见表1。

表1 术后肺部并发症的定义
1.3 研究方法
1.3.1 确定研究变量 在文献回顾的基础上,成立研究小组,对纳入的危险因素进行讨论并确定。小组由10 名成员组成,包括胸外科主任医师1 名、胸外科主治医师2 名、主任护师1 名、胸外科护士长1 名、胸外科护士(10 年以上)2 名、麻醉科医师1 名、手术室护士1 名和全日制研究生1 名。本研究综合考虑肺癌病人临床护理现状与相关文献[6-7],最终确定纳入肺癌病人相关指标19 项,包括:①病人一般信息,如年龄、性别、体重指数、吸烟史、第一秒用力呼气量(FEV1)/用力肺活量(FVC)等:②手术相关信息,如美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级、手术时间、手术部位、引流管放置个数等。
1.3.2 资料收集和质量控制方法 由两名经过统一培训的小组成员收集资料,查看医院电子病历系统及数字化病案系统相关数据,采用Excel 2019 软件录入数据资料,由研究者对录入的资料进行整理和归纳。若资料收集过程中存在问题,则研究者与收集资料者及时沟通和调整,所有病人资料信息均更新至本研究结束。
1.4 统计学分析 采用Excel 2019 软件进行数据录入,采用SPSS 25.0 软件和R 语言(4.2.0 版本)进行数据分析。定性资料采用例数、百分比(%)进行统计描述,组间比较采用χ2检验或Fisher 精确检验法进行分析。定量资料若服从正态分布,采用均数±标准差(±s)描述,组间比较采用独立样本t检验;若不服从正态分布,则使用中位数描述其集中趋势,四分位数间距(inter-quartile range,IQR)描述其离散趋势,组间比较采用Mann-WhitneyU检验进行分析,α=0.05 作为检验标准。在R 语言中,使用Caret 软件包将数据按照7∶3 的比例分为建模集和验证集;利用Glmnet 软件包进行Lasso 回归,在所进行的Lasso 回归分析中对所包含变量的集中化和归一化进行k 倍(本研究中为3 倍)交叉验证,然后选择最佳Lambda 值,初步筛选出风险因素变量;运用RMS 软件包进行Logistic 回归,通过引入Lasso 回归模型中选择的变量,使用多变量Logistic回归分析构建预测模型,绘制Nomogram 图。最后,采用受试者工作特征(ROC)曲线、校准曲线和Hosmer-Lemeshow 检验来评估预测效能。
2 结果
2.1 研究对象的一般资料 本研究初步纳入456 例病人,经过筛查和排除后,最终纳入435 例肺癌病人,以7∶3 的比例随机进入建模集和验证集,最终建模集纳入305 例,验证集纳入130 例,见图1。病人术后肺部并发症的发生率建模集为38.7%、验证集为32.3%。建模集及验证集病人一般临床资料见表2。

图1 研究人群纳入和分组流程图
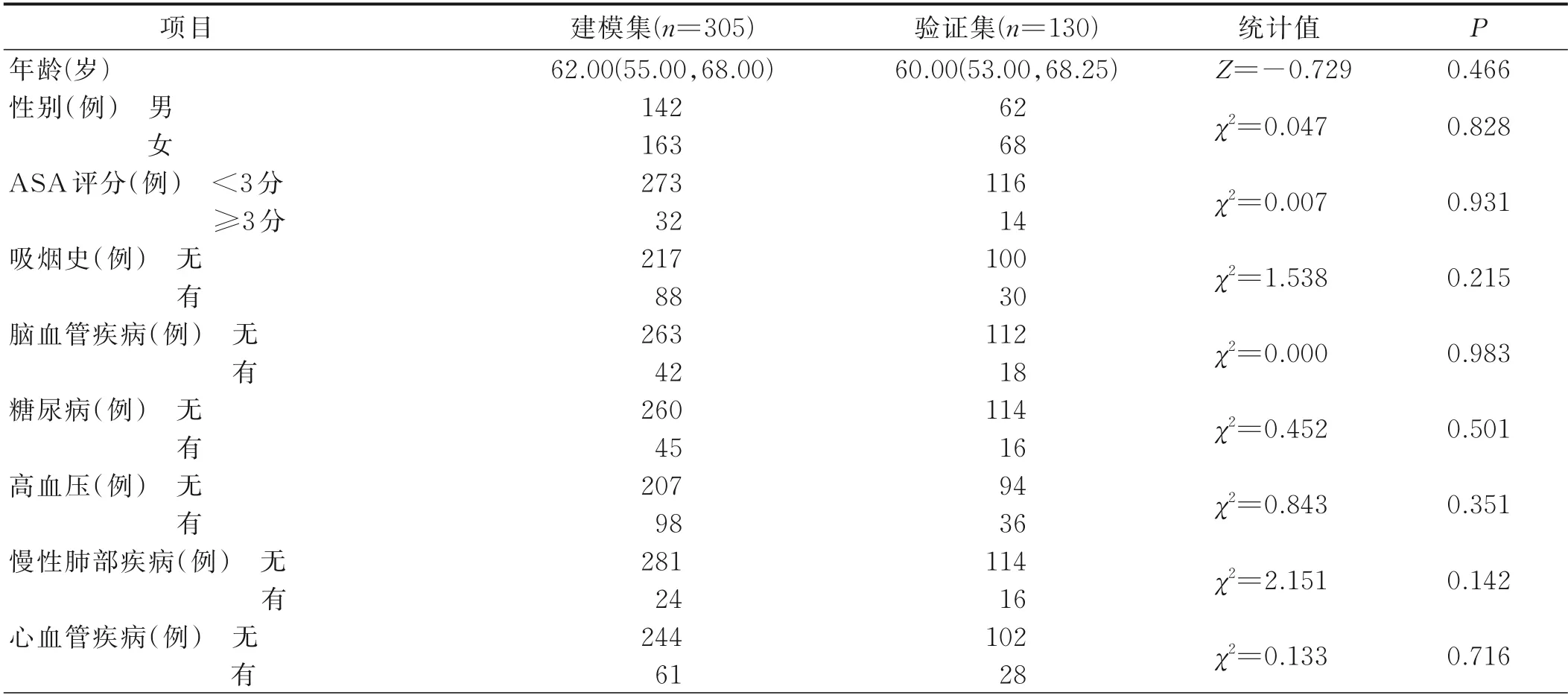
表2 建模集与验证集病人临床资料比较
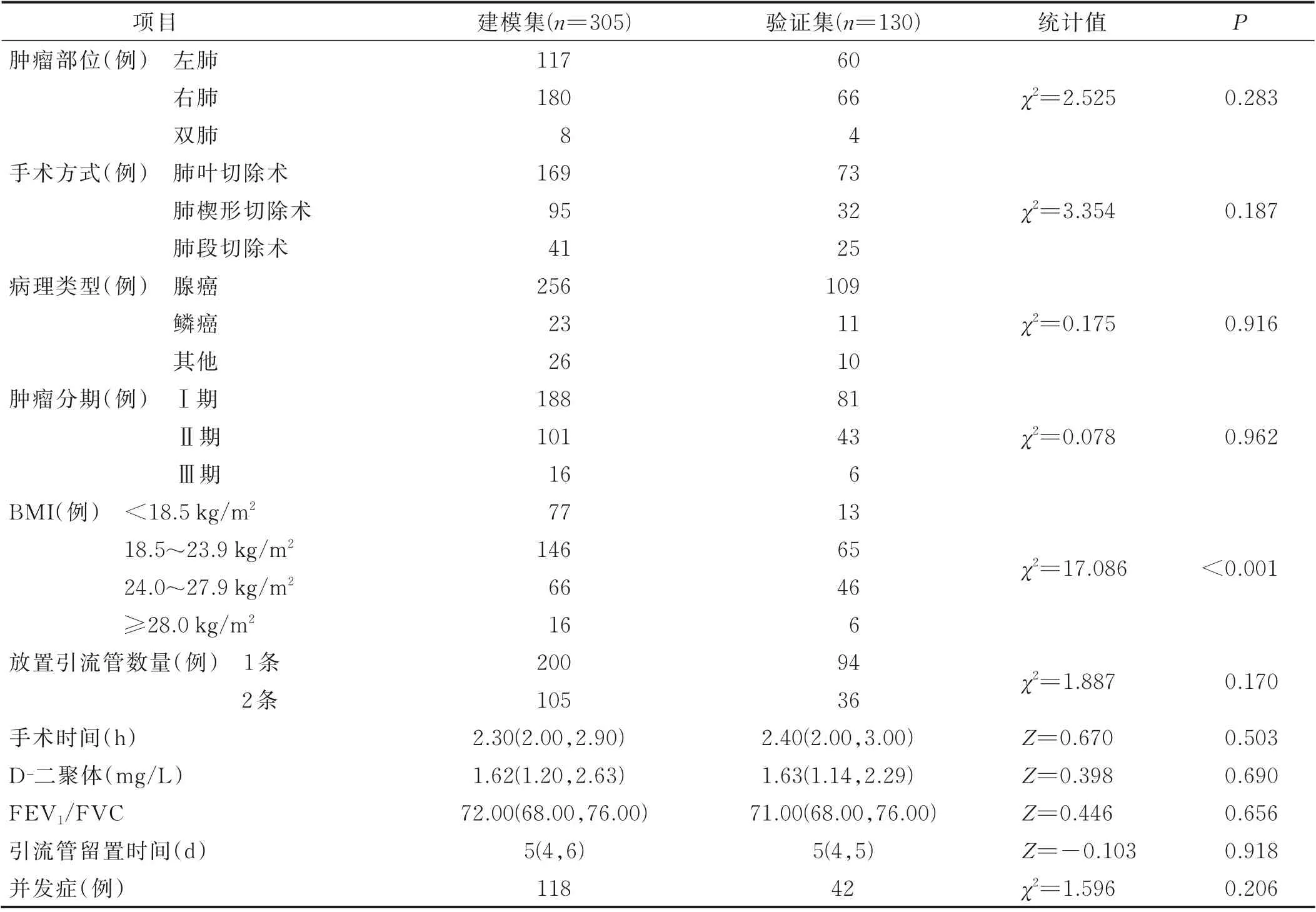
(续表)
2.2 胸腔镜肺癌病人发生术后肺部并发症的Lasso回归分析 在Lasso 回归分析中,通过推导最优Lambda,提取了5 个系数非0 的变量,分别是年龄、ASA 评分、慢性肺部疾病、病理分期和高血压,见图2,该图中横坐标是Lambda,纵坐标是回归系数值,可以发现Lambda 值减小,压缩参数也减小,而回归系数绝对值增大,反之,压缩参数增大,而回归系数绝对值减小;图上方的数字表示模型中自变量的个数,随着Lambda 的变化,自变量数目也在变化(图形是尽可能多地展示Lambda 所对应的结果,而并非只展示Lambda 最优值的结果)。另外,通过进一步交叉验证,绘制了均方误差与对数(Lambda)之间的关系,并根据标准误差绘制了两条虚线垂直线(第1 条虚线表示均方误差最小时对应的Lambda 对数值;第2 条虚线表示距离最小均方误差1 个标准误时对应的Lambda 对数值),见图3。总之,Lasso 回归表明,年龄、ASA 评分、慢性肺部疾病、病理分期和高血压为胸腔镜肺癌病人发生术后肺部并发症的危险因素。

图2 Lasso 回归系统剖面图

图3 交叉验证
2.3 胸腔镜肺癌病人发生术后肺部并发症的多因素分析及列线图预测模型的构建 将Lasso 回归分析筛选的变量作为自变量,是否发生术后肺部并发症作为因变量,构建二分类Logistic 回归分析。结果显示:年龄、ASA 评分、慢性肺部疾病和病理分期为胸腔镜肺癌病人发生术后肺部并发症的危险因素(P<0.05),而高血压不能作为预测术后肺部并发症的独立风险因素(P>0.05),见表3。使用Lasso-Logistic 回归分析筛选出的独立危险因素,以列线图的形式呈现胸腔镜肺癌病人发生术后肺部并发症的预测模型,见图4。在列线图中,每个研究变量都在最顶端的分数线上有相应的分值,将所有研究变量的分值相加得总分,总分对应的预测概率就是胸腔镜肺癌病人发生术后肺部并发症的概率。根据列线图模型,以1 例胸腔镜肺癌病人为例,建立动态列线图,见图5。可以看出,病人年龄在55 岁以上,未合并慢性肺部疾病,ASA 评分<3 分,病理分期为Ⅱ期,列线图模型预测该病人发生术后肺部并发症的概率为58%。
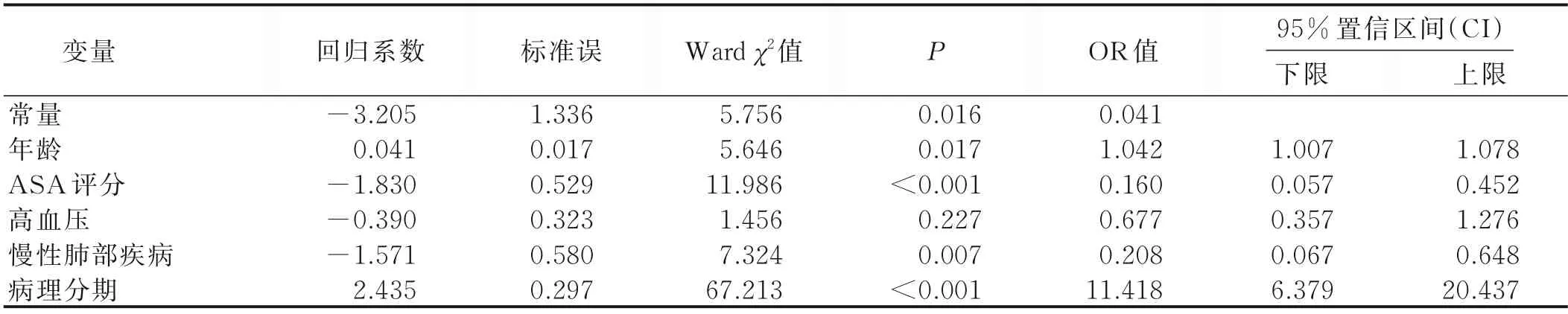
表3 Logistic 回归分析

图4 术后肺部并发症列线图预测模型

图5 动态列线图
2.4 胸腔镜肺癌病人发生术后肺部并发症的预测模型验证 内部验证:ROC 曲线用于评估预测模型的判别能力,其纵轴为灵敏度,横轴为1-特异度,即假阳性率。本研究中ROC 曲线下面积(AUC)为0.854,95%CI[0.808,0.900],表明预测模型具有良好的判别能力,见图6。Hosmer-Lemeshow 检验,χ2=7.350,P=0.500,灵敏度为78.8%,特异度为84.9%,准确率为82.6%。同时,校准曲线中预测模型的预测值与实际值显示较好的吻合性,表明预测模型具有良好的校准度,见图7。外部验证:本研究将验证集的130 例数据纳入预测模型中进行分析,显示AUC 为0.848,95%CI[0.774,0.921],见 图8。Hosmer-Lemeshow 检 验,χ2=7.672,P=0.466,校准曲线中预测模型的预测值与实际值显示较好的一致性,见图9。在外部验证中,灵敏度为70.2%,特异度为83.1%,准确率为78.5%,表明验证集数据与模型拟合良好,预测能力较强。

图6 建模集ROC 曲线

图7 内部验证校准曲线
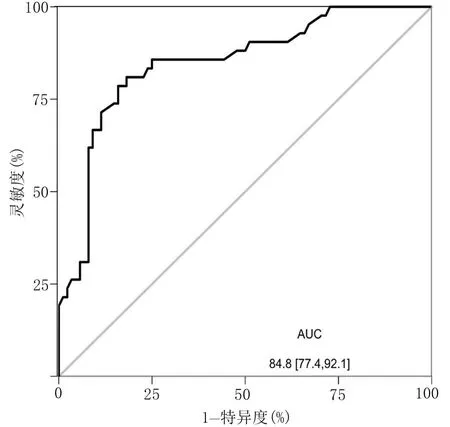
图8 验证集ROC 曲线

图9 外部验证校准曲线
3 讨论
3.1 胸腔镜肺癌病人发生术后肺部并发症的列线图预测模型具有科学性 术后肺部并发症在手术和麻醉相关的风险中占很大比例,并且是术后死亡率增高、住院时间延长和费用增加的主要原因,识别高风险病人是提高外科护理质量的重要步骤。本研究采用Lasso回归进行变量筛选,能够有效避免多重共线性的问题;根据筛选出的研究变量,构建可视化列线图预测模型,医护人员按照列线图的分值即可得出病人发生术后肺部并发症的风险概率,表明该模型具有直观性、实用性和便携性。采用ROC 曲线对模型的预测效果进行评估,当AUC 为0.5~0.7 时,提示模型预测能力较低;当AUC 为0.7~0.9时,提示模型预测能力较好;当AUC>0.9 时,提示模型预测能力强[8]。本研究内部验证和外部验证的AUC 分别为0.854 和0.848,说明该模型具有较好的预测能力。同时,本研究Hosmer-Lemeshow 拟合优度检验P>0.05,校准曲线预测值与实测值吻合程度较高,说明该模型对预测术后肺部并发症有较高的临床价值。
3.2 胸腔镜肺癌病人发生术后肺部并发症的相关因素
3.2.1 高龄胸腔镜肺癌病人易发生术后肺部并发症本研究显示,随着病人年龄的增加,发生术后肺部并发症的概率随之增加。相关研究表明,高龄可以作为预测术后肺部并发症的发生的独立风险因素[9-10],与本研究结果一致。多项研究[9,11-16]发现,年龄>60 岁或65 岁是一个危险因素,术后肺部并发症的风险随着年龄的增加而增加,可能与高龄所带来的身体虚弱有关,体弱多病也被证明与术后肺部并发症有关[17]。随着年龄的不断增加,病人在身体功能、认知、慢性疾病负担、行走速度、营养等方面发生不同程度的变化,年龄虽无法逆转,但可以通过适当锻炼等方式强健体魄、减慢衰老进程,进而改善体质,促进健康。
3.2.2 ASA 评分≥3 分的胸腔镜肺癌病人易发生术后肺部并发症 美国ASA 在1941 年根据病人体质状况和对手术危险性进行分类,推出了麻醉风险评分系统,经过不断更新,在2014 年修改为人们所熟知的ASA分级[18]。Ⅰ级:正常,健康,禁烟、不饮酒或有限度饮酒;Ⅱ级:轻度全身性疾病,没有实质性的功能限制;Ⅲ级:严重的全身性疾病,实质性功能限制,1 种或多种中度至重度疾病;Ⅳ级:对生命构成持续威胁的严重全身性疾病;Ⅴ级:濒死状态,未经手术无法存活;Ⅵ级:脑死亡器官捐献者。自ASA 评分系统引入以来,许多研究证明其与围术期风险预测的相关性[19]。Hackett等[20]研究首先提出ASA 评分具有很强的预测手术并发症和围术期死亡率的能力;Agostini 等[21]研究表明,肺切除术后ASA 分级≥Ⅲ级的病人术后肺部并发症的风险增加了3.9 倍;Wang 等[22]研究显示,随着ASA等级的升高,术后肺部并发症的风险比也在增加。美国国家卫生与保健研究所(The National Institute for Health and Care Excellence,NICE)建议,对于ASAⅢ级或Ⅳ级病人,可在术前进行肺活量测定和动脉血气分析[23]。
3.2.3 合并慢性肺部疾病的胸腔镜肺癌病人易发生术后肺部并发症 慢性肺部疾病包括支气管扩张、哮喘、慢性阻塞性肺疾病(chronic obstructive pulmonary diseases,COPD)、肺结核等,其中,COPD 是美国医师协会指南[24]所提出的术后肺部并发症中最常被识别的危险因素。合并慢性支气管炎或COPD 等慢性肺部疾病病人,存在阻塞性通气障碍、气道功能受损,同时气道炎症导致一定程度的肺结构破坏,病人对病原体的抵抗功能较差[25]。Hong 等[26]的研究发现,合并呼吸系统疾病的肺癌病人死亡率增加;合并COPD 的肺癌病人,风险比为1.32;合并哮喘的肺癌病人风险比为1.11。随着术前医疗措施的不断优化,合并症在一定程度上是可以改变的。COPD 和哮喘可以使用支气管扩张剂和类固醇药物进行治疗[27]。呼吸道感染与术后肺部并发症的发生密切相关,故择期手术应该推迟,直到症状和肺功能测试恢复到基线水平[28]。
3.2.4 病理分期高的胸腔镜肺癌病人易发生术后肺部并发症 本研究发现,随着临床分期的升高,病人发生术后肺部并发症的风险也在增加,与严晓霞等[29]研究结果一致。本研究对术后切除的标本进行病理分期,Ⅰ期:指非常局限的病变,尤其是3 cm 以下,没有肺门和纵隔淋巴结转移的病人;Ⅱ期:有肺门、淋巴结转移的病人;Ⅲ期:有纵隔淋巴结转移的病人。佟丽斐等[30]研究表明,临床分期对肺癌病人生存质量及生存时间有重要影响。吴杏尧等[31]研究肺癌分期与病人衰弱的相关性,发现分期越高,病人发生衰弱的危险性越大。病理分期作为不可改变因素,可以通过定期体检,达到早发现、早治疗的目的,从而改善病人预后。
4 小结
本研究基于年龄、ASA 评分、慢性肺部疾病和病理分期构建的术后肺部并发症列线图预测模型简单明了,预测效果良好,可为识别高风险病人及实施防治措施提供参考。但本研究存在一定局限性,由于样本量纳入有限且为回顾性研究,在资料收集过程中可能存在信息偏倚或选择偏倚。因此,未来需要大量的多中心的数据验证该模型的外推性,从而构建大数据术后肺部并发症预测模型。

