NEFA经MMPs途径对奶牛子宫内膜上皮细胞Ⅳ型胶原蛋白表达的影响
邢菲菲,罗胜缤,温小庆,曹一鸣,李美娟,罗春海,付世新
(黑龙江八一农垦大学 动物科技学院,黑龙江 大庆 163319)
奶牛在围产期由于胎儿生长和产奶量的需要,能量需求大于摄于,易发生能量负平衡(negative energy balance,NEB)。这一阶段因代谢方式转变,体内非酯化脂肪酸(non-esterified fatty acids,NEFA)的浓度大幅升高[1]。经查阅资料得知,高浓度的NEFA对动物和人类的生殖性能都有不利影响[2-3],SWANGCHAN-UTHAI等[4]发现产犊前最后1周高浓度的NEFA与胎衣不下(retained fetal membranes,RFM)的风险增加相关,OSPINA等[5]则表明NEFA与酮病、子宫炎和乳腺炎等疾病的风险增加相关,与RFM的风险增加更为相关。RFM是奶牛在分娩后常见并且影响奶牛繁殖健康的疾病,其定义为分娩后12 h未能排出胎衣[6]。奶牛RFM的发生率为5%~50%,且夏天气温高时发病率会更高[7]。RFM的负面影响包括子宫复旧延迟、履配不孕、妊娠率下降等,而这些又会导致牛群因繁殖能力下降和产奶量减少造成严重的经济损失。同时,RFM还是继发子宫炎、子宫内膜炎、酮症、皱胃变位和乳腺炎等疾病的危险因素[8]。
胎衣排出的基础是妊娠晚期的胎盘成熟,此时胎盘中血流减少血管收缩,子叶绒毛变小和塌陷,母体胎盘与胎儿胎盘处上皮细胞会发生凋亡,细胞外基质(extracellular matrix,ECM)降解重塑,最后经过子宫的收缩,胎儿子叶与母体肉阜分离,胎盘得以及时分离排出[9]。现如今公认的RFM主要病理学基础是胎盘组织ECM降解障碍,而母体和胎儿胎盘之间ECM中引起黏连的物质主要是Ⅳ型胶原蛋白(collagen-Ⅳ,COL-Ⅳ)。林宏甲[10]的研究发现,与胎衣正常排出奶牛的胎盘相比,RFM奶牛的胎盘中COL-Ⅳ大量表达,降解胶原蛋白的主要胶原酶基质金属蛋白酶-2(matrix metalloproteinase-2,MMP-2)和基质金属蛋白酶-9(matrix metalloproteinase-9,MMP-9)的表达水平显著降低。也有报道认为胎衣排出是一种炎症过程,围产期奶牛中性粒细胞功能受损及趋化性降低、炎症反应的改变与RFM有关[11]。与正常排出胎衣的奶牛相比,发生RFM的奶牛血液中白细胞介素1β(interleukin-1β,IL-1β)、IL-6、IL-8、肿瘤坏死因子-α(tumor necrosis factor -α,TNF-α) 4种促炎细胞因子的浓度均显著降低[8]。而且MMP-9在子宫收缩开始时是由IL-8通过趋化因子受体-2诱导释放,其分泌还触发了TNF-α的快速释放,TNF-α又可以募集中性粒细胞,中性粒细胞进一步的诱导释放MMP-2和MMP-9。妊娠末期胎盘处促炎细胞因子和免疫细胞的大量涌入,通过调节了MMPs的分泌而调节ECM降解,进而促使胎盘排出[12]。并且高浓度的NEFA会诱导奶牛子宫内膜上皮细胞发生炎症和细胞凋亡[13],在大鼠上还可以影响MMPs及其抑制剂之间的动态平衡[14]。由此可见,MMPs的表达与活性受到NEFA的调控。
目前关于NEFA是如何影响奶牛RFM发生的研究很少,故本试验拟通过使用不同浓度的NEFA刺激奶牛子宫内膜上皮细胞,来探讨NEFA是否通过影响MMPs和炎性因子的表达来调节胎盘处ECM的降解,进而影响RFM的发生。
1 材料与方法
1.1 主要试剂棕榈酸、硬脂酸、棕榈油酸、油酸、亚油酸购自美国Sigma公司;RPMI 1640培养液购自赛默飞世尔生物化学制品(北京)有限公司;青霉素-链霉素溶液、胰蛋白酶-EDTA消化液购自上海索莱宝公司;胎牛血清购自四季青公司;PrimeScriptTMRT Reagent Kit、TB Green®Premix Ex TaqTMⅡ购自日本TaKaRa公司;RIPA细胞裂解液、蛋白酶磷酸酶抑制剂混合物、BCA蛋白浓度测定试剂盒、彩色预染蛋白相对分子质量标准、二抗(兔抗鼠、山羊抗兔)购自上海碧云天生物技术有限公司;鼠源Anti-MMP-2单抗购自美国Merck公司;鼠源Anti-MMP-9单抗购自Cloud-Clone Corp公司;兔源Anti-Collagen Ⅳ多抗购自美国赛默飞公司;鼠源Anti-β-actin多抗购自中国博奥森公司;TRIzol购自美国Invitrogen公司。
1.2 奶牛子宫内膜上皮细胞的培养奶牛原代子宫内膜上皮细胞是由本实验室郑程远等[15]利用贴壁法分离培养的,经过纯化后,纯度可达90%以上。将冻存的细胞从液氮中拿出后迅速放入37℃水浴锅中摇晃,融化的细胞悬液吸入到EP管中,4 min、1 000×g离心后弃上清。加入新的培养液混匀细胞团,然后按适当比例将细胞接种至10 cm细胞培养皿中,放入37℃细胞培养箱内,隔2 d传代1次,在第3代后加药刺激,准备后续试验。
1.3 NEFA刺激子宫内膜上皮细胞将子宫内膜上皮细胞接种到6孔板中,待细胞融合度达到80%左右时,加入NEFA(含1.595 mmol/L棕榈酸、0.720 mmol/L 硬脂酸、0.265 mmol/L棕榈油酸、2.175 mmol/L 油酸、0.245 mmol/L亚油酸)刺激细胞。根据本实验室前期的试验结果按添加的NEFA浓度设置分组[16]:对照组(0 mmol/L)、低浓度组(0.2 mmol/L)和高浓度组(1.2 mmol/L)。刺激12 h 后弃去旧培养液,胰酶消化下细胞,PBS洗2遍后弃去上清,留下底部细胞团,以待后续RNA和蛋白质的提取。
1.4 总RNA的提取提取RNA过程中所有耗材皆为无RNA酶耗材,在冰上操作。取TRIzol加入到每个EP管中,每孔1 000 μL。裂解5 min后吸取液体到EP管中,每管加入200 μL的氯仿,剧烈震荡混匀,4℃、12 000×g离心10 min。小心吸取上层水相至新的EP管中,加入400 μL异丙醇,静置10 min 后4℃、12 000×g离心10 min。弃上清,往管中沉淀加入75%的乙醇,轻轻上下混匀,4℃、7 500×g离心5 min。弃上清后再4℃、7 500×g离心5 min,用枪头吸取残余的液体,最后晾干EP管。往管中加入适量的DEPC水,拿去测定RNA浓度。
1.5 总蛋白的提取向收集的细胞团中加入适量的RIPA裂解液和蛋白酶磷酸酶抑制剂混合物,冰上裂解30 min,每隔5 min震荡离心管。然后4℃、12 000×g离心30 min,小心吸取上清液至新的EP管中,使用BCA蛋白浓度测定试剂盒检测提取的蛋白浓度,加入PBS和Loading Buffer调整至相同浓度,煮沸10 min后-20℃保存。
1.6 qRT-PCR使用PrimeScriptTMRT reagent Kit将RNA反转录成为cDNA,反转录体系:4 μL的5×PrimeScript Buffer,1 μL的PrimeScript RT Enzyme MixⅠ、Oligo dT Primer、Random 6 mers,500 ng的总RNA,最后补加RNase Free dH2O至20 μL。将配置好的体系放入PCR仪中,37℃ 15 min、85℃ 5 s、4℃冷却。得到的产物-20℃保存。引物设计和购买来自上海生工生物工程有限公司,使用β-actin为内参,qRT-PCR法检测基质金属蛋白酶MMP-2、MMP-9,胶原蛋白COL-Ⅳ和炎性因子IL-1β、IL-6、IL-8、TNF-α的基因相对表达量,引物序列见表1,反应程序为:95℃ 30 s,95℃ 5 s,60℃ 30 s,39个循环;95℃ 10 s,melt curve 65~95℃。2-△△Ct法分析试验结果。

表1 引物序列
1.7 Western blot将提取的蛋白样品沸水煮5 min,冷却室温后将各组样品与彩虹预染Marker分别加入到SDS-PAGE凝胶的孔中,每孔10 μL。80 V 电压运行30 min,然后调为120 V电压运行45 min。电泳后的凝胶采用300 mA、3 h湿转的方法将蛋白转印到PVDF膜上后,膜用5%脱脂奶粉封闭3 h,TBST洗2次,每次5 min。之后分别使用一抗Anti-MMP-2(1∶1 000稀释)、Anti-MMP-9(1∶1 000稀释)和Anti-Collagen Ⅳ(1∶500稀释)4℃孵育过夜,TBST洗3次,每次5 min。二抗(1∶2 000稀释)室温孵育1 h,TBST洗3次后用凝胶成像分析系统照膜,Image Lab软件分析条带灰度值,记录试验结果。
1.8 数据分析qRT-PCR和Western blot试验重复3次,计算分析后的结果使用SPSS 26.0进行统计分析(ANOVA分析),“*”为差异显著(P<0.05),“**”为差异极显著(P<0.01)。
2 结果
2.1 NEFA对MMPs、COL-Ⅳ表达的影响如图1所示,NEFA处理细胞12 h后,与对照组相比,在低浓度组0.2 mmol/L和高浓度组1.2 mmol/L时细胞内MMP-2和COL-Ⅳ的mRNA表达极显著升高(P<0.01),MMP-9的mRNA表达在高浓度时被极显著下调(P<0.01)。Western blot的结果显示,与对照组相比,高浓度组的MMP-2和COL-Ⅳ的蛋白表达极显著上升(P<0.01),MMP-9的蛋白表达极显著下降(P<0.01)(图2)。
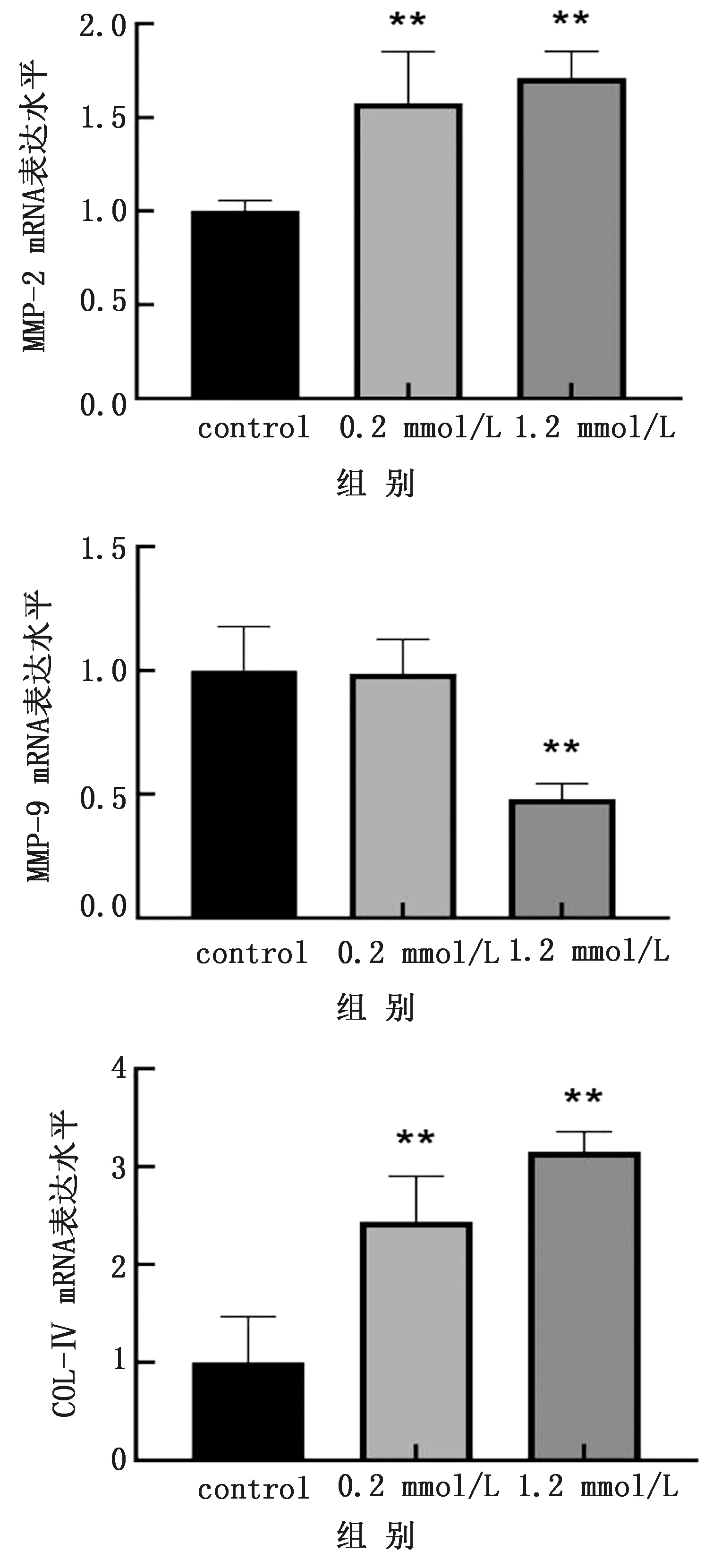
*.与对照组相比P<0.05; **.与对照组相比P<0.01。下同

A.MMP-2、MMP-9、COL-Ⅳ的Western blot结果;B.MMP-2、MMP-9、COL-Ⅳ的蛋白表达水平
2.2 NEFA对各炎性因子表达的影响经NEFA作用后,与对照组相比,炎性因子IL-1β、IL-6、IL-8、TNF-α的mRNA表达在高浓度组均极显著上调(P<0.01),在低浓度组,IL-6的mRNA基因被极显著上调(P<0.01),IL-8和TNF-α的mRNA基因被显著上调(P<0.05)(图3)。

图3 NEFA对子宫内膜上皮细胞炎性因子基因表达的影响
3 讨论
奶牛RFM的病因有很多,包括早产、难产、氧化应激、矿物质缺乏造成的营养不良等等,且这些因素影响RFM发生发展的具体机制还不完全清楚。但不论是免疫系统的反应、细胞凋亡、炎症还是MMPs系统,最终影响的还是ECM的降解,可以说ECM的降解程度才是胎衣排出的关键[12]。MMPs及其抑制剂—组织金属蛋白酶抑制剂(tissue inhibitor of matrix metalloproteinases,TIMPs)家族可以调节ECM的组装和降解[17-18]。其中MMPs里的明胶酶MMP-2和MMP-9在反刍动物中有很好的表达。MMP-2能够降解不同类型的胶原,包括Ⅳ、Ⅴ、Ⅶ和Ⅹ型明胶、弹性蛋白和纤维连接蛋白[19]。MMP-9可以降解Ⅳ和Ⅴ型胶原蛋白,存在于中性粒细胞的第三级颗粒中。有研究表明,RFM与非RFM奶牛胎盘中的蛋白酶存在差异,表明酶活性的改变在RFM的致病过程中起作用。例如,RFM奶牛胎盘中的MMP-2和MMP-9的活性下降[11]。可是在本研究中,MMP-2和COL-Ⅳ的基因和蛋白表达均显著升高,MMP-9的表达却显著下降。MMPs的表达对子叶和肉阜间的连接和胎盘的释放很重要,NEFA处理子宫内膜上皮细胞后,本研究检测到这些酶的表达跟之前的研究结果不完全一致,提示NEFA对细胞的影响可能还有别的方面,多种因素导致MMPs的活性表达出现了这样的结果。但是在奶牛胎盘处的ECM中,COL-Ⅳ才是主要的胶原蛋白,而MMP-9是体内降解COL-Ⅳ的主要基质金属蛋白酶,MMP-2虽然也可以降解COL-Ⅳ,但可能其在奶牛上与COL-Ⅳ的亲和力不如MMP-9,或者MMP-2还受到了其他物质的调控。故本试验结果也表明了NEFA可能通过调节了MMP-2和MMP-9的表达,调节了ECM的降解,从而影响RFM的发生。
IL-1β被认为是由各种类型的细胞分泌以应对损伤或炎症,并通过调节其吞噬活性(如黏附、细胞迁移、呼吸暴发、溶酶体酶释放和细胞表面受体表达)影响中性粒细胞,较低水平的IL-1β可能会损伤中性粒细胞的功能。IL-6在增强或限制免疫反应方面具有复杂作用[20],IL-6作为一种促炎因子,在某些情况下也可能抑制中性粒细胞的迁移。IL-8,也称为中性粒细胞激活因子,是一种由多种细胞类型在脂多糖等炎症刺激物存在下产生的细胞因子。IL-8还可引起宫颈扩张和胶原酶分泌增加[21],从而加速胎儿子叶与母体肉阜的分离[22]。而TNF-α在增强中性粒细胞功能方面具有重要作用,如中性粒细胞呼吸暴发和溶酶体酶释放,以响应各种可溶性和颗粒细胞刺激。这4种炎性因子都与中性粒细胞的功能相关,会影响胎衣排出时的炎症反应及MMP-2、MMP-9的释放。因此低水平的IL-1β、IL-6、IL-8、TNF-α在分娩后炎症过程中负面调节了中性粒细胞的功能,减少了MMPs的分泌,这是影响胎衣排出的关键[8]。正常范围内的炎症反应可以促进MMPs的释放,而过度的炎症反应可能反而会损害细胞功能。在本试验结果中,4种炎性因子的基因表达都是上调的,猜测NEFA可能通过影响炎症反应的程度来诱导RFM的发生。
综上所述,NEFA可直接通过降低MMP-9的表达,引起ECM降解障碍,并可通过增加炎性因子和MMP-2的表达,干扰ECM降解,但其具体的调控作用还有待于进一步研究。

