液相色谱串联质谱法测定大鼠血浆中知母皂苷A-Ⅲ质量浓度及其药物代谢动力学研究*
陈宝婷,陈举亮,詹亚坤,张素方
(广东省中医院珠海医院,广东 珠海 519015)
知母具有清热泻火、生津润燥功效,临床用于高热烦渴、骨蒸潮热、虚烦不眠等症,常与黄柏以药对形式配伍应用,经典方剂有滋肾通关丸、知柏地黄丸、大补阴丸等。知母总皂苷是知母中主要的有效甾体皂苷,知母皂苷A-Ⅲ(TA-Ⅲ)又称西陵皂苷A-Ⅲ,是知母总皂苷的主要活性成分,抗癌、抗衰老、抗血管生成、抗氧化、降血糖、抗抑郁、抗血小板聚集、扩张血管、改善记忆力等作用显著[1-9]。目前,关于测定生物基质中TA-Ⅲ的方法有液相色谱串联质谱(LC-MS/MS)法[10]和高效液相色谱串联质谱(HPLC-MS/MS)法[11],但存在血浆用量大、离子抑制效应严重、选择性和灵敏度低、线性范围窄、运行时间长等不足。为此,本研究中建立了测定大鼠血浆中TA-Ⅲ的LC-MS/MS法,并考察其药物代谢动力学(PK)特征,为其临床合理应用提供参考。现报道如下。
1 仪器、试药与动物
1.1 仪器
API4000+型液相色谱-三重四极杆质谱联用仪(美国Applied Biosystems公司),配有Turbo Ionspray离子源及Analyst 1.6数据处理系统;LC-20AD型高效液相色谱系统(日本Shimadzu公司),配有DGU-20A3型在线真空脱气机,LC-20AD型泵,SIL-20AC型自动进样器,CBM-20A型控制器,CTO-20A型色谱柱柱温箱;Microfuge 16型台式微量离心机(美国贝克曼库尔特公司);Milli-Q型超纯水机(美国Millipore公司)。
1.2 试药
TA-Ⅲ对照品(天津中新药业中药现代化技术工程中心,批号为MUST-15020108,纯度>99%);人参皂苷Rg2对照品(内标,中国食品药品检定研究院,批号为110406,纯度>99%);知母(批号为110501),黄柏(批号为120104991),均购自广州致信中药饮片有限公司;乙腈和乙酸铵均为色谱纯,水为超纯水。
1.3 动物
SPF级SD大鼠12只,雄性,体质量230~270 g,购自广东省医学实验动物中心,动物合格证号为(粤)0100527,实验动物使用许可证号为SYXK(粤)2018-0094。所有大鼠均饲养于温度为20~25℃、相对湿度为40%~70%的房间内,自然明暗循环1周。
2 方法与结果
2.1 色谱与质谱条件
1)色谱条件。色谱柱:Agilent XDB-C8柱(150 mm×2.1 mm,5µm);流动相:乙腈-2 mmol/L乙酸铵(55∶45,V/V);流速:250µL/min;柱温:35℃;进样量:5µL。
2)质谱条件。离子源:电喷雾离子源;喷雾电压:4 500 V;雾化温度:500℃;雾化气:60 psi;加热辅助气:40 psi;气帘气:20 psi;碰撞气:12 psi;检测方式:负离子多离子反应监测;用于定量分析的离子质荷比(m/z):739.5→577.4(TA-Ⅲ),783.5→475.2(内标)。
2.2 溶液制备
取TA-Ⅲ对照品1.50 mg,精密称定,加55%乙腈配制成质量浓度为150 µg/mL的TA-Ⅲ贮备液,置4℃冰箱保存,备用。
取人参皂苷Rg2对照品10 mg,精密称定,加55%乙腈配制成质量浓度为1 mg/mL的内标贮备液,继续加55%乙腈稀释成质量浓度为20µg/mL的内标工作液,置4℃冰箱保存,备用。
分别称取知母100 g和知母-黄柏(1∶1,m/m)200 g,加适量超纯水浸泡30 min,加热回流提取3次,每次60,60,45 min,3次加入的超纯水体积比为5∶3∶3(V/V/V),趁热滤过,合并滤液,浓缩得知母单煎液、知母-黄柏(1∶1,m/m)合煎液。采用LC-MS/MS法测定各煎液中TA-Ⅲ的质量浓度,加超纯水稀释,得TA-Ⅲ质量浓度均为0.117 mg/mL的知母供试品溶液和知母-黄柏(1∶1,m/m)供试品溶液。
2.3 样品处理
吸取大鼠血浆样品50µL,加内标工作液20µL,涡旋振荡30 s,加乙腈200µL,涡旋振荡2 min,离心(转速为13 000 r/min)10 min,吸取上清液150µL,加90µL超纯水,涡旋振荡30 s,离心(转速为13 000 r/min)30 s,0.2µm薄膜滤过,取滤液,按2.1项下试验条件进样测定。
2.4 方法学考察
专属性试验:取空白血浆、空白血浆+TA-Ⅲ+内标、灌胃TA-Ⅲ血浆样品各适量,按2.3项下方法处理,按2.1项下试验条件进样测定。结果TA-Ⅲ和内标保留时间分别为3.15 min和1.55 min,色谱峰峰形良好,分离完全,无内源性物质与其他物质干扰,表明方法专属性良好。色谱图见图1。
标准曲线与定量下限确定:取2.2项下TA-Ⅲ贮备液,用55%乙腈稀释至质量浓度为60 µg/mL,精密吸取0.5 mL,置10 mL容量瓶中,加空白血浆配制成质量浓度为3 000 ng/mL的TA-Ⅲ标准血样。加入空白血浆,稀释得质量浓度分别为0.3,1,3,10,30,100,300,1 000,2 500,3 000 ng/mL的系列TA-Ⅲ标准血样,按2.3项下方法处理,按2.1项下试验条件进样测定。以TA-Ⅲ和内标峰面积比值为纵坐标(Y)、TA-Ⅲ质量浓度为横坐标(X,ng/mL)进行加权线性回归(权重为1/X2),得回归方程Y=4.88×10-4X+1.31×10-4(r=0.999 3,n=10)。结果表明,TA-Ⅲ质量浓度在0.3~3 000 ng/mL范围内与TA-Ⅲ和内标峰面积比值线性关系良好。定量下限为0.3 ng/mL。
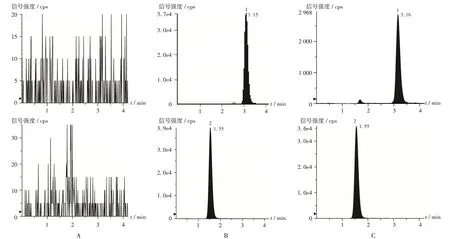
1.TA-Ⅲ2.人参皂苷Rg2A.空白血浆 B.空白血浆+TA-Ⅲ+内标 C.灌胃TA-Ⅲ血浆图1专属性试验液相色谱串联质谱图1.TA-Ⅲ2.Ginsenoside Rg2A.Blank plasma B.Blank plasma+TA-Ⅲ+internal standard C.Plasma obtained from rats after the gastrointestinal administration of TA-ⅢFig.1 LC-MS/MS chromatograms of the specificity test
精密度与准确度试验:取2.2项下TA-Ⅲ贮备液,用55%乙腈稀释至质量浓度为60 µg/mL,精密吸取0.5 mL,置10 mL容量瓶中,加空白血浆配制成质量浓度为3 000 ng/mL的TA-Ⅲ标准血样。加入空白血浆,稀释得质量浓度为1,1 500,2 500 ng/mL的系列TA-Ⅲ质控样品,各5份,按2.3项下方法处理,按2.1项下试验条件进样测定,于同1 d和连续3 d测定质控样品中TA-Ⅲ的质量浓度。以日内和日间相对标准偏差(RSD)考察方法的精密度,以相对回收率(实测浓度与真实浓度的比值)考察准确度。结果见表1。
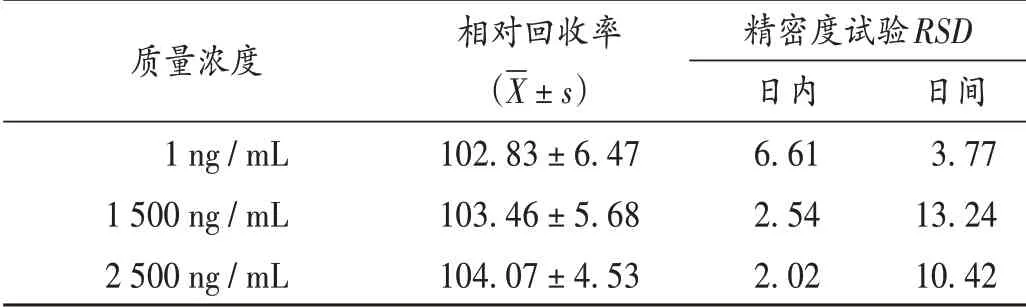
表1 血浆中TA-Ⅲ的精密度与准确度试验结果(%,n=5)Tab.1 Results of the precision and accuracy tests of TA-Ⅲin plasma(%,n=5)
提取回收率与基质效应试验:按精密度与准确度试验项下方法制备质量浓度为1,1 500,2 500 ng/mL的TA-Ⅲ质控样品,各5份,按2.3项下方法处理,按2.1项下试验条件进样测定,得峰面积(A1);取空白血浆,按2.3项下方法处理,按2.1项下试验条件进样测定,得峰面积(A2);用乙腈沉淀空白血浆,取上清液150µL,加内标工作液与TA-Ⅲ贮备液各适量,使TA-Ⅲ的质量浓度分别为1,1 500,2 500 ng/mL,按2.3项下方法处理,按2.1项下试验条件进样测定,得峰面积(A3)。按公式计算基质效应,基质效应(%)=(A3/A1×100%);按公式计算提取回收率,提取回收率(%)=(A2/A3×100%)。结果见表2。
表2 血浆中TA-Ⅲ的提取回收率与基质效应试验结果(±s,%,n=5)Tab.2 Results of the extraction recovery and matrix effect tests of TA-Ⅲin plasma(±s,%,n=5)

表2 血浆中TA-Ⅲ的提取回收率与基质效应试验结果(±s,%,n=5)Tab.2 Results of the extraction recovery and matrix effect tests of TA-Ⅲin plasma(±s,%,n=5)
质量浓度1 ng/mL 1 500 ng/mL 2 500 ng/mL提取回收率96.03±3.94 100.66±1.68 102.11±1.31基质效应90.63±6.45 83.57±0.26 88.88±0.49
残留效应试验:按精密度与准确度试验项下方法制备质量浓度为2 500 ng/mL的TA-Ⅲ质控样品,并取空白血浆样品,按2.1项下试验条件分别交替进样分析6次,考察TA-Ⅲ与内标的残留效应。结果高浓度的TA-Ⅲ进样后几乎无残留,符合方法学要求。
稳定性试验:按精密度与准确度试验项下方法制备质量浓度分别为1,1 500,2 500 ng/mL的TA-Ⅲ质控样品,各5份,分别将样品于室温下放置4 h、反复冻融3次、4℃放置24 h后,按2.3项下方法处理,按2.1项下试验条件进样测定。结果见表3。
表3 血浆中TA-Ⅲ的稳定性试验结果(±s,%,n=5)Tab.3 Results of the stability test of TA-Ⅲin plasma(±s,%,n=5)
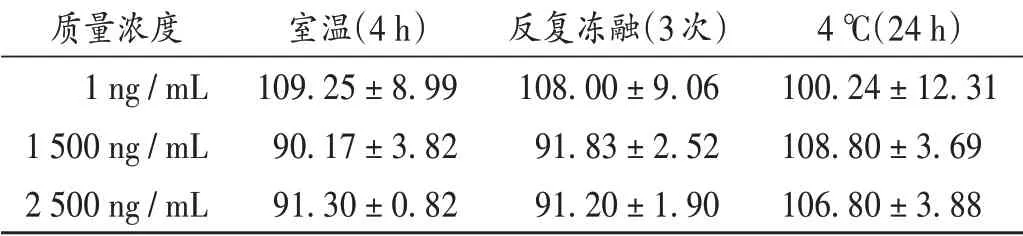
表3 血浆中TA-Ⅲ的稳定性试验结果(±s,%,n=5)Tab.3 Results of the stability test of TA-Ⅲin plasma(±s,%,n=5)
质量浓度1 ng/mL 1 500 ng/mL 2 500 ng/mL室温(4 h)109.25±8.99 90.17±3.82 91.30±0.82反复冻融(3次)108.00±9.06 91.83±2.52 91.20±1.90 4℃(24 h)100.24±12.31 108.80±3.69 106.80±3.88
2.5 PK研究
大鼠给药前禁食16 h,自由饮水。取12只大鼠,随机分为知母单煎液组和知母-黄柏(1∶1,m/m)合煎液组,各6只,均灌胃给药TA-Ⅲ1.17 mg/kg。分别于给药0,0.25,0.5,1,1.5,2,3,4,6,8,10,12,24,36 h时取眼眶血0.4 mL,置肝素化离心管中离心(转速为3 000 r/min)15 min,制备血浆,-80℃保存,待测。按2.3项下方法处理,按2.1项下试验条件进样测定TA-Ⅲ的血药浓度。采用DAS 2.1.1软件,根据非房室模型对血药浓度和时间数据进行分析,并计算PK参数(表4)。其中,药物最大浓度的时间点(tmax)和最大血药浓度(Cmax)均为实测值,采用梯形法计算血药浓度-时间曲线下面积(AUC),并绘制曲线图(图2)。结果知母单煎液组大鼠TA-Ⅲ的血药浓度低,药物吸收较慢,灌胃给药1 h后才检测到一定浓度的TA-Ⅲ。与知母单煎液组比较,知母-黄柏(1∶1,m/m)合煎液组TA-Ⅲ的血药浓度仍较低,但AUC增大,且0-∞的平均滞留时间(MRT0-∞)和消除半衰期(t1/2)均显著延长(P<0.01)。
表4 TA-Ⅲ的PK参数(±s,n=6)Tab.4 PK parameters of TA-Ⅲ(±s,n=6)
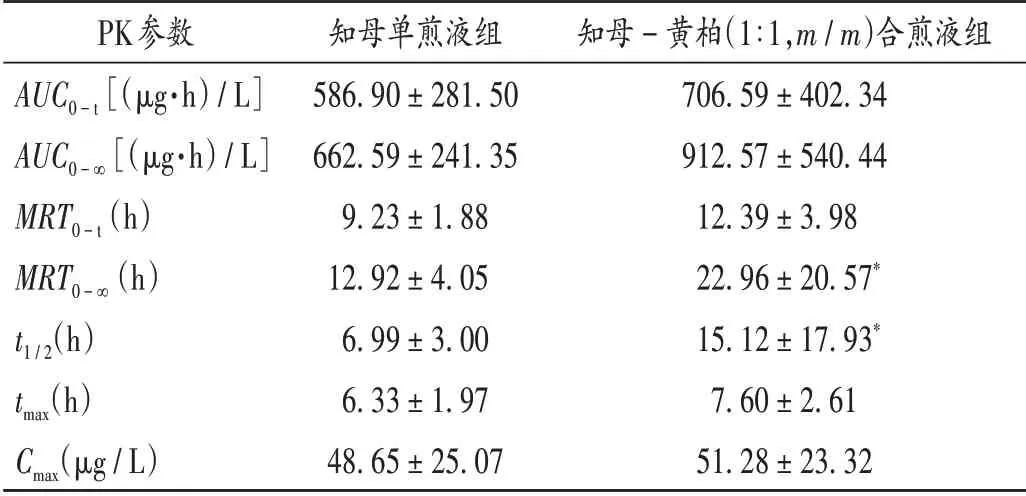
表4 TA-Ⅲ的PK参数(±s,n=6)Tab.4 PK parameters of TA-Ⅲ(±s,n=6)
注:与知母单煎液组比较,*P<0.01。Note:Compared with those in the Anemarrhenae Rhizoma decoction group,*P<0.01.
PK参数AUC0-t[(µg·h)/L]AUC0-∞[(µg·h)/L]MRT0-t(h)MRT0-∞(h)t1/2(h)tmax(h)Cmax(µg/L)知母单煎液组586.90±281.50 662.59±241.35 9.23±1.88 12.92±4.05 6.99±3.00 6.33±1.97 48.65±25.07知母-黄柏(1∶1,m/m)合煎液组706.59±402.34 912.57±540.44 12.39±3.98 22.96±20.57*15.12±17.93*7.60±2.61 51.28±23.32
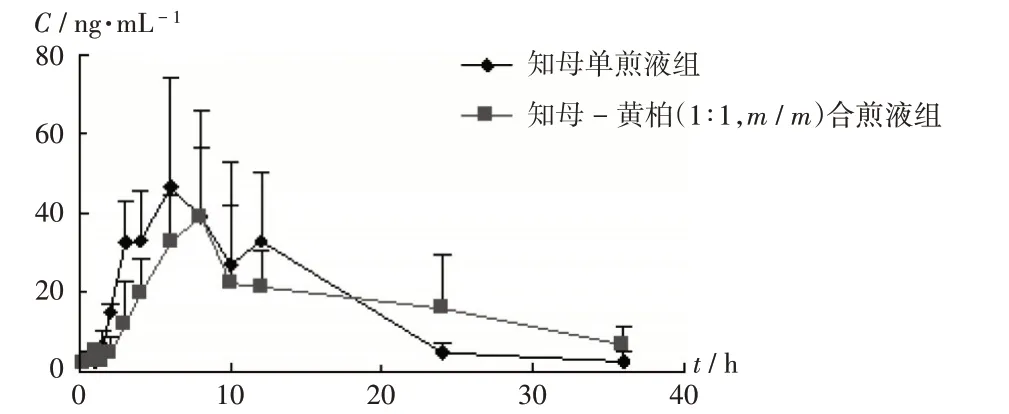
图2 TA-Ⅲ平均血药浓度-时间曲线(n=6)Fig.2 Mean drug concentration-time curves of TA-Ⅲ(n=6)
3 讨论
为进一步改善液相色谱的分离效能,参考文献[10-13],在水相中分别尝试了不同比例的甲酸和乙酸铵溶液,最终确定流动相为乙腈-2 mmol/L乙酸铵(55∶45,V/V)。结果色谱峰峰形良好,TA-Ⅲ和内标保留时间分别为3.15 min和1.55 min,分析周期仅4 min。在实验样品前处理中,仅需血浆样品50 µL,是文献[12]报道血浆用量的1/2。用血量的减少有利于实验动物在连续采血的PK研究中保持良好的生理状态,更加客观地反映药物的PK特征。TA-Ⅲ的定量下限为0.3 ng/mL,比文献[10]报道的更低,保留时间也缩短,可快速、准确、灵敏地完成TA-Ⅲ的测定。
在中药复方及临床应用中,知母-黄柏药对2味药材质量比多为1∶1(m/m),如知柏地黄丸、大补阴丸等。本研究中重点考察了知母-黄柏等量配伍后,知母有效成分TA-Ⅲ的体内PK特征,并与知母单独给药进行比较。结果知母单煎液组大鼠TA-Ⅲ的血药浓度低,药物吸收较慢,灌胃给药1 h后才检测到一定浓度的TA-Ⅲ。与知母单煎液组比较,知母-黄柏(1∶1,m/m)合煎液组TA-Ⅲ的血药浓度仍较低,但AUC增大,且MRT0-∞和t1/2均显著延长。提示知母等量配伍黄柏可促进TA-Ⅲ的吸收,提高药效。
综上所述,建立的方法操作简便、结果准确可靠,可用于测定大鼠体内TA-Ⅲ的血药浓度。知母-黄柏(1∶1,m/m)合煎液促进了TA-Ⅲ的吸收,可延长其MRT0-∞和t1/2。

