不同再矿化处理对漂白后釉质表面形貌及钙磷比的影响
王婧婵,李艳萍,何丽娜,牛玉梅
牙齿漂白作为一种减轻牙齿变色的保守方法[1],已经为患者带来了许多美学益处[2]。然而,漂白剂是否会影响釉质的表面性能现有的研究仍然存在争议[3-5]。尽管过氧化物不会引起牙釉质表面宏观结构的改变[6],但多数研究发现高浓度的过氧化物会导致釉质微观结构的改变[7-9],例如釉质粗糙度增加、显微硬度降低、表面形态改变以及钙磷含量降低。虽然造成这些不利影响的原因国内外学者报道不尽相同[10-11],但过氧化物漂白的风险不容忽视。研究表明,漂白后使用再矿化剂可以修复这种微观结构的改变[12]。
原花青素(procyanidins,PC)是一种天然的植物代谢物,因其良好的抗氧化、抗炎、抗菌、抗凋亡和抗癌性能备受关注。一些水果中存在的PC可以防止活性氧造成的伤害,抑制糖基转移酶和变形链球菌产生的酸。以往的研究表明,PC能够中和残留于牙面的氧以及氧自由基,促进漂白后牙体与复合树脂的即刻粘接,并且其对牙体硬组织的生物调节具有强效作用,可用作胶原蛋白交联剂,提高胶原强度,增强胶原耐酶解能力[13]。酪蛋白磷酸肽-无定形磷酸钙(casein phosphopeptide-amorphous calcium phosphate,CPP-ACP)从牛奶中提取出来,可以作为钙和磷酸盐的储存库,与主要使病变浅表区域再矿化的氟化物不同,CPP-ACP由于其分子尺寸较小,可以使病变的更深区域再矿化[14]。但目前关于其对漂白后釉质再矿化的作用鲜见报道,因此本实验通过观察PC及CPP-ACP对漂白后釉质再矿化能力以及颜色的影响,为漂白后釉质脱矿的防治提供新的思路和实验依据。
1 材料与方法
1.1 实验材料
1.1.1 仪器 低速切割机SYJ-150(中国沈阳科晶公司);色差仪ZE6000(日本电色);原子力显微镜(美国 Bruker DIMENSION ICON 公司);扫描电镜SU8010(日本日立公司);Element型氮化硅(Si3N4)超薄窗口电制冷能谱仪(美国EDAX公司)。
1.1.2 试剂 40% HP Opalescence Boost 皓齿诊室美白剂(Ultradent 公司,美国);原花青素(纯度>95%,合肥博美生物科技有限公司);CPP-ACP(日本 GC 株式会社);人工唾液:(ISO/TR10271标准)NaCl 0.4 g、KCl 0.4 g、CaCl20.795 g、NaH2PO4·2H2O 0.78 g、Na2S·2H2O 0.005 g、尿素1.0 g,蒸馏水稀释至1 000 mL,pH值为6.8(东莞市信恒科技有限公司)。
1.2 实验方法
1.2.1 牛切牙的处理 2021年6月10日在黑河市爱辉区养牛场购买60颗同一品种牛新鲜的离体切牙,彻底清除残留物,用低速切割机将冠根分离,去除冠髓,去离子水冲净,再用超声清洗30 min,选取大小均一、无裂痕的牙冠,使用前将牙冠保存在4 ℃生理盐水中。
1.2.2 釉质块的制备 牛切牙自然晾干,石膏包埋后,用低速切割机切成8 mm×8 mm小块,共获得符合实验要求的样本77个。丙烯酸树脂包埋,在流水下依次用500、1 000、2 000目碳化硅砂纸打磨抛光(磨除约100 μm),涂布抗酸指甲油,暴露5 mm×5 mm的釉质开窗区。随机选取11个样本作为漂白前对照组。
1.2.3 实验分组及处理 剩余66个样本使用皓齿诊室美白剂进行漂白,在釉质表面均匀涂抹一层美白剂,20 min后去除凝胶,重复2次,彻底冲洗吹干试件表面。随机选取11个样本作为漂白后对照组。其余55个样本随机分为5组(n=11):去离子水(deionized water,DW)组(阴性对照组);2%NaF组(阳性对照组);10%PC组;CPP-ACP组;PC+CPP-ACP组。分别在DW、2%NaF、10%PC、CPP-ACP、10%PC+CPP-ACP溶液中浸泡10 min,自然晾干5 min,去离子水冲洗1 min,3次/d,分别为每天的7:00、12:00和17:00,共1周。其余时间将样本置于人工唾液中,人工唾液需要每日更换。
1.2.4 色差仪检测 牙齿颜色测定采用ZE6000色差仪,光源为D65光源。以CIE-LAB颜色系统记录牙齿颜色的L、a、b值,然后按照公式ΔE*=[(ΔL*)2+(Δa*)2+(Δb*)2]1/2分别计算各组漂白后即刻、再矿化后与漂白前釉质表面的色差值ΔE1和ΔE2。
1.2.5 原子力显微镜分析 每组选取5个样本,每个样本选取3个位点,用原子力显微镜进行检测,使用数据处理软件NanoScope Analysis分析釉质表面形貌及粗糙度。以纳米为单位测量平均粗糙度(average roughness,Ra)和均方根粗糙度(root mean square roughness,Rq)两个参数。Ra、Rq从不同方面反映样本表面的综合状态。
1.2.6 扫描电镜及能谱分析 每组选取6个样本,梯度脱水后放在干燥器内干燥,然后在牙釉质表面真空沉积一层微米级的铂金薄膜,在每个样本观察界面上随机选取3个位点,用扫描电镜观察表面超微结构,再用能谱仪进行元素成分及含量分析。
1.3 统计学分析
采用SPSS 25.0统计软件进行数据分析,数值采用均值±标准差表示,采用单因素方差分析比较不同组间粗糙度、钙磷比值及颜色的差异,若总体比较有差异,则采用Bonferroni法进行两两比较,统计学分析检验水平定为0.05。
2 结 果
2.1 色差仪检测牙齿颜色改变
各组ΔE>8,漂白效果明显。各组ΔE值漂白后升高,再矿化处理后略有降低,降低值(ΔE1,ΔE2)为1.34~1.89,各组ΔE1、ΔE2间均无统计学意义(P>0.05)(表1)。
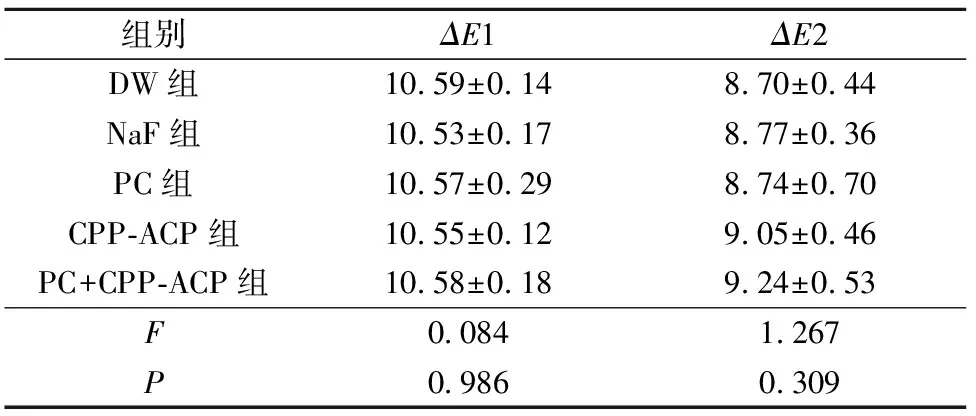
表1 不同再矿化处理各组间ΔE变化
2.2 扫描电镜观察表面超微结构
漂白前釉质表面形态(图1A):镜下可见其表面光滑平坦,结构均匀致密,磨痕不明显。漂白后即刻釉质表面形态(图1B):镜下可见表面因脱矿形成较大凹坑,并有散在孔隙。DW组釉质表面形态(图1C):与漂白后即刻相似,可见有大量孔隙,无沉积层。NaF组釉质表面形态(图1D):镜下可见釉质表面有排列整齐而致密的晶体沉积。PC组釉质表面形态(图1E):镜下可见排列紧密不均匀的晶体沉积。CPP-ACP组釉质表面形态(图1F):镜下可见大小不一的晶体沉积,有散在孔隙。PC+CPP-ACP组釉质表面形态(图1G):镜下可见排列均匀而致密的晶体沉积。
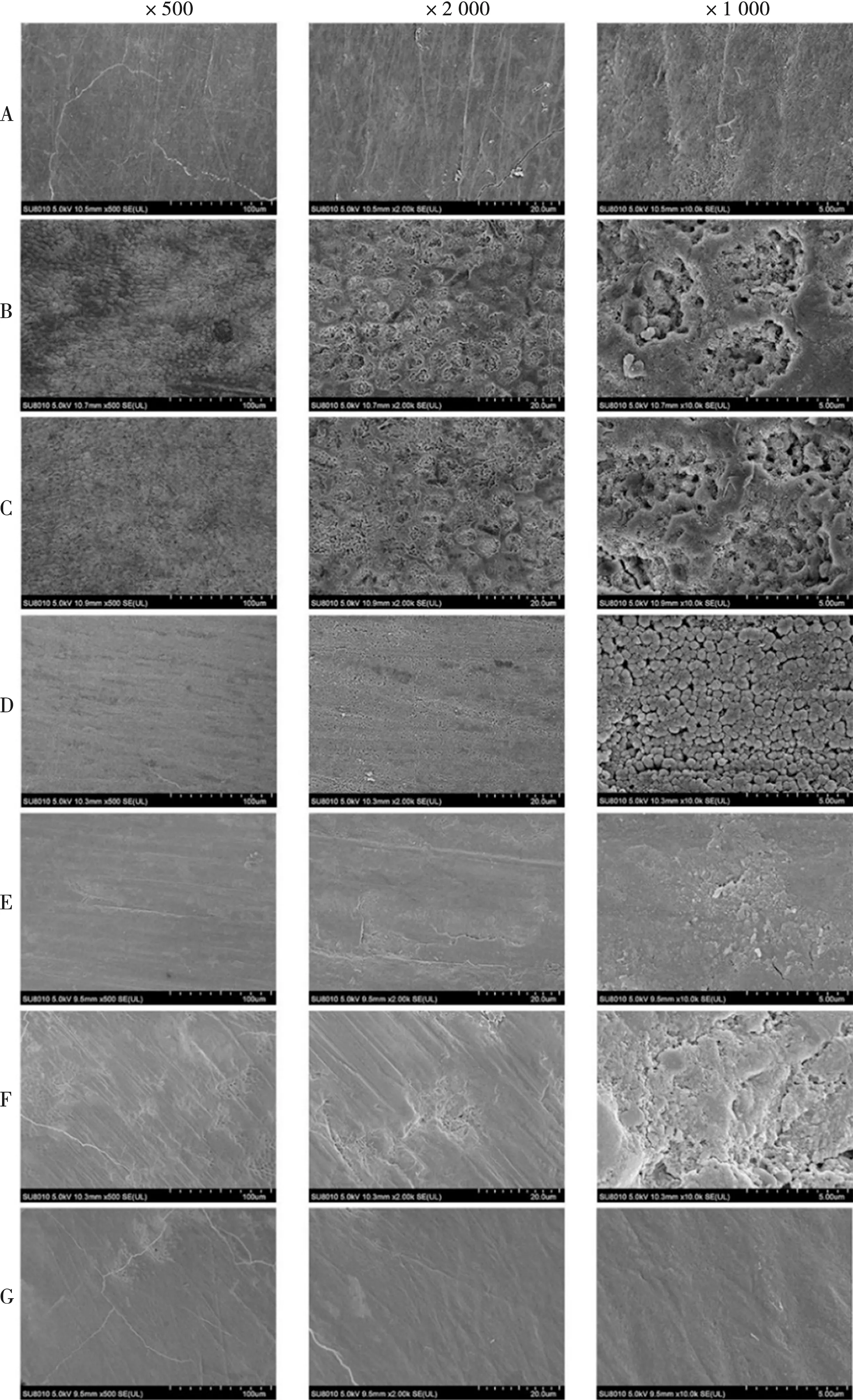
A:漂白前;B:漂白后即刻;C:DW组;D:NaF组;E:PC组;F:CPP-ACP组;G:PC+CPP-ACP组
2.3 能谱分析
X-射线能谱仪分析元素成分显示,NaF组主要含有 Ca、P、C、O、F 元素,其余各组主要含有 Ca、P、C、O 元素,而未观察到F元素沉积(图2)。
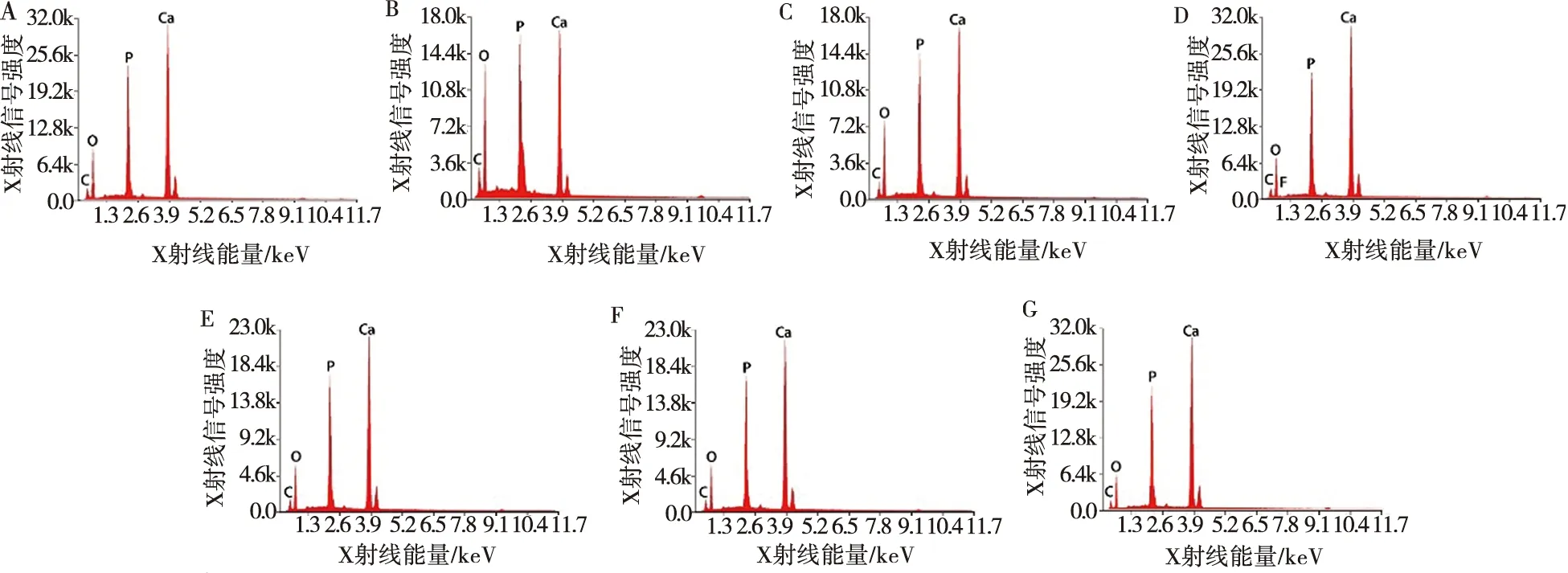
A:漂白前;B:漂白后即刻;C:DW组;D:NaF组;E:PC组;F:CPP-ACP组;G:PC+CPP-ACP组
由表2定量分析元素含量比值可知,漂白后釉质表面钙磷质量比、物质的量比均显著降低(P<0.005),再矿化后NaF、PC、CPP-ACP和PC+CPP-ACP组均有不同程度的升高(P<0.005),DW组无明显变化(P>0.005),两两比较显示从低到高的牙釉质表面钙磷比是:漂白后即刻、DW、CPP-ACP、PC、漂白前、PC+CPP-ACP和NaF组。其中,PC和CPP-ACP组钙磷比值均低于NaF组(P<0.005),而PC+CPP-ACP组与NaF组钙磷比相似,差异无统计学意义(P>0.005)。

表2 釉质表面钙磷比值
2.4 原子力显微镜检测结果
2.4.1 表面形貌 漂白前组(图3A)釉质表面平整,颗粒之间排列致密而有序,三维重建图黄色部分凸起均匀;漂白后即刻组(图3B)釉质表面粗糙不平,颗粒间隔较大,三维重建图凸起不均匀,高低起伏差距大,可见明显的凹陷状小坑;DW组(图3C)表面形态和三维重建图与漂白后即刻组相似,未见明显沉积物;NaF组(图3D)釉质表面有球状沉积物,分布较为均匀,三维重建图部分区域可见裂隙,凹陷小而浅;PC组(图3E)釉质表面有较疏松的颗粒状沉积物,三维重建图部分区域可见小而浅的凹陷;CPP-ACP组(图3F)釉质表面较为粗糙,但仍较DW组较为平整,有散在的颗粒状沉积物,三维重建图部分区域可见少量坑状和尖锐突起结构;PC+CPP-ACP组(图3G)釉质表面较为平整,但仍比漂白前组略粗糙,有均匀、致密的颗粒状沉积物,三维重建图黄色部分凸起较为均匀。

A:漂白前;B:漂白后即刻;C:DW组;D:NaF组;E:PC组;F:CPP-ACP组;G:PC+CPP-ACP组
2.4.2 粗糙度 对各组样本的表面粗糙度进行统计学分析(表3),漂白后Rq、Ra均显著升高(P<0.001),经不同处理后各组均有不同程度的降低(P<0.001),两两比较显示从高到低的釉质表面粗糙度是漂白后即刻、DW、NaF、CPP-ACP、PC、PC+CPP-ACP和漂白前组。其中,PC+CPP-ACP组粗糙度值最接近漂白前,明显小于NaF、PC和CPP-ACP组(P<0.001)。

表3 釉质表面粗糙度
3 讨 论
天然产品用于医药已有数千年历史,资源丰富并且安全性较好,在预防和治疗牙齿脱矿中有着广阔前景。PC作为天然抗氧化剂和自由基清除剂,已被证明在各种临床应用中以及作为膳食补充剂是安全的。现代药理研究显示[17],PC可以通过诱导胶原交联和降低生物降解率增加胶原蛋白的稳定性,进而促进牙本质再矿化。CPP-ACP易溶于唾液,能够显著提高唾液中钙及磷酸根离子水平,有助于再矿化。此外,CPP-ACP分子有亲水和疏水区域,可以掩盖细菌表面的疏水蛋白,从而阻止细菌黏附牙齿表面[18]。
由于牙釉质的矿物质是基于钙和磷酸盐形成的,当与这些离子相关的不饱和溶液接触时,可能会发生羟基磷灰石溶解。反之,当与过饱和溶液接触时,会发生矿物沉淀或再矿化。唾液中存在钙、磷等矿物离子,在一定程度上可修复脱矿釉质,封闭微小孔隙,但这一再矿化进程非常缓慢且作用轻微。因此,本实验去离子水处理后各项指标都无明显变化。
Poorni等[19]发现牙釉质钙磷比可以反映釉质表面钙磷得失,进而判定其再矿化程度。本实验能谱分析结果发现,NaF、PC、CPP-ACP和PC+CPP-ACP组的钙磷比值均有不同程度的恢复,这表明它们都能促进漂白后的釉质再矿化,并且可以发现与漂白前相比新形成的沉积物的主要元素种类没有发生改变,这表明在釉质表面有新的晶体生成,具体成分仍需进一步探索,推测可能是磷酸盐、碳酸盐或有机酸钙的其他螯合物等。虽然PC、CPP-ACP对恢复钙磷比值的作用不及NaF的效果显著,但二者联合应用的效果与其接近。
扫描电镜和原子力显微镜实验结果表明,再矿化处理后各组釉质表面均有程度不一的矿物质沉积,正如预期那样,PC与CPP-ACP联合应用的沉淀物最为致密。推测其原因可能是,CPP-ACP能维持溶液中钙、磷离子的过饱和状态,保证矿化所需的离子渗透梯度[20-21],PC能清除漂白剂残留的活性氧,并且其携带的大量酚羟基首先与溶液中的钙离子结合形成含钙络合物,然后与釉原蛋白中的氨基发生反应,通过这两个过程络合物中的钙离子转移到了釉原蛋白中,使得游离的钙离子聚集到釉原蛋白中[22],从而增强了釉质再矿化。因此,二者联用能发挥更大的再矿化优势,但具体作用机制有待进一步研究。
综上所述,漂白后使用PC和CPP-ACP均有良好的再矿化效果,且联合应用的效果优于单独应用。虽然天然药物的具体有效成分目前仍不十分明确,但其不良反应较小且资源丰富,有进一步研发利用的价值。
利益冲突:作者声明没有竞争利益。

