S-scheme ZnO/MoS2异质结构筑与对盐酸四环素降解性能
胡怀生, 张鹏会
(陇东学院 化学化工学院, 甘肃 庆阳 745000)
近年来,随着新冠疫情的出现,人们越来越重视抗生素制药废水对环境的污染问题.抗生素废水作为一种独特的化学合成类废水,具有难降解、COD高等特点[1-2],同时在生产抗生素类药品时,其前驱体、中间体等物质均会随着生产的过程进入排放的水体中,严重危害生态平衡和人类健康,抗生素的不断积累对人体健康和生态环境的危害越来越大[3].
抗生素的常见去除方法包括物理、化学和生物方法,光催化技术相比于其他方法而言,降解效果更佳,污染物去除彻底且成本较低,可有效去除水体中的有机污染物[4-8].ZnO是N型半导体材料,由于其具有稳定性能好,无毒,价格低廉,在紫外光照射下能降解有机污染物等优点,在光催化应用中已被广泛关注[9-11].但ZnO仅对紫外光具有响应,可见光条件下不易激发,限制了其应用,因此,可通过掺杂其他类型催化剂来提高ZnO的催化活性[12-18].MoS2分子具有夹层结构,Mo处于两个硫原子中间[19],由于MoS2表面积大,表面共价力和强边缘效应,MoS2在污染物吸附,电化学性能和催化降解中的研究均受到广泛关注[20-25].然而,MoS2纳米片具有相对低的分散性并且易于聚集,从而影响光催化效率.而S-scheme异质结主要由功函数较小、费米能级较高的还原型半导体光催化剂(RP)和功函数较大、费米能级较低的氧化型半导体光催化剂(OP)通过错开型方式构建而成,可以有效实现强氧化还原能力的电子空穴对分离[26],从而有效提高光催化效率,实现抗生素污染物的高效降解.
本研究通过制备一种具有高催化活性的S-scheme ZnO/MoS2复合光催化剂,研究其对水体中盐酸四环素(tetracycline hydrochloride,TC)类抗生素污染物的降解性能.通过调控盐酸四环素浓度、催化剂投入量、光照条件等因素,研究ZnO/MoS2对TC的降解性能,实现低能耗、高效降解污染物.
1 材料与方法
1.1 实验材料
实验所用试剂除特殊标注外,均为分析纯,C6H12O6·H2O、Zn(CH3COO)2·2H2O、CO(NH2)2、Na2MoO4·2H2O(98%)、乙二醇(>99%, GC)与盐酸四环素均购买于上海阿拉丁生化科技股份有限公司,无水乙醇与硫脲分别购买于天津市永达化学试剂有限公司与上海展云化工有限公司,抗生素废水为实验室模拟废水.
1.2 光催化剂的制备方法
1) 中空多孔ZnO微球的制备.使用葡萄糖和乙酸锌作为碳源和锌源,通过简便的溶剂热法制备ZnO微球.将50 mmol葡萄糖一水合物(C6H12O6·H2O),25 mmol乙酸锌二水合物(Zn(CH3COO)2·2H2O)与50 mmol尿素(CO(NH2)2)溶解在120 mL蒸馏水中剧烈搅拌直至溶液变为透明.将以上溶液转移至100 mL聚四氟乙烯内衬的不锈钢高压釜中,并在160 ℃的室内烘箱中加热16 h.将反应物冷却至室温后,过滤黑色沉淀物后用蒸馏水和无水乙醇分别洗涤3次.之后,将洗涤后的沉淀物在真空烘箱中于70 ℃干燥12 h.最后,在空气氛围中,以2 ℃·min-1的升温速率,将产物分别在600、900 ℃下煅烧3 h,以获得ZnO催化剂.
2) ZnO/MoS2复合物通过水热合成法制备,制备流程如图1所示,取3个烧杯,分别标记为1∶1、1∶2、1∶3.依次向其中分别加入50 mL乙二醇之后,将1 mmol钼酸钠和5 mmol硫脲混合溶于乙二醇中.分别加入0.3、0.15、0.1 g的ZnO,将其放置于超声清洗机内超声30 min.超声结束后,将混合溶液分别转移至3个100 mL的反应釜中,在室内烘箱中于210 ℃加热24 h.等反应釜温度下降到室温后,取出混合溶液,装入离心管内以8 000 r·min-1离心5 min,用去离子水和无水乙醇分别清洗3次,置于真空干燥箱中,70 ℃干燥8 h,制得1∶1、1∶2、1∶3 比例的ZnO/MoS2复合材料.

图1 催化材料制备Fig.1 Preparation of catalytic materials
1.3 样品表征
采用Evolution 220紫外可见漫反射光谱仪测定1∶1、1∶2、1∶3的ZnO/MoS2催化材料的紫外可见漫反射光谱(UV-Vis DRS),在200~800 nm扫描,分析催化材料的光吸收性能.采用Inspect F50扫描电子显微镜观察ZnO与ZnO/MoS2的形貌结构.
1.4 四环素降解性能测试
在自然光下,取50 mL质量浓度为50 mg·L-1的盐酸四环素溶液置于烧杯中,将50 mg不同复合比的ZnO/MoS2粉末分别置于不同烧杯中,做好相应标记.将烧杯放于黑暗环境下静置30 min,完成暗吸附.吸附前,取3 mL溶液置于离心管中标记为0 min,开始曝气,反应的第一个小时每隔10 min取一个样品分别标记为10、20、30、40、50、60 min,后一个小时每隔15 min取一个样品,分别标记为75、90、105、120 min,采用UV-1901双光束紫外分光光度计测定溶液吸光度.根据采用该仪器测定的标准曲线公式y=0.030 5x+0.0057(其中,x表示TC浓度,y表示吸光度),计算TC浓度,并计算降解率(C0-Ct)/C0,其中,C0为溶液初始浓度,Ct为t时刻溶液浓度.
2 结果与讨论
2.1 紫外可见漫反射吸收光谱表征
对不同比例的ZnO/MoS2光催化剂进行紫外可见漫反射光谱扫描,比较ZnO、1∶1、1∶2、1∶3的ZnO/MoS2的光吸收特性,结果如图2所示.由图可见,单一ZnO仅在紫外光区有响应,ZnO/MoS2复合材料在可见光区均有响应,其中,1∶1复合比的ZnO/MoS2复合材料具有更好的可见光吸收性能,表明1∶1复合比的ZnO/MoS2较1∶2、1∶3的ZnO/MoS2有更好的可见光吸收性能,更有利于光电催化反应的进行.
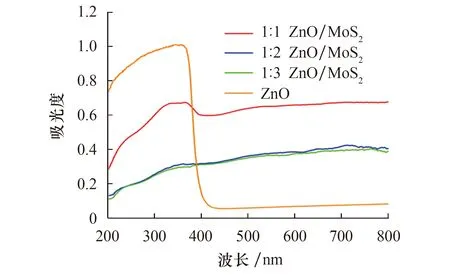
图2 紫外可见漫反射光谱Fig.2 UV-visible diffuse reflectance spectroscopy
2.2 扫描电镜(SEM)分析
通过扫描电子显微镜观察所制样品的形貌,ZnO的形貌如图3a所示,可以观察到ZnO较分散,呈小球状.ZnO/MoS2(1∶1)复合催化材料表面如图3b所示,由图可见,其附着的颗粒较小,ZnO被MoS2覆盖,均匀分散于ZnO之上,复合材料较单一材料表面颗粒小,具有更大的比表面积,可增加催化反应活性位点,有利于催化反应的进行.

图3 ZnO和1∶1 ZnO/MoS2复合材料SEM图像Fig.3 SEM image of ZnO and 1∶1 ZnO/MoS2 composite
2.3 不同比例ZnO/MoS2对盐酸四环素的降解性能
将相同质量的不同复合比催化剂(1∶1,1∶2,1∶3)分别置于3个烧杯中,于0、10、20、30、40、50、60、75、90、105、120 min分别取5 mL盐酸四环素溶液,在波长357 nm处测定盐酸四环素溶液的吸光度,并带入标准曲线,计算盐酸四环素溶液浓度,计算去除率.结果如图4所示.由图可见,随着降解时间的延长,不同比例催化材料对盐酸四环素溶液的降解效率都呈现不断上升趋势,1∶2 的ZnO/MoS2催化材料对盐酸四环素溶液的降解效率为12%,1∶3的ZnO/MoS2催化材料对盐酸四环素溶液的降解效率只达到10%,降解效果并不是十分理想,且含量越多,降解效率越低,这可能是由于随着MoS2含量的增加,将ZnO完全覆盖,影响了异质结的形成,与溶液接触的催化剂仅为MoS2;而1∶1复合比的ZnO/MoS2催化材料在50 min内快速提升,随着时间增加降解效率也在显著提高,100 min时,降解效率高达88%.由此可以得出在自然光条件下,比例为1∶1的ZnO/MoS2催化材料对盐酸四环素溶液的降解效率更好,与紫外可见漫反射吸收光谱结果相对应,根据紫外可见漫反射吸收光谱可知,1∶1的ZnO/MoS2较其他比例复合催化剂具有更大的可见光吸收范围,吸光度更好,有利于催化反应的进行.
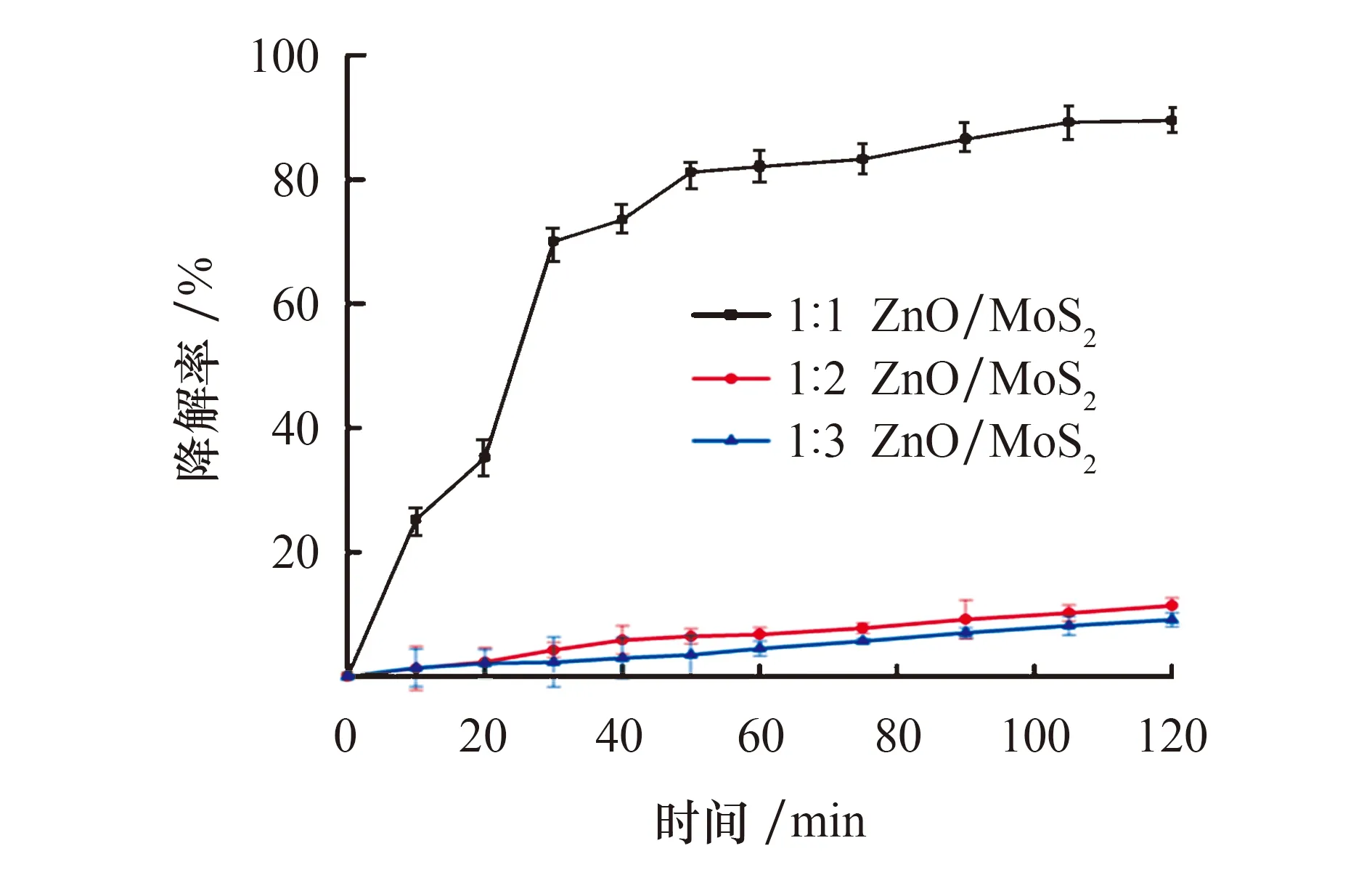
图4 自然光条件下50 mg不同比例ZnO/MoS2对盐酸四环素溶液的降解效率Fig.4 Degradation efficiency of 50 mg ZnO/MoS2 in different proportions for TC under natural light conditions
2.4 ZnO/MoS2 (1∶1)在不同光照条件下的抗生素降解性能
图5为不同光照条件下1∶1 ZnO/MoS2对盐酸四环素溶液的降解效率随时间变化曲线,由图可知,不论在黑暗条件还是氙灯照射条件下,1∶1的ZnO/MoS2对于盐酸四环素溶液的降解效率都在不断增加.在氙灯条件下,降解效率在0~40 min迅速升高,40 min之后便缓慢提升,降解效率在120 min时到达77%.在黑暗条件下,降解效率在0~45 min迅速升高,45 min后缓慢提升,降解效率在120 min时到达73%.整个降解过程中,处于氙灯条件下,1∶1的ZnO/MoS2催化材料对盐酸四环素溶液的降解效率都比黑暗条件下更好,在盐酸四环素废水实际处理过程中,也可以考虑在太阳光状态下进行降解.而无光照时降解效果并未显著降低,这是由于ZnO与MoS2均具有压电性能,在废水净化过程中存在的水流动与曝气震动会产生机械能,可激发催化的电子与空穴分离,因此,在无外加光照时,催化剂仍具有较好的污染物降解性能.

图5 不同光照条件1∶1 ZnO/MoS2对盐酸四环素溶液的降解效率随时间变化Fig.5 Degradation efficiency of 1∶1 ZnO/MoS2 for TC with time under different light conditions
2.5 ZnO-MoS2(1∶1)对不同TC溶液浓度的影响
分别配制40、50、60 mg·L-1的盐酸四环素溶液待用.在黑暗条件下,分别取50 mL上述TC溶液置于3个烧杯中,做好相应标记.再分别取50 mg 1∶1的 ZnO/MoS2粉末倒入烧杯中,考察不同TC溶液浓度对抗生素降解性能的影响,如图6所示,由图可知,在氙灯条件下,1∶1的ZnO/MoS2对浓度60 mg·L-1的TC溶液降解效果最好.0~30 min时,同种催化材料对不同浓度TC溶液的降解效果都在迅速升高,这是由于催化剂具有较好的吸附性能,先将污染物吸附至催化剂表面,因而前30 min污染物去除性能最优,而后降解率缓慢提高,这是由于吸附后的污染物被催化剂逐渐降解.30 min时,1∶1的ZnO/MoS2催化材料对60 mg·L-1的TC溶液降解效果尤为显著,105 min时,降解效率达88%.因此,1∶1 的ZnO/MoS2催化材料对质量浓度为60 mg·L-1的TC溶液呈现出较好的降解效果.
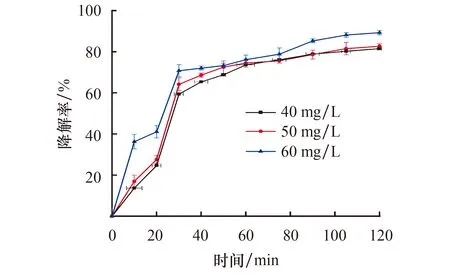
图6 1∶1 ZnO/MoS2对不同浓度盐酸四环素溶液降解效率随时间变化Fig.6 Degradation efficiency of 1∶1 ZnO/MoS2 for TC of different concentrations with time
2.6 催化机理分析

图7 捕获剂实验Fig.7 Experiment of capture agent

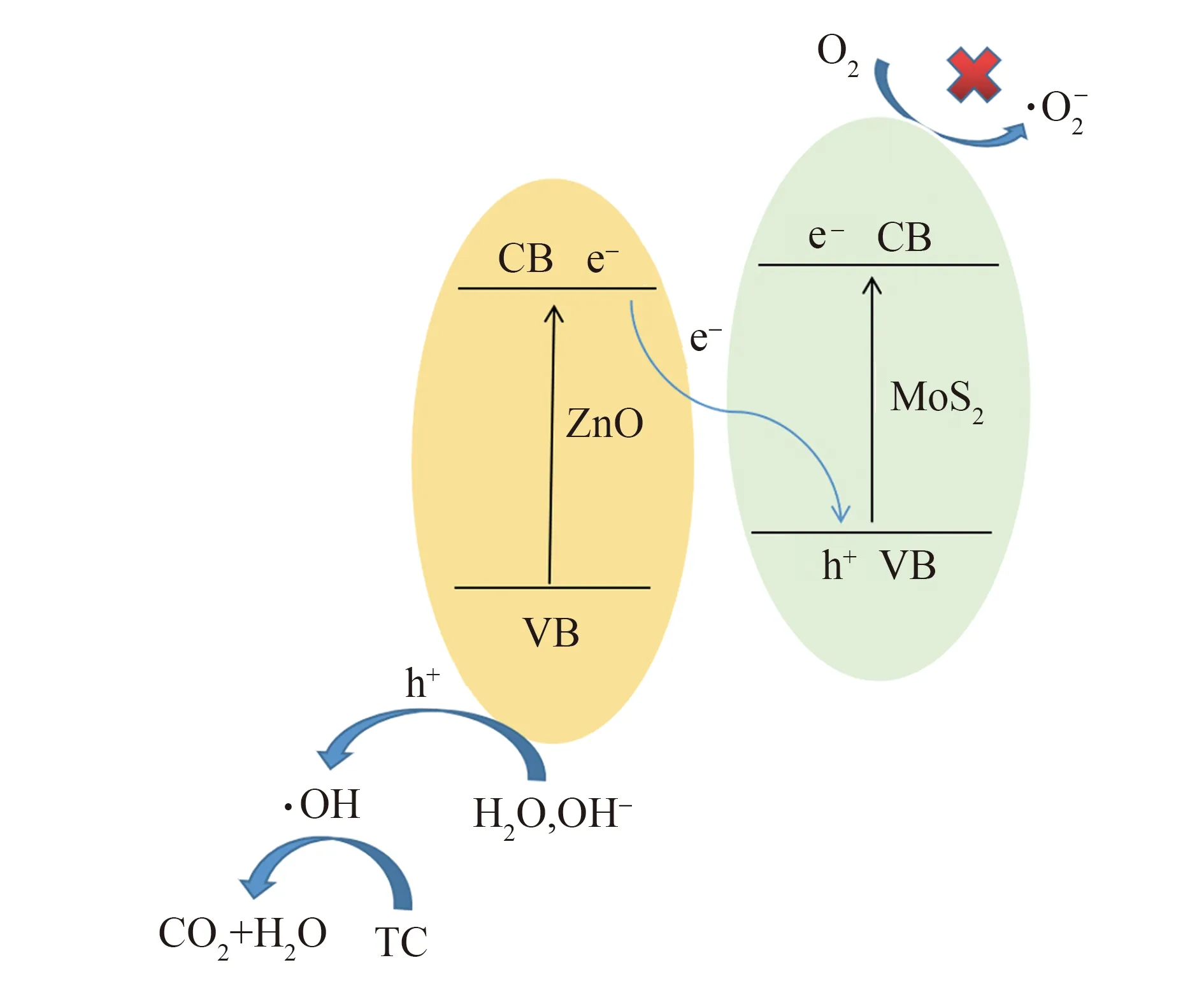
图8 抗生素降解机理分析Fig.8 Analysis of antibiotic degradation mechanism
3 结论
采取一种绿色经济、低成本、可持续发展的光催化材料去除废水中的抗生素.通过改变ZnO与MoS2的复合比例、光照条件、废水浓度、催化材料加入量等条件,得出催化剂最佳复合比例以及盐酸四环素降解的最优条件.研究结果表明:
1) 1∶1 的ZnO/MoS2催化材料对降解TC具有更好的效果,在氙灯下可达77%,而在黑暗下可达到73%.1∶1 的ZnO/MoS2催化材料加入量为50 mg时,对质量浓度为60 mg·L-1的TC溶液降解效果最佳,可达88%.
2) 复合催化剂ZnO/MoS2中,ZnO与MoS2形成内建电场,电子由ZnO导带迁移至MoS2价带,形成S-scheme异质结,ZnO价带h+被有效保留,h+将H2O或OH-氧化成·OH,体系中h+、·OH共同将TC转变为小分子H2O或CO2.

