炼钢粉尘中锌分离和回收的研究进展
蒋刘东, 李萍萍, 杜传明, 于景坤
(1.东北大学 冶金学院, 辽宁 沈阳 110819;2.北京首钢股份有限公司, 河北 唐山 063009)
锌是一种重要的有色金属,被广泛应用于钢铁、机械、电气、化工等领域,其中全球约50%的金属锌用于镀锌,主要是钢材和钢结构件的表面镀层[1-3]。随着经济的快速发展,全球对金属锌的需求不断增加,锌整体处于供不应求的状态。 目前,锌主要来自于硫化锌矿的冶炼,生产工艺主要包括焙烧、酸浸、净化和电沉积等流程。 据统计,按目前锌的消费量,现有锌矿储量不足以支撑未来的发展需求[4]。 另外,国内可用于工业冶炼的锌矿资源较少,锌矿资源主要依靠进口。 因此,从工业固废中回收二次锌资源是解决我国锌短缺的重要途径。 由于废钢返回钢铁企业再利用,大量被用于镀层的金属锌进入到钢铁冶金流程中。 金属锌熔点较低,在炼钢过程中容易挥发,导致大部分锌富集到炼钢粉尘中[5]。 因此,炼钢粉尘被视为一种重要的二次锌资源。
1 炼钢粉尘成分及锌的存在形式
目前,我国的粗钢产量达到了10 亿t,炼钢粉尘的年产量已超过1 000 万t。 炼钢粉尘主要由铁氧化物组成,也含有丰富的锌、铅等金属元素[6-7]。 因铁含量较高,炼钢粉尘通常作为配料返回烧结工艺再利用,实现内部循环利用,但是粉尘中锌等有害元素也会进入高炉,并不断富集,导致高炉锌负荷超标,对生产顺利进行和高炉寿命造成危害[8-9]。 此外,由于炼钢粉尘中锌含量远不及传统炼锌原料,回收锌的价值有限,通常也无法作为原料直接供给炼锌企业使用[10-11]。 因此,大部分炼钢粉尘被直接堆弃或填埋,这不仅造成了资源的巨大浪费,也带来了严重的环境负担[12-14]。如何实现炼钢粉尘的资源化利用一直是钢铁企业亟待解决的重要课题之一。
我国炼钢粉尘中铁含量为15% ~50%,Zn 含量为3% ~15%,表1 为我国一些钢铁企业炼钢粉尘的化学成分,其中铁和锌含量差别较大,这与炼钢工艺和原料成分有关。 图1 为某钢厂炼钢粉尘的XRD 分析结果,主要物相有铁氧化物、含铁相、氧化锌(ZnO)和铁酸锌(ZnFe2O4),锌主要以ZnO 和ZnFe2O4的形式存在[15]。 若炼钢粉尘中的锌能被有效分离,回收的锌可替代锌矿用于金属锌的生产,而剩余的含铁矿物可作为原料返回冶金流程再利用。 因此,锌的分离是实现炼钢粉尘资源化利用的关键所在。
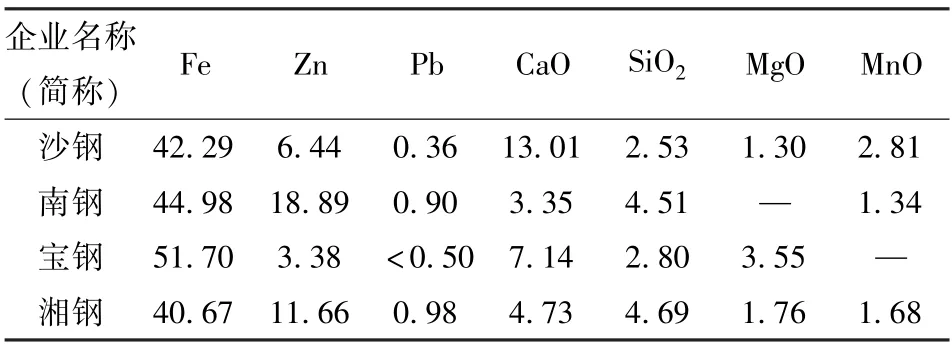
表1 国内钢厂炼钢粉尘的化学成分Table 1 Chemical composition of steelmaking dust in domestic plants wt%
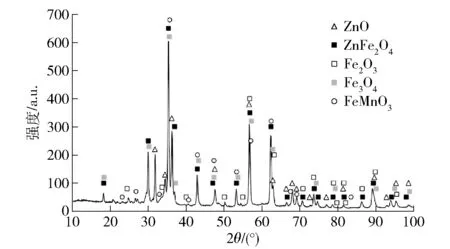
图1 某钢厂炼钢粉尘XRD 图Fig.1 XRD diagram of steelmaking dust in a steel plant
基于各物相物化性质的不同,科研工作者提出了多种方法来分离回收炼钢粉尘中的锌,主要分为火法工艺、湿法工艺和湿法火法联合工艺[16-20]。 本文对近些年来炼钢粉尘中锌分离的最新研究成果以及开发的工艺进行了系统总结和分析。
2 火法工艺
2.1 碳热还原法
关于炼钢粉尘的碳热还原工艺,国内外学者也进行了大量的基础性研究。 Omran 等[21]利用微波加热选择性还原电炉粉尘中的锌。 首先将电炉粉尘与石墨混合压制成球,然后在微波炉中加热20 min,发现锌的回收率随温度的升高而增加,在1 223 K 时锌的回收率达到94%,剩余粉尘主要由金属铁和铁酸钙组成。 炼钢粉尘中的ZnO 易被还原, 但ZnFe2O4结构稳定,难以被分解和还原,导致粉尘中锌和铁的分离不完全。 为了解决ZnFe2O4还原不彻底的难题,邬桂婷等[22]提出了强化ZnFe2O4选择性分解的新方法。 该方法是将ZnFe2O4在1 023 K 的还原性气氛(CO 浓度20%)下焙烧,使其分解为ZnO 和铁氧化物,然后在CO2气氛下将过还原的氧化亚铁转化为磁性的Fe3O4,以便于后续通过磁选分离铁和锌。 许继芳等[23]采用热力学软件分析了ZnFe2O4在CO 气氛下还原分解的热力学过程,发现控制CO/(CO+CO2)体积比在0.05 ~0.20,温度在873 ~973 K,可实现ZnFe2O4的高效分解,并抑制铁氧化物的过还原。 LYU 等[24]研究了添加CaO 对ZnFe2O4还原焙烧的影响,发现在未添加CaO 时需要较高的CO 浓度才能将ZnFe2O4中的锌彻底还原;添加CaO 后,发生反应(1),难还原的ZnFe2O4转变成铁酸钙和ZnO,只需较低的CO 浓度即可将锌还原,锌的还原率可达80% 以上。 Wu 等[25]研究了CO 作为还原剂时ZnFe2O4在不同温度下的还原行为,发现在723 ~1 123 K 时ZnFe2O4分解形成了含锌量较低的尖晶石,锌、铁氧化物在1 223 K 时完全还原为金属锌和铁。 Peng 等[26]提出了一种分解ZnFe2O4的新方法,是将CO 和氩气混合气作为还原剂,通过还原焙烧将ZnFe2O4分解为氧化锌和磁铁矿,在最优条件下,锌和铁的分解率分别为75.5%和25.0%。

碳热还原法是目前处理炼钢粉尘最常用的方法,其原理是在高温下利用碳或CO 还原粉尘中的金属氧化物,利用锌沸点低的特性,使还原的锌以蒸气形式挥发进入烟气回收系统,最后得到氧化锌或金属锌,从而实现与固相的有效分离。 在碳热近原法中,发展比较成熟的工艺有回转窑工艺和转底炉工艺[27]。
回转窑工艺是以碳作为还原剂和燃料,回转窑作为反应容器。 工业中应用范围最广的是Waelz 回转窑。 Waelz 工艺流程是先将炼钢粉尘与碳和熔剂充分混合,然后将混合料加入回转窑中进行加热,在1 373 ~1 573 K 进行碳热还原,锌等金属氧化物被碳还原,易挥发的锌、铅等金属进入烟气并发生氧化反应,生成的氧化锌通过冷却塔和电集尘器来进行收集,其工艺如图2 所示。 2016 年,马钢投产了一条处理能力为15 万t/a 的回转窑脱锌生产线,通过该生产线可得到ZnO 质量分数为42% ~65%的粗锌粉和ZnO 质量分数低于1%的富铁窑渣,经磁选分离后得到副产品铁精粉,选铁后的尾渣可返回水泥厂配料使用。 回转窑工艺具有操作简单、技术成熟等特点,但是生产中易发生结圈现象,不利于连续生产。 对于锌含量大于15%的炼钢粉尘,利用回转窑工艺可回收90%以上的锌,但对于锌含量较低的粉尘,锌和铁的回收率均不高[28]。
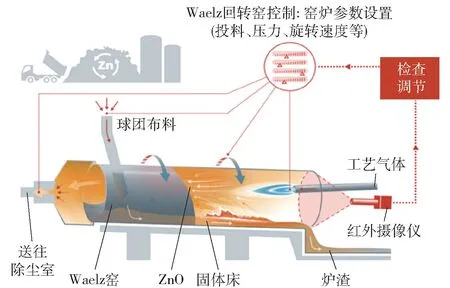
图2 Waelz 回转窑工艺示意图Fig.2 Schematic diagram of Waelz rotary kiln process
转底炉法的工艺流程如图3 所示。 该工艺是先将炼钢粉尘、煤粉与黏结剂混匀,并制成粒度均匀、强度好的球团,然后将生球均匀铺在转底炉炉底上,逆着转底炉转动方向加热至还原温度,球团中ZnO 和ZnFe2O4被碳还原,还原后的金属锌挥发进入烟气中,并被氧化成氧化锌,沉降后被回收[29]。 还原的金属球团从转底炉排出后,经冷却和筛分后,按锌、硫含量供料高炉或转炉等。 目前,国内很多钢铁企业已采用转底炉工艺来处理冶金尘泥,取得了良好的效果。2016 年,宝钢湛江钢铁建成了1 座产能20 万t/a 的转底炉,可生产成品金属球约14 万t,粗锌粉约1 万t,脱锌率大于85%,金属化率大于75%,实现含铁粉尘100%的回收利用[30]。 转底炉工艺虽然技术成熟,生产效率高,但需要较高的还原温度和大量的还原剂,能耗和一次性投资较大,而且产物基本为粗产品,需要进一步处理才能得到金属锌。
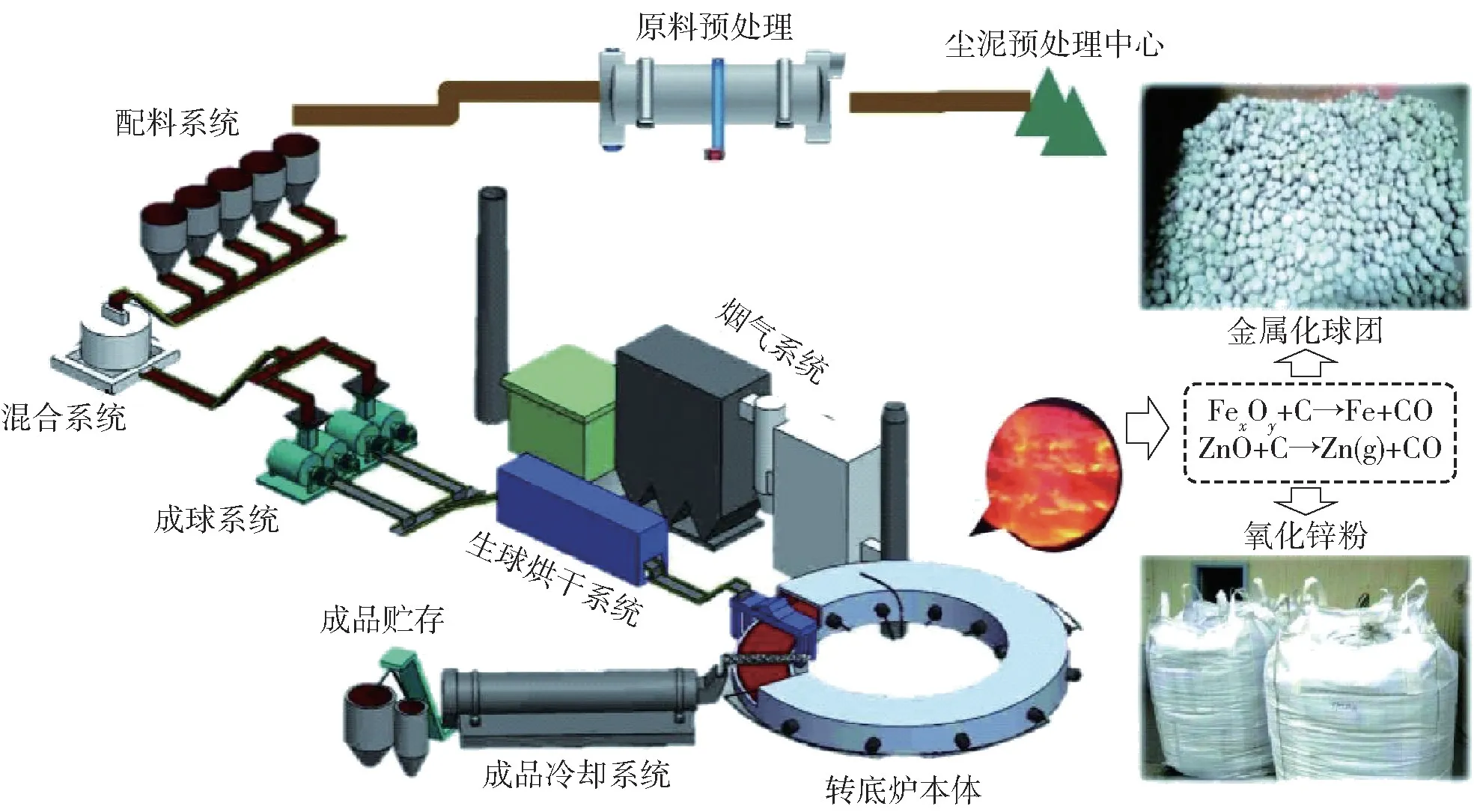
图3 转底炉工艺示意图Fig.3 Schematic diagram of rotary hearth furnace process
2.2 选择性氯化法
基于炼钢粉尘中各化合物组分在高温下与氯气反应能力的不同,Matsuura 等[31]提出了利用氯气选择性分离炼钢粉尘中锌的方法。 炼钢粉尘与氯气反应如式(2) ~(4)所示,在1 073 K 粉尘中的锌、铅能与氯气反应,分别形成ZnCl2和PbCl2,而Fe2O3难以被氯化。 氯化物沸点较低,在高温下容易挥发,可从固态粉尘中分离。 图4 为Fe-Zn-Pb-O-Cl 体系在1 073 K 时的化学势图,可知在高Cl2和O2分压下,锌和铅以氯化物形式存在,而铁以氧化物形式存在。因此,通过选择性氯化可实现炼钢粉尘中锌和铁的分离。

图4 Fe-Zn-Pb-O-Cl 体系在1 073 K 下的化学势图Fig.4 Chemical potential diagram of Fe-Zn-Pb-O-Cl system at 1 073 K

Matsuura 等[32]研究了Fe2O3-ZnFe2O4-ZnOPbO 混合物在Ar-Cl2-O2气氛中的氯化行为,发现在1 073 K 时,氯化速度随着Cl2分压的增加而增大,反应后粉尘中ZnO 和PbO 含量分别降至0.1%和0.03%,只有3%的铁氧化物被氯化,证明了选择性氯化法的可行性。 Sun 等[33]发现当温度从923 K 升高至1 073 K,锌和铅的氯化和分离速度增加,反应60 min 后,锌和铅的分离率分别为98%和99%,只有极少量的铁被氯化挥发。 选择性氯化后的粉尘主要由Fe2O3组成,可作为炼铁原料再利用,同时分离得到粗ZnCl2。 通过置换反应或蒸馏反应,可将粗ZnCl2中的其他氯化物(PbCl2、CdCl2等)去除,得到纯ZnCl2。 最后通过熔盐电解,纯ZnCl2被分解为高纯金属锌和氯气,氯气可返回氯化反应循环利用,工艺流程如图5 所示。 该工艺可直接回收金属锌,实现含锌炼钢粉尘的资源化利用[34-35]。

图5 选择性氯化工艺流程简图Fig.5 Selective chlorination process flow chart
综上所述,火法工艺具有生产效率高、处理能力强、原料来源广泛等优点,但普遍存在能耗高、污染严重、设备投资大等缺点。 碳热还原法需要消耗大量的碳,且反应不充分,未能实现能源的有效利用。选择性氯化法需要复杂的工艺和设备,而且产物还需要进一步提纯,导致处理成本较高。
3 湿法工艺
3.1 酸浸法
酸浸原理是通过酸液中H+离子与炼钢粉尘中ZnO 和ZnFe2O4的反应,使锌以离子的形式进入浸出液,然后净化去除浸出液中的杂质离子,再利用电解从浸出液中沉积金属锌。 炼钢粉尘中ZnO 能在稀酸溶液中溶解,而ZnFe2O4性质稳定,在常温下几乎不与稀硫酸或稀盐酸反应。 为了浸出分离锌,通常采用强酸浸出,在浓盐酸中,ZnFe2O4的溶解反应如式(5) ~(6)所示,大量的铁也会同时溶出[36]。
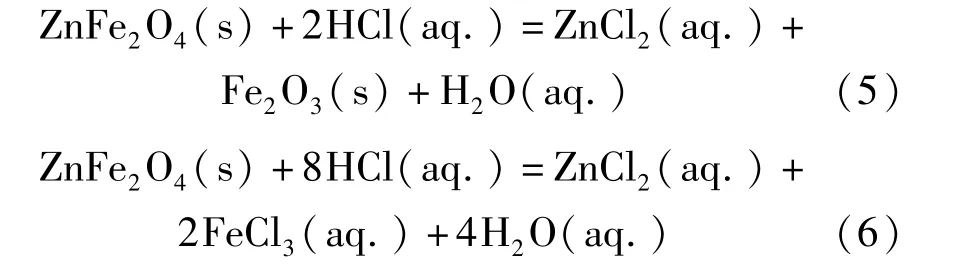
Baik 等[37]研究发现提高温度和盐酸浓度有利于电炉粉尘中锌的溶出,在363 K,浓度为1 ~2 mol/L 的盐酸溶液中锌的浸出率超过90%。 为了减少铁的溶出,采用了两段浸出法,首先用稀盐酸浸出ZnO,剩余难溶的ZnFe2O4再与高浓度热盐酸反应;浸出后,残渣中的铁以Fe2O3和FeOOH 形式存在;利用热酸浸出液再去溶解新粉尘中的ZnO,此时pH 值会升高至4.0 左右,浸出液中的铁离子发生水解反应并沉淀。 通入空气可以加快铁离子的水解过程,该法能实现锌和铁的分离。
当硫酸作为浸出剂时,炼钢粉尘中钙、铅等元素会形成难溶的硫酸盐沉淀,而锌、铁等元素能进入浸出液中,可实现锌和铅的分离。 Tsakiridi 等[38]在333 K 下利用3 mol/L H2SO4溶液浸出炼钢粉尘中80%的锌。 Kukurugya 等[39]在333 K、0.1 mol/L 稀H2SO4溶液中浸出炼钢粉尘,锌的溶出率可达65%,铁的溶出率仅为5%。 为了促进ZnFe2O4溶解,Kalpakl 等[40]提出了机械活化法浸出电炉粉尘,球磨转速为500 r/min 时在2 mol/L H2SO4溶液中锌和铁的溶出率分别为94%和31%。 浸出后,向浸出液中加入D2EHPA[二-(2-已基己基)磷酸]进行萃取提纯,然后向萃取液中加入草酸得到ZnC2O4沉淀,通过热分解得到高纯度的ZnO,锌的总回收率达到86%。与盐酸浸出相比,硫酸浸出速率更快,但尾渣中存在硫酸盐,若作为炼铁原料使用会增加硫含量,因此限制了尾渣的再利用。
3.2 碱浸法
ZnO 和PbO 为两性氧化物,不仅能溶于酸也能溶于碱,而Fe2O3是难溶于碱性溶液的。 因此,可利用碱液来选择性分离炼钢粉尘中的锌。 在NaOH 浸出过程中,粉尘中的锌和铅能够溶解,分别发生反应(7)、(8),而铁残留在尾渣中[41]。 添加Na2S 提纯浸出液后(反应式如式(9)所示),得到净化的Na2ZnO2溶液,再通过电解反应,制得金属锌和碱性溶液。 但是,炼钢粉尘中大部分的锌以ZnFe2O4的形式存在,ZnFe2O4在NaOH 溶液中的溶解率较低,导致锌回收率不高,而且碱浸净化回收工艺复杂,处理成本较高。 为了促进ZnFe2O4的溶解,通常需要与火法工艺相结合,这将在后面进行详述。
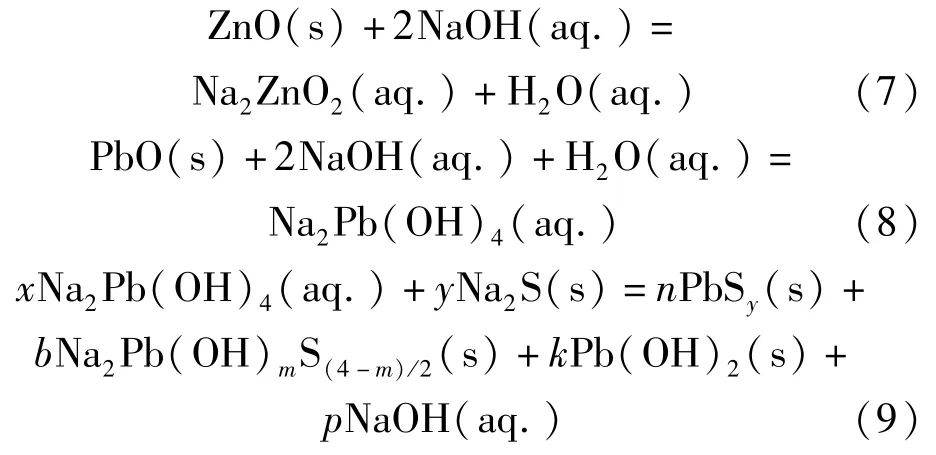
3.3 盐浸法
除了酸浸和碱浸外,铵盐浸出也被用于炼钢粉尘的处理。 Ezinex 法[42]是一种成熟且在工业上应用的铵盐浸出工艺,其原理为:铵根离子与ZnO 反应生成络合物(反应式(10))进入溶液,但不与铁氧化物反应。 工艺步骤包括浸出、渣分离、净化、电解。与酸浸和碱浸相比,铵盐浸出对锌的选择性更高,但对ZnFe2O4的浸出率不高。 Rodriguez 等[43]提出了一种混合铵盐处理炼钢粉尘的新方法,工艺流程如图6 所示。 因为NH3和(NH4)2CO3对锌的选择性更好,且不会产生硫酸盐和氯化物杂质,因此该混合液被选为浸出剂。 在最优浸出条件下,锌的浸出率达到81%,而铁浸出率仅为1.3%。 浸出后,通入空气将浸出液中的Fe2+氧化,促进其水解产生Fe(OH)3沉淀,实现铁和锌的分离。 最后,加入(NH4)2S 溶液沉淀Zn2+,得到高品质ZnS。

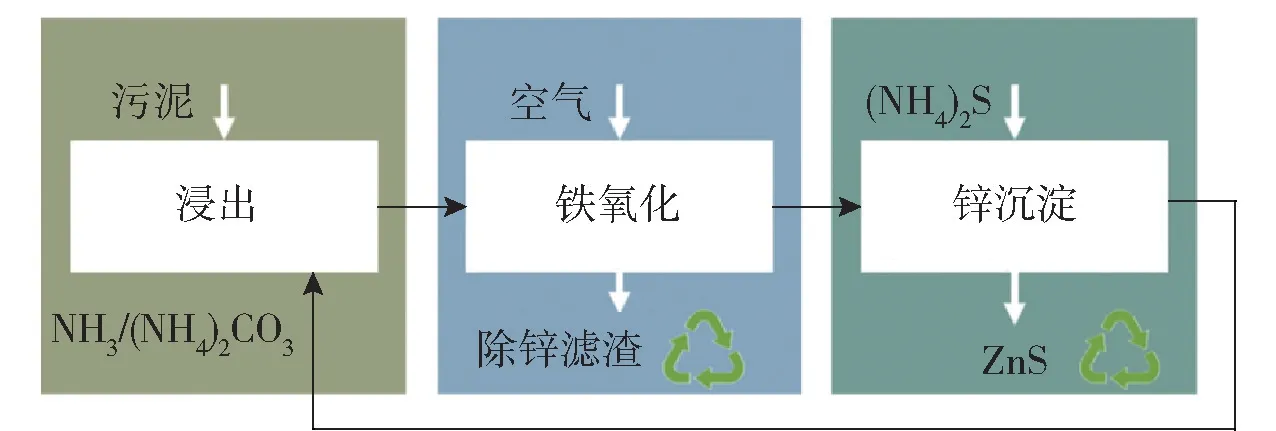
图6 NH3/(NH4)2CO3浸出工艺流程简图Fig.6 Flow chart of NH3/(NH4) 2CO3 leaching process
Wang 等[44]利用FeCl3·6H2O 浸出纯ZnFe2O4中的锌,反应如式(11)所示。 首先将FeCl3·6H2O 与ZnFe2O4混合加热至423 ~473 K,电炉粉尘中锌的浸出率可达94.5%。 然后加水过滤分离,向滤液中加入NaOH 溶液调节pH 以促使锌、铁分离,最后将分离得到的氢氧化铁和氢氧化锌煅烧,得到高纯度的氧化铁和氧化锌,其工艺流程如图7 所示。 该方法很好实现锌、铁分离且产物纯度高,但工艺流程复杂,反应时间较长且滤液未循环利用,造成了资源浪费。

图7 FeCl3·6H2O 浸出工艺流程简图Fig.7 Flowchart of FeCl3·6H2O leaching process

与火法工艺相比,湿法工艺具有能耗低、投资少等优点,但存在工艺流程复杂、设备要求高、耗酸大、易产生二次污染、对原料适应性窄等问题。 直接酸浸也会造成粉尘中其他元素的溶出,给后续锌的分离和提纯带来困难。 直接碱浸需要较长的反应时间,且碱浸浓度过高会增加溶液的黏性,降低反应速率。 盐浸法需要较高的温度,且后续分离、提纯工序较长,经济效益不如直接碱浸和酸浸。
4 火法湿法联合工艺
ZnFe2O4性质稳定,很难被直接还原和浸出,为了提高锌的回收率,国内外学者提出了高温焙烧与湿法浸出相结合的方法来处理炼钢粉尘。 首先通过高温焙烧破坏ZnFe2O4的结构,形成易溶于酸碱的ZnO,然后通过浸出回收锌。 主要工艺有还原焙烧-浸出工艺、NaOH 焙烧-浸出工艺和CaO 改质焙烧—浸出工艺。
4.1 还原焙烧-浸出法
Yu 等[45]采用了选择性还原-酸浸方法来分离ZnFe2O4中的锌和铁。 在温度973 ~1 023 K、CO 体积分数6%、CO/(CO +CO2)体积比为30%的条件下煅烧,可将ZnFe2O4还原为Fe3O4和ZnO。 酸浸中,还原焙烧粉尘中锌的溶出率可达到70%,而铁的溶出率为18.4%,证明了该方法能分离ZnFe2O4中的锌。
氧化锌在ChCl-urea 低共熔溶剂具有较高的溶解度,而铁氧化物在其中难于溶解。 基于此,杨莹等[46]提出了ChCl-urea 低共熔溶剂型离子液体选择性浸出炼钢粉尘中锌的方法。 首先在973 K 下还原焙烧粉尘,将ZnFe2O4分解为铁氧化物和ZnO,然后使用ChCl-urea 离子液体浸出还原焙烧产物,浸出液经恒压电沉积,得到均匀致密且锌含量较高的沉积层,实现锌的回收,但是该工艺的回收率较低,而且浸出剂成本较高,经济效益不高。
4.2 NaOH 焙烧-浸出法
Zhao 等[47]研究了ZnFe2O4与NaOH 的熔融反应,发现ZnFe2O4直接与氢氧化钠反应后,在碱性浸出液中锌的溶出率为75% ~80%。 在熔融反应前先用水或稀NaOH 溶液水解ZnFe2O4,锌的回收率可提高至90%以上。
Halli 等[48-50]系统研究了利用NaOH 焙烧分解炼钢粉尘中的ZnFe2O4,焙烧后ZnFe2O4转化为Na2ZnO2和NaFeO2,反应见式(12)。 在此基础上,提出了回收电炉粉尘中锌的新工艺,如图8 所示。首先将电炉粉尘与NaOH 混合并进行焙烧,然后用柠檬酸选择性浸出焙烧产物,锌的溶出率可达100%,而铁的溶出率低于10%。 过滤分离后,得到的滤渣可作为炼铁原料再利用。 对于滤液,先加入硫酸沉淀Pb2+,得到的PbSO4可作为铅冶炼的原料。然后,向净化后的滤液中加入D2EHPA 溶剂来富集锌离子。 最后,通过电解溶液,得到金属锌和硫酸溶液。


图8 柠檬酸浸出工艺流程简图Fig.8 Flow chart of citric acid leaching process
4.3 CaO 改质焙烧-浸出法
为了提高锌的回收率,Chairaksa-Fujimoto 等[51]研究了利用CaO 改质置换ZnFe2O4中的ZnO。 当添加的CaO 与粉尘中Fe2O3的摩尔比大于1.1 时,在温度1 173 K 加热1 h 可将粉尘中的ZnFe2O4转化为ZnO 和铁酸二钙(Ca2Fe2O5),发生反应(1)。 CaO改质后,电炉粉尘中的锌主要以ZnO 的形式存在,有利于锌和铁的分离。 因此,Itoh 等[52]提出了利用CaO 改质和磁选来分离电炉粉尘中ZnO 的新方法,研究发现在强磁场下CaO 改质粉尘中的ZnO 能与Ca2Fe2O5分离,但是分离率较低,不利于后续锌的回收。
因Ca2Fe2O5在弱酸性溶液中的溶解度较低,Chairaksa-Fujimoto 等[53]在CaO 改质的基础上,提出了氯化铵选择性浸出法。 首先,向Zn 含量为23.6%的电炉粉尘中加入充足的CaO 煅烧,然后在2 mol/L 的NH4Cl 溶液中浸出改质后的粉尘。 在温度为343 K 和固液比为1∶300 的条件下,改质粉尘中大部分的锌被溶解,而铁几乎不溶,钙的溶出率只有20%左右。 过滤分离后,残渣中主要含有Fe2O3和Ca2Fe2O5,可作为一种优良的冶金熔剂返回烧结再利用。 浸出液中主要含有Zn2+,并且杂质元素含量较少,因此可通过电解从该溶液中提取金属锌。基于这些研究结果,日本东北大学Nagasaka 团队提出了一种电炉粉尘中锌回收的新工艺,流程如图9所示。
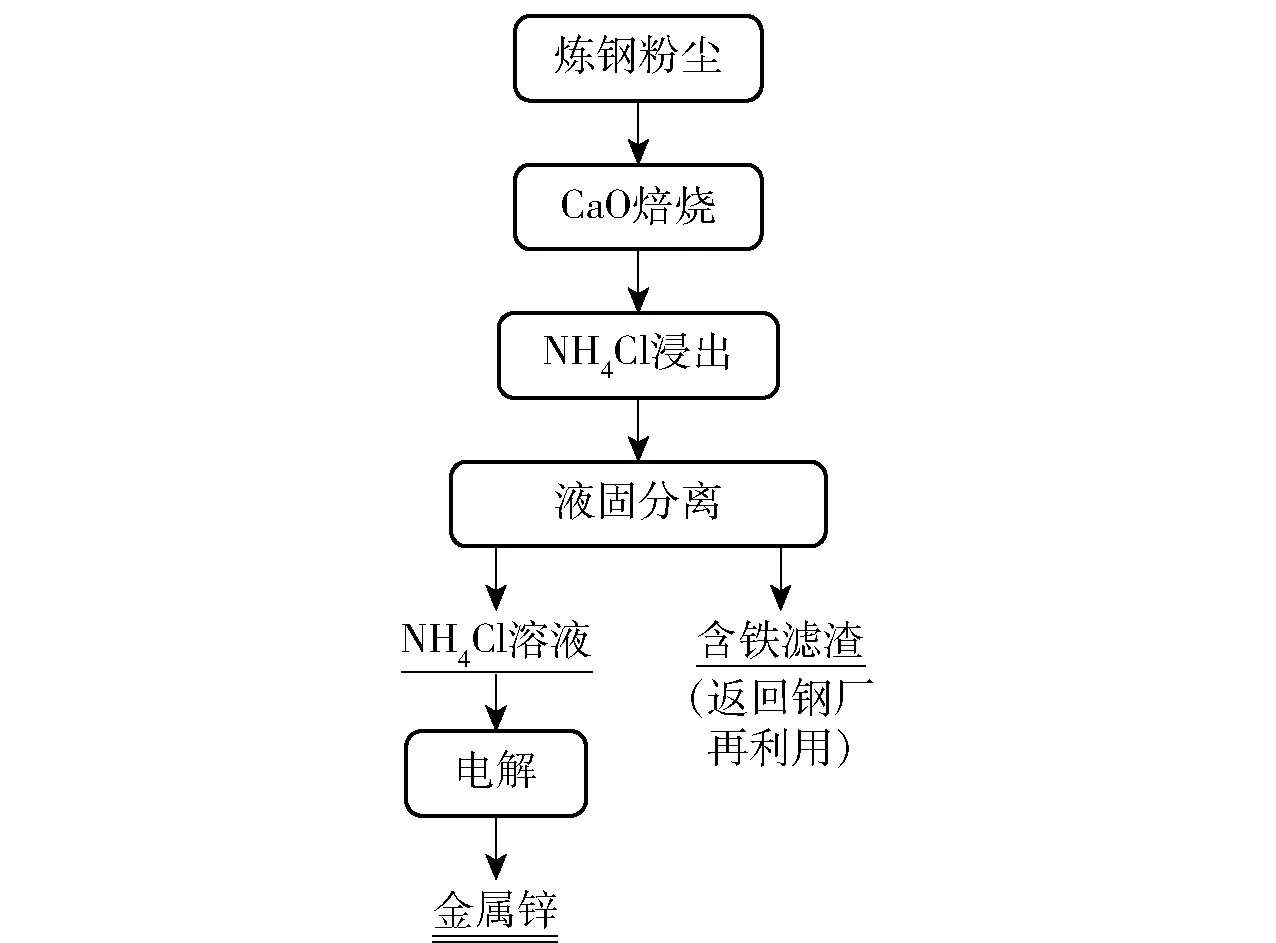
图9 CaO 改质电炉粉尘的浸出工艺流程简图Fig.9 Flow chart of leaching of EAF dust by CaO modification
为了进一步抑制电炉粉尘中钙和铁的溶解,Chairaksa-Fujimoto[54]研究了CaO 改质粉尘在碱性溶液中的溶出行为,发现在2 mol/L NaOH 溶液中锌能够全部溶解,而铁和钙难溶解。 浸出后,改质粉尘中的钙和铁能全部保留在尾渣中,提高了其利用价值。 虽然CaO 改质-碱浸法能有效分离电炉粉尘中的锌,但需要消耗大量的NaOH 溶液,而且高碱性的溶液还要进一步处理,才能用于电解提锌。
火法湿法联合工艺虽然在焙烧过程中需要一定的能耗,但能彻底重构铁酸锌,将其转换为氧化锌,实现低浓度酸浸或碱浸,且部分焙烧工艺不需要碳热还原反应,符合低碳冶金的发展趋势。 其中,CaO改质焙烧碱浸法中铁、钙浸出率几乎为零,不需要提纯即可实现锌资源的回收利用,具有广阔的应用前景,是未来炼钢粉尘资源化利用的方向之一。
5 结论与展望
炼钢粉尘中锌的主要以铁酸锌(ZnFe2O4)形式存在,因其性质稳定,给锌资源的回收利用带来了困难。 目前,分离回收炼钢粉尘中锌的方法主要有火法工艺、湿法工艺和火法湿法联合工艺。
火法工艺具有生产效率高、原料适应性广等优点,但能耗较高。 目前,钢铁企业回收炼钢粉尘主要采用碳热还原法,需要消耗大量的碳与能源,随着国家节能环保压力的增大,钢铁企业加快炼钢粉尘处理技术的升级,进行工艺创新、推动钢厂可持续发展已势在必行。
湿法工艺具有能耗低、投资少等优点,但普遍存在工艺流程复杂、锌回收效率低、设备腐蚀严重、易产生二次污染等问题。 直接酸浸和碱浸需要高浓度的酸和碱,而且产生的废液属于危废,难以处理,不利于大规模生产;铵盐浸出会产生废气,易造成环境污染。 湿法工艺回收炼钢粉尘中锌经济性和环境性较差,不适合单独使用。
相比之下,火法湿法联合工艺,只需要简单焙烧处理,就避免能源过度消耗,且无废气产生;此外,所用浸出液浓度较低,且锌的选择性浸出效果好,应用前景广阔。
综上所述,建议先对钢渣粉尘进行氧化钙焙烧重构,再根据各物质溶解度的差异,选择合适、经济的浸出工艺,在不引入二次污染的前提下,实现铁、锌分离。 这样既降低了能源消耗,也实现了固废资源的循环利用。

