染色体拷贝数变异测序联合STR分型在流产物遗传学分析中的应用
庞 宇,王朝红,唐俊湘,王森林,朱健生
胚胎染色体异常是导致自然流产的重要原因之一,占自然流产因素的50%~70%[1],主要为染色体数目异常如染色体三体、多倍体、X染色体单体等,其次为染色体结构异常如染色体微重复/微缺失、染色体嵌合体、染色体易位等[2]。自然流产不仅对女性的健康造成一定的伤害,而且给社会和家庭增加了负担。对流产物的染色体检测,为探究流产的病因,指导孕妇下一次备孕,实现优生优育,具有重要的意义,本研究采用拷贝数变异测序(copy number variation sequencing,CNV-Seq)联合短串联重复序列(short tandem repeats,STR)分型的方法,对150例流产物进行遗传学检测,并对结果进行分析,为探究自然流产的遗传学病因积累临床资料。
1 资料与方法
1.1 一般资料 选择2020年2-7月在安徽省妇幼保健院妇产科就诊的150例流产病人。其中初发流产63例,复发流产87例,年龄21~44岁;孕6~36+6周,超声诊断为胚胎停育,其中流产组织46份,绒毛104份;经遗传咨询,自愿接受流产的病因学检查,留取流产物(流产组织或绒毛)经处理并保存备用,所有病人均签署知情通知书。
1.2 方法
1.2.1 流产物的CNV-Seq测序 送检的流产组织或绒毛,用0.9%氯化钠溶液反复冲洗,尽量去除母体细胞的污染,放置专用试管内,-20 ℃冰箱保存。选取10 mg的流产组织或绒毛,应用Qiaqen QIAamp DNA Blood Mini Kit试验盒,提取基因组DNA,利用Covaris S220超声波破碎仪将DNA打断,文库构建、纯化、定量、DNA混合文库在illumina Nocaseq6000测序仪上进行双端测序,利用Nx Clinical生信分析软件对染色体非整倍体及100 kb以上的拷贝数变异(CNV)进行分析,对比至人类基因库[hg19]或[GRCh37],并通过OMIM、DGV、 GLINGEN、ClinVar、PubMed、DECIPHER、ISCA、 NCBI、UESC等数据库比对,对检测结果进行判读。
1.2.2 流产物STR分型检测 把DNA样本进行多重荧光PCR扩增,将其产物在ABI 3500 Dx遗传分析仪上进行毛细管电泳,检测出不同分型的相对定位,应用Genc Mapper软件对结果进行计算分析。
2 结果
2.1 流产物染色体检测结果 本研究检测流产物150例,均成功检测,检测成功率100%,染色体正常71例(47.33%),染色体异常79例(52.67%)(见表1)。
2.2 染色体非整倍体、多倍体、嵌合体检测结果 本研究共检出染色体非整倍体49例(染色体三体38例,X染色体单体11例);多倍体7例(69,XXY,4例;69,XXX,3例),染色体数目异常在X、16、21号染色体发生率较高;嵌合体14例,其中16、X号染色体嵌合体发生率较高(见表2)。

表1 不同类型染色体异常的检测结果
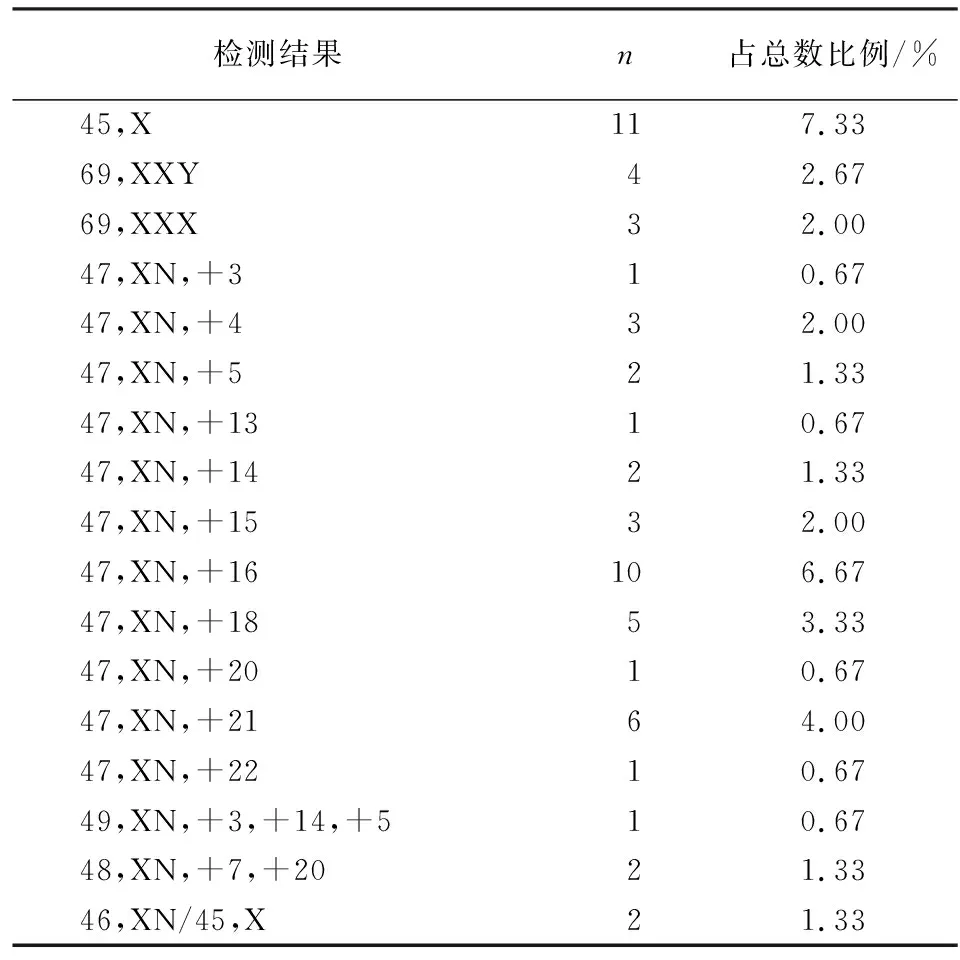
表2 150例流产物染色体非整倍体、多倍体、嵌合体检测结果
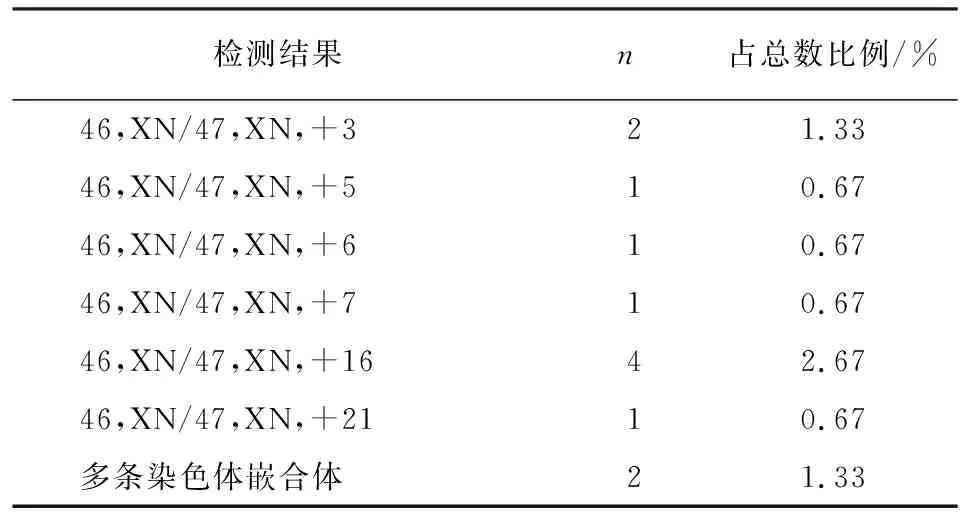
续表2
2.3 染色体CNV的检测结果 本研究共检出染色体微重复/微缺失4例(2.67%),同时存在染色体数目、结构异常3例(2.00%)。涉及1、13、14、17、18号染色体,经数据库查询,均存在不同类型的致病性表型(见表3)。
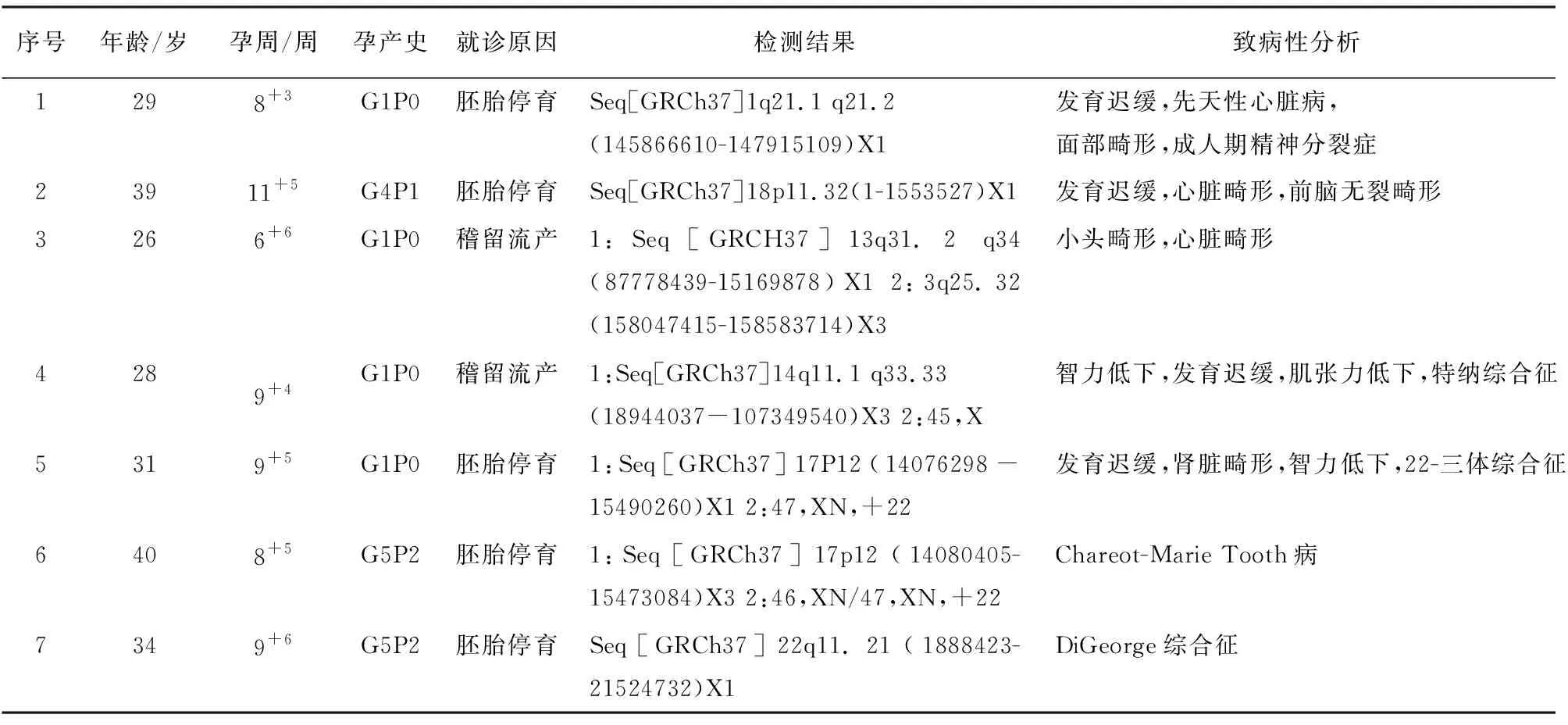
表3 流产物染色体CNV的检测结果
3 讨论
基于高通量测序的CNV-Seq对流产物染色体的测序,是通过将目标染色体的DNA剪切成小片段,构建文库,PCR扩增,以及遗传学信息检测,克服了传统细胞核型技术的染色体制备不良、培养失败、分辨率低等缺点,对染色体非整倍体和染色体CNV可以提供更加准确的遗传学信息,但对染色体多倍体、单亲二倍体、母源性细胞污染的鉴别仍显不足[3]。而STR分型方法是设计荧光引物扩增特定的序列,再进行毛细管电泳,由荧光峰值面积来表达产物扩增的数量,通过等倍基因的剂量变化,来诊断染色体数目异常,对排除母源性细胞污染,以及染色体多倍体、单亲二倍体、性染色体数目异常的诊断具有快速、准确的特点,可弥补CNV-Seq的不足[4]。CNV-Seq联合STR分型方法应用于流产物染色体异常的检测,可覆盖更大范围的染色体异常,能实现对流产物的遗传信息更加准确、全面的诊断,为合理备孕提供科学的依据。
本研究共检出染色体异常79例(52.67%),其中染色体数目异常56例,包括染色体非整倍体49例;三倍体7例;嵌合体14例;染色体微重复/微缺失4例;同时存在染色体数目、结构异常3例;单亲二倍体2例。本研究的结果提示:导致自然流产最主要的染色体异常为染色体数目异常(37.33%),其中主要是染色体非整倍体(32.67%);其次为嵌合体(9.33%)和三倍体(4.67%)。与自然流产密切相关的染色体异常依次为:45,X、16-三体;69,XNN、21-三体;18-三体;16-三体嵌合体。在染色体异常中的占比依次为13.92%、12.66%、8.86%、7.59%、6.33%、5.06%。相关的临床表现为:69,XNN,常于孕早期出现流产,胎儿可表现为先天性心脏病,肾脏畸形、脑积水、脑部畸形和脊髓脊膜膨出等;45,X,表现为特纳综合征,胎儿发育迟缓,身体矮小,先天性性腺发育不良等,部分胎儿发生孕早期流产;16染色体三体,表现为早孕期胚胎停育。其他染色体三体也有表现为不同程度的,多样性的胎儿畸形,胚胎停育、胎儿宫内生长发育迟缓等临床表现,但检出率较低。NIKITINA 等[5]分析了563例自然流产物染色体,染色体正常为296(52.6%),染色体异常为267(47.4%);导致自然流产最主要的染色体异常依次为非整倍体、三倍体等,且先前胚胎具有异常核型的孕妇再次受孕后,发生复发流产的频率仍很高。因此,自然流产物的遗传学检查,对指导再次妊娠具有积极意义。
本研究中染色体嵌合体检出14例(9.33%),分布于3、5、6、7、16、21、X号染色体,其中16号染色体三体嵌合体检出率率最高(2.67%)。16号染色体三体嵌合主要是胚胎早期“三体自救”形成单亲二倍体,或为16-三体/16-二体的复合体,临床表现为:胎儿宫内生长受限、胚胎停育、先天性心脏病、多脏器畸形等[6]。嵌合体的形成可能会增加自然流产的发生率,且嵌合体中异常核型比例越高,临床症状就越明显[7]。单亲二倍体可能因涉及遗传印迹基因、隐性基因纯合突变等,使胎儿出现各种临床综合征,表现为胎儿宫内生长受限、器官畸形、胚胎停育等临床症状。本研究中染色体微重复/微缺失以及同时合并染色体数目异常的共7例(4.67%),均存在不同类型的致病性表型。其中22q11.2微缺失可能导致DiGeorge综合症、腭心面综合症、TaKao综合症等,临床表现包括多种先天畸形:先天性心脏、胸腺发育不全、甲状旁腺功能减退和/或面部畸形。随着时间的推移可能出现的其他临床问题是自身免疫、肾功能不全、发育迟缓、胚胎流产、恶性肿瘤和神经系统表现,如精神分裂症等[8]。17q12微重复涉及Chareot-Marie Tooth病1A型的发生以及压迫麻痹性神经病变,表现为一种慢性进行性肌萎缩症[9]。 1q21.1微缺失综合症表现为小头畸形 、癫痫发作、发育迟缓和各种先天性异常,如心脏异常和泌尿生殖系统异常等,以及成人期精神分裂症的发生相关[10]。 18p11.32微缺失最常见的特征包括严重程度不一的智力低下、身材矮小、流产、前脑无裂畸形、颅面畸形以及言语和认知发育迟缓。其他较少见的临床症状包括行为障碍、心脏畸形、肌张力障碍、生长激素缺乏和自身免疫性疾病[11]。染色体CNV也是导致自然流产的重要因素[12-13],但其检出率较染色体数目异常低。如检查结果为致病性CNV,还需进一步明确其为新发突变,还是来源于父母。对于检查结果为非致病性的CNV,可能应寻找CNV遗传因素之外的自然流产病因如精子畸形、妇科疾病、内分泌疾病、感染、药物、化学毒物、自身免疫疾病等,可为再次备孕的产前诊断、遗传咨询提供有价值的临床资料。
综上所述,染色体非整倍体是自然流产的主要遗传学原因。流产物的遗传学的检测,仍需更多的样本量的临床研究。对流产物染色体易位、倒位、单基因病等检测仍面临着一定的困难,仍需选择更多精准的检测方法,避免漏检。对流产物染色体异常的病人,还应结合夫妻双方染色体的检测,从而明确染色体异常的来源,指导再次妊娠。总之,对流产物的遗传学检测可以从基因层面揭示自然流产的病因,对提高生育质量,减少出生缺陷,实现优生优育具有重要的意义。

