经皮迷走神经刺激在精神障碍应用中的研究进展
向 伟, 李 伟, 李春波
(上海交通大学医学院附属精神卫生中心,上海 200030)
随着社会变迁,疾病谱的改变,精神障碍也越来越为各界所重视[1]。纵观精神障碍的治疗变迁,从约束、管制,发展为药物治疗,心理治疗和康复治疗齐头并进。近年来,随着物理治疗的革新和发展,改良电抽搐治疗、重复经颅磁刺激治疗等治疗手段均获得了比较肯定的临床疗效,但受制于其安全性、经济性和便利性等问题,使其较难在治疗巩固期和维持期患者中推广。
迷走神经刺激(vagus nerve stimulation, VNS)最初应用于癫痫患者,有明确疗效,且发现对情绪和认知有改善作用,引起了研究者们的浓厚兴趣。经皮迷走神经刺激(transcutaneous vagus nerve stimulation, tVNS)则是经皮刺激迷走神经以求达到和VNS同样治疗效果的物理疗法,它避免了侵入性刺激和手术副反应。作为一种较新的物理疗法,因其相对廉价、便利性,应用越来越广泛。因此,本文对该技术在精神障碍中的研究现状进行综述。
1 VNS的演化
迷走神经(vagus nerve, VN)是第10对颅神经,为12对颅神经中最长且分布范围最广的一对,是由80%的感觉传入纤维和20%的运动传出纤维组成的混合神经[2]。VN除能调节多个外周脏器功能外,其传入信号还可影响脑自身功能[3]。VNS需分别在患者左颈部迷走神经周围和左胸部皮肤下经手术植入双极电极及脉冲发射器,脉冲发射器以低频率发送间歇性电信号刺激颈部VN。美国食品和药品监督管理局于1997年和2005年批准其用于难治性癫痫和难治性抑郁症的治疗[4]。
由于VNS需进行昂贵的侵入性外科手术,并且容易出现术后感染,因此非侵入性的tVNS被开发为替代方案。2000年Ventureyra[5]首次在出版物上提出了经皮电刺激神经系统,建议开发一种助听器大小的刺激器,对迷走神经进行非侵入性的经皮刺激,以控制癫痫发作。后续研究表明,tVNS的确可以对神经中枢产生调节作用,且与VNS对神经活动的调节作用有明显重叠[6]。tVNS分两种: 经皮颈迷走神经刺激(transcutaneous cervical vagus nerve stimulation, tcVNS)和经皮耳迷走神经刺激(trans-cutaneous auricular vagus nerve stimulation, taVNS)。tcVNS刺激迷走神经颈支,已被美国食品和药品监督管理局批准用于治疗偏头痛和丛集性头痛;而taVNS刺激迷走神经耳支,已经欧盟认证用于治疗癫痫和抑郁症、慢性疼痛及焦虑症[7]。
2 tVNS的神经机制研究
tVNS的具体作用机制尚不明确。从解剖学角度看,VN起源于延髓4个核团: 迷走神经背核、疑核、三叉神经脊束核和孤束核(nucleus tractus solitarius, NTS)。其中NTS接收大约95%的VN后直接投射到蓝斑(locus coeruleus, LC),然后向不同的大脑区域投射,包括丘脑、杏仁核、内侧隔、海马和前额叶皮层。NTS和LC都是tVNS调节作用的关键节点,可以认为这两个部位的激活是VN活动的间接证据。
tVNS与特定神经递质释放有关,已知不同神经递质驱动不同认知过程[8-9]。
2.1 迷走神经传入纤维和去甲肾上腺素(norepi-nephrine, NE)
传入信号经迷走神经传入纤维传导后能够调节大脑NE合成与分泌[10]。LC是大脑合成分泌NE的主要部位,NE可调节认知过程,如情景记忆、工作记忆和抑制无关信息,参与了VNS的主要治疗作用[11]。有证据表明,LC神经元数量随着年龄增长而减少,保持LC神经元密度可以防止衰老时的认知衰退[12]。功能磁共振成像(functional magnetic resonance imaging, fMRI)研究证实,taVNS激活了脑干区域的迷走神经传入纤维,并在包括LC在内的脑干区域产生了更多激活[11]。唾液α淀粉酶(salivary alpha amylase, sAA)被认为是NE激活的间接标志物。2项taVNS研究表明,与伪刺激相比,真刺激中sAA水平升高,这为tVNS调节NE系统的假设提供了支持[13-14]。
2.2 迷走神经传入纤维与γ-氨基丁酸(gamma-amino-butyric acid, GABA)
尽管VN和GABA之间联系的研究比较少,但仅有的3项研究表明,刺激VN能增加GABA。Frangos等[6]和Yakunina等[11]的fMRI证实,tVNS通过激活NTS来促进GABA释放。此外,Capone等[15]发现与GABAA有关的短间隔皮质内抑制(short interval intracortical inhibition, SICI),在施加tVNS后,右运动皮质区显著增强。
2.3 迷走神经传出纤维与乙酰胆碱(acetylcholine, Ach)
与仅仅激活迷走神经传入纤维的taVNS不同,tcVNS能够激活传入和传出纤维[16]。Bonaz等[17]研究表明,传入纤维能调节NE和GABA,而传出纤维能调节Ach。目前对VNS增加Ach仍有待进一步的研究。随后,Borges等[18]发现与伪刺激相比,施加不同刺激强度的taVNS,对健康成人心脏迷走神经活动的影响没有显著差异,并认为Ach可能只与传出纤维有关,而心脏迷走神经活动受传出纤维的控制,也就是说,由于没有直接的传出纤维连接耳迷走神经和心脏,双侧taVNS是安全的。
研究[6,10-18]提示,tVNS作为VNS发展而来的一种新手段,不仅能调节NE,还能增强GABA与Ach,在治疗精神障碍中具有潜力。而且,taVNS与tcVNS相比,基于对心脏电活动没有直接影响,因此更具有安全性。
3 经皮迷走神经刺激在精神障碍治疗的应用进展
由于经皮迷走神经刺激的安全性,便利性,相对廉价,其在精神障碍中的应用也越来越广泛,见表1。
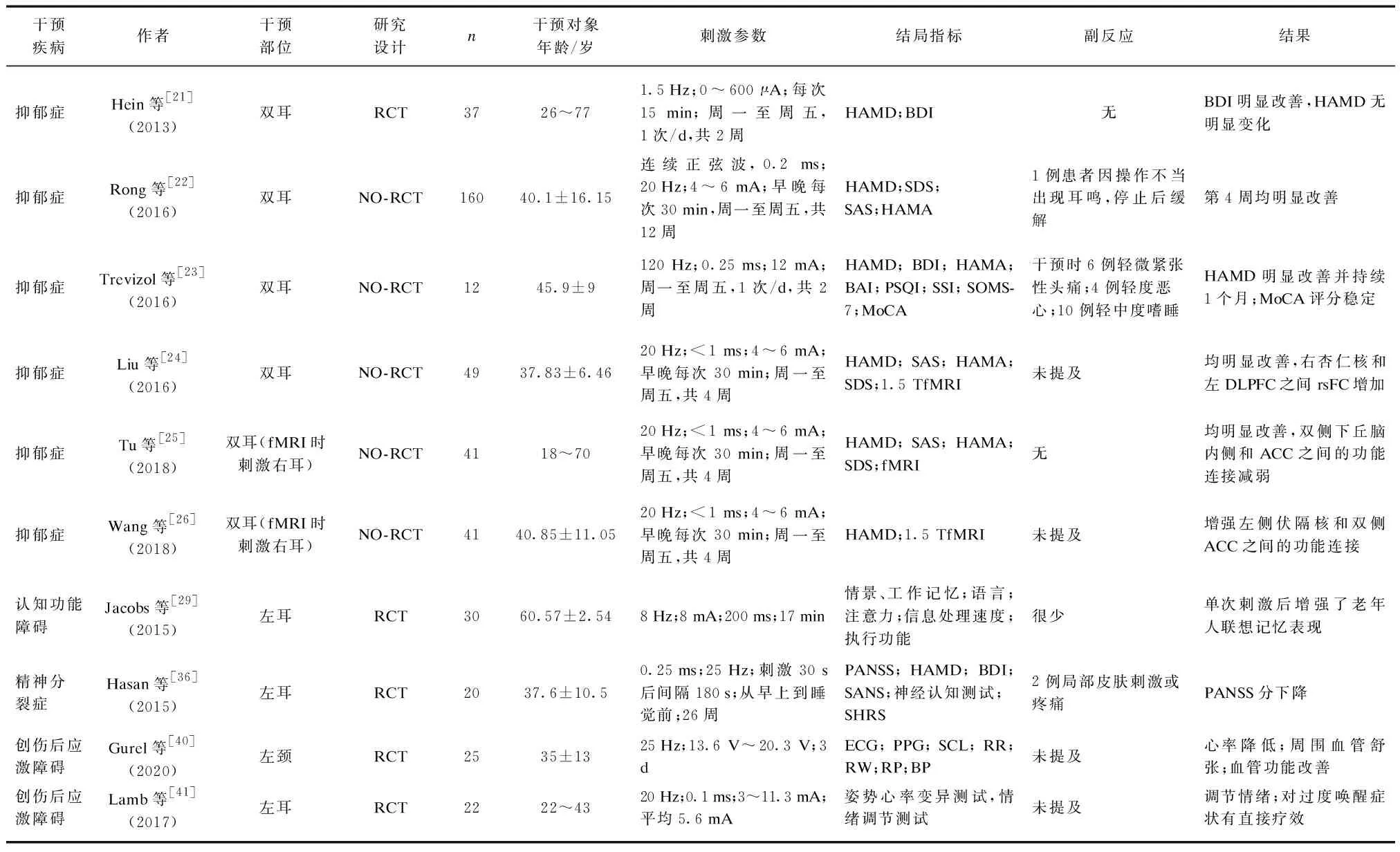
表1 经皮迷走神经刺激在精神障碍中的应用Tab.1 The treatment in mental disorders by transcutaneous vagus nerve stimulation
3.1 经皮迷走神经刺激在抑郁症中的应用
抑郁症被认为是多种遗传和环境因素相互作用的结果,进而导致患者对应激的高易感性,涉及大脑的海马、下丘脑和杏仁核,以及背侧额叶、背侧扣带回、顶下皮质和后扣带回等结构[19]。在分子层面,抑郁症的产生是某些神经递质,如多巴胺,五羟色胺及NE等单胺类递质失衡所导致。抑郁症的认知功能缺陷,如注意力缺陷、记忆损害和消极偏见可能与胆碱功能障碍以及海马、前额叶皮质和杏仁核等大脑的结构和功能改变有关[20]。
Hein等[21]首次以37例抑郁症患者为研究对象开展taVNS随机对照研究,发现干预2周后taVNS组抑郁量表评分较伪刺激组显著降低。随后Rong等[22]对160例抑郁症患者进行taVNS研究表明,taVNS组抑郁评分减分值及有效应答率均显著高于伪刺激组。Trevizol等[23]对抑郁症患者进行taVNS干预,发现干预前后抑郁显著下降。上述研究[21-23]发现taVNS可以显著改善抑郁症患者焦虑、精神运动抑制、睡眠障碍和绝望情绪等症状,同时还观察到认知障碍的好转趋势。
Liu等[24]发现tVNS能够增强抑郁症患者右侧杏仁核和左背外侧前额叶皮质之间静息态功能连接(resting-state functional connectivity, rsFC)。Tu等[25]发现tVNS能够减弱双侧下丘脑内侧和前扣带回(anterior cingulate cortex, ACC)之间的功能连接,而Wang等[26]发现tVNS导致左侧伏隔核和双侧ACC之间的功能连接增强。以上研究[24-26]从脑网络的角度表明了tVNS通过调节神经网络的功能连接达到改善抑郁症状的效果。
这些临床试验证实了tVNS能改善抑郁症状,一般认为其抗抑郁机制与皮质-边缘系统-丘脑-纹状体神经回路有直接和间接的联系,能够影响这些区域的活动,调节了神经递质的合成与分泌。
3.2 经皮迷走神经刺激在阿尔茨海默病中的应用
从最早的胆碱能假说,到随后淀粉样蛋白级联假说,神经血管假说,线粒体级联假说,Tau传播假说,这些机制都没有完整解释阿尔茨海默病。目前NE和LC重塑在阿尔茨海默病中的作用越来越受到重视。与同年龄对照组相比,阿尔茨海默病患者的LC神经元数量平均减少60%,LC变性发生在阿尔茨海默病进展早期[27-28]。NE主要来源于LC,并且LC的退化已被证明会显著破坏多个认知过程。LC投射到广泛区域,包括海马、大脑皮质、基底前脑、视前区和下丘脑,这意味着LC功能任何中断都会产生广泛影响。
tVNS在阿尔茨海默病中的应用仍在起步阶段,Jacobs等[29]首次对30例健康老年人开展tVNS随机对照研究,发现即使在1次tVNS后,也可改善老年人联想记忆,适用于认知能力下降的患者。可能的机制为VN激活后导致NE在皮质和皮质下脑区释放,包括杏仁核和海马,促进了海马突触的可塑性。
3.3 经皮迷走神经刺激在精神分裂症中的应用
精神分裂症引起大脑皮质活动兴奋性或抑制性失常以及纹状体多巴胺的去抑制,从而导致阳性,阴性和认知症状[30]。精神分裂症阴性症状和认知功能缺损发生和大脑皮质神经回路有关,关键区域是额叶、颞叶、顶叶、扣带回、枕后回和海马等部位[31-32]。在精神分裂症患者心理测试中发现,杏仁核网络的功能障碍参与认知障碍发病,精神分裂症患者认知和社会情绪处理之间的相互作用,与涉及这些功能区域的神经系统之间的连接异常模式相关联[33-34]。而皮层和皮质下结构、前额叶-皮质下联结模式上的异常,被认为在精神分裂症患者情感和认知过程之间相互作用的破坏中发挥重要作用[35]。
目前仅有一项对精神分裂症患者开展taVNS的案例报道[36]。研究者对20例稳定期精神分裂症患者开展taVNS随机对照研究,发现干预12周后,taVNS组精神症状减分值显著高于伪刺激组,抑郁评分和神经认知功能也都有变化。不过,该研究中患者可以自主调节刺激强度,干预依从性较差,只有9例被试遵守了治疗方案。
3.4 经皮迷走神经刺激在其他精神障碍中的应用
研究者[37-39]相继提出了tVNS治疗精神障碍的潜在目标,包括注意力缺陷多动障碍(attention deficit hyperactivity disorder, ADHD),孤独症谱系障碍以及术后认知功能障碍等(postoperative cog-nitive dysfunction, POCD)。在对创伤后应激障碍(posttraumatic stress disorder, PTSD)的研究中,发现tVNS治疗减轻了患者与创伤性记忆相关的压力[40],能够调节患者的情绪状态,对PTSD的过度唤醒症状有直接疗效[41]。
4 展 望
研究提示,精神分裂症患者停药2年内90%会复发,但众多精神分裂症患者及其家属仍然希望尽早停药[42],故而非药物治疗在精神障碍中的应用日益得到重视,经皮迷走神经刺激作为抑郁症的辅助治疗已经获得越来越广泛的认可,不过现有研究仍存在局限性: 样本量相对较小,刺激治疗部位与参数不统一,功能评估指标和工具不一致等。因此,tVNS对精神障碍的疗效尚需进一步研究: 一方面,开展大样本临床随机对照试验,比较tVNS与抗精神病药物、心理治疗等对精神障碍患者的疗效,以提供循证证据;另一方面,tVNS可协同其他干预方案治疗精神障碍患者,希望将来能为临床治疗提供更多选择。

