裸花紫珠的化学成分研究
陈倩倩,邹献亮,侴桂新, 2*
• 化学成分 •
裸花紫珠的化学成分研究
陈倩倩1,邹献亮3,侴桂新1, 2*
1. 上海中医药大学中药研究所,上海 201203 2. 上海中药标准化研究中心,上海 201203 3. 萍乡卫生职业学院,江西萍乡 337000
研究裸花紫珠叶的化学成分。采用多种现代分离色谱技术进行分离纯化,通过波谱数据和理化性质进行结构鉴定,以及ECD确定新化合物的绝对构型;采用CCK-8法对新化合物的细胞毒活性进行筛选。从裸花紫珠叶70%乙醇提取物中分离鉴定出34个化合物,其中化合物1~5为裸花紫珠烷A1(1)、(4,6)-4,6-二羟基-α-松油醇(2)、(1)-2,2-二甲基-3-羟甲基-3-环己烯-1-甲酸(3)、(1,4)-2,2-二甲基-3-亚甲基-4-羟基环己烷-1-甲酸(4)、(1)-2,2-二甲基-4-羟甲基-3-环己烯-1-甲酸(5);化合物6~34为2,6-二甲氧基-对-苯醌(6)、对薄荷-8-烯-1,2-二醇(7)、天目地黄素B(8)、北玄参素G(9)、黄牡丹醇B(10)、香桂酮(11)、8-羟基-2,6-二甲基-(2,6)-辛二烯酸(12)、8-羟基-2,6-二甲基-(2)-辛烯酸(13)、裸花紫珠烷A(14)、丁子香烷-2β,9α-二醇(15)、丁香烷-1,9β-二醇(16)、(8,9)-异丁香烷-8,9-二醇(17)、()-(+)-去氢催吐萝芙叶醇(18)、(3,5,6,7)-5,6-环氧-3-羟基-7-大柱香波龙烯-9-酮(19)、脱落酸(20)、紫珠醌B(21)、12-羟基茉莉酸(22)、(−)-12-羟基茉莉酸甲酯(23)、齐墩果酸(24)、熊果酸(25)、蔷薇酸(26)、5,4-二羟基-3,7,3-三甲氧基黄酮(27)、毡毛美洲茶素(28)、5,7,4′-三羟基-3′-甲氧基黄酮(29)、柳叶柴胡酚(30)、九里香亭(31)、芥子醛(32)、香草醛(33)和丁香酸(34)。化合物1~5为新化合物,分别命名为裸花紫珠烷A1~E1,化合物6~13、17~18和31均为首次从马鞭草科中分离鉴定,化合物30、32~33均为首次在紫珠属植物中发现,化合物15、21和28均为首次从裸花紫珠中分离得到。体外细胞毒活性筛选结果表明,化合物4对人肝癌HepG2细胞具有细胞毒活性,其半数抑制浓度(half inhibition concentration,IC50)值为24.0 μmol/L。
马鞭草科;裸花紫珠;裸花紫珠烷A1;(1,4)-2,2-二甲基-3-亚甲基-4-羟基环己烷-1-甲酸;丁子香烷-2β,9α-二醇;紫珠醌B;毡毛美洲茶素;柳叶柴胡酚
裸花紫珠为马鞭草科植物裸花紫珠Hook. et Arn的干燥叶,在我国主产于海南、广东、广西等地,具有消炎、解肿毒、化湿浊、止血等功效,已作为新增药材收录于《中国药典》2020年版[1]。裸花紫珠作为传统的黎药而被广泛应用于临床[2],目前上市的裸花紫珠制剂主要为单味药制剂,包括片剂、颗粒剂和胶囊剂等[3]。有关裸花紫珠化学成分研究逐年增加,包括挥发油、黄酮类、三萜类、二萜类、倍半萜类、环烯醚萜类、苯丙酸、木脂素和苯乙醇苷等,其中二萜类、倍半萜类和环烯醚萜等成分是研究的热点[4]。为进一步丰富裸花紫珠的化学信息,为阐明裸花紫珠的药效物质基础提供资料。本研究对裸花紫珠70%乙醇提取物的二氯甲烷部位化学成分进行系统的分离得到34个化合物,其中化合物1~5为新化合物,命名为裸花紫珠烷A1(1)、裸花紫珠烷B1(2)、裸花紫珠烷C1(3)、裸花紫珠烷D1(4)、裸花紫珠烷E1(5);其他29个已知化合物分别鉴定为2,6-二甲氧基-对-苯醌(2,6- dimethoxy--benzoquinone,6)、对薄荷-8-烯-1,2-二醇(-menth-8-ene-1,2-diol,7)、天目地黄素B(rehmachinin B,8)、北玄参素G(buergerinin G,9)、黄牡丹醇B(paeoveitol B,10)、香桂酮(subamone,11)、8-羟基-2,6-二甲基-(2,6)-辛二烯酸 [8-hydroxy-2,6-dimethyl-(2,6)-octadienoic acid,12]、8-羟基-2,6-二甲基-(2)-辛烯酸[8-hydroxy- 2,6-dimethyl-(2)-octenoic acid,13]、裸花紫珠烷A(callnudoid A,14)、丁子香烷-2β,9α-二醇(clovane-2β,9α-diol,15)、丁香烷-1,9β-二醇(caryolane-1,9β-diol,16)、(8,9)-异丁香烷-8,9-二醇 [(8,9)-isocaryolane-8,9-diol,17]、()-(+)-去氢催吐萝芙叶醇 [()-(+)-dehydrovomifoliol,18]、(3,5,6,7)-5,6-环氧-3-羟基-7-大柱香波龙烯-9-酮 [(3,5,6,7)-5,6-epoxy-3-hydroxy-7-megastigmen- 9-one,19]、脱落酸(abscisic acid,20)、紫珠醌B(callicarpaquinone B,21)、12-羟基茉莉酸(12-hydroxyjasmonic acid,22)、(−)-12-羟基茉莉酸甲酯 [(−)-methyl 12-hydroxyjasmonate,23]、齐墩果酸(oleanolic acid,24)、熊果酸(ursolic acid,25)、蔷薇酸(euscaphic acid,26)、5,4′-二羟基-3,7,3′-三甲氧基黄酮(5,4′-dihydroxy-3,7,3′-trimethoxy- flavone,27)、毡毛美洲茶素(velutin,28)、5,7,4′-三羟基-3′-甲氧基黄酮(5,7,4′-trihydroxy-3′- methoxyflavone,29)、柳叶柴胡酚(salicifoliol,30)、九里香亭(murrangatin,31)、芥子醛(sinapaldehyde,32)、香草醛(4-hydroxy-3-methoxybenzaldehyde,33)、丁香酸(syringic acid,34)。化合物1和14为降半日花烷型二萜,化合物15~23为倍半萜,化合物2~5、7~13为单萜,化合物6为醌类,化合物24~26为三萜,化合物27~29为黄酮,化合物30为木脂素,化合物31为香豆素,化合物32~34为酚酸。并对分离得到的5个新化合物进行体外抗人肝癌HepG2细胞增殖活性筛选,结果表明,化合物4有明显的抑制HepG2细胞增殖活性,其半数抑制浓度(median inhibition concentration,IC50)值为24.0 μmol/L。
1 仪器与材料
Bruker AVANCE-III型核磁共振波谱仪(400 MHz,内标为TMS,德国Bruker公司);Waters UPLC Premior Q-TOF质谱仪、e2695型高效液相色谱仪、制备型1260高效液相色谱仪(美国安捷伦公司);FT-IR红外光谱仪(PerkinlEmer公司);制备色谱柱(Shiseido Capcellpak C18,250 mm×20 mm,5 μm,日本资生堂);Reveleris X2 Flash中压液相色谱仪(MPLC,美国Grace公司);Synergy H4酶联免疫检测仪(美国BioTek公司);Sephadex LH-20凝胶(瑞典乌普萨拉阿默森生物科学公司);MCI GEL CHP20P(75~150 μm,日本东京三菱化学工业公司);柱色谱硅胶(100~200、200~300、300~400目,中国青岛湾精细化工有限公司);薄层色谱及制备型薄层色谱HSGF254硅胶板(烟台江友硅胶开发有限公司);高效液相色谱用乙腈(色谱级,美国Dikma公司);薄层色谱用试剂均为分析纯(中国医药集团有限公司);柱色谱用试剂均为工业级(上海润捷化学试剂有限公司),CCK-8试剂盒(日本,同仁500T,批号C8216990),96微孔板(Corning 3599,批号02222601),DMEM培养基(美国Gibco公司,批号MA0212-Jun-08H),胰酶-EDTA(美伦生物,批号MA0233-Jul-01H),PBS磷酸盐缓冲液(美伦生物,批号MA0015-Jun-29H),无水乙醇(分析纯,上海国药化学试剂公司);紫杉醇(taxol,PTX,质量分数>98%,批号H15F10X80839,上海源叶生物科技有限公司)
裸花紫珠药材于2019年6月在海南省五指山采收,由上海中医药大学吴立宏教授鉴定为裸花紫珠Hook. et Arn的干燥叶,标本(LHZZ- 20190806)保存于上海中医药大学中医药研究所标准化研究中心标本室。
2 提取与分离
干燥裸花紫珠叶50 kg,粉碎,用70%乙醇回流提取2次,减压浓缩得到8.3 kg的干浸膏。干浸膏溶于甲醇后与等量硅胶拌样,干燥后依次用石油醚、二氯甲烷、醋酸乙酯、甲醇抽提,回收溶剂分别得到石油醚部位(25.8 g)、二氯甲烷部位(129.1 g)、醋酸乙酯部位(657.2 g)和甲醇部位。
二氯甲烷部位经硅胶柱色谱分离(石油醚-醋酸乙酯100∶1~0∶1、醋酸乙酯-甲醇1∶1~0∶1),结合制备薄层色谱(PTLC)分析,合并得到11个组分(Fr. C1~C11)。
Fr. C7经PTLC色谱以石油醚-醋酸乙酯(2∶1)洗脱得到化合物27(20 mg)、28(4.6 mg)。
Fr. C4经MPLC色谱(甲醇-水3∶7~1∶0)分离纯化,得到28个亚组分(Fr. C4-1~C4-28)。Fr. C4-5(0.195 g)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)等度洗脱得到9个次组分(Fr. C4-5-1~C4-5-9)。Fr. C4-5-2(23.7 mg)经PTLC色谱以石油醚-醋酸乙酯(2∶1)洗脱得到化合物11(13.4 mg)。Fr. C4-14(0.152 g)经过Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)等度洗脱得到8个次组分(Fr. C4-14-1~C4-14-9)。Fr. C4-14-6(34.7 mg)为粗结晶,经二氯甲烷洗脱得到化合物21(6.3 mg)。Fr. C4-27(0.248 g)经硅胶柱色谱(石油醚-醋酸乙酯100∶1~1∶1)洗脱得到12个次组分(Fr. C4-27-1~C4-27-12)。Fr. C4-27-9(140 mg)和Fr. C4-27-11(109 mg)分别经制备液相色谱(乙腈-水65∶35)得到化合物24(40 mg,R=28.5 min)和25(19 mg,R=3.5 min)。
Fr. C8(27.0g)经硅胶柱色谱梯度洗脱(石油醚-二氯甲烷5∶1~0∶1、二氯甲烷-甲醇150∶1~0∶1)系统洗脱得到7个不同亚组分(Fr. C8-1~C8-7)。Fr. C8-2(1.479 g)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)等度洗脱得到8个次组分(Fr. C8-2-1~C8-2-8)。Fr. C8-2-7(29 mg)经制备HPLC色谱(乙腈-水60∶40)分离纯化得到化合物33(6.9 mg,R=0.7 min)。Fr. C8-3(2.2 g)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)洗脱得到9个次组分(Fr. C8-3-1~C8-3-9)。Fr. C8-3-2(2.16 g)经MCI柱色谱(甲醇-水3∶7~1∶0)梯度洗脱得到11个流分(Fr. C8-3-2-1~C8-3-2-11)。Fr. C8-3-2-2(60 mg)经PTLC色谱(二氯甲烷-甲醇100∶1)分离以及制备HPLC(乙腈-水70∶30)纯化得到化合物9(6.7 mg,R=17.4 min)。Fr. C8-3-2-8(53.6 mg)经制备HPLC(乙腈-水60∶40)得到化合物1(9.8 mg,R=12.4 min)。Fr. C8-3-2-3(60.8 mg)以30%甲醇洗涤晶体得到化合物6(4 mg)。Fr. C8-3-3(243 mg)经Sephadex LH-20柱色谱(甲醇)洗脱得7个流分(Fr. C8-3-3-1~C8-3-3-7)。Fr. C8-3-3-5(51.3 mg)经制备HPLC色谱(乙腈-水15∶85)分离纯化得到化合物32(18 mg,R=5.7 min)。Fr. C8-3-4(59 mg)经制备HPLC(乙腈-水15∶85)分离纯化得到化合物30(25 mg,R=8.1 min)。Fr. C8-4(9.2 g)经MPLC色谱(甲醇-水3∶7~1∶0)梯度洗脱得到28个次组分(Fr. C8-4-1~C8-4-28)。Fr. C8-4-7(1.2 g)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)得到5个流分(Fr. C8-4-7-1~C8-4-7-5)。Fr. C8-4-7-2(72 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得化合物8(20 mg)。Fr. C8-4-7-5(50 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物34(30 mg)。Fr. C8-4-8(412 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)梯度洗脱得到5个流分(Fr. C8-4-8-1~C8-4-8-5)。Fr. C8-4-8-2(12 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物22(2 mg)。Fr. C8-4-9(215 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到2个流分(Fr. C8-4-9-1~C8-4-9-2)。Fr. C8-4-9-2(105 mg)经PTLC色谱(二氯甲烷-甲醇20∶1)分离得到化合物18(18 mg)。Fr. C8-4-11(249 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)洗脱得到5个流分(Fr. C8-4-11-1~C8-4-11-5)。Fr. C8-4-11-1(72 mg)经PTLC色谱(二氯甲烷-甲醇20∶1)分离得到化合物19(26 mg)。Fr. C8-4-11-4(19 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物7(3 mg)。Fr. C8-4-12(140 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)洗脱得到3个流分(Fr. C8-4-12-1~C8-4-12-3)。Fr. C8-4-12-2(25 mg)经PTLC色谱(二氯甲烷-甲醇20∶1)分离得到化合物23(20 mg)。Fr. C8-4-23(511 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到6个流分(Fr. C8-4-23-1~C8-4-23-6)。Fr. C8-4-23-6(107 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)以及制备HPLC(乙腈-水60∶40)分离纯化得到化合物17(25 mg,R=2.7 min)。Fr. C8-6(9.3 g)经MPLC色谱(甲醇-水3∶7~1∶0)梯度洗脱得到22个次组分(Fr. C8-6-1~C8-6-22)。Fr. C8-6-4(141 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)洗脱得到5个流分(Fr. C8-6-4-1~C8-6-4-5)。Fr. C8-6-4-1(76 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物2(18.4 mg)。Fr. C8-6-4-4(16 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物3(6 mg)。Fr. C8-6-6(103 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到3个流分(Fr. C8-6-6-1~C8-6-6-3)。Fr. C8-6-6-2(31 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物10(19 mg)。Fr. C8-6-6-3(20 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物31(8 mg)。Fr. C8-6-7(97 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到5个流分(Fr. C8-6-7-1~C8-6-7-5)。Fr. C8-6-7-4(35 mg)和Fr. C8-6-7-5(20 mg)分别经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物4(18 mg)和5(4.8 mg)。Fr. C8-6-9(277 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)得到6个流分(Fr. C8-6-9-1~C8-6-9-6)。Fr. C8-6-9-3(95 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物20(26 mg)。Fr. C8-6-9-5(44 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物12(22 mg)。Fr. C8-6-10(456 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到6个流分(Fr. C8-6-10-1~C8-6-10-6)。Fr. C8-6-10-5(238 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物13(21 mg)。Fr. C8-6-13含有大量黄色晶体,用二氯甲烷洗脱后,得到化合物29(20 mg)。Fr. C8-6-14(760 mg)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到8个流分(Fr. C8-6-14-1~C8-6-14-8)。Fr. C8-6-14-2(202 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物16(14 mg)。Fr. C8-6-14-5(196 mg)经制备HPLC(乙腈-水45∶55)得到化合物14(25 mg,R=11.7 min)。Fr. C8-6-16(1.03 g)经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1系统)分离得到8个流分(Fr. C8-6-16-1~C8-6-16-8)。Fr. C8-6-16-2(491 mg)经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物15(15 mg)。Fr. C8-6-19经Sephadex LH-20柱色谱(石油醚-二氯甲烷-甲醇5∶5∶1)分离得到7个流分(Fr. C8-6-19-1~C8-6-19-7)。Fr. C8-6-19-6经PTLC色谱(二氯甲烷-甲醇10∶1)分离得到化合物26(15 mg)。
3 结构鉴定
化合物1:黄色油状物;通过高分辨质谱(HR-ESI-MS)/289.177 7 [M+Na]+(计算值289.177 4,C16H26O3Na),确定其分子式为C16H26O3,不饱和度为4。IR光谱显示具有羟基3416 cm−1、羰基1732 cm−1、双键1644 cm−1等特征吸收峰;1H-NMR(表1)显示有3个甲基信号,2个为单峰H1.15 (3H, s, 19-Me), 0.67 (3H, s, 20-Me),1个双峰H0.94 (3H, d,= 6.9 Hz, H-11);2个末端烯质子信号H4.77 (1H, d,= 1.7 Hz, H-17b), 4.56 (1H, d,= 1.7 Hz, H-17a);1个甲氧基质子信号H3.68 (3H, s, 3-OMe)。13C-NMR(表1)结合DEPT显示共有16个碳信号,包括1个羰基碳C176.0 (C-3)、2个烯碳C150.4 (C-8), 107.3 (C-17)、3个甲基碳C23.6 (C-19), 13.3 (C-20), 10.7 (C-11)、1个甲氧基碳C51.9 (3-OMe)、4个亚甲基碳C41.3 (C-1), 44.9 (C-18), 22.7 (C-6), 36.8 (C-7)、3个次甲基碳C38.3 (C-2), 56.3 (C-5), 49.9 (C-9),另有2个季碳C72.2 (连氧季碳,C-4), 39.4 (C-10)。以上数据结合不饱和度分析,表明化合物1含有2个环。化合物1的波谱数据与本研究分离得到的已知化合物14[5]波谱数据非常相似。不同之处在于化合物1中多出1个甲氧基[H3.68 (s),C51.9] 信号,HMBC谱中,甲氧基与C-3的相关,表明化合物1为裸花紫珠烷A的甲酯化物。综上分析,确定了化合物1的平面结构。
在NOESY谱(图1)中,Me-20与Me-19和Me-11相关,H-2与Me-19和Me-20相关表明,H-2、Me-11、Me-19和Me-20在同一平面,定为β取向。H-9与H-5相关,表明H-9与H-5在同一平面,定为α取向。通过实验和计算的ECD光谱(图2)分析,推断出化合物1的绝对构型为2、4、5、9、10。最后,确定了化合物1的结构(图1),命名为裸花紫珠烷A1。
化合物2:无色针状晶体(二氯甲烷-甲醇);通过HR-ESI-MS/209.114 2 [M+Na]+(计算值209.114 8,C10H18O3Na)确定其分子式为C10H18O3,不饱和度为2。IR光谱示有羟基3334 cm−1;1H-NMR(表1)显示有3个甲基单峰信号分别为H1.21 (3H, s, 9-Me), 1.18 (3H, s, 10-Me), 1.81 (3H, brs, 7-Me),1个烯质子信号H5.46 (1H, m, H-2),1个连氧次甲基质子信号H4.00 (1H, brs, H-6)。13C-NMR(表1)结合DEPT显示有10个碳信号,2个烯碳C135.4 (C-1), 122.6 (C-2)、3个甲基碳C24.5 (C-9), 24.4 (C-10), 21.0 (C-7)、2个亚甲基碳C34.1 (C-3), 35.3 (C-5)、1个连氧次甲基碳C69.7 (C-6)、2个连氧季碳C76.3 (C-4), 75.2 (C-8)。结合1H-1H COSY、HMQC和HMBC相关信号,推测化合物2的结构为对薄荷烷型单萜类化合物,其结构与α-松油醇[6]相似,区别在于化合物2的C-4为连氧季碳C76.3 (C-4),C-6为连氧次甲基H4.00 (1H, H-6),C69.7 (C-6);而α-松油醇中C-4为次甲基,C-6为亚甲基。结合相对分子质量可知化合物2比α-松油醇多了2个羟基,分别连接于C-4和C-6位上,其结构见图3。

表1 化合物1和2的1H-NMR和13C-NMR数据(400/100 MHz)
-CDCl3-CD3OD,下表同
-CDCl3-CD3OD, same as below tables

图1 化合物1关键的1H-1H COSY、HMBC和NOESY相关

图2 化合物1~5的实验和计算ECD
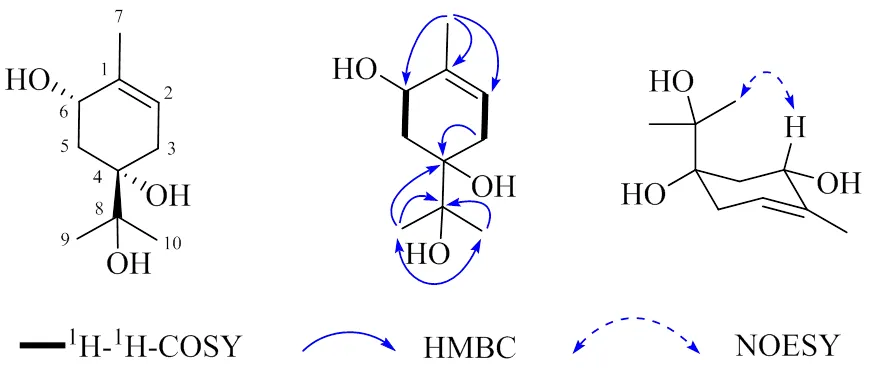
图3 化合物2的关键1H-1H COSY、HMBC和NOESY相关
根据MM2力场计算,得化合物2的优势构象为半椅式,H-6和异丙醇片段处于直立键,4-OH和6-OH处于平伏键。在NOESY谱中,可观察到H-6与Me-9相关,故确定H-6和异丙醇片段为β取向,而4-OH和6-OH为α取向。NOESY相关信号见图3。将化合物2实验获得的ECD谱与2种构型的计算ECD谱(4, 6-2a;4, 6-2b) 进行比较,化合物2的实验ECD谱与2a的计算ECD谱Cotton效应基本一致,由此推断化合物2的绝对构型为4,6,鉴定结构为(4,6)-二羟基-α-松油醇,命名为裸花紫珠烷B1。
化合物3:无色油状物;通过HR-ESI-MS/207.099 3 [M+Na]+(计算值207.099 2,C10H16O3Na)确定分子式为C10H16O3,不饱和度为3。1H-NMR(表2)显示有2个甲基单峰信号H0.88 (3H, s, 8-Me), 1.08 (3H, s, 9-Me),1个烯质子信号H5.58 (1H, m, H-4)。13C-NMR(表2)结合DEPT135显示共有10个碳信号,包括1个羰基碳C179.3 (C-7),2个烯碳C151.6 (C-4), 123.3 (C-3),2个甲基碳C20.9 (C-8), 25.9 (C-9),3个亚甲基碳(其中1个为连氧亚甲基碳)35.7 (C-5), 34.7 (C-6), 60.0 (C-10),1个次甲基碳C46.9 (C-1),1个季碳C46.4 (C-2)。以上数据表明化合物3是单环单萜类化合物,其1H-和13C-NMR谱与2,2,3-三甲基-3-环己烯-1-羧酸[7]相似,唯一不同的是2,2,3-三甲基-3-环己烯-1-羧酸中C-10处的甲基信号,在化合物3中被羟甲基[H4.18 (2H, brs, H-10),C60.0 (C-10)] 所取代,进一步由HMBC谱中H-10与C-2 (C46.4), C-3 (C151.6), C-4 (C123.3) 的相关信号所证实。确定了化合物3的平面结构为2,2-二甲基-3-羟甲基-3-环己烯-1-羧酸,比较化合物3的实验ECD谱和计算的ECD谱,表明化合物3的ECD谱与计算的1构型的谱具有相同的趋势,因此确定其C-1的绝对构型为,结构鉴定为(1)-2,2-二甲基-3-羟甲基-3-环己烯-1-甲酸,如图4所示,命名为裸花紫珠烷C1。
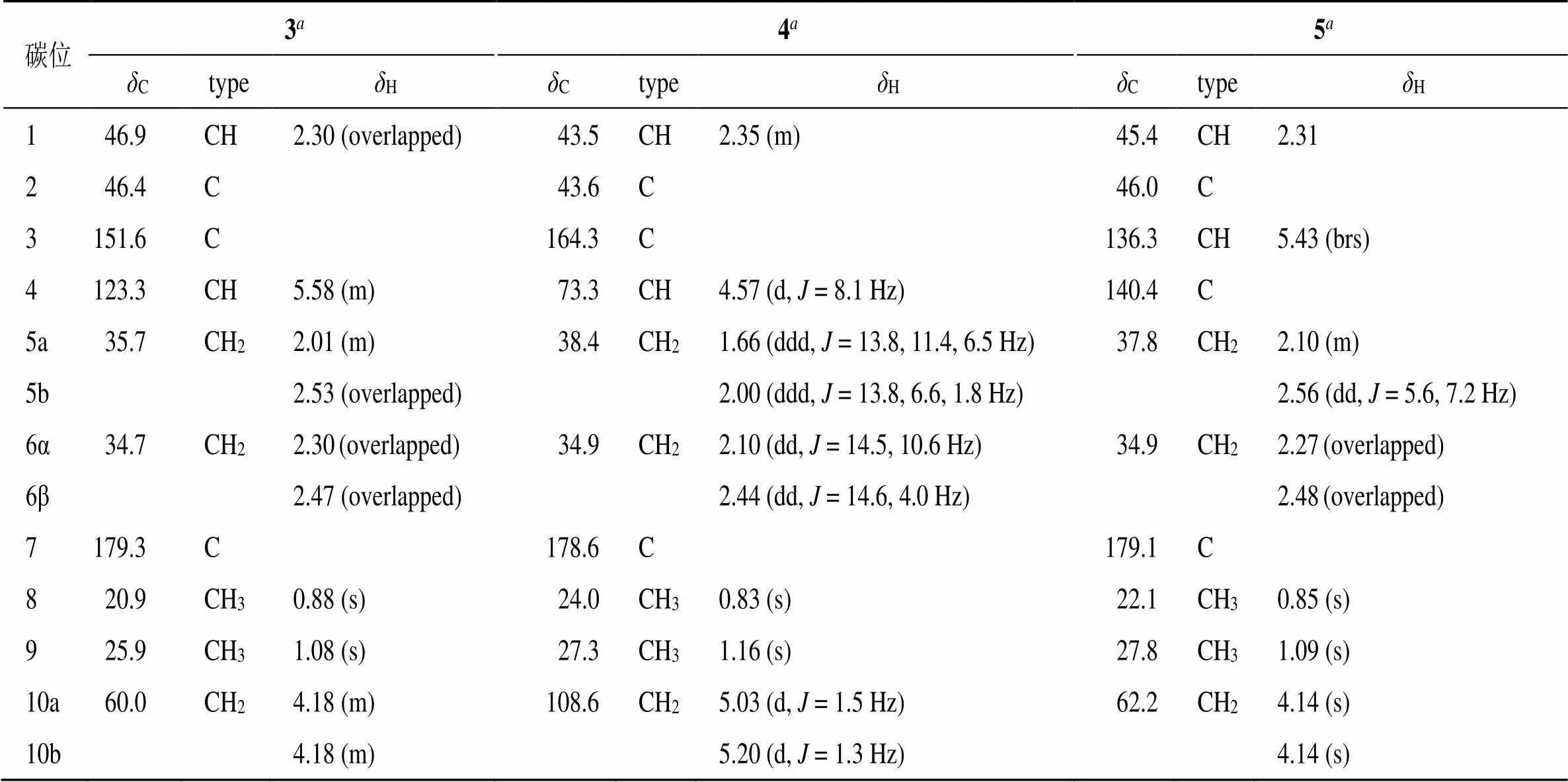
表2 化合物3~5的1H-NMR 和13C-NMR数据(400/100 MHz)

图4 化合物3的关键1H-1H COSY和HMBC相关
化合物4:无色油状物,HR-ESI-MS/202.143 5 [M+NH4]+(计算值202.143 8,C10H20NO3)推断其分子式为C10H16O3,不饱和度为3。1H-NMR(表2)显示有2个甲基单峰信号H0.83 (3H, s, H-8), 1.16 (3H, s, H-9),1个环外亚甲基,2个质子的特征信号H5.03 (1H, d,= 1.5 Hz, H-10a), 5.20 (1H, d,= 1.5 Hz, H-10b),2个次甲基,其中1个为连氧次甲基信号H4.57 (1H, d,= 8.1 Hz, H-4),以及2个亚甲基信号。13C-NMR(表2)结合DEPT示有10个碳信号,包括1个羰基碳C178.6 (C-7),环外双键碳C164.3 (C-3), 108.6 (C-10),2个甲基碳C27.3 (C-9), 24.0 (C-8),2个亚甲基碳C38.4 (C-5), 34.9 (C-6),2个次甲基碳(其中1个为连氧次甲基碳)43.5 (C-1), 73.3 (C-4),1个季碳C43.6 (C-2)。上述数据结合不饱和度表明化合物4为具有羧基和环外双键的单环单萜类化合物。化合物4的1H-1H COSY波谱显示-CH(C-4)-CH2(C-5)-CH2(C-6)-CH(C-1)-片段。在化合物4的HMBC谱中,Me-8和Me-9与C-1、C-2和C-3相关,H-10与C-2、C-3、C-4相关,综合上述信息,推断出化合物4为2,2-二甲基-3-亚甲基-4-羟基环己烷-1-甲酸。在NOESY谱中,H-1与Me-9相关,H-4与Me-8相关,表明H-1和H-4不在同一平面,将H-1定为α取向,则H-4为β取向。化合物4的绝对构型由实验与计算的ECD(图2)确定为(1,4),最终鉴定化合物4为(1,4)-2,2-二甲基-3-亚甲基-4-羟基环己烷-1-甲酸,结构如图5所示,命名为裸花紫珠烷D1。

图5 化合物4的关键1H-1H COSY、HMBC和NOESY相关
化合物5:黄色油状物;通过HR-ESI-MS/207.098 8 [M+Na]+(计算值207.099 2,C10H16O3Na)确定其分子式为C10H16O3,不饱和度为3。它的1H-和13C-NMR(表2)数据与化合物3的基本一致,均可见1个羧基、2个甲基、1个羟甲基及1个环己烯基团。比较二者1H-1H COSY,化合物3给出的是-C4-C5-C6-C1-连接片段,而化合物5给出的是-C5-C6-C1-连接片段,表明C-4位的烯碳在化合物3中为次甲基,而在化合物5中为季碳,说明化合物5的C-4有取代基团。化合物5的HMBC中,H-10与C-3、C-4、C-5相关,进一步证实羟甲基连接在C-4位。与化合物3一样,化合物5的绝对构型(1)也由ECD光谱确定(图2),最终确定化合物5的结构为(1)-2,2-二甲基,4-羟甲基-3-环己烯-1-甲酸,结构如图6所示,鉴定为裸花紫珠烷E1。

图6 化合物5的关键1H-1H COSY和HMBC相关
化合物6:黄色针状晶体(甲醇);1H-NMR (400 MHz, CDCl3): 5.85 (2H, s, H-3, 5), 3.82 (6H, s, 2, 6-OCH3);13C-NMR (100 MHz, CDCl3):187.0 (C-4), 176.8 (C-1), 157.4 (C-2, 6), 107.6 (C-3, 5), 56.6 (2, 6-OCH3)。以上数据与文献进行对比[8],确定化合物6为2,6-二甲氧基-对-苯醌。
化合物7:黄色油状物;1H-NMR (400 MHz, CDCl3): 4.73 (2H, s, H-9), 3.64 (1H, t,= 3.6 Hz, H-2), 2.27 (1H, m, H-4), 1.93 (1H, m, H-3a), 1.78 (1H, overlapped, H-5a), 1.73 (3H, s, H-10), 1.67 (1H, t,= 4.0 Hz, H-3b), 1.57 (3H, overlapped, H-5b, 6a, 6b), 1.27 (3H, s, 7-Me);13C-NMR (100 MHz, CDCl3): 149.5 (C-8), 109.1 (C-9), 74.1 (C-2), 71.5 (C-1), 37.6 (C-4), 34.2 (C-3), 33.8 (C-6), 26.8 (C-7), 26.3 (C-5), 21.2 (C-10)。以上数据与文献报道一致[9],鉴定化合物7为对薄荷-8-烯-1,2-二醇。
化合物8:黄色油状物;1H-NMR (400 MHz, CDCl3): 5.61 (1H, q,= 2.0 Hz, H-7), 3.97 (1H, d,= 12.0 Hz, H-1a), 3.53 (1H, d,= 12.1 Hz, H-1b), 3.07 (1H, m, H-5), 2.93 (1H, m, H-4a), 2.67 (1H, m, H-6a), 2.33 (1H, d,= 5.7 Hz, H-4b), 2.12 (1H, dq,= 17.2, 2.3 Hz, H-6b), 1.72 (3H, q,= 2.1 Hz, 10-Me);13C-NMR (100 MHz, CDCl3): 177.7 (C-3), 137.6 (C-8), 130.5 (C-7), 101.2 (C-9), 64.1 (C-1), 38.0 (C-5), 37.7 (C-4), 37.7 (C-6), 12.5 (C-10)。以上数据与文献报道一致[10],鉴定化合物8为天目地黄素B。
化合物9:黄色油状物;1H-NMR (400 MHz, CDCl3): 4.87 (1H, dd,= 6.8, 2.0 Hz, H-1), 4.03 (1H, dd,= 12.2, 6.4 Hz, H-7a), 3.71 (1H, td,= 12.4, 3.9 Hz, H-7b), 2.78 (1H, d,= 18.0 Hz, H-4a), 2.55 (1H, overlapped, H-4b), 2.51(1H, overlapped, H-9a), 2.30 (1H, dt,= 12.8, 6.4 Hz, H-6a), 2.23 (1H, dd,= 14.9, 2.1 Hz, H-9b), 1.52 (3H, s, 10-Me), 1.49 (1H, overlapped, H-6b);13C-NMR (100 MHz, CDCl3): 174.7 (C-3), 107.9 (C-8), 86.1 (C-5), 84.4 (C-1), 60.1 (C-7), 42.9 (C-9), 39.4 (C-4), 29.9 (C-6), 24.1 (C-10)。以上数据与文献报道一致[11],鉴定化合物9为北玄参素G。
化合物10:白色无定形粉末;1H-NMR (400 MHz, CD3OD): 7.00 (1H, m, H-2), 2.47 (1H, dt,= 17.4, 4.7, 2.3 Hz, H-7a), 2.33 (1H, m, H-3a), 2.11 (1H, m, H-7b), 2.01 (1H, overlapped, H-6a), 1.98 (1H, overlapped, H-3b), 1.53 (1H, m, H-4), 1.21 (1H, dd,= 12.4, 5.1 Hz, H-6b), 1.17 (6H, s, 8, 9-Me);13C-NMR (100 MHz, CD3OD): 170.8 (C-10), 140.9 (C-2), 131.2 (C-1), 72.7 (C-5), 45.2 (C-4), 28.3 (C-3), 26.9 (C-8), 26.4 (C-7), 26.1 (C-9), 24.3 (C-6)。以上数据与文献对照[12],鉴定化合物10为黄牡丹醇B。
化合物11:无色油状物;1H-NMR (400 MHz, CD3OD): 6.74 (1H, t,= 1.8 Hz, H-2), 4.31 (1H, dt,= 9.8, 2.1 Hz, H-7), 2.39 (1H, dd,= 16.0, 3.8 Hz, H-5a), 2.28~2.11 (2H, overlapped, H-4, 5b), 1.93 (1H, m, H-6), 1.76 (1H, t,= 1.6 Hz, H-8), 0.98 (1H, d,= 7.1 Hz, H-10), 0.92 (1H, d,= 6.9 Hz, H-9);13C-NMR (100 MHz, CD3OD): 202.5 (C-1), 152.1 (C-2), 135.6 (C-3), 69.6 (C-7), 51.4 (C-6), 37.4 (C-5), 27.4 (C-4), 21.0 (C-10), 16.9 (C-9), 15.5 (C-8)。以上数据与文献对照[13],鉴定化合物11为香桂酮。
化合物12:黄色油状物;1H-NMR (400 MHz, CDCl3): 6.87 (1H, t-like,= 7.4 Hz, H-3), 5.44 (1H, t-like,= 6.9 Hz, H-7), 4.18 (2H, d,= 6.8 Hz, H-8), 2.34 (2H, q,= 7.6 Hz, H-4), 2.17 (2H, t,= 7.6 Hz, H-5), 1.84 (3H, brs, 9-Me), 1.70 (3H, brs, 10-Me);13C-NMR (400 MHz, CDCl3): 173.2 (C-1), 144.1 (C-3), 138.4 (C-6), 127.6 (C-2), 124.2 (C-7), 59.3 (C-8), 38.0 (C-5), 27.2 (C-4), 16.3 (C-10), 12.2 (C-9)。以上数据与文献对比[14],鉴定化合物12为8-羟基- 2,6-二甲基-(2,6)-辛二烯酸。
化合物13:黄色油状物;1H-NMR (400 MHz, CDCl3): 6.88 (1H, t-like,= 7.5 Hz, H-3), 3.69 (2H, m, H-8), 2.19 (2H, qt,= 14.2, 7.8 Hz, H-4), 1.82 (3H, s, H-9), 1.62 (2H, overlapped, H-6, 7a), 1.45 (2H, overlapped, H-5a, 7b), 1.30 (1H, m, H-5b), 0.92 (3H, d,= 6.3 Hz, H-10);13C-NMR (100 MHz, CDCl3): 173.3 (C-1), 145.1 (C-3), 127.2 (C-2), 61.0 (C-8), 39.6 (C-7), 35.7 (C-5), 29.4 (C-6), 26.5 (C-4),19.5 (C-10), 12.1 (C-9)。以上数据与文献对比[15],鉴定化合物13为8-羟基-2,6-二甲基-(2)-辛烯酸。
化合物14:无色油状物;1H-NMR (400 MHz, CD3OD): 4.77 (1H, q,= 1.7 Hz, H-17a), 4.57 (1H, q,= 1.7 Hz, H-17b), 2.49 (1H, overlapped, H-2), 2.43 (1H, overlapped, H-7a), 2.08 (1H, td,= 13.0, 5.2 Hz, H-7b), 1.99 (1H, overlapped, H-18a), 1.96 (1H, overlapped, H-6a), 1.95 (1H, overlapped, H-9), 1.90 (1H, overlapped, H-1a), 1.53 (1H, t,= 12.9 Hz, H-18b ), 1.46 (1H, dd,= 12.6, 2.6 Hz, H-5), 1.34 (1H, td,= 12.7, 4.2 Hz, H-6b), 1.25 (1H, t,= 12.9 Hz, H-1b), 1.13 (3H, s, 19-Me), 0.96 (3H, d,= 6.8 Hz, 11-Me), 0.70 (3H, s, 20-Me);13C-NMR (100 MHz, CD3OD): 179.8 (C-3), 151.8 (C-8), 107.4 (C-17), 72.9 (C-4), 57.1 (C-5), 51.2 (C-9), 45.9 (C-18), 42.7 (C-1), 40.3 (C-10), 39.3 (C-2), 38.0 (C-7), 23.8 (C-6), 23.3 (C-19), 13.6 (C-20), 11.0 (C-11)。以上数据与文献报道一致[5],鉴定化合物14为裸花紫珠烷。
化合物15:无色针状晶体(二氯甲烷-甲醇);1H-NMR (400 MHz, CDCl3): 3.79 (1H, dd,= 10.2, 5.7 Hz, H-2), 3.32 (1H, s, H-9), 1.98 (1H, m, H-10a), 1.70 (2H, overlapped, H-3a, 11a), 1.64 (1H, overlapped, H-10b), 1.53 (2H, overlapped, H-3b, 12a), 1.44 (1H, overlapped, H-7a), 1.40 (1H, overlapped, H-5), 1.37 (1H, overlapped, H-6a), 1.29 (1H, m, H-6b), 1.11 (1H, overlapped, H-7b), 1.06 (1H, overlapped, H-11b), 1.03 (3H, s, 14-Me), 0.95 (3H, s, 15-Me), 0.90 (1H, d,= 13.7 Hz, H-12b) 0.85 (3H, s, H-13);13C-NMR (100 MHz, CDCl3): 81.0 (C-2), 75.3 (C-9), 50.7 (C-5), 47.6 (C-3), 44.3 (C-1), 37.2 (C-4), 35.6 (C-12), 34.8 (C-8), 33.2 (C-7), 31.5 (C-14), 28.5 (C-15), 26.5 (C-11), 26.1 (C-10), 25.5 (C-13), 20.8 (C-6)。以上数据与文献报道一致[16],鉴定化合物15为丁子香烷-2β,9α-二醇。
化合物16:无色针状晶体(二氯甲烷-甲醇);1H-NMR (400 MHz, CDCl3): 3.45 (1H, t,= 3.3 Hz, H-9), 2.23 (1H, m, H-2), 2.05 (1H, m, H-10a), 1.90 (1H, m, H-5), 1.79 (1H, m, H-10b), 1.66 (1H, td,= 12.4, 5.3 Hz, H-11a), 1.17 (1H, m, H-7b), 1.60~1.47 (5H, overlapped, H-3a, 3b, 6a, 6b, 11b), 1.46~1.36 (3H, overlapped, H-7a, 12a, 12b), 1.17 (1H, m, H-7b), 1.03 (3H, s, 14-Me), 1.01 (3H, s, 13-Me), 0.94 (3H, s, 15-Me);13C-NMR (100 MHz, CDCl3): 72.4 (C-9), 70.9 (C-1), 44.1 (C-5), 42.6 (C-12), 39.5 (C-8), 38.3 (C-2), 35.6 (C-7), 35.2 (C-4), 34.2 (C-3), 33.6 (C-11), 30.7 (C-14), 28.3 (C-10), 26.8 (C-15), 21.0 (C-13), 20.6 (C-6)。以上数据与文献对照[17],鉴定化合物16为丁香烷-1,9β-二醇。
化合物17:无色针状晶体(甲醇);1H-NMR (400 MHz, CD3OD): 3.45 (1H, dd,= 9.4, 7.8 Hz, H-9), 2.13 (1H, m, H-2), 2.00 (1H, m, H-10a), 1.84~1.72 (4H, overlapped, H-5, 6a, 6b, 10b), 1.65(1H, m, H-11a), 1.51 (1H, dd,= 9.6, 7.9 Hz, H-3a), 1.47~1.37 (3H, overlapped, H-7a, 12a, 12b), 1.36 (1H, overlapped, H-3b), 1.28 (1H, m, H-11b), 1.05 (1H, overlapped, H-7b), 1.03 (3H, s, 14-Me), 1.02 (3H, s, 13-Me), 0.83 (3H, s, 15-Me);13C-NMR (100 MHz, CD3OD): 79.6 (C-9), 77.4 (C-8), 49.1 (C-12), 46.6 (C-5), 39.2 (C-2), 38.7 (C-11), 36.8 (C-3), 35.8 (C-4), 34.0 (C-1), 33.3 (C-7), 31.0 (C-15), 29.9 (C-10), 26.6 (C-13), 21.8 (C-14), 21.1 (C-6)。以上数据与文献对照[18],鉴定化合物17为(8,9)-异丁香烷-8,9-二醇。
化合物18:黄色油状物;1H-NMR (400 MHz, CDCl3): 6.83 (1H, d,= 15.7 Hz, H-7), 6.45 (1H, d,= 15.7 Hz, H-8), 5.93 (1H, s, H-4), 2.47(1H, m, H-2a), 2.34 (1H, d,= 1.1 Hz, H-2b), 2.29 (3H, s, 10-Me), 1.87 (3H, d,= 1.4 Hz, 11-Me), 1.08 (3H, s, 13-Me), 1.00 (3H, s, 12-Me);13C-NMR (100 MHz, CDCl3): 197.8 (C-9), 197.4 (C-3), 161.1 (C-5), 145.4 (C-7), 130.5 (C-8), 127.7 (C-4), 79.3 (C-6), 49.7 (C-2), 41.6 (C-1), 28.4 (C-10), 24.5 (C-13), 23.1 (C-12), 18.9 (C-11)。以上数据与文献数据[19]对比,鉴定化合物18为()-(+)-去氢催吐萝芙叶醇。
化合物19:无色油状物;1H-NMR (400 MHz, CDCl3): 7.00 (1H, d,= 15.6 Hz, H-7), 6.25 (1H, d,= 15.6 Hz, H-8), 3.86 (1H, m, H-3), 2.35 (1H, ddd,= 14.4, 5.1, 1.7 Hz, H-4a), 2.25 (3H, s, H-10), 1.64 (1H, m, H-4b), 1.59 (1H, m, H-2a), 1.23 (1H, m, H-2b), 1.16 (6H, s, 11, 13-Me), 0.94 (3H, s, 12-Me);13C-NMR (100 MHz, CDCl3): 197.7 (C-9), 142.7 (C-7), 132.6 (C-8), 69.6 (C-6), 67.4 (C-5), 63.9 (C-3), 46.7 (C-4), 40.6 (C-2), 35.2 (C-1), 29.4 (C-11), 28.3 (C-10), 25.0 (C-12), 19.9 (C-13)。以上数据与文献对照[20],鉴定化合物19为(3,5,6,7)-5,6-环氧-3-羟基-7-大柱香波龙烯-9-酮。
化合物20:黄色油状物;1H-NMR (400 MHz, CDCl3): 7.80 (1H, d,= 16.0 Hz, H-4), 6.16 (1H, d,= 16.1 Hz, H-5), 5.97 (1H, brs, H-8), 5.74 (1H, brs, H-2), 2.48 (1H, d,= 17.2 Hz, H-10a), 2.28(1H, d,= 17.2 Hz, H-10b), 2.03 (3H, d,= 1.3 Hz, 15-Me), 1.92 (3H, d,= 1.4 Hz, 14-Me), 1.10 (3H, s, Me-12), 1.02 (3H, s, 13-Me);13C-NMR (100 MHz, CDCl3): 198.5 (C-9), 171.0 (C-1), 163.2 (C-3), 151.7 (C-7), 137.0 (C-5), 128.4 (C-4), 127.1 (C-8), 118.1 (C-2), 80.0 (C-6), 49.8 (C-10), 41.8 (C-11), 24.4 (C-14), 23.2 (C-13), 21.5 (C-15), 19.2 (C-12)。以上数据与文献对照[21],鉴定化合物20为脱落酸。
化合物21:黄色针状晶体(甲醇);1H-NMR (400 MHz, CDCl3): 12.17(1H, s, 5-OH), 7.75 (1H, dd,= 7.4, 1.2 Hz, H-8), 7.61( 1H, dd,= 8.5, 7.5 Hz, H-7), 7.26 (1H, dd,= 8.4, 1.2 Hz, H-6), 6.81 (1H, s, H-11), 1.69 (6H, s, 14, 15-Me);13C-NMR (100 MHz, CDCl3): 186.8 (C-4), 172.8 (C-1), 168.4 (C-12), 162.4 (C-5), 152.0 (C-2), 136.4 (C-7), 132.9 (C-9), 131.2 (C-3), 125.4 (C-6), 120.1 (C-8), 115.3 (C-10), 102.4 (C-11), 69.6 (C-13), 28.9 (C-14, 15)。以上数据与文献报道一致[22],鉴定化合物21为紫珠醌B。
化合物22:黄色油状物;1H-NMR (400 MHz, CDCl3): 5.46 (2H, overlapped, H-9, 10), 3.70 (2H, t,= 6.1 Hz, H-12), 2.65 (1H, m, H-2a), 2.50~2.22 (8H, overlapped, H-2b, 3, 4a, 5a, 8a, 8b, 11a, 11b), 2.12 (1H, m, H-5b), 1.94 (1H, m, H-7), 1.53 (1H, m, H-4b);13C-NMR (100 MHz, CDCl3): 219.2 (C-6), 176.0 (C-1), 129.0 (C-9), 128.5 (C-10), 62.4 (C-12), 54.5 (C-7), 39.0 (C-2), 38.0 (C-5), 37.9 (C-3), 30.9 (C-11), 27.6 (C-4), 25.6 (C-8)。以上数据与文献报道一致[23],鉴定化合物22为12-羟基茉莉酸。
化合物23:黄色油状物;1H-NMR (00 MHz, CDCl3)5.45 (2H, m, H-9, 10), 3.68 (3H, s, 13-Me), 3.64 (2H, t,= 6.3 Hz, H-12), 2.68 (1H, m, H-2a), 2.47~2.17 (8H, overlapped, H-2b, 3, 4a, 5a, 8a, 8b, 11a, 11b), 2.10 (1H, m, H-5b), 1.91 (1H, m, H-7), 1.48 (1H, m, H-4b);13C-NMR (100 MHz, CDCl3): 219.3 (C-6), 172.8 (C-1), 128.6 (C-9), 128.4 (C-10), 62.2 (C-12), 54.1 (C-7), 51.9 (C-13), 38.9 (C-2), 37.9 (C-5), 37.9 (C-3), 31.0 (C-11), 27.4 (C-4), 25.5 (C-8)。以上数据与文献对比[24],鉴定化合物23为(−)-12-羟基茉莉酸甲酯。
化合物24:白色无定形粉末;1H-NMR (400MHz, CDCl3):5.27 (1H, brs, H-12), 3.22 (1H, dd,= 11.0, 4.7 Hz, H-3α), 2.81 (1H, dd,= 13.9, 4.6 Hz, H-18β), 1.13 (3H, s, 27-Me), 0.98 (3H, s, 23-Me), 0.92 (3H, s, 29-Me), 0.91 (3H, s, 24-Me), 0.90 (3H, s, 30-Me), 0.77 (3H, s, 25-Me), 0.74 (3H, s, 26-Me);13C-NMR (100 MHz, CDCl3):183.7 (C-28), 143.7 (C-13), 122.8 (C-12), 79.2 (C-3), 55.3 (C-5), 47.8 (C-9), 46.7 (C-19), 46.0 (C-17), 41.7 (C-14), 41.1 (C-18), 39.4 (C-8), 38.9 (C-4), 38.5 (C-1), 37.2 (C-10), 33.9 (C-21), 33.2 (C-30), 32.7 (C-22), 32.6 (C-7), 30.8 (C-20), 28.2 (C-23), 27.8 (C-15), 27.3 (C-2), 26.1 (C-27), 23.7 (C-29), 23.5 (C-16), 23.0 (C-11), 18.4 (C-6), 17.3 (C-26), 15.7 (C-25), 15.5 (C-24)。以上数据与文献对比[25],鉴定化合物24为齐墩果酸。
化合物25:白色无定形粉末;1H-NMR (400 MHz, CD3OD): 5.25 (1H, t,= 3.7 Hz, H-12), 3.17 (1H, dd,= 11.1, 4.9 Hz, H-3), 2.23 (1H, d,= 11.3Hz, H-18), 1.14 (3H, s, 23-Me), 1.00 (3H, s, 29-Me), 0.99 (3H, s, 27-Me), 0.98 (3H, s, 26-Me), 0.90 (3H, d,= 6.4 Hz, 30-Me), 0.87 (3H, s, 24-Me), 0.79 (3H, s, 25-Me);13C-NMR (100 MHz, CD3OD):139.7 (C-13), 126.8 (C-12), 79.7 (C-3), 56.7 (C-5), 54.4 (C-18), 49.8 (C-17), 43.3 (C-14), 40.8 (C-4), 40.5 (C-19), 40.4 (C-20), 40.0 (C-1), 39.8 (C-8), 38.2 (10), 38.1 (C-22), 34.3 (C-7), 31.8 (C-21), 29.2 (C-2), 28.8 (C-23), 27.9 (C-15), 25.4 (C-16), 24.4 (C-27), 24.1 (C-11), 21.6 (C-30), 19.5 (C-6), 17.8 (C-29), 17.7 (C-24), 16.4 (C-26), 16.0 (C-25)。以上数据与文献中熊果酸比对[26],发现氢谱一致,化合物25的碳谱比熊果酸少了1个羰基信号,经TLC多个体系展开与对照品的f值均一致,故鉴定化合物25为熊果酸。
化合物26:白色无定形粉末;1H-NMR (400 MHz, CD3OD): 5.30 (1H, s, H-12), 3.93 (1H, ddd,= 12.0, 4.4, 2.8 Hz, H-2), 3.33 (1H, d,= 2.9 Hz, H-3), 2.59 (1H, td,= 14.4, 13.2, 5.8 Hz, H-16a), 2.50 (1H, s, H-18), 1.35 (3H, s, 29-Me), 1.20 (3H, s, 27-Me), 0.99 (6H, s, 26-Me), 0.93 (3H, d,= 6.6 Hz, 25-Me), 0.87 (3H, s, 24-Me), 0.79 (3H, s, 23-Me);13C-NMR (100 MHz, CD3OD): 182.3 (C-28), 140.0 (C-13), 129.3 (C-12), 80.1 (C-3), 73.6 (C-19), 67.2 (C-2), 55.1 (C-18), 49.3 (C-5), 49.3 (C-17), 48.2 (C-9), 43.1 (C-20), 42.7 (C-14), 42.5 (C-1), 41.2 (C-4), 39.5 (C-10), 39.4 (C-8), 39.0 (C-22), 34.1 (C-7), 29.6 (C-15), 29.2 (C-23), 27.3 (C-11), 27.1 (C-27), 26.6 (C-16), 24.9 (C-29), 24.7 (C-6), 22.5 (C-24), 19.3 (C-21), 17.5 (C-25), 16.9 (C-30), 16.6 (C-26)。以上数据与文献对比[27],鉴定化合物26为蔷薇酸。
化合物27:黄色针状晶体(石油醚-醋酸乙酯);1H-NMR (400 MHz, CDCl3): 12.63 (1H, s, 5-OH), 7.67 (1H, overlapped, H-2′), 7.64 (1H, overlapped, H-6′), 7.02 (1H, d,= 8.4 Hz, H-5′), 6.41 (1H, d,= 2.0 Hz, H-8), 6.32(1H, d,= 2.0 Hz, H-6), 5.27 (1H, s, 4′-OH), 3.96 (3H, s, 3′-OCH3), 3.85 (3H, s, 7-OCH3), 3.83 (3H, s, 3-OCH3);13C-NMR (100 MHz, CDCl3): 178.9 (C-4), 165.6 (C-7), 162.2 (C-9), 156.9(C-5), 156.1 (C-2), 148.6 (C-4′), 146.6 (C-3′), 139.0 (C-3), 122.9 (C-6′), 122.6 (C-1′), 114.8 (C-5′), 111.1 (C-2′), 106.2 (C-10), 98.1 (C-6), 92.4 (C-8), 60.4 (3-OCH3), 56.3 (7-OCH3), 56.0 (3′-OCH3)。以上数据与文献对比[28],鉴定化合物27为5,4-二羟基-3,7,3-三甲氧基黄酮。
化合物28:黄色针状晶体(石油醚-醋酸乙酯);1H-NMR (400 MHz, CD3OD): 7.53 (1H, s, H-4′), 7.45 (1H, d,= 8.3 Hz, H-6′), 7.38 (1H, s, H-3), 6.94 (1H, d,= 8.4 Hz, H-5′), 6.56 (2H, overlapped, H-2′, 8), 6.33 (1H, d,= 2.0 Hz, H-6), 3.96 (3H, s, 7-OMe), 3.88 (3H, s, 3′-OMe);13C-NMR (100 MHz, CD3OD): 183.2 (C-4), 166.4 (C-7), 165.7 (C-2), 162.1 (C-5), 158.5 (C-9), 151.3 (C-4′), 148.7 (C-3′), 123.0 (C-1′), 121.3 (C-6′), 116.3 (C-5′), 109.9 (C-2′), 105.8 (C-10), 104.1 (C-3), 98.9 (C-6), 93.2 (C-8), 56.4 (7-OCH3), 56.2 (3′-OCH3)。以上数据与文献报道一致[29],鉴定化合物28为毡毛美洲茶素。
化合物29:黄色针状晶体(二氯甲烷);1H-NMR (400 MHz, Pyr-5): 13.83 (1H, s, OH-5), 7.67 (1H, dd,= 8.3, 2.1 Hz, H-6′), 7.62 (1H, d,= 2.1 Hz, H-2′), 7.29 (1H, d,= 8.3 Hz, H-5′), 6.99 (1H, s, H-3), 6.88 (1H, d,= 2.0 Hz, H-6), 6.78 (1H, d,= 2.0 Hz, H-8), 3.83 (3H, s, 3′-OMe);13C-NMR (100 MHz, Pyr-5): 183.1 (C-4), 166.3 (C-7), 164.9 (C-2), 163.5 (C-9), 158.9 (C-5), 152.8 (C-4′), 149.3 (C-3′), 122.9 (C-1′), 121.7 (C-6′), 117.3 (C-5), 110.7 (C-2′), 105.4 (C-10), 104.6 (C-3), 100.4 (C-6), 95.3 (C-8), 56.4 (3′-OMe)。以上数据与文献报道一致[30],鉴定化合物29为5,7,4′-三羟基-3′-甲氧基黄酮。
化合物30:黄色油状物;1H-NMR (400 MHz, CDCl3): 6.97~6.83 (2H, overlapped, H-2, 5), 6.80 (1H, dd,= 8.1, 2.0 Hz, H-6), 5.74 (1H, s, 4-OH), 4.61 (1H, d,= 6.9 Hz, H-2), 4.49 (1H, dd,= 9.8, 6.8 Hz, H-8a), 4.35 (1H, overlapped, H-4a), 4.31 (1H, overlapped, H-8b), 4.17 (1H, dd,= 9.3, 3.8 Hz, H-4b), 3.90 (3H, s, 3-OCH3), 3.44 (1H, m, H-5), 3.12 (1H, m, H-1);13C-NMR (100 MHz, CDCl3):178.3 (C-6), 147.1 (C-3), 146.0 (C-4), 130.7 (C-1), 119.2 (C-6), 114.6 (C-5), 108.6 (C-2), 86.2 (C-2), 70.1 (C-4), 70.0 (C-8), 56.1 (3-OMe), 48.3 (C-5), 46.1 (C-1)。以上数据与文献对比[31],鉴定化合物30为柳叶柴胡酚。
化合物31:黄色油状物;1H-NMR (400 MHz, CDCl3): 7.62 (1H, d,= 9.4 Hz, H-4), 7.39 (1H, d,= 8.6 Hz, H-5), 6.87 (1H, d,= 8.6 Hz, H-6), 6.25 (1H, d,= 9.5 Hz, H-3), 5.30 (1H, d,= 8.4 Hz, H-1′), 4.64 (1H, s, H-4′a), 4.58 (1H, s, H-4′b), 4.52 (1H, d,= 8.3 Hz, H-2′), 3.96 (3H, s, 7-OCH3), 1.77 (3H, s, H-5′);13C-NMR (100 MHz, CDCl3): 160.3 (C-2), 160.2 (C-7), 153.0 (C-9), 143.9 (C-4), 143.9 (C-3′), 128.7 (C-5), 116.1 (C-8), 113.9 (C-10), 113.6 (C-4′), 113.2 (C-3), 107.9 (C-6), 78.5 (C-2′), 69.7 (C-1′), 56.4 (7-OCH3), 17.5 (C-5′)。以上数据与文献对比[32],鉴定化合物31为九里香亭。
化合物32:黄色油状物;1H-NMR (400 MHz, CDCl3): 9.64 (1H, d,= 7.7 Hz, H-9), 7.37 (1H, d,= 15.8 Hz, H-7), 6.80 (2H, s, H-2, 6), 6.60 (1H, dd,= 15.8, 7.7 Hz, H-8), 5.99 (1H, s, 4-OH), 3.92 (6H, s, 3, 5-OCH3);13C-NMR (100 MHz, CDCl3): 193.6 (C-9), 153.4 (C-7), 147.5 (C-3, 5), 138.2 (C-4), 126.8 (C-8), 125.6 (C-1), 105.7 (C-2, 6), 56.5 (3,5-OCH3)。以上数据与文献对比[33],鉴定化合物32为芥子醛。
化合物33:黄色油状物;1H-NMR (400 MHz, CDCl3): 9.83 (1H, s, 1-CHO), 7.43 (1H, overlapped, H-6), 7.42 (1H, overlapped, H-2), 7.04 (1H, d,= 8.5 Hz, H-5), 3.97 (3H, s, 3-OCH3);13C-NMR (100 MHz, CDCl3): 191.3 (1-CHO), 152.0 (C-4), 147.5 (C-3), 130.2 (C-1), 127.9 (C-6), 114.7 (C-5), 109.1 (C-2), 56.5 (3-OCH3)。以上数据与文献报道一致[34],鉴定化合物33为香草醛。
化合物34:无色针状晶体(二氯甲烷-甲醇);1H-NMR (400 MHz, CD3OD): 7.32 (2H, s, H-2, 6), 3.88 (6H, s, 3, 5-OCH3);13C-NMR (100 MHz, CD3OD): 169.9 (C-7), 148.8 (C-3, 5), 141.7 (C-4), 121.8 (C-1), 108.2 (C-2, 6), 56.7 (3, 5-OCH3)。以上数据与文献报道一致[35],鉴定化合物34为丁香酸。
4 体外抗HepG2细胞增殖活性筛选
HepG2细胞培养于含10%胎牛血清、100 U/mL青霉素和100 U/mL链霉素的DMEM培养基中,置于37 ℃、5% CO2细胞培养箱中培养至细胞达到90%融合状态,消化接种于96微孔板,每孔8000个细胞,置培养箱中孵育12 h后,设置对照组、PTX组及实验组,分别加入100 μL DMEM培养基、PTX及待测化合物,每组5个复孔,给药后继续放入培养箱中孵育24 h后取出,用吸液泵吸去孔内上清液后,向每孔中加入100 μL 10% CCK-8试剂的DMEM培养基,在细胞培养箱中共同孵育30 min。重复3次实验。使用酶标仪在450 nm处检测吸光度()值,并计算细胞存活率。结果(图7)显示,化合物4在25 μmol/L时细胞存活率约为50%。采用SPSS 20.0软件计算IC50值,得化合物4的IC50为24.0 μmol/L。
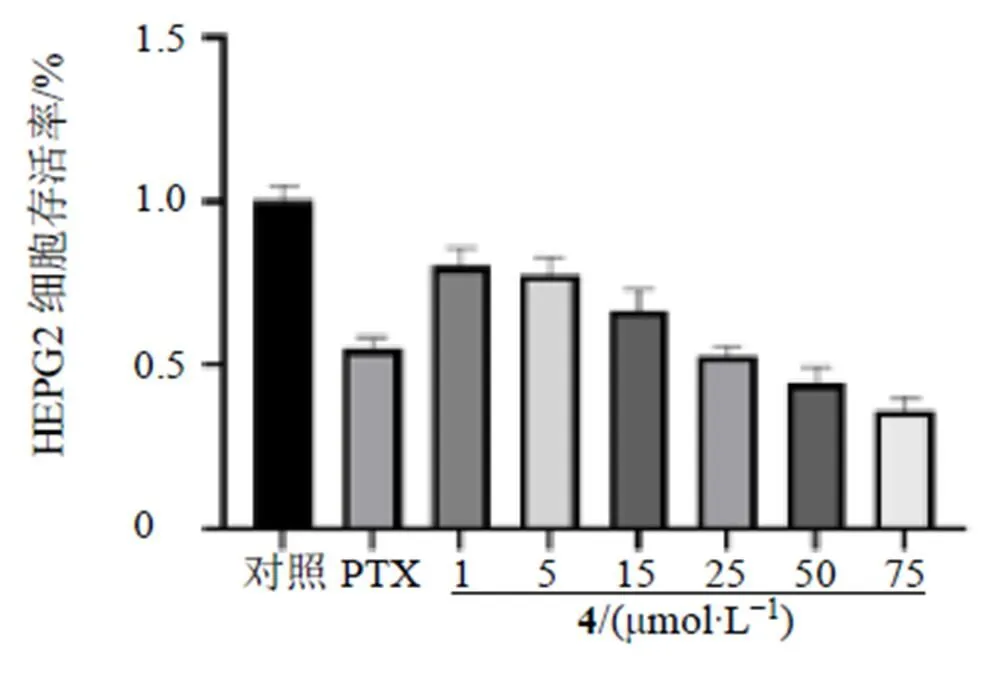
图7 化合物4对HepG2细胞活性的影响
5 讨论
本研究报道了裸花紫珠中的34个化合物,包括5个新化合物和22个首次从裸花紫珠中报道的化合物。化合物类型以萜类成分为主,共25个,表明裸花紫珠中的萜类成分值得进一步关注。本研究结果不仅丰富了裸花紫珠的化学成分和信息,也可为裸花紫珠的进一步开发利用提供一定的依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 378.
[2] 王祝年, 韩壮, 崔海滨, 等. 裸花紫珠的化学成分 [J]. 热带亚热带植物学报, 2007, 15(4): 359-362.
[3] 康兴东, 叶阳. 裸花紫珠化学成分、药理活性及临床应用研究进展 [J]. 特产研究, 2021, 43(4): 95-101.
[4] 周志强. 裸花紫珠化学成分的研究 [D]. 南昌: 南昌大学, 2013.
[5] Yu Z X, Wang C H, Nong X H,. Callnudoids A-H: Highly modified labdane diterpenoids with anti- inflammation from the leaves of[J]., 2022, 201: 113253.
[6] Reynolds M. Composition of monoterpenoids having bactericidal properties: US9023888 [P]. 2015-05-05.
[7] van Tamelen E E, Judd C I. Reactivity of 7-substituted camphenes. structure of β-isocamphor [J]., 1958, 80(23): 6305-6312.
[8] 胡疆, 张卫东, 柳润辉, 等. 两面针的化学成分研究 [J]. 中国中药杂志, 2006, 31(20): 1689-1691.
[9] 李永利. 三种冷杉属植物的化学成分与生物活性研究 [D]. 上海: 上海交通大学, 2013.
[10] Liu Y F, Shi G R, Wang X,. Nine new compounds from the whole plants of[J]., 2016, 18(6): 509-519.
[11] Lin S J, Jiang S H, Li Y M,. Two novel iridoids from[J]., 2000, 41(7): 1069-1071.
[12] 李红亮, 李俊, 赵海清, 等. 新疆千叶蓍中化学成分及其抗氧化和抗菌活性研究 [J]. 天然产物研究与开发, 2019, 31(1): 122-128.
[13] 田云刚, 郭洪伟, 刘一涵, 等. 白头婆花化学成分的分离与鉴定 [J]. 天然产物研究与开发, 2020, 32(4): 607-612.
[14] Iwagawa T, Asai H, Hase T,. Monoterpenoids from[J]., 1990, 29(6): 1913-1916.
[15] Kakuda R, Imai M, Machida K,. A new glycoside from the flower buds of[J]., 2000, 54(6): 314-317.
[16] Heymann H, Tezuka Y, Kikuchi T,. Constituents ofMIQ. I. isolation and NMR spectral analysis of sesquiterpenes from the dried pods [J]., 1994, 42(1): 138-146.
[17] 朱华旭, 唐于平, 闵知大, 等. 夜香牛全草的生物活性化学成分研究(II) [J]. 中国中药杂志, 2009, 34(21): 2765-2767.
[18] Ascari J, Boaventura M A D, Takahashi J A,. Biotransformation of bioactive isocaryolanes by[J]., 2011, 74(8): 1707-1712.
[19] Häusler M, Montag A. Isolation, identification and quantitative determination of the norisoprenoid ()-(+)- dehydrovomifoliol in honey [J]., 1989, 189(2): 113-115.
[20] D'Abrosca B, DellaGreca M, Fiorentino A,. Structure elucidation and phytotoxicity of C13 nor-isoprenoids from[J]., 2004, 65(4): 497-505.
[21] Wilairat R, Kijjoa A, Pinto M,. Constituents ofverruculosa. and their cytotoxic effect on human cancer cell lines [J]., 2006, 44(6): 411-415.
[22] Asiri S M, Shaari K, Abas F,. Two new naphthoquinone derivatives from the stem bark of[J]., 2012, 7(10): 1333-1336.
[23] Fujita T, Terato K, Nakayama M. Two jasmonoid glucosides and a phenylvaleric acid glucoside from[J]., 1996, 60(4): 732-735.
[24] Nakamura Y, Miyatake R, Inomata S,. Synthesis and bioactivity of potassium beta--glucopyranosyl 12-hydroxy jasmonate and related compounds [J]., 2008, 72(11): 2867-2876.
[25] Carvalho L M, Seita J. A new oleanic acid derivative from[J]., 1993, 59(4): 369-372.
[26] 刘加祥, 卢志远, 张冉, 等. 黄棉木的化学成分研究 [J]. 云南农业大学学报: 自然科学, 2017, 32(6): 1145-1150.
[27] 苗青, 包海燕, 朴淑娟, 等. 蛇莓乙酸乙酯萃取物的化学成分 [J]. 第二军医大学学报, 2008, 29(11): 1366-1370.
[28] 张广文, 马祥全, 苏镜娱, 等. 广藿香中的黄酮类化合物[J]. 中草药, 2001, 32(10): 871-874.
[29] Dawé A, Mbiantcha M, Yakai,. Flavonoids and triterpenes fromfragrans with anti-inflammatory, antioxidant and antidiabetic potential [J]., 2018, 73(5/6): 211-219.
[30] 高飞鹏, 汪豪, 叶文才, 等. 裸花紫珠叶的化学成分 [J]. 中国药科大学学报, 2010, 41(2): 120-123.
[31] González A G, Estévez-Reyes R, Mato C. Salicifoliol, a new furolactone-type lignan from[J]., 1989, 52(5): 1139-1142.
[32] Imai F, Itoh K, Kishibuchi N,. Constituents of the root bark ofcollected in Indonesia [J]., 1989, 37(1): 119-123.
[33] 魏秀丽, 杨春华, 梁敬钰. 中药秦皮的化学成分 [J]. 中国天然药物, 2005, 3(4): 228-230.
[34] 王彦予, 张喆, 史浩男, 等. 北桑寄生醋酸乙酯部位化学成分研究[J]. 中草药, 2022, 53(4): 965-972.
[35] 周宇娟, 王俊豪, 薛亚甫, 等. 铁皮石斛醋酸乙酯部位化学成分研究[J]. 中草药, 2021, 52(17): 5218-5225.
Chemical constituents from
CHEN Qian-qian1, ZOU Xian-liang3, CHOU Gui-xin1, 2
1. Institute of Chinese Materia Medica, Shanghai University of Traditional Chinese Medicine, Shanghai 201203, China 2. Shanghai R&D Centre for Standardization of Chinese Medicines, Shanghai 201203, China 3. Pingxiang Health Vocational College, Pingxiang 337000, China
To study the chemical constituents from.A variety of modern separation chromatography techniques were used for separation and purification, structural identification through spectroscopic data and physicochemical properties, and ECD was used to determine the absolute configuration of new compounds. The cytotoxic activity of new compounds was screened by CCK-8 method.A total of 34 compounds were isolated and identified from, of which compounds 1—5 were named as callnudoid A1 (1), (4,6)-4,6-dihydroxy-α-terpineol (2), (1)-2,2-dimethyl-3-methylol-3-cyclohexene-1-carboxylic acid (3), (1,4)-2,2-dimethyl-3-methylene-4-hydroxy-cyclohexane- 1-carboxylic acid (4), (1)-2,2-dimethyl-4-methylol-3-cyclohexene-1-carboxylic acid (5); Compounds 6—34 were identified as 2,6- dimethoxy--benzoquinone (6),-menth-8-ene-1,2-diol (7), rehmachinin B (8), buergerinin G (9), paeoveitol B (10), subamone (11), 8-hydroxy-2,6-dimethyl-(2,6)-octadienoic acid (12), 8-hydroxy-2,6-dimethyl-(2)-octenoic acid (13), callnudoid A (14), clovane-2β,9α-diol (15), caryolane-1,9β-diol (16), (8,9)-isocaryolane-8,9-diol (17), ()-(+)-dehydrovomifoliol (18), (3,5,6,7)-5,6-epoxy-3-hydroxy-7-megastigmen-9-one (19), abscisic acid (20), callicarpaquinone B (21), 12-hydroxyjasmonic acid (22), (−)-methyl 12-hydroxyjasmonate (23), oleanolic acid (24), ursolic acid (25), euscaphic acid (26), 5,4-dihydroxy- 3,7,3-trimethoxyflavone (27), velutin (28), 5,7,4-trihydroxy-3-methoxyflavone (29), salicifoliol (30), murrangatin (31), sinapaldehyde (32), 4-hydroxyl-3-methoxybenzaldehyde (33) and syringic acid (34).Compounds 1—5 were new compounds, named as callnudoid A1 (1), (4,6)-4,6-dihydroxy-α-terpineol (2), (1)-2,2-dimethyl-3-methylol-3-cyclohexene-1- carboxylic acid (3), (1,4)-2,2-dimethyl-3-methylene-4-hydroxy-cyclohexane-1-carboxylic acid (4), (1)-2,2-dimethyl-4- methylol- 3-cyclohexene-1-carboxylic acid (5). Compounds 6, 7—13, 17—18 and 31 were all isolated and identified from Verbenaceae for the first time, compounds 30 and 32—33 were found for the first time in the genus, and compounds 15, 21 and 28 isolated for the first time from. Cytotoxicity screening results showed that compound 4 possessed the cytotoxicity on HepG2 cell line with the IC50values of 24.0 μmol/L.
Verbenacase;Hook. et Arn; callnudoids A1; (1,4)-2,2-dimethyl-3-methylene-4-hydroxy-cyclohexane-1-carboxylic acid; clovane-2β,9α-diol; callicarpaquinone B; velutin; salicifoliol
R284.1
A
0253 - 2670(2023)01 - 0015 - 14
10.7501/j.issn.0253-2670.2023.01.003
2022-09-02
重大新药创制专项基金资助项目(2019ZX09735002-004)
陈倩倩,女,硕士研究生,研究方向为中药化学成分及质量标准。Tel: 19821267292 E-mail: 598029330@qq.com
通信作者:侴桂新,男,研究员,从事中药化学成分与质量标准研究。E-mail: chouguixinzyb@126.com
[责任编辑 王文倩]