以急性脑梗死为表现的神经梅毒临床特点及高分辨率磁共振对其病因诊断价值的研究
王志丽, 秦 伟, 杨 磊, 米荷音, 胡文立
梅毒在发展中国家依然是一个重要的公共卫生问题,约有23%~40%的早期未治疗或部分治疗的梅毒患者可存在中枢神经系统受累即神经梅毒[1]。神经梅毒的表现形式多样[2],其中脑膜血管梅毒可引起感染性动脉炎导致卒中样症状,与常见的急性缺血性卒中表现无法区分。在脑卒中人群中神经梅毒的患病率约为0.31%~4.7%[1],以缺血性脑卒中为表现就诊的脑膜血管梅毒误诊率较高,在我国甚至高达80.95%[3]。在急性脑梗死患者中早期识别神经梅毒以及合并存在动脉粥样硬化危险因素神经梅毒患者发生急性脑梗死,如何确定梗死是动脉粥样硬化所致还是梅毒感染性动脉炎所致是一项重要的问题。高分辨率磁共振血管壁成像(high-resolution magnetic resonance vessel wall imaging,HR-VWI)可对血管病壁直接成像,能更好地了解颅内血管病变病因包括血管炎[4]等。目前国内外有关HR-VWI对以急性脑梗死为主要表现的神经梅毒诊断价值的研究数据非常有限,仅见2例个案报告[5,6]。故我们回顾性分析7例以急性脑梗死为主要表现的神经梅毒患者的临床特征、实验室检测及影像学包括HR-VWI成像结果,并探讨HR-VWI在其病因诊断中的价值。
1 材料与方法
1.1 研究对象 回顾性分析2018年1月-2022年9月在我院神经内科收治的以急性脑梗死为主要表现的神经梅毒病例。纳入标准:(1)急性起病且具有局灶性神经功能缺损症状及体征;(2)经MRI-DWI序列证实存在急性脑梗死病灶;(3)符合《梅毒、淋病和生殖道沙眼衣原体感染诊疗指南(2020年)》神经梅毒疑似病例及确诊病例诊断标准[7]。排除标准:(1)存在其他脑病或中枢神经系统感染性疾病;(2)合并存在其他系统性自身免疫性疾病;(3)缺少HR-VWI检查等临床资料不全者。共纳入7例患者,其中男性6例,女性1例,年龄34~59岁,平均(46.43±10.01)岁。
1.2 研究方法
1.2.1 临床资料收集 采集患者的年龄、性别、动脉粥样硬化危险因素、临床症状、体征、NIHSS评分等资料,常规血液学检测,HIV、梅毒血清学试验结果[包括梅毒螺旋体特异性抗体(syphilis,TP),梅毒螺旋体明胶颗粒凝集试验(treponema pallidum particle agglutination test,TPPA);梅毒甲苯胺红不加热血清试验(toludine red unheated serum test,TRUST)],腰椎穿刺脑脊液常规、生化和梅毒抗体检测结果[包括荧光梅毒螺旋体抗体吸附试验(fluorescence treponemal antibody absorption test,FTA-ABS)],以及心电图和心脏彩超结果。记录随访结果包括改良Rankin评分量表(mRS)和随访时症状。
1.2.2 影像学检查 所有患者于发病7 d内完善了头颈部影像学检查包括头部MRI和(或)CT检查、颈部CTA、头部MRA或CTA。其中HR-VMI扫描所采用机型、成像序列及扫描参数先前的研究已详细阐述[8]。
2 结 果
2.1 临床资料 7例患者均急性起病,最常见临床表现为偏瘫(5例,71.4%),其次为构音障碍(4例,57.1%)、偏身感觉障碍(2例,28%)和四肢瘫(2例,28%),1例患者(14%)存在认知功能障碍(MoCA 23分和MMSE 28分)。入院时NIHSS评分0~5分。合并存在1项或多项动脉粥样硬化危险因素患者6例,2例患者(28%)有不洁性生活史,2例合并HIV感染(见表1)。
2.2 辅助检查 (1)血液及脑脊液化验:7例患者梅毒特异性抗体阳性,其中5例TRUST试验阳性。7例患者脑脊液TPPA阳性,3例脑脊液TRUST试验阳性,3例完善了脑脊液FTA-ABS,均IgG阳性(见表1)。6例脑脊液细胞数增多和(或)蛋白质增高,所有患者脑脊液糖和氯化物、细菌、分枝杆菌和真菌培养结果均阴性,排除了其他中枢神经系统感染或脑病。(2)影像学特点:头部MRI-DWI序列显示位于放射冠或基底节区(4个)、脑桥(3个)、中脑(1个)、丘脑(1个)、颞枕叶(1个)急性梗死灶,且符合血管分布(见表2)。3例患者存在轻度脑萎缩改变。颅内血管检查包括MRA及CTA,仅1例见基底动脉不规则节段性狭窄的血管炎表现(病例1),其余6例存在梗死相关血管狭窄、闭塞或非特异性血管改变。HR-VWI显示5例(病例1、2、4、6和7)患者存在梗死相关血管动脉炎改变,其中2例经青霉素及抗血小板聚集治疗后管壁厚度和(或)环形强化程度较前改善(病例1和4,见图1);1例梗死责任血管存在动脉粥样硬化表现(病例3,见图2);1例多发梗死灶中基底节区梗死相关责任血管见动脉炎改变,而脑桥梗死相关血管未见动脉炎改变,同时完善了经食道心脏超声等,排除了心源性栓塞(病例5)。
2.3 治疗和临床结局 脑梗死急性期,3例患者予阿司匹林和氯吡格雷双联抗血小板聚集治疗,4例予单抗血小板聚集治疗,均联合他汀类药物稳定斑块治疗。同时根据指南[7]予规范化抗生素治疗(6例使用青霉素,1例青霉素过敏使用米诺环素)。治疗后5例患者外院复查脑脊液(包括传染病专科医院规范化HIV治疗2例),常规、生化、梅毒抗体转阴4例,1例脑脊液参数改善,2例未再复查。所有患者接受诊室或电话随访,平均随访时间为34.8个月,完全康复2例,5例患者预后良好,遗留少许症状(1例mRS评分2分,4例评分1分),无脑梗死复发及死亡患者。
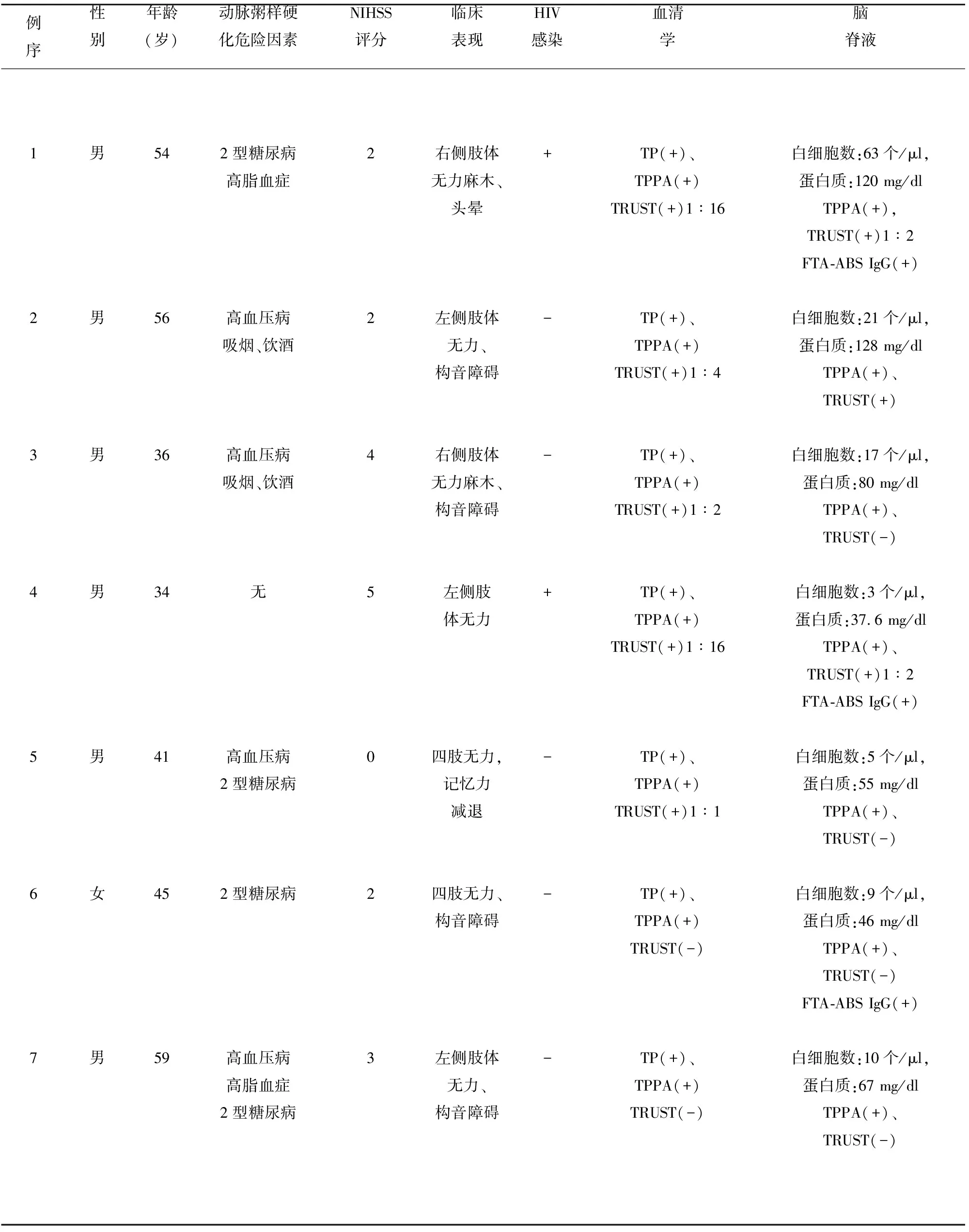
表1 7例神经梅毒患者的人口学特征及临床资料
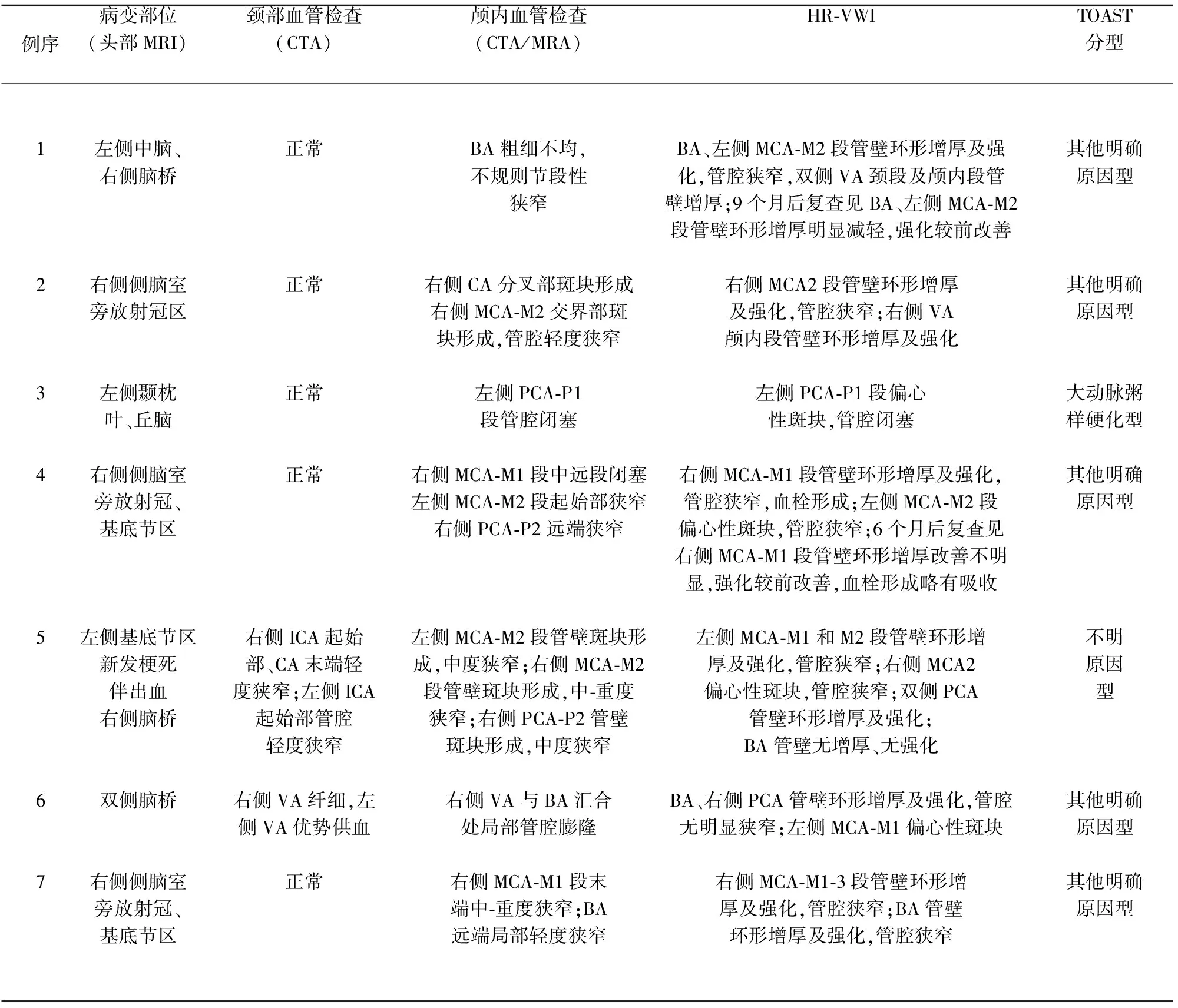
表2 7例神经梅毒患者影像学资料及TOAST分型
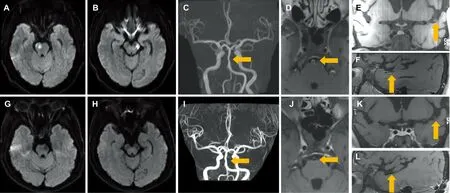
图1 病例1头部影像学结果。A和B:发病第3天DWI序列示右侧脑桥、左侧中脑大脑脚新发梗死灶;C:发病第3天MRA示基底动脉粗细不均,不规则节段性狭窄;D:发病第7天轴位HR-VWI示基底动脉管壁环形增厚伴明显强化、管腔狭窄;E和F:发病第7天冠状位及矢状位HR-VWI示左侧大脑中动脉M2段管壁环形增厚伴明显强化、管腔狭窄;G和H:发病9个月DWI序列示右侧脑桥、左侧中脑大脑脚软化灶;I:9个月3D TOF MRA示基底动脉狭窄明显改善;J :9个月HR-VWI示基底动脉狭窄、管壁厚度及强化均较前明显改善;K和L:9个月冠状位及矢状位HR-VWI示左侧大脑中动脉M2段管壁厚度及强化较前明显改善
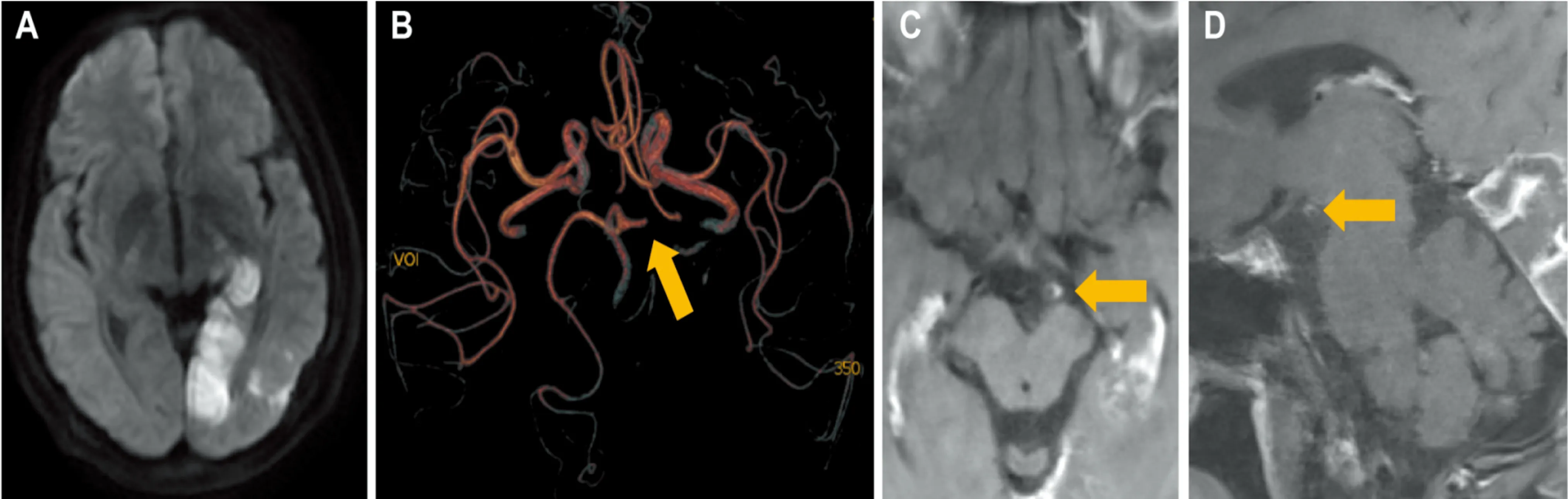
图2 病例3头部影像学结果。A:发病第4天DWI序列示左侧颞枕叶及丘脑新发梗死灶;B:MRA示左侧大脑后动脉P1段管腔闭塞;C:发病第8天轴位HR-VWI示左侧大脑后动脉偏心性斑块伴不均匀强化,远端管腔闭塞;D:发病第8天矢状位HR-VWI示左侧大脑后动脉偏心性斑块伴不均匀强化
3 讨 论
梅毒感染通过血管炎机制可导致颅内血管狭窄、闭塞和(或)血栓形成,出现急性缺血性卒中表现[2]。目前尚无针对神经梅毒的金标准实验室检测,尤其是脑膜血管梅毒。根据2021年美国[9]和2020年中国[7]CDC发布的梅毒诊疗指南,建议对存在神经系统症状或体征、梅毒血清学检查阳性、脑脊液三项中满足一项[性病研究实验室试验(venereal disease research laboratory test,VDRL)和/或FTA-ABS阳性、细胞数增多、蛋白质升高],排除其他疾病即可诊断神经梅毒并进行规范化治疗。然而,由于急性脑卒中患者可能出现细胞数增高或蛋白质增加的脑脊液异常,而卒中本身可能是神经梅毒表现[1]。因此,对发生急性脑梗死的梅毒患者,仅基于脑脊液异常诊断神经梅毒的标准可能还有待进一步完善[1],尤其是脑膜血管梅毒合并动脉粥样硬化,如何鉴别脑梗死的病因为动脉粥样硬化还是血管炎,仍较困难。HR-VWI作为一种无创性研究脑血管壁病理学变化的新的检测技术,可清晰地显示包括颅内动脉粥样硬化和血管炎病变。本研究回顾性分析了以急性脑梗死为表现的神经梅毒患者的临床特点,应用HR-VWI分析了合并存在动脉粥样硬化危险因素的梅毒患者发生急性脑梗死的病因。
本研究中所有患者均急性起病、存在明确的中枢神经系统受累症状及体征,包括偏瘫、偏身感觉障碍、构音障碍等,与常见急性脑梗死表现相同。头部MRI可检测到局灶性急性脑梗死病变,病灶分布区域包括放射冠、基底节、颞枕叶、丘脑、脑干,也存在多发性梗死灶(1例),与既往报道的脑膜血管梅毒病灶分布一致[10,11]。其中基底节区或脑干的小梗死较常见,认为可能是由于动脉内膜炎对穿支动脉的损伤所致[12]。既往研究发现,脑膜血管梅毒以大脑中动脉分布区域最常见,其次是基底动脉及其分支[13],在本研究中两者均较常见,数量持平。
对于相对年轻的成年人、既往有梅毒病史或者HIV阳性患者,尤其是在脑血管病危险因素极少或无明显危险因素者,发生急性脑梗死需要怀疑脑膜血管梅毒的可能,脑脊液检查是目前诊断脑膜血管梅毒的基础[14]。有研究使用MRA或DSA对脑膜血管梅毒的颅内血管进行评估,部分患者可显示脑动脉的不规则节段性狭窄的血管炎表现,认为可作为辅助诊断手段,然而两者均无法提供血管壁的详细信息[15,16]。值得注意的是,本组7例患者仅1例头部MRA显示动脉炎表现,因此,认为MRA辅助鉴别诊断价值有限。既往研究显示HR-VWI可显示血管壁增厚和多灶性均匀、光滑、明显的环形强化的血管炎表现[6],与偏心性动脉壁增厚伴不均匀强化的动脉粥样硬化斑块表现明显不同。
目前有关神经梅毒HR-VWI的研究极少,国际上仅见2例单个病例报道。文章阐述了以急性脑梗死为表现的脑膜血管梅毒患者血管壁环形增厚和强化的炎症表现及经治疗后血管壁强化消失、狭窄改善的随访结果,认为HR-VWI可反映梅毒感染性血管炎相关的血管壁改变、可作为评估脑膜血管梅毒治疗效果的手段[5,6]。
本研究HR-VWI结果显示7例梅毒患者中5例可见梗死灶相关血管的动脉炎表现,尽管其中4例合并存在动脉粥样硬化危险因素,部分合并存在非责任血管的动脉粥样硬化改变,责任血管的狭窄或闭塞归因于动脉炎,符合TOAST分型的其他明确原因型脑梗死。尤其是综合考虑部分患者经治疗后HR-VWI示管壁厚度和(或)环形强化程度较前改善也证实了存在动脉炎的病理过程。1例患者(病例3)梗死相关责任血管——大脑后动脉存在偏心性斑块、管腔狭窄,在没有伴随动脉炎表现的情况下将其归因于动脉粥样硬化,符合TOAST分型的大动脉粥样硬化型脑梗死。1例(病例5)多发梗死灶中前循环梗死相关血管见动脉炎改变,然脑桥梗死灶相关的基底动脉未见动脉炎改变,但由于伴随着双侧大脑后动脉动脉炎表现,考虑到脑膜血管梅毒可通过小型(Nissl-Alzheimer)动脉炎机制导致血管狭窄闭塞[17],本例患者脑桥梗死的责任血管——旁正中动脉不能排除动脉炎,同时该患者也存在动脉粥样硬化的危险因素及其他血管的动脉粥样硬化证据,认为符合TOAST分型的不明原因型脑梗死。本研究表明,神经梅毒患者发生脑梗死并不总意味着直接的因果关系,因为动脉粥样硬化病变可能与动脉炎并存,甚至动脉粥样硬化可能是唯一的血管异常表现,HR-VWI在帮助确定脑膜血管梅毒的动脉炎病变、以及鉴别合并动脉粥样硬化危险因素患者的卒中机制是动脉炎还是动脉粥样硬化上,具有重要的辅助诊断价值,同时也可随访评估神经梅毒的治疗效果。
文献显示脑膜血管梅毒患者脑梗死的治疗目前有3种考虑:针对病原体的抗生素(青霉素)治疗、抗血小板聚集治疗和血管炎的免疫治疗[18]。目前各国指南推荐使用青霉素静脉滴注10~14 d治疗神经梅毒[2]。已有研究建议联合使用青霉素和长期阿司匹林口服治疗,认为既可防止动脉粥样硬化病变导致的血栓栓塞亦可抑制Nissl动脉内皮细胞增殖引起的血小板活化[16]。此外,研究认为单独使用青霉素和抗血小板聚集治疗不足以改善脑梗死的预后[18]。目前没有证据表明皮质类固醇联合预防性抗血小板治疗对于感染性脑梗死尤其是梅毒性血管炎有效[18~20]。对于合并HIV感染患者经评估青霉素早期梅毒治疗失败风险高的患者,需要考虑联合皮质类固醇的应用[19]。有报告建议皮质类固醇联合青霉素治疗,但尚无评估其疗效和安全性的随机临床试验[18,21]。
本组所有患者使用抗生素联合阿司匹林抗血小板聚集治疗,在随访期间均未出现卒中复发,部分患者遗留轻微症状。我们也比较了入院时和治疗后随访HR-VWI(2例)结果,发现血管狭窄、血管壁增厚或环形强化现象均有好转。然而,本研究中HR-VWI随访的病例数量较少,为了更好地评估神经梅毒患者的抗生素、抗血小板聚集和皮质类固醇治疗效果,需要进行前瞻性临床试验。
本研究的局限性为回顾性研究,病例数量少,限制了研究结果的外延性。另外,本组病例中2例合并HIV感染,既往有研究报道HIV患者的神经梅毒(包括脑膜血管梅毒)发病率更高[2],没有神经梅毒的HIV感染也可引发小血管炎症进而导致脑卒中,是可能的潜在混杂因素[22]。鉴于目前国内外尚无大样本总结以急性脑梗死为主要表现的神经梅毒的HR-VWI相关研究,本研究结果值得关注。
综上所述,梅毒患者发生脑梗死的临床表现与常见缺血性脑卒中的临床表现常无法区分,HR-VWI是一种识别具有急性起病的神经系统缺损症状、梅毒血清学阳性的患者脑动脉炎表现并监测治疗效果的新诊断方法。对合并存在动脉粥样硬化的梅毒患者发生急性脑梗死进行该项检查,可早期识别脑膜血管梅毒并为梗死病因的确定提供更多依据,以指导后续治疗方案的制订。

