咔唑修饰的2-(2′-羟基苯基)-苯并噻唑衍生物合成及发光性能研究
钱 隆,刘世强,韩明虎,赵玉玲,俞天智*
(1.兰州交通大学 光电技术与智能控制教育部重点实验室,兰州 730070;2.兰州交通大学 化学化工学院,兰州 730070)
20世纪以来,光电材料在薄膜晶体管、发光二极管、太阳能电池等领域的应用日益广泛,而有机发光二极管(OLED)因具有高画质、大视角、自发光、质量轻薄、易卷曲拉伸和低启动电压等优点,逐渐成为最有前景的新生代显示与照明器件[1-3].在OLED器件的研究与应用中,实现高效的电致发光(EL)性能是关键因素,为了获得更好的EL性能,研究人员开发出了很多新型发光材料[4-9].其中,2-(2′-羟基苯基)-苯并噻唑(BTZ)由于具有良好的光热稳定性与激发态分子内质子转移(ESIPT)特质,被大量应用于荧光探针[10-11]、生物成像[12]和OLED[13-15]等产品的制造.
激发态分子内质子转移(ESIPT)是指一种在激发态下的特定π共轭结构分子因光诱导发生分子内质子转移的光物理过程,大多出现在具有较强氢键的分子上[16-17].而在非极性溶剂中,BTZ的酚羟基会与相邻的氮原子相互作用生成分子内氢键,使分子处于烯醇式构象结构(enol-form),受到激发后,酚羟基的氢质子从原位置转移到相邻的氮原子上发生分子内转移,形成酮式结构(keto-form),与烯醇式发射相比,酮式结构的分子发射波长更长,Stokes位移大,荧光覆盖范围广,能够实现白光发射.2014年,Cheng等[18]将三氟甲基与三苯胺基引入到BTZ分子骨架中,构建了两个具有典型ESIPT性质的分子,在乙腈/乙醇混合溶液中呈现出少见的白光发射.此外,ESIPT特性引起的大Stokes位移,使分子的酮式发射与吸收带完全隔开,避免了因自吸收而导致的能量损耗,有利于明显提高器件性能[19-20].
咔唑基团是一种经典的有机光电材料构建单元,因良好的发光特性和空穴传输能力,常被用于发光分子和空穴传输材料的基本单体[21-24].在分子骨架中引入咔唑基团,其共轭π电子结构将有望赋予材料优异的光电性能,可以有效提高其耐久性、热稳定性和玻璃化转变温度,从而增强器件性能[25-26].因此,本文通过Suzuki反应将2-(2′-羟基苯基)-苯并噻唑核与1,3-二(9H-咔唑-9-基)-苯单元和9-苯-9H-咔唑单元连接,合成两种发光良好的ESIPT分子,表征确定结构,制造相应器件,并检测光电性能,为新型OLED的开发及应用提供理论参考.
1 实验部分
1.1 目标产物的合成路线
在PCl3的催化下,邻氨基苯硫酚与5-溴水杨酸经缩合反应生成溴代BTZ核,再通过Suzuki反应将BTZ与两种咔唑电子供体(DCz和Cz)结合制备目标产物(见图1).

图1 目标产物BTZ-DCz和BTZ-Cz的合成路线Fig.1 Synthetic route of standard products BTZ DCz and BTZ Cz
1.2 材料与仪器
邻氨基苯硫酚、5-溴水杨酸、三氯化磷(PCl3)、1,3,5-三溴苯、咔唑、9-(4-溴苯基)咔唑、[1,1′-双(二苯基膦基)二茂铁]二氯化钯(Pd(dppf)Cl2)、四(三苯基磷)钯(Pd(PPh3)4)和1,10-邻菲咯啉均购于安耐吉化学.乙酸酐、无水硫酸钠、联硼酸频那醇酯、醋酸钾、无水碳酸钾和碘化亚铜分别购于国药集团化学试剂有限公司、毕得医药、天津市光复精细化工研究所、烟台市双双化工有限公司和上海中秦化学试剂有限公司.超干DMF购自岩峰科技,甲苯、1,4-二氧六环、四氢呋喃、二氯甲烷和N,N′-二甲基甲酰胺(DMF)购于利安隆博华(天津)医药化学有限公司、天津市大茂化学试剂厂、成都市科隆化学品有限公司和广东光华科技股份有限公司,上述试剂均为分析纯.
分子结构表征由BRUKER AVANCE 500 NEO核磁共振仪和Bruker Esquire 6000质谱仪完成.UV光谱和PL光谱由Shimadzu UV-2550紫外分光光度计、Hitachi F-7100荧光光谱仪进行检测.热稳定性和电化学性质通过Shimadzu Thermal Analyzer Japan热重分析仪和CHI660E电化学工作站完成.本文以0.10 mol/L Bu4NPF6干燥的三氯甲烷溶液作电解质,铂碳电极作工作电极,铂丝和Ag/Ag+电极分别作对电极和参比电极,内标为二茂铁(Fc/Fc+).
1.3 目标产物的合成方法与结构表征
中间体I~IV的合成方法见参考文献[27-30],具体核磁共振数据如下:
2-(苯并[d]噻唑-2-基)-4-溴苯乙酸酯(中间体I)[27]:白色固体,收率52.8%,1H NMR(500 MHz,CDCl3,δ,ppm):8.51(s,1H),8.10(d,J=8.0 Hz,1H),7.94(d,J=8.0 Hz,1H),7.60(d,J=8.5 Hz,1H),7.53(t,J=7.5 Hz,1H),7.44(t,J=7.5 Hz,1H),7.15(d,J=8.5 Hz,1H),2.48(s,3H).13C NMR(126 MHz,CDCl3,δ,ppm):168.7,160.7,152.7,147.2,135.5,134.1,132.7,127.8,126.6,125.7,125.4,123.6,121.4,119.7,21.7.
9,9′-(5-溴-1,3-亚苯基)双(9H-咔唑)(中间体II)[28-29]:灰白色固体,收率25%,1H NMR(500 MHz,CDCl3,δ,ppm):8.14(d,J=8.0 Hz,4H),7.86(s,2H),7.79(s,1H),7.54(d,J=8.0 Hz,4H),7.46(t,J=7.0 Hz,4H),7.33(t,J=7.0 Hz,4H).13C NMR(126 MHz,CDCl3,δ,ppm):140.5,140.3,128.7,126.4,124.1,124.0,123.8,120.8,120.6,109.6.
硼酯化的9,9′-(5-溴-1,3-亚苯基)双(9H-咔唑)(中间体III)[30]:白色固体,收率51.6%,1H NMR(500 MHz,CDCl3,δ,ppm):8.15(d,J=7.5 Hz,4H),8.11(s,1H),7.87(s,1H),7.50(d,J=8.5 Hz,4H),7.44(t,J=7.0 Hz,4H),7.30(t,J=7.5Hz,4H)1.35(s,12H).13C NMR(126 MHz,CDCl3,δ,ppm):140.80,138.88,132.21,128.32,126.10,123.54,120.40,120.19,109.75,84.46,24.93.
硼酯化的9-(4-溴苯基)咔唑(中间体IV)[30]:米白色固体,收率46.1%,1H NMR(500 MHz,CDCl3,δ,ppm):8.06(d,J=8.0 Hz,2H),7.98(d,J=8.0 Hz,2H),7.52(d,J=8.0 Hz,2H),7.37(d,J=8.0 Hz,2H),7.33(t,J=7.0 Hz,2H),7.21(t,J=7.0 Hz,2H),1.33(s,12H).13C NMR(126 MHz,CDCl3,δ,ppm):140.61,140.38,136.39,126.09,125.97,123.53,120.31,120.06,109.86,84.10,77.62,24.94.
3-(苯并[d]噻唑-2-基)-3′,5′-二(9H-咔唑-9-基)-[1,1′-联苯]-4-酚(化合物BTZ-DCz):淡黄色固体,收率为49.3%,m.p.=254℃.1H NMR(500 MHz,CDCl3,δ,ppm):12.73(s,1H),8.18(d,J=5.0 Hz,2H),8.01(d,J=10.0 Hz,1H),7.98(d,J=5.0 Hz,1H),7.94(s,2H),7.90(d,J=5.0 Hz,1H),7.81(t,J=5.0 Hz,1H)7.74(d,J=5.0 Hz,1H)7.63(d,J=10.0 Hz,4H),7.54-7.40(m,7H),7.34(t,J=5.0 Hz,4H).13C NMR(126 MHz,CDCl3,δ,ppm):168.84,158.36,151.76,143.68,140.62,139.95,132.61,131.52,130.87,126.87,126.28,125.84,123.91,123.69,123.63,122.33,121.66,120.55,120.46,118.89,117.34,109.77.HRMS:Calcd.for C43H27N3OS,632.1802[M-H]-;Found:632.180 4.
3-(苯并[d]噻唑-2-基)-4′-(9H-咔唑-9-基)-[1,1′-联苯]-4-酚(化合物BTZ-Cz):淡黄色固体,收率为68.8%,m.p.=250℃.1H NMR(500 MHz,CDCl3,δ,ppm):12.62(s,1H),8.17(d,J=7.5 Hz,2H),8.03(d,J=8.0 Hz,1H),7.98(s,1H),7.94(d,J=8.0 Hz,2H),7.82(d,J=8.0 Hz,2H),7.72(d,J=6.5 Hz,1H),7.66(d,J=8.0 Hz,2H),7.55-7.422(m,6H),7.31(t,J=7.0 Hz,2H),7.25(s,1H),7.24(s,1H).13C NMR(126 MHz,CDCl3,δ,ppm):169.17,157.77,151.87,140.89,139.23,136.73,132.65,132.00,131.61,128.11,127.52,126.88,126.80,126.00,125.77,123.46,122.33,121.64,120.37,120.02,118.62,117.15,109.82.HRMS:Calcd.for C31H20N2OS,469.1369[M+H]+;Found:469.137 2.
1.4 器件的制备
基于两种分子的多层OLED器件采用溶液旋涂法制备,最佳掺杂器件结构为ITO/PEDOT:PSS(45 nm)/26DCzPPy:BTZ-DCz或BTZ-Cz(20 wt%)(30 nm)/TPBi(20 nm)/Liq(2 nm)/Al(150 nm).其中,26DCzPPy为主体材料,PEDOT:PSS为空穴注入材料,TPBi为电子传输材料,Liq为电子注入材料,ITO和Al分别作为阳极和阴极,BTZ-DCz和BTZ-Cz的最佳掺杂浓度为20 wt%.将PEDOT:PSS旋涂到预清洁和O2等离子体处理的氧化铟锡(ITO)基板上,并在120℃下加热20 min,去除残余水分.将发光分子与26DCzPPy混合溶于氯苯溶液,然后旋涂于PEDOT:PSS层上,获得厚度约为45 nm的薄膜.随后,真空蒸镀法制造TPBi层、Liq层和Al层,蒸发速率分别为2Å/s,0.5Å/s和4Å/s;厚度分别为20 nm、2 nm和150 nm,器件发光面积为4 mm2,用Spectra Scan PR655和Keithley 2400 Sourcemeter记录器件性能(EL光谱、J-V曲线、EQE),器件结构和能级示意图如图2所示.
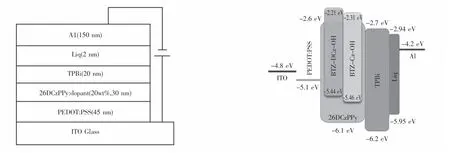
图2 器件结构和能级示意图Fig.2 Device structure and energy level diagram
2 结果与讨论
2.1 光物理性能
采用紫外吸收光谱(UV)检测不同状态下分子的光致发光性能(PL),BTZ-DCz和BTZ-Cz的UVPL谱和薄膜PL谱如图3所示.

图3 BTZ-DCz和BTZ-Cz的UV-PL谱和薄膜PL谱Fig.3 UV-PL Spectra and thin film PL spectra of BTZ-DCz and BTZ-Cz
由图3可见,由于分子的π→π*跃迁,BTZ-DCz和BTZ-Cz均出现一个291 nm处强的高能吸收带和340 nm处强的低能吸收带[31-32].在300 nm的紫外光激发下,2种化合物均表现出双峰发射,BTZ-DCz的发射峰位于348 nm和530 nm处,BTZ-Cz的发射峰位于388 nm和541 nm处,其中短波长的发射来源于烯醇式(enol-form)结构,长波长的发射来源于酮式(keto-form)发射[14],双峰发射特征意味着在特定极性的溶剂中2种化合物均可以实现白光发射.同时,BTZ-DCz和BTZ-Cz的薄膜发射峰分别为533 nm和552 nm,在固态薄膜条件下的发光源于其酮式结构[14],与二氯甲烷溶液中的发射峰相比,薄膜PL表现出明显的红移,表明存在固态下分子间的相互作用[33].
2.2 热稳定性和电化学性质
器件工作时会产生大量热量,因而材料的热稳定性对于器件的工作寿命和性能至关重要.课题组以Shimadzu Thermal Analyzer Japan分析仪为测试平台,仪器内通氮气,升温速率:10℃/min,测试温度范围:室温0~800℃.检测结果如图4(a)所示,两种分子的热分解温度(Td)分别为419℃和395℃,表明材料具有优秀的热稳定性,有利于器件长期稳定工作,符合生产制造要求.
为了获得更好的器件性能,需要选择合适能级的功能层材料,与发光材料能级匹配,可通过循环伏安法(CV)来计算化合物能级.由图4(b)可见,BTZ-DCz和BTZ-Cz的氧化电位(EOX)分别为1.14 V和1.16 V.相同条件下,测得的Fc/Fc+电位为0.50 V,依据公式EHOMO=-(EOX+4.8-EFc/Fc+)(eV)计 算 出HOMO能级为-5.44 eV和-5.46 eV[34];公式ELUMO=(EHOMO+EOPTg)(eV)计算出LUMO能级为-2.21 eV和-2.31 eV[35],其中:为化合物的光学带隙.2种分子的光物理、热稳定及电化学性质如表1所列.由表1和图2可知,化合物BTZDCz和BTZ-Cz的能级与制备器件所用材料的能级匹配度高,有利于器件电致发光性能的增强.

图4 化合物BTZ-DCz和BTZ-Cz的热重分析图和循环伏安曲线图Fig.4 Thermogravimetric and cyclic voltammetric diagrams of compounds BTZ DCz and BTZ Cz

表1 BTZ-DCz和BTZ-Cz的光物理、热稳定及电化学性质Tab.1 Photophysical,thermal stability and electrochemical properties of BTZ DCz and BTZ Cz
2.3 电致发光(EL)性能
图5是基于BTZ-DCz和BTZ-Cz掺杂器件的电致发光(EL)光谱和电流密度-电压-亮度(J-V-L)曲线.由图5可见,基于BTZ-DCz和BTZ-Cz器件的发射峰分别位于542 nm和560 nm,启动电压分别为3.9 V和4.1 V.与相应的PL光谱相比,其EL光谱的红移不大(<10 nm),表明器件性质稳定且效率良好,而且较低的启动电压,也有助于器件的实际应用.随着电压的上升,器件的亮度先快速上升然后趋于稳定,最大亮度分别为1 730 cd/m2和2 012 cd/m2,在4~5 V内器件的电流密度增幅很小,但当电压超过5 V时,电流密度的增幅变得非常大,器件的EL性能如表2所列.

表2 器件的电致发光性能Tab.2 Electroluminescent properties of devices

图5 器件的EL谱和电流密度-电压-亮度曲线Fig.5 EL spectra and current density voltage luminance curves of devices
图6是基于BTZ-DCz和BTZ-Cz掺杂器件的电流效 率-亮度-功率效率曲线和EQE-亮度曲线.如图6(a)所示,由于三重态激子浓度过大导致激子湮灭,器件的电流效率和功率效率均先增长后下降,基于BTZ-DCz和BTZCz器件的最大电流效率分别为3.09 cd/A和2.79 cd/A,最大功率效率分别为1.63 lm/W和1.57 lm/W.如图6(b)所示,曲线变化情况与效率-亮度曲线的变化情况相似,先增长后下降,最大EQE分别为0.95%和0.91%.与之前报道的基于ESIPT分子器件[13]的电致发光性能(最大电流效率≤2.8 cd/A)相比,基于BTZ-DCz和BTZ-Cz器件表现出较好的电致发光性能,在OLED领域具有一定的实用价值.

图6 器件的电流效率-亮度-功率效率曲线和EQE-亮度曲线Fig.6 Current efficiency brightness power efficiency curve and EQE brightness curve of devices
3 结论
将电子供体单元DCz和Cz与BTZ主核连接合成了发光分子BTZ-DCz和BTZ-Cz,表征确定分子结构,测定光物理、热稳定和电化学性质,制造掺杂器件并检测EL性能.结果表明,在紫外光激发下,BTZDCz和BTZ-Cz的溶液PL均呈现出双发射,薄膜PL均为单发射.同时,2种分子的热稳定性良好,HOMO/LUMO能级分别为-5.44/-2.21 eV和-5.46/-2.31 eV,能级匹配度高.其中,基于BTZ-DCz的最佳掺杂器件的启动电压、最大亮度、电流效率、功率效率和EQE分别为3.9 V、1 730 cd/m2、3.09 cd/A、1.63 lm/W和0.95%.基于BTZ-DCz的最佳掺杂器件的启动电压、最大亮度、电流效率、功率效率和EQE分别为4.1 V、2 012 cd/m2、2.79 cd/A、1.57 lm/W和0.91%,相比BTZ主核分子在溶液下的微弱荧光[27],咔唑基团的引入优化了分子晶型结构与能级匹配度,明显改善了其光电性能,可为光电材料的开发与应用提供理论参考.目前,俞天智课题组正在开展进一步的研究.

