《肝脏靶向腺相关病毒(AAV)血友病B 基因治疗研究》解读
孙 婷,张 磊
[中国医学科学院血液病医院(中国医学科学院血液学研究所),实验血液学国家重点实验室,国家血液系统疾病临床医学研究中心,细胞生态海河实验室,天津市血液病基因治疗研究重点实验室,中国医学科学院血液病基因治疗重点实验室,中国医学科学院干细胞医学中心,北京协和医学院干细胞与再生医学系,天津,300020;
1 研究背景
血友病B 是由于编码凝血因子9(FⅨ)的基因突变导致FⅨ缺少而引起的一种单基因遗传病,主要表现为全身各部位的自发性出血或损伤后出血不止。 根据患者血液中缺少的凝血因子的活性可以分为轻度(5%~40%)、中度(1%~5%)、重度(<1%)。血友病的治疗在过去几十年经历了从全血、血浆到重组凝血因子替代治疗的发展。 当前无抑制物的血友病B 患者的标准治疗方式为定期规律性替代治疗(即预防治疗),但需终生频繁输注,为患者带来沉重负担[1]。 基因治疗是基于血友病发病机制而产生的一种新型治疗方法,通过基因治疗有可能实现单次输注、快速平稳持久提升凝血因子活性的目标,为患者带来巨大临床获益。
基因治疗一般分为两种:一种是通过基因编辑技术对缺陷基因本身直接进行原位校正,另一种是通过转运载体将具有正常功能的基因拷贝引入受体细胞,以补偿或补充突变基因。 腺相关病毒(adenoassociated virus,AAV)具有低整合能力、低免疫源性和高组织向性的特征,能够在不整合进入宿主细胞基因组的情况下在特定组织中特异性高表达目标蛋白,是血友病基因治疗的理想载体。 2003 年和2006年Manno 等分别发表了第1 例肌肉注射AAV 治疗血友病B 和第1 例静脉输注AAV 治疗血友病B 的临床研究,证明了AAV 载体的安全性并实现了外源性FⅨ的体内表达[2-3]。 2011 年首次通过静脉注射肝脏靶向AAV 载体治疗血友病B 的Ⅰ期临床试验取得良好预期疗效[4],长期随访疗效显著,安全性高[5]。 2017 年优化载体血友病B 患者基因治疗中等剂量注射即可取得稳定的FⅨ表达,且无严重不良事件发生[6]。 但是,2021 年发表在blood 上的一项旨在研究BAX335 治疗血友病B 疗效的研究中仅1/8 例入组患者获得持续表达,推测可能是由于CpG 序列引起的免疫反应所造成了转基因表达的丧失[7]。 我国在血友病基因治疗领域也进行了长期、深入的探究:血友病B 临床试验最早由复旦大学的薛京伦教授团队发起,其后中国医学科学院血液病医院的杨仁池教授团队进行了肌肉注射血友病B基因治疗的研究,湖南大学的陈方平教授尝试灌肠给药的方式进行血友病B 基因治疗。 目前已有多项中国血友病基因治疗研究在ClinicalTrials 注册。
虽然关于血友病B 基因治疗已取得了阶段性的成果,但该方法仍面临许多亟待解决的问题。 病毒感染的肝细胞引起细胞免疫,导致无症状的转氨酶升高,通常与FⅨ表达下降甚至完全丧失有关。本研究使用的载体BBM-H901 采用了具有自主知识产权的AAV843 血清型衣壳,具有强肝脏靶向性和低中和抗体分布的特征,能够特异性高效感染人肝脏细胞。 此外,BBM-H901 载体所携带的表达元件含有LXP2.1 肝特异性启动子,能够显著提高外源基因在肝脏的表达,允许以更低的载体剂量进行输注,减少载体相关副作用,并且本研究中肝脏靶向AAV 携带的FⅨ基因具有低CpG 含量,能够降低免疫反应。 既往的临床试验常采用载体输注后使用以糖皮质激素为主的免疫抑制药物来抑制AAV 衣壳诱导的免疫反应所引起的基因表达下降或丧失,但是这种方法疗效并不肯定[6-8]。 本研究开创性地采用了在AAV 载体输注前预防性使用糖皮质激素的方案,以期获得更加平稳持久的因子活性和临床疗效。 在临床前研究中,给FⅨ敲除的血友病B 小鼠静脉注射BBM-H901,1 周后FⅨ活性显著升高至97.4%(5.0×1011vg/kg)和338.96(1.0×1012vg/kg),因子活性维持至实验观察终点(28 周)。 在临床前研究的基础上,我们使用BBM-H901 开展了此项血友病B 基因治疗的Ⅰ期临床试验。
2 研究概述
2.1 研究方案 本研究是一项预防性使用糖皮质激素的肝脏靶向AAV 治疗血友病B 的单中心、单臂、Ⅰ期、前瞻性临床试验,共纳入10 例FⅨ活性≤2%且AAV843 中和抗体滴度<1 ∶5 的成年男性血友病B 患者。 载体输注前预防性使用糖皮质激素,载体输注后观察随访52 周(主观察期),后进行长期扩展随访。 主要终点为安全性和耐受性终点,次要终点为AAV 载体BBM-H901 的动力学特点,并采用单细胞测序对受试者不同时间点的免疫状态进行实时追踪检测。 (图1)。

图1 研究流程简图
2.1.1 BBM-H901 可快速持久平稳提升FⅨ活性,且无严重不良反应 10 例受试者累计随访达705周,无严重不良事件和FⅨ抑制物报告。 静脉注射BBM-H901 后24 小时内,载体DNA 在受试者血清中快速减少至少3 logs(图2C)。 载体DNA 在血浆和唾液中检测阴性的时间点为BBM-H901 注射后28 天,在精液中检测阴性的时间点为56 天。 在第0天(d0)和整个随访期的尿液标本中均未检测到载体DNA。
BBM-H901 注射后1 天即可检测到载体衍生的FⅨ表达,注射后1 周,载体衍生FⅨ:C 迅速达到平均57.1 IU/dL(SD 20.2)(图2B),截止至中位随访时间58 周,FⅨ:C 平均值>36.9 IU/dL (SD 20.5)(图2A)。 整个随访期,4 例受试者凝血因子活性稳定,4 例凝血因子活性维持在正常水平,2 例转氨酶有所升高的受试者凝血因子活性有所下降。 受试者靶关节的中位数、年化出血率以及FⅨ浓缩物输注量在基因治疗后均明显下降,临床疗效显著(图2D、2E、2F)。 同时,本研究提示,转氨酶曲线下面积与疗效相关。
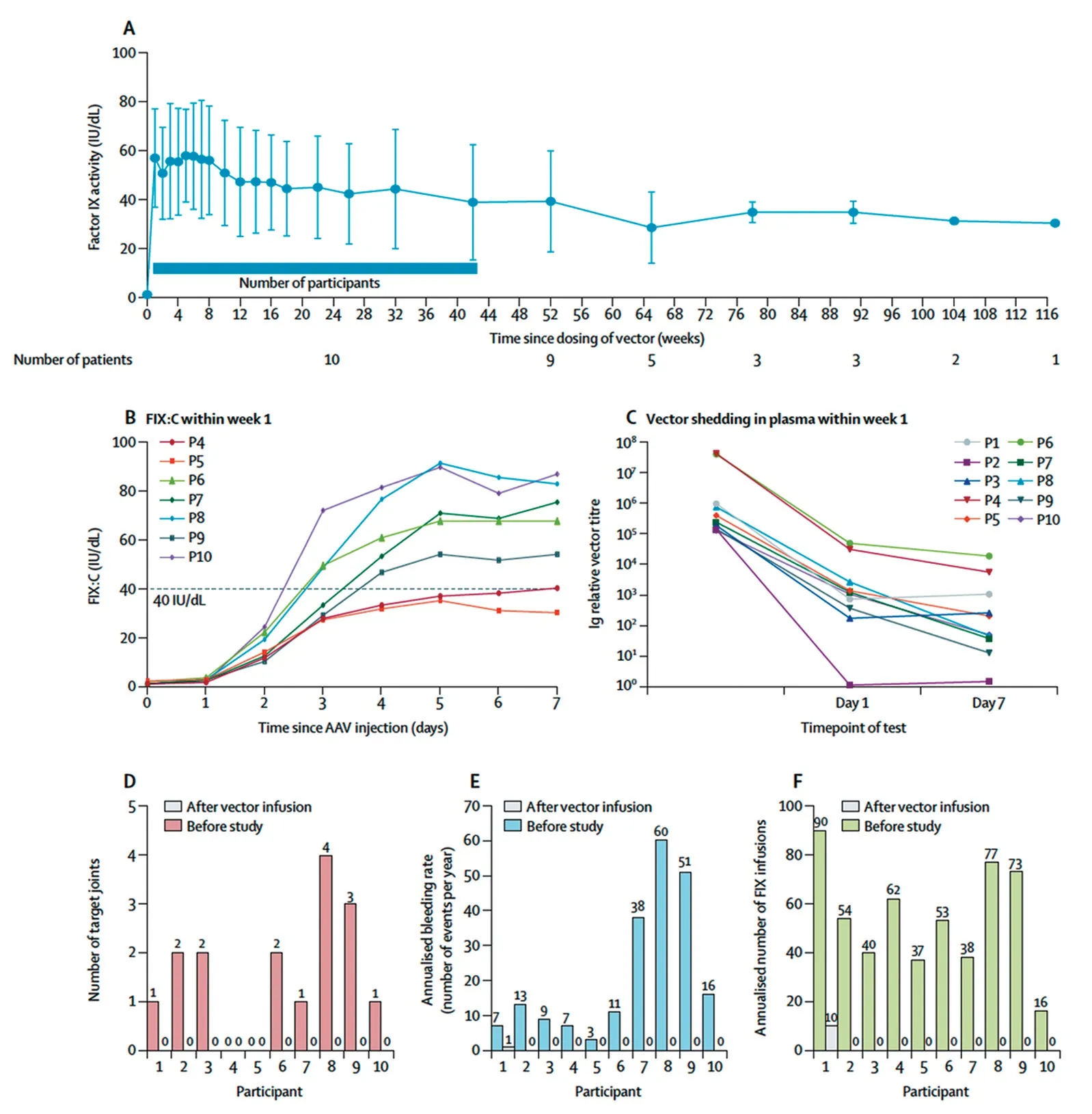
图2 基因治疗前后的因子活性、载体脱落和临床参数
2.1.2 单细胞测序揭示预防性使用糖皮质激素可减轻BBM-H901 引起的免疫反应 本研究在强的松前(d-7)、输注载体前(d0)、输注载体后7 天(d7)、强的松停药后14 天(stopGC)的时间点对受试者的血液样本进行了单细胞RNA 测序,拟通过分析疗效满意组(SE:FⅨ:C>40 IU/dL)和疗效欠佳组(IE:FⅨ:C<40 IU/dL)患者激素使用和基因治疗前后的免疫状态,从单细胞层面发现对提高基因治疗安全性和获得更加持久稳定因子活性有指导意义的信息。 单细胞测序发现疗效欠佳组患者的细胞免疫水平显著增高,而本研究开创性地使用糖皮质激素预防性治疗,可以明显下调细胞毒T 细胞的比例,促进调节性T 细胞(Treg)活化,显著抑制抗原递呈细胞(APC)的功能。
2.2 研究意义
本研究评估了肝脏靶向AAV 载体BBM-H901在中国血友病B 患者基因治疗中的安全性和有效性。 整个研究期内无3 至4 级不良反应事件发生,2例受试者发生可能与载体BBM-H901 相关的不良事件(2 级发热和转氨酶升高),在积极干预后好转。和既往的研究相似,所有受试者均产生了针对载体衣壳的高滴度结合抗体和中和抗体,这意味着每个参与者只有一次接受基于AAV 的基因治疗的机会,除非新型的AAV 衣壳与已使用的血清型没有交叉反应,或将来能研发出其他有效的干预措施。 本研究中的10 例中国血友病B 患者输注BBM-H901 后均无FⅨ抑制物产生,这也是基因治疗的一项重要安全性特征。
尽管之前的许多肝脏靶向血友病基因治疗也成功实现了载体来源的FⅨ表达并有效减少了患者的出血和血制品输注,但是载体病毒感染的肝脏细胞引起的T 细胞免疫反应所导致的安全性问题和因子表达减低甚至丧失仍是基因治疗所面临的一大挑战。 基因序列中CpG 含量过高可能会诱发免疫反应[7],本研究所采用的基因表达盒具有低CpG 特征,能够有效减低免疫反应。 既往的研究均在载体输注后使用免疫抑制剂(主要是糖皮质激素)预防或治疗免疫反应所引起的转氨酶升高和因子活性下降,但并不完全有效。 本研究首次在载体输注前预防性使用糖皮质激素,并通过临床参数检测和探索性的单细胞数据分析发现,预防性使用糖皮质激素可以有效抑制基因治疗所引起的T 细胞免疫反应及其与APCs 之间的细胞通讯,有利于获得更加持久平稳的因子活性。 本研究也观察到一些与糖皮质激素预防相关的不良事件,但所有不良事件均为1级或2 级,比较轻微。 因此,这种载体输注前短期预防性使用糖皮质激素的潜在价值需要进一步探索。
与其他B 型血友病基因治疗试验相比,本研究中载体基因表达速度更快[4,6,7,9],载体输注后1 天内即观察到载体基因表达,并在1 周内快速达到峰值。 并且本研究在AAV 输注后1 年实现了FⅨ:C持久稳定的高水平表达,7 例受试者的FⅨ:C 大于30 IU/dL,4 例患者的FⅨ:C 大于50 IU/dL 或更高。持久而稳定的高FⅨ:C 能够有效预防出血、改善靶关节和减低外源性FⅨ产品注射需求,受试者临床获益显著。 但是由于本研究的时间周期相对较短,这样一个相对较短的时间内无法清楚地观察到关节病变或假肿瘤等临床参数的改善,因此仍需在未来数年进行长期监测以评估载体基因持续表达时间和临床获益。 此外该研究为单中心研究,未来需要开展纳入更多患者的多中心研究以全面评估该疗法的安全性和有效性。
综上,该研究是中国首个肝脏靶向AAV 血友病B 基因治疗临床试验,也是亚洲首个基因治疗药物的临床研究成果,证实BBM-H901 在中国血友病B患者中是安全的,并且能够有效表达载体基因,提高患者体内载体来源FⅨ活性。 我们探索性的单细胞RNA 测序分析也表明,预防性使用糖皮质激素降低了接受基因治疗的血友病B 患者体内APCs、CD4+T细胞和CD8+T 细胞的基线数量,并促进了Treg 激活。 因此,这种预防性给予糖皮质激素的方案也可能有助于减弱其他血友病基因治疗患者的免疫反应,提高基因治疗的安全性和保障载体来源凝血因子的表达活性。
作者贡献声明孙婷负责撰写文章,张磊负责修改文章语言并监督此项目
利益冲突所有作者均声明不存在利益冲突

