三角籽骨综合征的CT及MRI表现
孙惠芳,丁长青(通讯作者),孙迎迎
(南通大学附属丰县医院(江苏省丰县人民医院)影像科,江苏 262500)
与后踝撞击相关的疼痛临床上统称为后踝撞击综合征 (Posterior ankle impingement Syndrome,PAIS),是以跖屈时及踝关节重复负重动作时踝后部疼痛为特征的一组临床疾病,系由踝关节后部的骨或软组织在跖屈时撞击引起的,最常见于重复性踝跖屈运动者[1]。反复跖屈、过度使用、反复创伤、先天性解剖变异导致这种综合征。影像学上与PAIS相关的异常主要有距骨三角籽骨 (os trigonum)、斯蒂达突(Stieda process)、后距小腿和距下关节积液-滑膜炎、踇长屈肌腱腱病和腱鞘炎及后踝骨髓水肿等[2]。三角籽骨是足部第二常见的副骨,发生率一般为2%~13%,在一些PAIS的临床研究中,发生率可达 20%~30%,是 PAIS最为常见的原因[3]。
临床上,三角籽骨综合征难以和跟腱病/肌腱撕裂、足踝关节病、急性距骨后突骨折、踇长屈肌腱鞘炎、Haglund综合征、骨软骨损伤和跟骨后滑囊炎等相鉴别。三角籽骨在常规X线片可能正常,但斜位X线片可明确诊断;多层螺旋CT(MSCT)可行二维多层面重建(MPR),矢状位MPR易于观察三角骨;MRI多序列、多方位成像,还具有优越的软组织对比特征,能准确评估引起PAIS的各种异常,尤其是可显示三角骨中的骨髓水肿,成为影像学最佳的诊断手段[2]。因而,影像学检查对提示或证实本病的诊断具有相当重要的作用[4]。鉴于目前本症的文献报道仍较少,为提高认识,现收集2019年1月-2022年5月本院诊治的26例OTS临床及影像学资料,并复习相关文献,报道如下。
1 资料与方法
1.1 一般资料
26例OTS患者中,男14例,女12例,年龄17-69岁,平均45岁。患者均有不同程度的后踝部疼痛及活动受限,跖屈时显著,伴后踝软组织肿胀15例,后踝部感觉异常4例。1例以慢性后踝疼痛伴急性足外伤就诊。查体:被动跖屈实验阳性。病程中17例曾行足踝X线平片检查,10例行MSCT检查并行矢状位二维多平面重建 (MPR)及三维容积再现(VR)重建,16例行MRI检查。本研究获得本院医学伦理委员会审查许可及患者本人的知情同意。
1.2 CT及MRI检查方法
CT使用飞利浦 Brilliance型16排及64排螺旋CT成像设备。患者取仰卧位、足先进,双足并排置于检查床中心、患肢制动,扫描范围自胫距关节间隙上缘3-4cm至足底。主要参数:120kV,120-190mA,矩阵512×512,层厚3mm,螺距0.75-1.0。将薄层原始数据在专用工作站上行多平面重组(MPR)、最大密度投影(MIP)、容积再现(VR)等图像后重建及处理。
MRI检查使用飞利浦Achieva 1.5T及3.0T成像仪。患者取仰卧位,踝关节自然位,使用关节表面线圈,扫描范围包括踝关节、内外踝及跟骨。扫描方位及序列:轴位PDSPAIR(Proton density weighted Spectral attenuated inversion recovery,即质子相频率选择反转恢复衰减序列),矢状位SE T1WI及PDSPAIR,冠状位 PDSPAIR。主要参数:T1WI(TR/TE:500-550ms/15-20ms),T2WI (TR/TE:3200-3500ms/100ms);PDSPAIR(TR/TE:3000-3200ms/30-40 ms);层厚/层间距:3.0-3.5mm/0.3mm;扫描野(FOV):矢状位为160 mm×160mm,冠状位为160 mm×160mm,横轴位为 160 mm×140mm;矩阵:512×512。
由两名高年资诊断医师分别对踝关节CT及其二维、三维后重建图像、MRI各序列图像观察分析,重点观察后踝关节附属骨与软组织结构的改变。其中,骨性结构主要观察距骨后突形态、距后三角籽骨存在与否及是否存在合并损伤、有否游离体或骨块;CT上重点观察关节间隙、骨赘增生及骨质异常;软组织结构主要在MRI上观察,重点观察距腓后韧带、胫腓后下韧带、踝间韧带、踇长屈肌、胫距和距下关节滑膜及周围脂肪垫形态信号有无异常。
1.3 纳入、排除标准及影像学分型标准
纳入标准:入选病例符合公认的三角籽骨影像学诊断标准[4-5];知情同意。排除标准:既往脚踝或足部骨折史、手术史;足踝炎症、肿瘤、代谢性疾病;由骨软骨坏死或退化引起的脚踝或足部变形;其他先天畸形;足踝部伪影较大影响评价者;患者拒绝公开相关资料者。根据与距骨连接方式,三角骨被分为3种类型:I型是未与距骨连接的孤立骨块,II型是经透明软骨连接到距骨后突,III型是Stieda突(即矢状面延伸超出下胫骨延长线的部分)[6]。鉴于Stieda突是否归入距骨三角骨尚有争议[2],本研究未将Stieda突病例纳入。在矢状位上测量距骨三角籽骨的斜长轴长度[5]。
2 结果
本组共26例,左右踝关节分别为12例、14例。
影像学上以矢状位显示三角籽骨最佳,形态表现为三角形(n=13)、圆形(n=1)、扁圆形(n=3)或不规则形(n=9)。三角骨发生率分别为Ⅰ型 (38.5%)、Ⅱ型(61.5%),大小:3.9mm×3.2mm×2.9mm-21.6mm×9.8mm×6.1mm。CT及其二维、三维后重建可多层面及立体观察三角籽骨(图1、图2)。CT还较好地显示了3例三角籽骨骨质硬化、2例囊变、3例后踝软组织肿胀、1例三角籽骨骨折;MRI较好地显示了距骨三角籽骨囊性变4例、骨髓水肿12例、三角籽骨周围软组织水肿16例、踇长屈肌腱腱鞘积液15例。CT诊断了7例踝关节骨关节病、1例跟骨骨折。MRI诊断了5例踝关节骨关节病,后胫腓下韧带(n=5)、后距腓韧带(n=4)及后踝韧带(n=3)增厚并 PDSPAIR高信号。
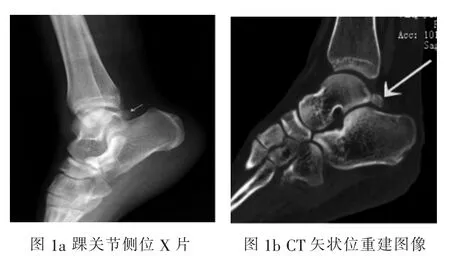
图1 女性39岁三角籽骨综合征患者的踝部X线平片及CT矢状位重建图像
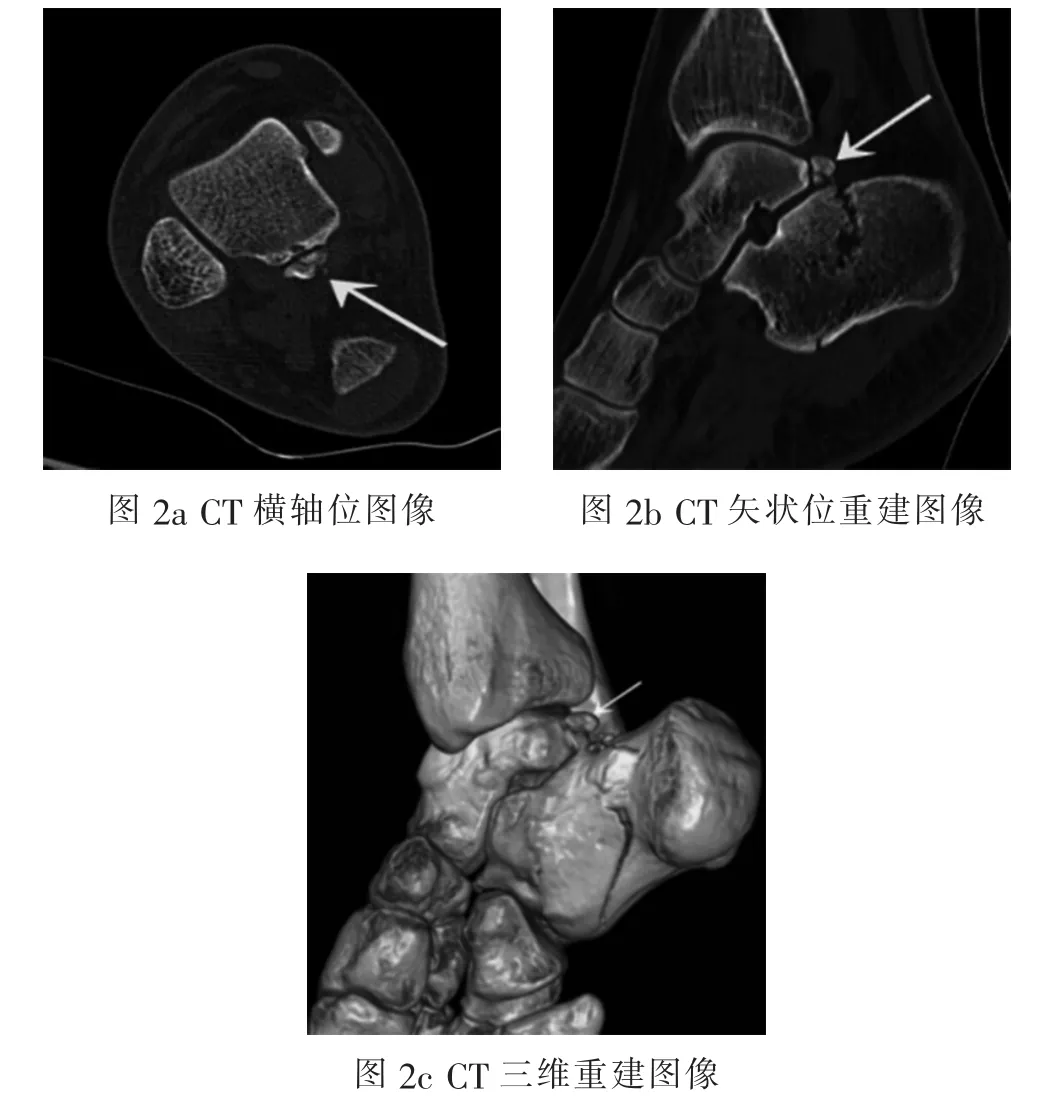
图2 男性24岁CT三角籽骨综合征伴急性骨折患者的CT及其后重建图像
3 讨论
OTS是引起后踝关节慢性反复疼痛常见的病因之一,首次报道于1804年。距骨后外侧的二次骨化中心发生在8-15岁之间,并多在1年内与距骨融合,但约7% 的病例不融合[2]。距骨后突被踇长屈肌腱沟分为外侧结节和较小的内侧结节,当距骨后外侧突较长较大时称为stieda突,若不融合则形成三角籽骨,后者通过软骨与距骨后缘相连[6]。因此,有必要将 Stieda突与距骨三角籽骨区分开来[2]。OTS的损伤机制被描述为“胡桃夹现象”,因为在足部跖屈期间,后距骨和周围的软组织在胫骨和跟骨之间受到压缩。在需要高度的跖屈应变如芭蕾舞、足球等运动人群中,施加在后踝上的慢性压力会增加其骨和软组织损伤的风险。因此,运动人群中OTS的发病率可高达50%[7]。涉及OTS撞击机制的两个骨结构是胫骨的后部(可能有明显的后下倾斜)及跟骨结节的上表面(可能有突起)。涉及OTS撞击机制的解剖区域的软组织成分包括踇长屈肌的滑膜鞘、胫距和距下关节的后滑膜隐窝[7]。因踇长屈肌腱的正常解剖路径,其运动范围也可能引起后外踝区域疼痛[8]。英文文献中三角籽骨骨折的报道仅为个位数(本组仅1例)。X射线、CT和MRI扫描可用于诊断三角籽骨骨折及其伴随损伤[9]。无骨折的单纯踝关节脱位也是极为罕见的损伤,三角籽骨的存在与踝外侧韧带的信号强度增加之间存在关联,表明外踝存在慢性不稳定,提示三角籽骨也可能为单纯踝关节脱位的危险因素[10]。

图3 女性62岁三角籽骨综合征患者MRI矢状位T1WI及PDSPAIR图像
有学者根据三角籽骨与距骨连接方式将三角籽骨分为3种基本类型。一组研究发现,I型的发生率最少(本组也较少),体积也较小,距胫骨下段较远而距跟骨结节较近。II型的发生率较高,体积也较大,与其他类型相比,长短轴之比差异最明显;此型附着结节处的软组织增厚是疼痛的主要原因。III型的存在尚有争议,可能是因为存在 Stieda的过程,而被一些学者归类为三角籽骨的一种,在芭蕾舞演员中的发病率可达44%,可能因舞蹈者从小训练,导致三角骨的发育受到影响;此型患者的疼痛,多为踇长屈肌腱鞘炎及周围软组织水肿引起踝关节后囊增厚所致[5,11]。 三角籽骨的形态可为圆形、椭圆形、三角形或不规则形[12]。有研究提示,三角籽骨类型、骨髓信号、性别与PAIS临床表现无统计学相关性,但三角籽骨大小是引起PAIS的重要因素,导致PAIS 的三角骨大小平均为 9±3.4 mm[2]。
MRI抑脂序列易于观察到外侧距骨结节和(或)三角籽骨呈高信号的骨髓水肿,其发生与三角籽骨机械过载造成的骨髓内的毛细血管渗漏和间质细胞外液积聚,进而导致微小梁骨折、水肿和(或)出血有关[7]。临床上有骨髓水肿的患者疼痛多较明显,MRI上骨髓水肿常于数月甚至更长时间才能消失[12]。
OTS的主要影像学征象包括:①根据其发生机制,累及的骨质包括三角籽骨、距骨后缘、跟骨上缘、胫骨后下缘,早期表现为受累骨质软骨破损、表面不规则,软骨下骨髓水肿,骨质边缘毛糙不整,晚期可出现软骨融合、骨质增生硬化及小囊变等退变[13-14]。三角籽骨与距骨后缘间距增宽、低信号影中断并见液性信号,提示之间的透明软骨连接撕裂[15-16]。三角籽骨本身也可碎裂成多个结节状或发生骨折[2,9]。②三角籽骨周围软组织肿胀、滑膜炎[17-18]。③累及踇长屈肌腱可出现腱鞘积液(肌腱腱鞘炎),抑脂序列呈高信号。踇长屈腱从内侧穿过三角籽骨,跖屈时对肌腱的重复压力或压迫会导致骨关节炎、滑膜炎和后韧带增厚[2,17]。
常规X线片可能正常,但应仔细观察侧位X线片以评估是否存在Stieda突或三角籽骨。跖屈位X线侧位平片可观察后踝骨性撞击,足部外旋斜位X片有助于识别距骨骨折[6]。X线标准侧位平片仅可显示三角籽骨的存在与否、大致形态结构及其他骨质结构异常,此种内在局限性已被MSCT的矢状面重建图像或MRI矢状位图像所替代。相比X线平片,CT具有更高的密度分辨力,易于清晰显示三角籽骨变形、碎裂、囊变、增生等改变以及后踝其他骨性结构的异常。CT二维及三维后重建成像技术可以多方位、多维度展现三角籽骨与距骨后缘的对应关系,以评估三角骨的存在、类型及是否存在骨折,并能精确测量相关解剖参数;同时还能较好地显示周围软组织肿胀及关节囊内积液等征象[4-5]。但X线片及CT主要局限于骨性结构的观察,其软组织分辨力远不及MRI[4]。放射性核素骨扫描仅能提示OTS的可能存在。而MRI以其无创、高软组织分辨力及对比度,多方位、多序列成像的优势,是目前OTS影像学检查中最敏感、最准确的成像手段,可以提供更加完整全面的诊断信息。MRI图像可用来评估三角籽骨的存在、大小、软骨损伤、软骨下骨髓水肿、距骨融合、滑膜炎症、邻近肌腱损伤、腱鞘炎、外侧韧带损伤及其他软组织异常[2,18]。 MRI 多采用横轴位及矢状位成像,其中以矢状面最为重要[4]。T1WI可较佳显示后踝区域的基本解剖结构,抑脂序列(本研究中采用质子相抑脂序列)更易于显示骨髓水肿或囊变,还可更好显示周围软组织水肿、韧带损伤、滑膜炎及踇长屈肌腱鞘炎[19]。跖屈及伸展位矢状位GRE序列可动态观察三角籽骨的运动,以更好地证实后踝撞击损伤机制[4]。MRI是揭示PAIS及其原因的最有用的成像方法,在OTS的诊断及评估后踝部疼痛方面显示出良好的应用前景。因此,MRI成为诊断OTS及PAIS首选的放射学检查工具[20-21]。
影像学上主要的鉴别诊断如下:①三角籽骨易于误诊为距骨后外侧结节撕脱性骨折 (shepherd骨折)[6,20]。 后者在临床上会出现急性后外踝压痛,伴有距下关节运动疼痛和踇长屈肌被动运动,CT可见到清晰锐利的骨折线,MRI上周围伴骨髓水肿[6]。②距骨后内侧结节的骨折(Cedell骨折),为旋前背屈损伤所致的三角韧带的撕脱性骨折;伴后踝内侧触痛,偶可触及肿块[6];CT可见到清晰锐利的骨折线,MRI上周围伴骨髓水肿。③踝关节骨关节病:多见于中老年人,也可表现为后踝疼痛、关节肿胀、僵硬及活动受限等。影像学上累及全关节的退行性改变,以关节间隙变窄、关节膨大畸形、关节软骨退化损伤、关节边缘及软骨下增生囊变为主要表现,部分可见关节腔内钙化灶及游离体[16]。④踇长屈肌腱鞘炎,MRI上可见单纯肌腱信号增高及腱鞘积液。⑤跟腱病/肌腱撕裂,临床上也表现为跖屈抗阻痛[14],MRI上可见肌腱信号增高、部分可伴肌腱增粗;跟骨后滑囊炎,MRI可见跟骨后滑囊肿胀、积液;Haglund综合征,为跟骨后上方的异常骨性突出所致的跟骨后疼痛性滑囊炎,也是造成后踝疼痛的原因之一[22]。⑥胫骨后肌腱撕裂:偏内侧疼痛,MRI可见胫骨后肌腱信号增高,重者可不连续,无距骨后三角突起或三角籽骨的骨结构改变[4]。
综上所述,OTS具有特征性的影像学表现,多层螺旋CT及MRI检查均可作为三角籽骨综合征的影像学诊断手段,MRI可以提供更加完整全面的诊断信息,宜将MRI作为诊断OTS首选的放射学检查工具。本研究不足之处在于样本量较少,未行多模态影像学对比分析,病例多未经手术或关节镜证实,尚需积累病例进行系统研究。

