舒诺颗粒质量控制研究
田 元,屈小娟,刘建书,刘玉凤,赵玉珍,陈丽英,韩晓玲*
(1.西安力邦制药有限公司,陕西 西安 710000;2.陕西功能食品工程中心有限公司,陕西 西安 710003;3.杨凌职业技术学院,陕西 杨凌 712100)
随着社会经济的发展及人民饮食结构的改变,高血糖、高血压、高血脂等疾病发病率日益上升。在医学上,当空腹血糖≥7 mmol/L时可判定为糖尿病[1]。目前,全球4位糖尿病患者中,中国患者即占1人,中国成人糖尿病患病率居世界第1位[2-3],糖尿病及其并发症严重危害着国民生命健康。
基于此,西安力邦制药有限公司联合陕西功能食品工程中心有限公司,依据中医糖尿病发病理论,合作开发了舒诺颗粒保健食品,该产品以一定量的玉米须、枸杞子、葛根、生地黄、黄芪、五味子、西洋参、富铬酵母及其他辅料加工制成。经功能试验证明该产品能降血糖,可起到辅助预防和治疗糖尿病的作用。
舒诺颗粒配方中:①黄芪[4-7]:可增加胰岛素敏感性,改善胰岛素抵抗,抑制脑干神经元的细胞凋亡,显著改善高血糖和氧化应激引起的中枢神经损伤;还可以防治糖尿病视网膜、心脑血管和肾脏病变等并发症;②西洋参[8-9]:通过保护和恢复胰岛β细胞,增加胰岛素敏感性等多种方式,促进胰岛素分泌;③枸杞子[10]:可保护胰岛功能,改善胰岛素抵抗,预防及控制糖尿病并发症发生。此外,因产品中含葛根素、粗多糖、皂苷等多种生理活性物质,这些成分协同作用,具有辅助降血糖的功能。
因此,本研究对舒诺颗粒中黄芪、西洋参、枸杞子进行定性鉴别,将葛根素、粗多糖、皂苷作为该产品的功效成分,采用薄层色谱法(TLC)鉴定黄芪、西洋参、枸杞子,高效液相色谱法(HPLC)测定葛根素含量,紫外可见分光光度法测定粗多糖、总皂苷含量,并制定葛根素、粗多糖、总皂苷的含量限度,以期为舒诺颗粒质量控制提供依据。
1 材料
1.1 药品与试剂
舒诺颗粒(陕西功能食品工程中心有限公司生产,批号:20171001、20171002、20171003,规格:6 g/袋);舒诺颗粒阴性样品(分别缺少黄芪、西洋参、枸杞子,按舒诺颗粒制备工艺自制);糖化酶(上海惠诚生物科技有限公司);人参皂苷Rb1(批号:110704-201726,纯度91.1%)、人参皂苷Re(批号:110754-201626,纯度97.4%)、人参皂苷Rg1(批号:110703-201731,纯度93.6%)、拟人参皂苷F11(批号:110841-201607)、西洋参对照药材(批号:120997-201309)、黄芪甲苷对照品(批号:110781-201717,纯度:96.9%)、枸杞子对照药材(批号:121072-201611)、葛根素(批号:110752-201615,纯度95.4%)、D-葡萄糖对照品(批号:110833-201707,纯度99.9%)购自中国食品药品检定研究院;硅胶G254薄层色谱板、硅胶G薄层色谱板均购自青岛圣浦林环保科技有限公司;实验用水为超纯水,甲醇为色谱纯,其余试剂为分析纯。
1.2 仪器
离心机(德国sigma 型号:3-30KS);高效液相色谱仪(安捷伦科技有限公司 型号:Agilent 1260);电子天平(德国赛多利斯科学仪器有限公司 型号:BSA224S);数显水浴锅(北京科伟永兴仪器有限公司 型号:HH4);超声清洗仪(昆山市超声仪器有限公司 型号:KQ3200E);紫外分析光度计(上海光谱仪器有限公司 型号:SP-756P)。
2 方法与结果
2.1 薄层色谱法
2.1.1 黄芪鉴别 (1)样品溶液制备。黄芪甲苷对照品溶液[11]:以甲醇为溶剂,制成黄芪甲苷浓度为1 mg/mL的溶液。
黄芪药材溶液[11]:按照2015年版《中国药典》一部黄芪鉴别中规定方法制备。
舒诺颗粒供试品溶液、舒诺颗粒阴性对照液(缺黄芪)[11-12]:按照2015版《中国药典》一部黄芪鉴别中规定方法制备供试品溶液及阴性对照溶液,过D101型大孔树脂柱(内径1.2 cm,柱高15 cm),分别用水50 mL、35% 乙醇50 mL、70% 乙醇80 mL洗脱,收集70% 乙醇洗脱液,蒸干,残渣加甲醇0.1 mL溶解,得舒诺颗粒供试品溶液、舒诺颗粒阴性对照液(缺黄芪)。
(2)鉴别方法[11]。按照2015年版《中国药典》一部中黄芪薄层色谱法规定鉴别。见图1。
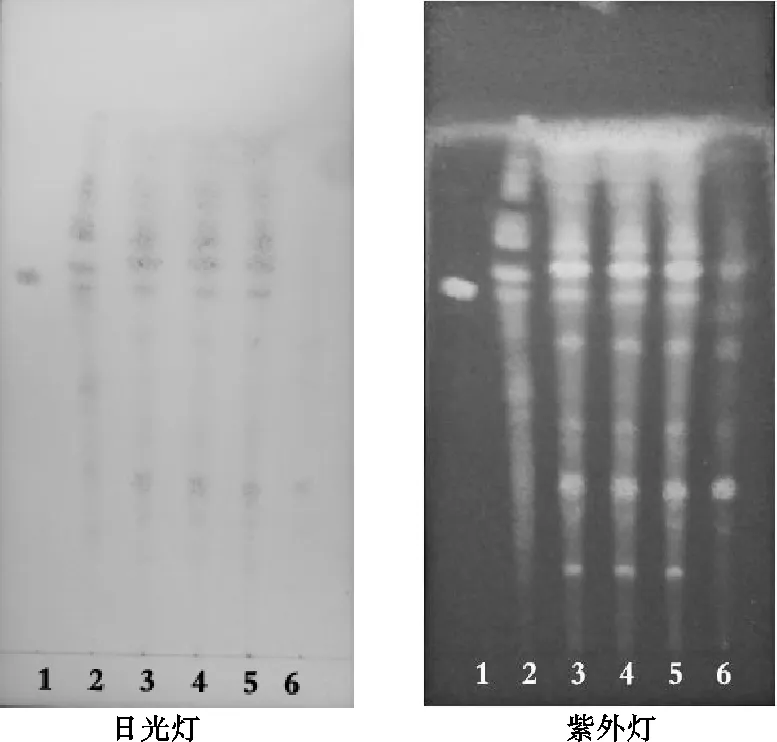
注:1.黄芪甲苷;2.黄芪药材;3.20171001号样品;4.20171002号样品;5.20171003号样品;6.阴性对照。
由图1可知,在薄层色谱中,舒诺颗粒供试品与黄芪甲苷对照品、黄芪对照药材图谱相应位置、荧光斑点逐一对应,清晰可见,且阴性对照无干扰,表明该法具有专一性,可用于舒诺颗粒中黄芪鉴别。
2.1.2 西洋参鉴别 (1)样品溶液制备。混合对照品溶液、西洋参对照药材溶液、西洋参药材溶液[13]:按照2020年版《中国药典》一部西洋参鉴别中规定方法制备。
舒诺颗粒供试品溶液、舒诺颗粒阴性对照溶液(缺西洋参)[13-14]:按照2020年版《中国药典》一部西洋参鉴别中规定方法制备供试品溶液及阴性对照溶液,上D101型大孔吸附树脂柱(内径12 mm,柱高15 cm),以水50 mL洗脱,弃水液,用35% 乙醇50 mL洗脱,弃洗脱液,继用70% 乙醇 80 mL洗脱,收集洗脱液,蒸干,残渣加甲醇0.5 mL溶解,得舒诺颗粒供试品溶液、舒诺颗粒阴性对照溶液(缺西洋参)。
(2)鉴别方法。除以三氯甲烷-甲醇-水(31∶14∶5)5~10 ℃ 放置12 h的下层溶液为展开剂外,其余步骤按照2020版《中国药典》四部中薄层色谱法(通则0502)试验规定进行。见图2。

注:1.混合对照;2.西洋参对照药材;3.西洋参药材;4.20171001号样品;5.20171002号样品;6.20171003号样品;7.阴性对照。
由图2可知,在薄层色谱中,供试品与混合对照品、西洋参对照药材、西洋参药材图谱相应位置、荧光斑点逐一对应,清晰可见,表明该法具有专一性,可用于舒诺颗粒中西洋参鉴别。
2.1.3 枸杞子鉴别 (1)样品溶液制备。枸杞子对照药材溶液、枸杞子药材溶液[13]:按照2020版《中国药典》一部枸杞子鉴别中规定方法制备。
舒诺颗粒供试品溶液、舒诺颗粒阴性对照溶液(缺枸杞子)[13]:取样1.5 g研制成粉末,加水70 mL,其余步骤按照2020版《中国药典》一部枸杞子鉴别中规定方法制备。
(2)鉴别方法。按照2020版《中国药典》四部中薄层色谱法(通则0502)[13]试验规定进行。见图3。
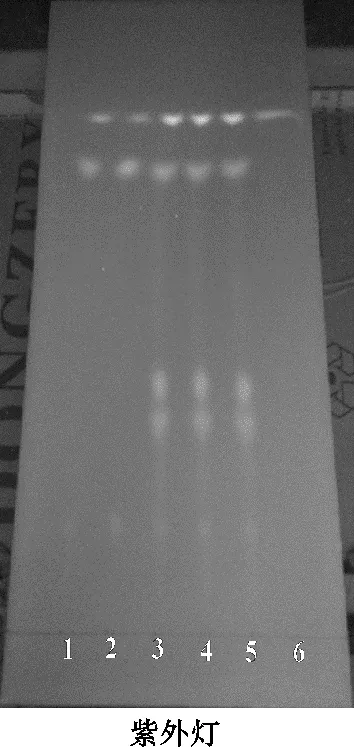
注:1.枸杞子对照药材;2.枸杞子药材;3.20171001号样品;4.20171002号样品;5.20171003号样品;6.阴性对照。
由图3可知,在薄层色谱中,供试品与枸杞子对照药材、枸杞子药材图谱相应位置、荧光斑点逐一对应,清晰可见,表明该法具有专一性,可用于舒诺颗粒中枸杞子鉴别。
2.2 高效液相色谱法
2.2.1 葛根素含量测定 (1)样品溶液制备。标准储备液:精密称取葛根素对照品8.14 mg,用30% 乙醇于100 mL量瓶中溶解定容,得每1 mL含77.66 μg葛根素的标准储备液。
供试品溶液[15]:精密称取舒诺颗粒0.3 g于具塞锥形瓶中,加入30%的乙醇50 mL,称定重量,加热回流30 min,放冷,再称定质量,用30%的乙醇补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液。
(2)色谱条件与系统适应性试验。分别取标准储备液和供试样溶液按照色谱条件:色谱柱:C18色谱柱(4.6 mm×250 mm,5 μm);流动相:甲醇-水(25∶75);流速:1 mL/min;波长:250 nm,进样量10 μL,记录图谱。见图4。
由图4可知,在此色谱条件下,对照品和供试品溶液中被测组分均可达到基线分离,且峰型对称、分离度好。
(3)方法学考察。线性关系考察:分别取标准储备液1 mL、2 mL、3 mL、5 mL、7 mL于10 mL量瓶中,用 30% 乙醇定容。按“2.2.1(2)”色谱条件测定,以对照品浓度为横坐标,峰面积为纵坐标,绘制标准曲线,求回归方程。得葛根素的标准曲线方程为:y=47 597x+33 785(r=0.999 8),结果表明,葛根素在7.766~54.362 μg/mL质量浓度范围内与峰面积呈良好线性关系。
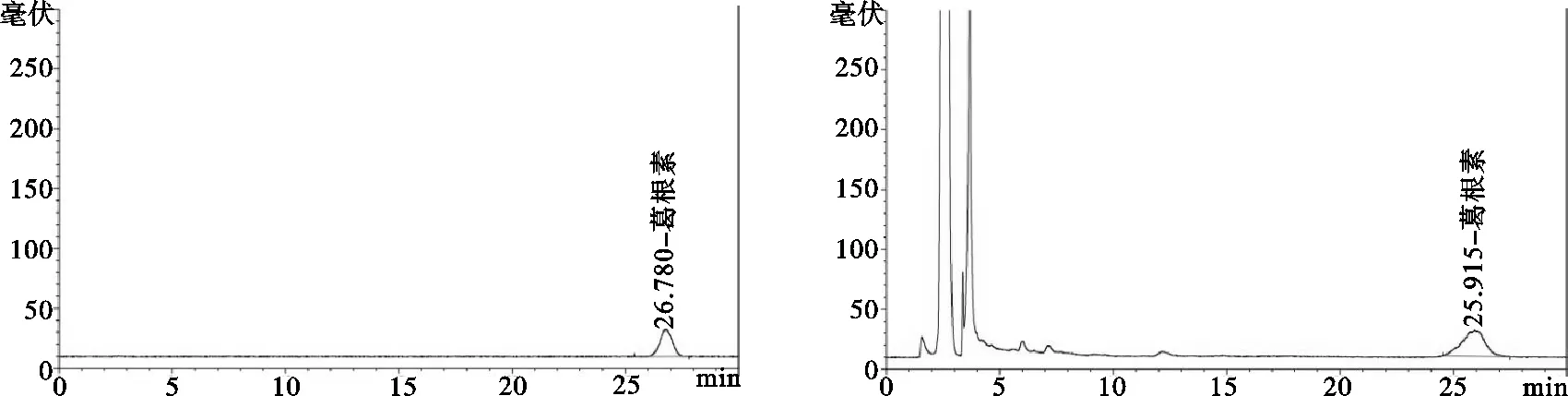
图4 葛根素对照品(A)、舒诺颗粒样品(B)HPLC色谱
检出限试验:以信噪比3∶1相应浓度为检出限,测定葛根素的检出限。结果得出,葛根素的检出限为2.33 mg/100 g。
精密度试验:分别取线性测定中的标3溶液和供试品溶液,各重复进样6次,记录峰面积。结果显示,葛根素面积的RSD分别为0.01%(n=6)、0.35%(n=6),表明仪器精密度良好。
重复性试验:按照“2.2.1(2)”的色谱条件测定同一批次舒诺颗粒样品中葛根素含量,平行测定6份,记录峰面积。结果显示,葛根素平均含量为0.313 6 g/100 g,RSD为0.31%(n=6),表明该方法重复性较好。
稳定性试验:按照“2.2.1(2)”的色谱条件,分别在相对0 h、2 h、4 h、8 h、12 h、24 h时测定同一批次舒诺颗粒样品中葛根素含量,记录峰面积。结果显示,葛根素峰面积的RSD=0.81%,表明室温条件下供试品在24 h内稳定。
加标回收率试验:取已知含量舒诺颗粒(批号:20171001,葛根素含量为0.313 6 g/100 g)0.15 g,各9份,置具塞锥形瓶,分为3组,每组分别加入浓度为77.66 μg/mL的葛根素标准储备液3 mL、6 mL、9 mL,按照“2.2.1(2)”的色谱条件测定,记录峰面积,计算加标回收率。见表1。

表1 葛根素回收率试验结果
由表1可知,葛根素的平均加样回收率为101.92%,RSD为2.56%(n=9),该方法可用于舒诺颗粒中葛根素含量测定。
2.2.2 样品中葛根素含量测定 按照“2.2.1(1)”项下供试溶液的制备方法,制备3批次(20171001、20171002、20171003)舒诺颗粒供试液各2份,按照“2.2.1(2)”的色谱条件测定,记录峰面积并计算葛根素含量。见表2。
由表2计算可得,3批次舒诺颗粒平均葛根素含量为:0.304 9 g/100 g,按平均含量的90%设限,规定葛根素含量不低于0.27%。

表2 葛根素含量测定结果
2.3 紫外可见分光光度法
2.3.1 粗多糖测定 (1)样品溶液制备:标准储备液:称取无水葡萄糖对照品10.01 mg,置10 mL量瓶中,加适量水溶解,稀释至刻度,摇匀,即得每mL含1.00 mg无水葡萄糖标准储备液。
供试品溶液:精密称取舒诺颗粒1.6 g,加乙醚100 mL,40 ℃加热回流1 h,静置冷却,弃乙醚液,残渣水浴挥尽乙醚。加80% 乙醇100 mL,80 ℃加热回流1 h,过滤,滤渣与滤器用80%热乙醇多次洗涤,滤渣及滤器置烧瓶中,加水150 mL,100 ℃加热回流2 h。趁热滤过,用少量热水洗涤滤器,合并滤液和洗液。添加30 mg糖化酶于60 ℃、pH=4.5条件下酶解2 h,电炉上加热至沸,冷却,过滤,取滤液定容至150 mL。取滤液30 mL,置于250 mL锥形瓶,再加入200 mL无水乙醇,混匀,于4 ℃冰箱静置4 h以上,以6 000 r/min离心15 min,弃上清液,残渣用水溶解并定容至50 mL,得供试品溶液。
(2)测定方法:①绘制标准曲线:精密量取1 mL标准储备液于10 mL量瓶中,用水定容至刻度,得到含葡萄糖0.10 mg/mL标准溶液。精密量取标准溶液0 mL、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.2 mL分别置于10 mL的具塞试管中,加水补至2.0 mL,摇匀,精密加入1 mL 5%苯酚溶液,摇匀,迅速精密加入5 mL硫酸,摇匀,放置10 min,100 ℃水浴2 min,取出,迅速冷却至室温,以相应的试剂为空白,在485 nm处测定吸光度,重复3次,以吸光度值(A)为纵坐标,葡萄糖的浓度(μg/mL)为横坐标,进行线性回归。
②含量测定:准确取供试品溶液1 mL于10 mL具塞试管,按照“2.3.1(2)①”步骤测定吸光度并计算粗多糖含量。
(3)方法学考察:线性范围考察:按照“2.3.1(2)”方法绘制标准曲线,得曲线方程为:A=0.046 6×C+0.006 8(r=0.999 6),结果表明,葡萄糖在0~15.00 μg/mL呈良好线性关系。
检出限测定:以20次空白测定值的3倍标准偏差除以标准曲线之斜率(即D.L.=3SD/S)计算,可得粗多糖的检出限。结果得出,粗多糖的检出限为0.04 mg/100 g。
精密度试验:取葡萄糖标准溶液(0.10 mg/mL)0.6 mL,加水补至2 mL,依法测定吸光度值,结果表明葡萄糖吸光度的RSD为0.10%(n=6),仪器精密度良好。
重复性试验:取20171001批次舒诺颗粒1.6 g,共6份,按“2.3.1(1)”方法制备供试品溶液,依法测定,测量并计算粗多糖平均含量。测得粗多糖平均含量为0.968 2 g/100 g,RSD为1.010 9%,结果表明,该方法重复性较好。
稳定性试验:取同一供试品溶液,分别在0、2、4、8、12、24 h时依法测定吸光度,可得各时间样品吸光度的RSD=1.25%,表明室温条件下供试品在24 h内稳定。
加标回收率试验:取20171001批号舒诺颗粒(粗多糖含量为0.968 2 g/100 g)0.8 g,各9份,分3组,每组分别加入浓度为1.00 mg/mL的葡萄糖标准贮备液4 mL、8 mL、12 mL,按“2.3.1(1)”项下方法制备供试品溶液,依法测定,记录吸光度,并计算加标回收率。见表3。

表3 回收率试验结果
由表3可知,粗多糖的平均加样回收率为98.27%,RSD为1.22%(n=9),该方法可用于舒诺颗粒中粗多糖含量测定。
(4)样品中粗多糖含量测定。分别测定不同生产批号的3批样品,计算粗多糖含量。见表4。
由表4计算可得,3批次舒诺颗粒平均粗多糖含量为:0.966 g/100 g,按平均含量的90%设限,规定粗多糖含量不低于0.87%。
2.3.2 总皂苷测定 (1)样品溶液制备:标准贮备液[16]:取人参皂苷标准品0.024 2 g,用甲醇溶解定容至10 mL,制成2.36 mg/mL的人参皂苷Re标准液。
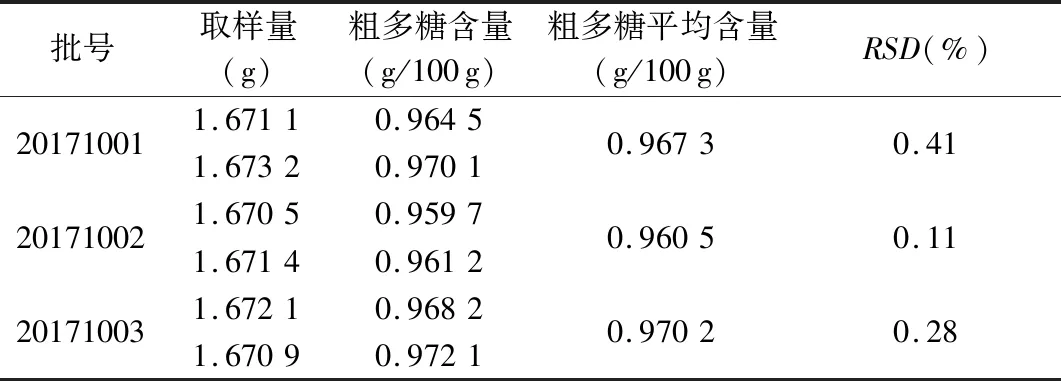
表4 粗多糖含量测定结果
供试品溶液[16]:称取舒诺颗粒1 g,置于25 mL量瓶中,加适量水超声30 min,再用水定容至25 mL,摇匀,放置,滤过。吸取上清液1.0 mL进行柱层析。柱层析方法按照2020年版《保健食品理化及卫生指标检验与评价技术指导原则》中总皂苷测定方法进行。
(2)测定方法:标准曲线绘制:精密吸取标准贮备液20 μL、40 μL、60 μL、80 μL、100 μL、120 μL于蒸发皿中水浴挥干(低于60 ℃),在已挥干的蒸发皿中准确加入0.2 mL 5% 香草醛冰乙酸溶液,转动蒸发皿,使残渣溶解,加0.8 mL高氯酸,混匀后移入10 mL带塞刻度离心管中,60 ℃水浴10 min,取出,冰浴冷却后,准确加入冰乙酸5.0 mL摇匀,以1 cm比色池于560 nm波长处与标准管共同进行比色测定。以吸光度为纵坐标,人参皂苷Re浓度(μg/mL)为横坐标,进行线性回归。
含量测定:准确移取供试品溶液1 mL于10 mL具塞试管,按照“2.3.2(2)”步骤测定吸光度值并计算总皂苷含量。
(3)方法学考察:线性范围考察:按照“2.3.2(2)”方法绘制标准曲线,得回归方程为:y=240.84x-9.6157(R2=0.999 1),结果表明,人参皂苷Re在47.20~283.20 μg/mL内呈良好线性。
检出限测定:以20次空白测定值的3倍标准偏差除以标准曲线之斜率(即D.L.=3SD/S)计算,可得总皂苷的检出限。结果得出,总皂苷的检出限为0.17 mg/100 g,检出限越低,灵敏越度高。
精密度试验:取人参皂苷标准溶液(2.36 mg/mL)60 μL,依法测定吸光度值,结果人参皂苷Re吸光度的RSD为0.324 8%(n=6),表明仪器精密度良好。
重复性试验:取20171001批次舒诺颗粒1 g,共6份,按“2.3.2(1)”项下方法制备供试品溶液,依法测定,测得总皂苷(以人参皂苷Re计)平均含量为0.324 7 g/100 g,RSD为1.85%,表明该方法重复性较好。
稳定性试验:取同一供试品溶液,分别在0、2、4、8、12、24 h时依法测定吸光度,可得各时间样品吸光度的RSD=1.97%,表明室温条件下供试品在24 h内稳定。
加标回收率试验:取20171001批号舒诺颗粒(总皂苷(以人参皂苷Re计)含量为0.324 7 g/100 g)0.5 g,各9份,置100 mL量瓶中,分为3组,分别精密加入人参皂苷Re标准贮备液(2.36 mg/mL)0.4、0.8、1.2 mL,依法测定吸光度,并计算加标回收率。见表5。

表5 回收率试验结果
由表5可知,总皂苷的平均加样回收率为99.02%,RSD为1.63%(n=9),该方法可用于舒诺颗粒中总皂苷含量测定。
(4)样品中总皂苷含量测定。按正文分析方法分别测定不同生产批号的3批样品,计算含量。见表6。
由表6计算可得,3批次舒诺颗粒平均总皂苷含量为:0.320 3 g/100 g,按平均含量的90%设限,规定总皂苷含量不低于0.28%。
3 讨论
尽管单成分鉴定、含量测定易于实现,但在复方制剂中,由于受多种因素干扰,因而成分鉴别、含量检测方法需根据实际情况调整。

表6 总皂苷含量测定结果
3.1 薄层色谱
采用《中国药典》方法对黄芪和西洋参进行薄层鉴别试验时,供试品色谱背景较重,斑点较淡,本研究遂对方法进行了调整。
(1)黄芪薄层色谱鉴别。与《中国药典》鉴定方法相比,增加了供试样品溶液大孔吸附树脂分离纯化步骤,其中70%乙醇洗脱,结果薄层试验条带背景较浅,薄层结果斑点清晰,分离度好。
(2)西洋参薄层色谱鉴别。与《中国药典》鉴定方法相比,增加了供试样品溶液大孔吸附树脂分离纯化步骤,并以三氯甲烷-甲醇-水(31∶14∶5) 5~10 ℃放置12 h的下层溶液为展开剂,得到的薄层色谱斑点清晰、分离好,且各特征成分Rf值适宜,阴性对照无干扰。
3.2 紫外分光光度计
本研究粗多糖含量测定与保健食品中粗多糖含量测定方法比较,增加了糖化酶水解糊精步骤。最终结果表明,当糖化酶添加量为30 mg,酶解时间2 h时,糊精酶解完全,去除了干扰,确保了检测结果的准确性。
4 结论
本研究建立了舒诺颗粒中黄芪、西洋参、枸杞子的鉴定方法,以及葛根素、粗多糖、总皂苷的含量测定方法,并规定葛根素含量不低于0.27%,粗多糖含量不低于0.87%,总皂苷含量不低于0.28%,为该产品的质量控制提供了可靠的依据。

