负载纳米零价铁的铁碳材料制备及其降解抗生素性能研究
权 衡,牛 琳,2,时 迪,汪 霞,梁为纲,赵晓丽*
1.中国环境科学研究院,环境基准与风险评估国家重点实验室,北京 100012
2.清华大学环境学院,北京 100084
抗生素是20世纪最伟大的医学发现之一,因其强大的灭活和杀灭微生物的能力而被广泛应用于人类健康医治[1].磺胺类抗生素是我国生产和使用最多的抗生素之一,是一类广泛用于兽医临床的抗菌药物[2],但是有研究表明,大部分磺胺类抗生素在使用后会以原始形态或代谢物的形式进入并残留于环境[3],有研究在水体中检测出300、500和1 000 ng/L的磺胺噻唑(sulfathiazole,STZ)、磺胺甲恶唑和磺胺甲嘧啶[4].磺胺类抗生素会导致细菌抗药性变强,并且对水生生物具有毒性,进而对生态环境造成危害[5],因此需要探索一种高效可行的方法降解水体中残留的磺胺类抗生素.
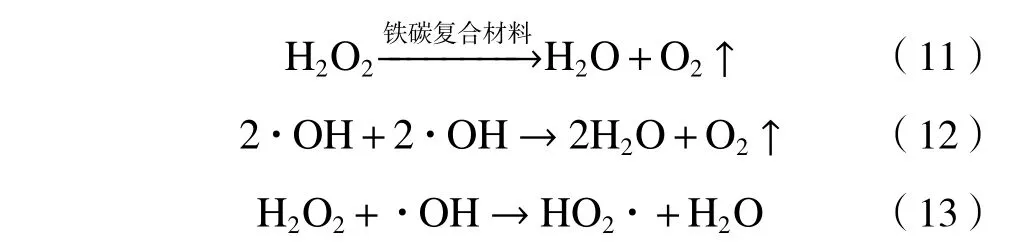
目前,常用的降解抗生素的方法包括吸附[6]、生物降解[7]和高级氧化工艺(advanced oxidation process,AOPs)[8-9],其中属于高级氧化技术的Fenton氧化法由于能够快速高效地降解抗生素而受到了广泛关注[10],这是因为反应产生的羟基自由基(∙OH)具有极强的氧化性,能够快速高效地氧化有机污染物,具体反应过程[11]如下:
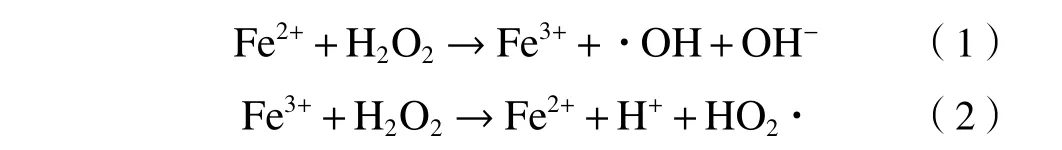
但是,由于传统Fenton法存在着二次污染、需要调节pH以及催化材料难以回收利用等问题[12],因此研究人员将目光转向了非均相Fenton技术.
近年来,基于纳米零价铁(nano zero-valent iron,nZVI)的非均相Fenton催化剂成为研究热点,这是因为与普通铁材料相比,nZVI具有较大的比表面积和较强的反应活性,能够更快更高效地降解目标有机污染物[13],然而,nZVI颗粒具有较强的磁吸引力和范德华力而极易团聚形成大颗粒或被空气中的氧气氧化使其活性降低,因此限制了实际应用[14-15],为了解决该问题,通常将nZVI固定在载体材料上[16],在众多载体材料中,碳材料具有优异的化学稳定性和热稳定性,又因为其具有成本低、易于制备的特点,因此被认为是一种理想的nZVI载体[17].
目前国内外研究中常见的碳负载nZVI的合成方法有液相还原法[18]、电化学沉积法[19]和碳热法[20-21],其中,碳热法具有易操作以及nZVI负载量大的优点,是一种常用的合成方法之一[22].然而,当前常被用作合成碳负载nZVI碳源的葡萄糖、蔗糖等有机化合物与铁之间形成的Fe−O键在高温条件下不稳定,容易造成nZVI的聚集[23].近年来,单原子铁催化剂成为非均相Fenton催化剂的研究热点,这是因为Fe−N键在高温条件下比Fe−O键更稳定,并且铁和含氮有机物之间的强相互作用能够阻止铁原子的迁移和聚集,从而产生nZVI及单原子铁[24],同时,有机组分碳化为石墨碳,能够作为载体固定nZVI和单原子铁.
该研究借鉴了单原子铁催化剂的合成策略,选择2种含氮有机化合物作为配体,含有有机组分的醋酸亚铁作为铁源,采用机械化学研磨法制备了2种含铁有机聚合物,以制备的聚合物为前驱体,高温裂解后得到高负载nZVI的铁碳材料,并对材料进行表征,以STZ为目标污染物,评价了铁碳复合材料的催化性能,研究了铁碳比(醋酸亚铁与有机配体的质量比)、初始pH、过氧化氢(H2O2)投加量、铁碳复合材料投加量和STZ初始浓度等因素对降解反应的影响,评估了铁碳复合材料的重复利用性和稳定性,同时也探究了2种铁碳复合材料的Fe@C-H2O2体系降解STZ的机理.STZ是一种常见的磺胺类抗生素,磺胺类抗生素会导致细菌抗药性变强,并且对水生生物具有毒性,进而对生态环境造成危害[5],然而由于抗生素的难生物降解性和较好的水溶性,很难通过传统污水处理工艺降解,因此研究STZ的非均相Fenton氧化降解对于解决STZ在水体中的污染具有重要意义.
1 材料与方法
1.1 试验试剂
三聚氰胺(MA)(99%)、乙二胺四乙酸(EDTA)(99%)、醋酸亚铁、叔丁醇、1,4-苯醌、糠醇、2,4-二硝基苯肼(98%)和二甲基亚砜均购自百灵威化学有限责任公司(北京),H2O2(30%)购自上海国药化学试剂有限公司,所有化学物质均为分析级,超纯水为屈臣氏蒸馏水.
1.2 铁碳复合材料的合成
选择醋酸亚铁作为含铁前体,以EDTA和MA为配体,采用机械化学法制备了铁-配体复合物,即原材料在行星球磨机(BM400,北京研磨仪器有限公司)中以300 r/min的转速研磨3 h.醋酸亚铁与有机配体的质量比(铁碳比)分别为1∶3、1∶1、2∶1、3∶1和4∶1.然后将2种铁-配体复合物在N2气氛以及800℃条件下热解2 h,得到负载nZVI的铁碳复合材料.
1.3 表征方法
采用日本日立(Hitachi)超高分辨冷场发射扫描电子显微镜(Regulus8100配套能谱仪,Octane Elect EDS系统Octane Elect Super-70 mm2,美国EDAX公司)和场发射TEM(Tecnai G2 F30场发射透射电子显微镜,电压300 kV,美国FEI公司)对铁碳复合材料的形貌和晶体结构进行研究.X射线衍射分析仪(XRD)的型号为D8 Advance,由德国布鲁克公司生产,电压为40 kV,电流为40 mA,步长为0.02°,测试速度为0.1 s/步,铜靶,入射线波长为0.154 18 nm.傅里叶变换红外光谱(FTIR)由美国赛默飞世尔科技公司的尼高力红外光谱仪Nicolet iS5记录,波数范围为400~4 000 cm−1.X光电子能谱仪(XPS)的型号为ESCALAB 250Xi,由美国赛默飞世尔科技公司生产,单色Al Ka(hv为1 486.6 eV),功率为150 W,500μm直径束斑,结合能以C 1s 284.8校准.分别使用Brunauer-Emmett-Teller (BET)和Barrett-Joyner-Halenda(BJH)方法,根据77 K下的N2吸附-解吸等温线(美国Quantachrome Instruments Quadrasorb EVO仪器),估算铁碳复合材料的比表面积.
1.4 降解试验
所有降解试验均在100 mL塑料瓶中进行,用0.1 mol/L HCl或NaOH溶液调节溶液初始pH.反应液于室温下在摇床中振荡(300 r/min),每隔一定时间取出1 mL样品,用0.22μm尼龙膜过滤后,经高效液相色谱(high-performance liquid chromatography,HPLC)测定.试验研究了2种铁碳复合材料不同铁碳比、溶液初始pH(3~11)、H2O2投加量(5~40 mmol/L)、铁碳复合材料投加量(5~50 mg/L)、STZ初始浓度(10~160 mg/L)等因素对降解试验的影响.STZ降解率(η)的计算公式:
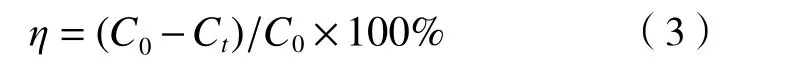
式中:C0、Ct分别为STZ在初始时刻和t时刻的浓度,mg/L;η为STZ的降解率,%.
1.5 分析方法
STZ浓度使用Waters E2695高效液相色谱仪(美国安捷伦公司)测定,流动相为甲醇和水(体积比为35∶65),流速为1.0 mL/min,安捷伦C18柱(4.6 mm×250 mm,5μm),柱温为35℃.使用PDA紫外检测器测定STZ浓度,检测波长为286 nm.使用DELTA-320 pH计(梅特勒-托利多仪器有限公司)测量溶液的pH.采用显色法检测∙OH浓度,∙OH与过量的二甲基亚砜反应生成甲醛(HCHO),甲醛与2,4-二硝基苯肼(DNPH)反应生成甲醛-2,4-二硝基苯肼(DNPH-HCHO),使用Waters E2695高效液相色谱仪测定DNPH-HCHO的量,从而定量反应过程中生成∙OH的量.总有机碳(TOC)浓度由TOC分析仪(TOC-L CPH,日本岛津公司)检测.反应后铁离子的浸出浓度采用电感耦合等离子体质谱仪(ICP-MS,美国安捷伦公司)测定.
1.6 动力学模型
为了确定铁碳复合材料在STZ降解中的催化作用,采用3种典型的动力学模型−零级动力学模型〔见式(4)〕、拟一级动力学模型〔见式(5)〕和拟二级动力学模型〔见式(6)〕对STZ降解动力学进行拟合.
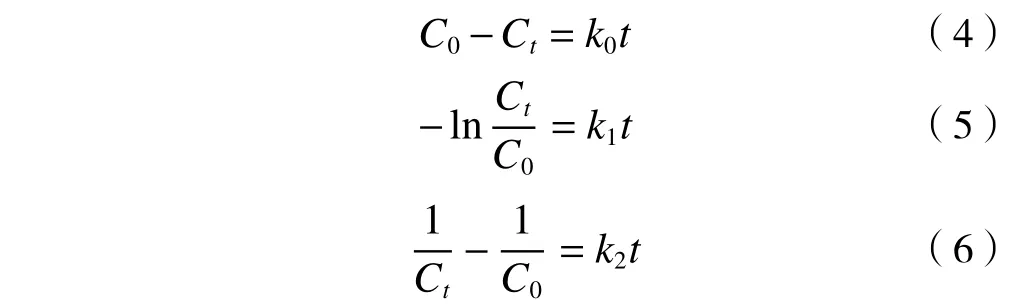
式中:k0为零级动力学模型的反应速率常数,mol/(L∙min);k1为拟一级动力学模型的反应速率常数,min−1;k2为拟二级动力学模型的反应速率常数,L/(mol∙min).
2 结果与讨论
2.1 铁碳复合材料的表征
为研究铁碳复合材料的结构和形貌,采用高分辨率透射电镜对Fe@EDTA和Fe@MA材料进行表征.Fe@EDTA材料由碳层和均匀分布在碳层中的超细nZVI组成〔见图1(a)〕,Fe@MA材料的零价铁团聚形成直径400 nm的大颗粒,并被厚度约为30 nm的碳壳包裹〔见图1(c)〕.在SEM图像〔见图1(b)(d)〕中,2种材料的表面分别能够观察到均匀分布的Fe0颗粒和大粒径的碳层.

图1 Fe@EDTA和Fe@MA材料的电镜表征Fig.1 The electronics symbol of the Fe@EDTA and Fe@MA materials
在红外光谱中,Fe@EDTA和Fe@MA材料在3 435和3 437 cm−1处的特征峰对应于羟基基团和表面吸附的H2O的伸缩振动[25],1 629和1 622 cm−1处的C=C峰值为石墨化碳的拉伸振动[26]〔见图2(a)〕.在晶体的PXRD图谱〔见图2(b)〕中,44.7°、65.1°和82.4°处的衍射峰表明铁碳复合材料含有大量Fe(JCPDS No.06-0696),在43.5°和73.5°处观察到强度较低的氧化铁特征峰(JCPDS No.39-1088),这可能是因为铁碳复合材料在存储和使用的过程中被氧化造成的[27].
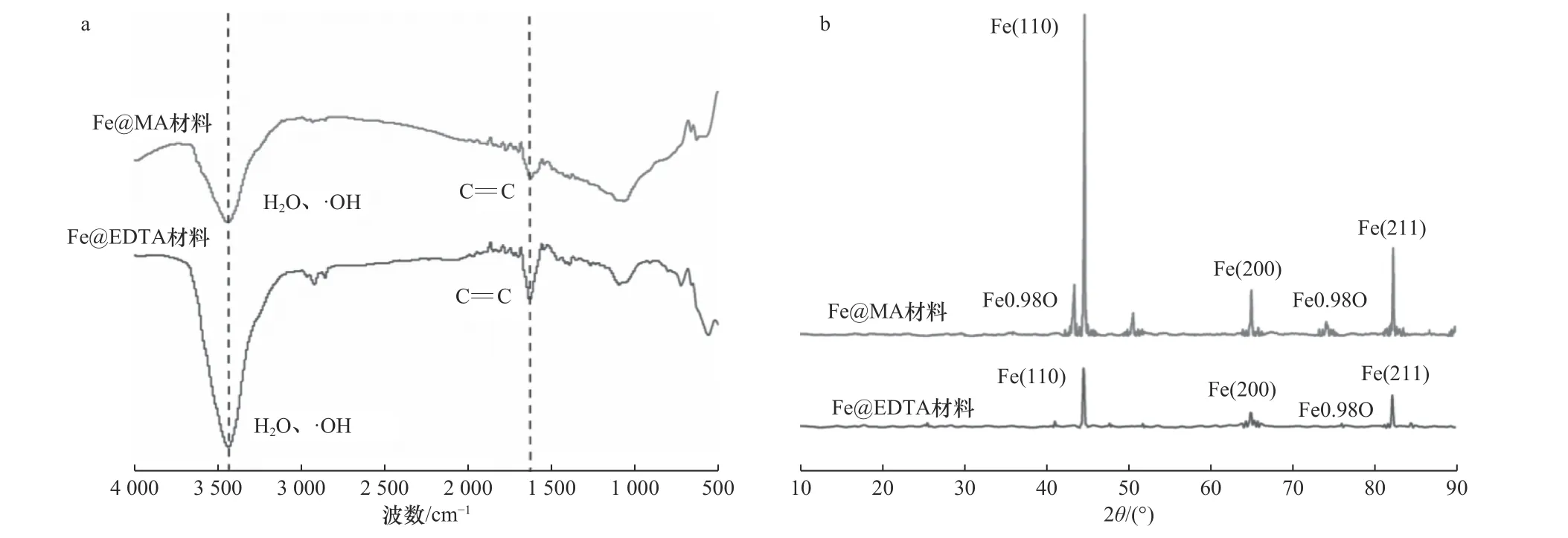
图2 Fe@EDTA、Fe@MA材料的傅立叶红外光谱和XRD衍射图谱Fig.2 The FTIR and XRD patternsof the Fe@EDTA and Fe@MA materials
采用XPS分析铁碳复合材料的表面元素组成.在Fe@EDTA和Fe@MA材料的全扫描谱图中观察到N、Fe和O峰(见图3和图4),N 1s图谱可以拟合成石墨-N(402.1~402.2 eV)、Fe-N(400.7 eV)和吡啶-N(398.4~398.6 eV)3个峰[28-29],表明石墨烯层中的碳原子被氮原子所取代,形成了具有一对p电子的π-共轭体系[28],另外由于氮原子比碳原子更容易与铁原子成键,因此氮原子与铁原子配位形成了Fe−N键,证明了富氮单原子铁结构的存在[30](见图3和图4);C 1s图谱可以拟合为C−C/C−H(284.8 eV)、C−O(285.2~285.3 eV)和C=O(288.5~288.6 eV)[31](见图3和图4);Fe 2p谱图可以拟合出6个峰,包括Fe 2p3/2峰(710.43、712.78 eV)、Fe 2p1/2峰(724.03、726.14 eV)、卫星峰(719.5 eV)[32]和Fe0峰(706.94 eV),其中,结合能为706.94 eV的峰证明了零价铁的存在,710.43 eV处的峰说明了Fe−N键的存在,进一步证明了单原子铁催化剂合成策略的成功,结合能位于710.43和724.03 eV处的峰对应于Fe(Ⅱ),位于712.78和726.14 eV处的峰对应于Fe(Ⅲ),这说明零价铁表面被膜状的氧化铁(FeO、Fe2O3和Fe3O4)部分覆盖[33](见图3和图4);O 1s图谱可以拟合成530.03~533.07、531.51 ~531.79和533.07~533.4 eV处的3个峰,分别为Fe−O、C−O和C=O键[34],进一步论证了铁碳复合材料表面氧化膜的存在(见图3和图4).以上结果表明,利用碳热法制备的nZVI均匀分布在石墨碳上,有效地防止了nZVI的团聚和迁移,说明富氮单原子铁合成策略对于改性nZVI材料具有重要意义.
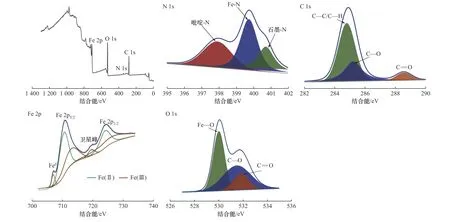
图3 Fe@EDTA材料的XPS谱图Fig.3 XPSspectra of the Fe@EDTA materials
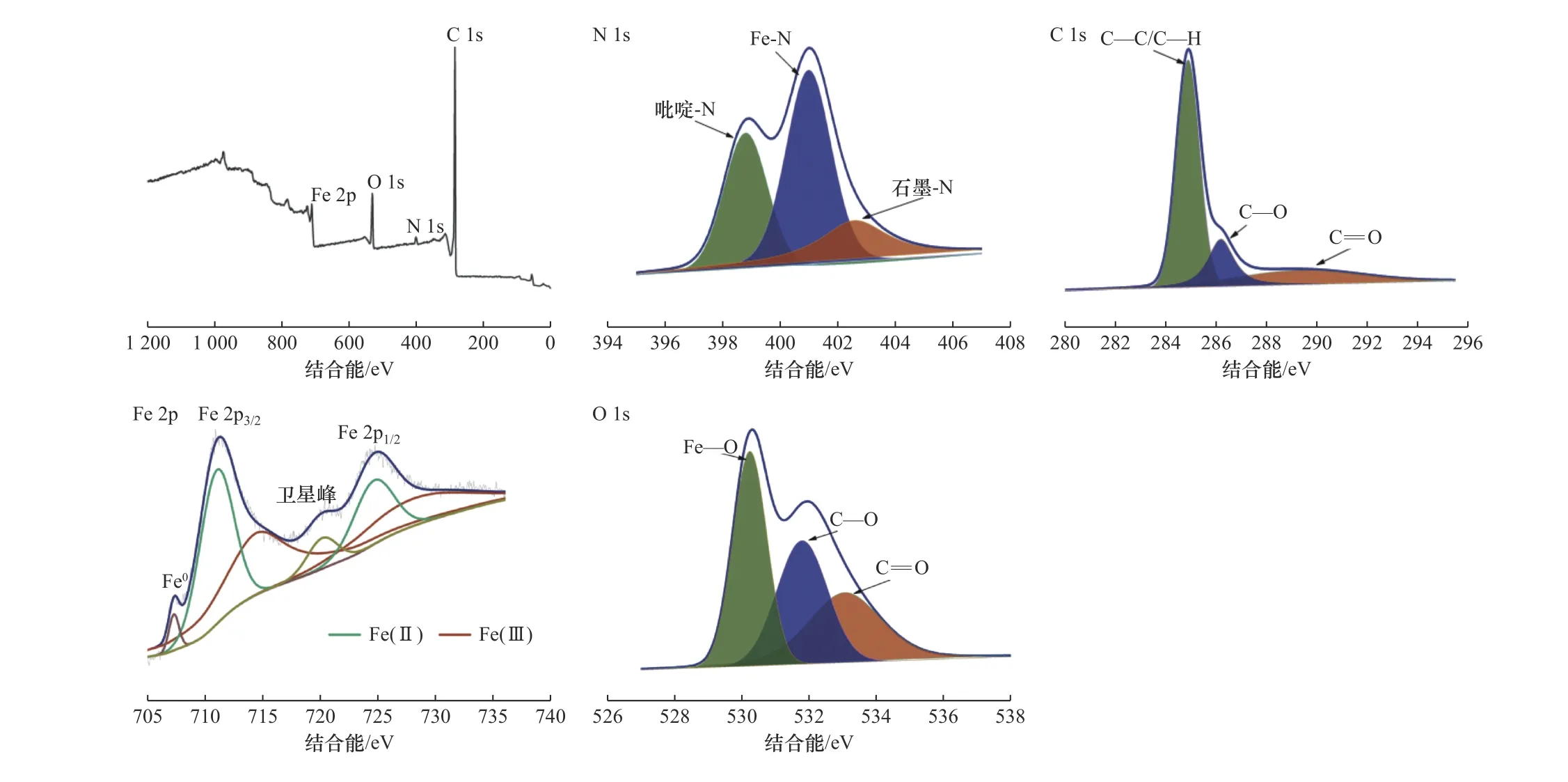
图4 Fe@MA材料的XPS谱图Fig.4 XPSspectra of the Fe@MA materials
为了分析铁碳复合材料的孔隙率和比表面积,进行77 K下N2的吸附和解吸试验,Fe@EDTA和Fe@MA材料均为可逆的IV型等温线,说明铁碳复合材料中含有介孔结构[35]〔见图5(a)〕.另外,Fe@EDTA和Fe@MA材料的BET比表面积分别为31.029和23.814 m2/g,Fe@EDTA的孔径为3.94和6.22 nm,Fe@MA材料的孔径分布较广,为3.71、4.31、5.05、6.8和9.55 nm,表明该铁碳复合材料含有介孔结构〔见图5(b)〕.
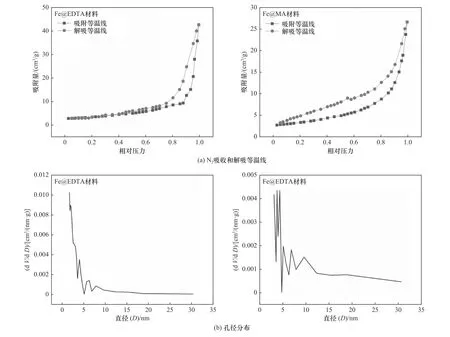
图5 Fe@EDTA和Fe@MA材料的N2吸收和解吸等温线及其孔径分布Fig.5 N2 absorption and desorption isotherms and pore sizedistribution of the Fe@EDTA and Fe@MA materials
2.2 不同催化体系下STZ的降解性能
该研究考察了Fe@EDTA和Fe@MA材料对STZ的降解性能,结果如图6所示.由图6可见,在只加入H2O2而不添加铁碳复合材料的条件下,几乎无法降解STZ;在中性溶液和pH=4的酸性溶液且未外加H2O2的条件下,Fe@EDTA材料几乎无法降解STZ;而在pH=4的酸性溶液中,Fe@EDTA材料在25 mmol/L H2O2活化作用下100 min内可完全降解STZ,值得注意的是,在相同条件下使用普通nZVI对STZ的降解率仅为68%,可能是由于nZVI在储存与使用的过程中因团聚与氧化而降低了反应活性.该结果表明,铁碳复合材料需要在酸性且外加H2O2的条件下才能实现STZ的有效降解,是进行后续降解试验的基础,并且经过改性的铁碳复合材料表现出比普通nZVI更好的反应活性.
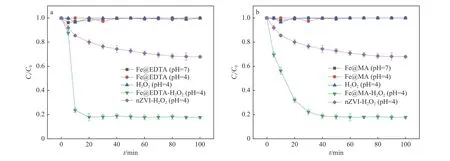
图6 不同催化体系下STZ的降解效果Fig.6 Effect of STZ degardation under different catalytic systems
2.3 不同反应条件对STZ降解效果的影响
2.3.1 铁碳比
Fe@EDTA和Fe@MA材料各设计5组试验,考察铁碳比分别为1∶3、1∶1、1∶2、1∶3和1∶4时2种铁碳复合材料降解20 mg/L STZ的效果,结果如图7所示.从图7(a)可以看出,120 min内,铁碳比为1∶3的Fe@EDTA材料(Fe@EDTA-1∶3)对STZ的降解率为40%,而Fe@EDTA-1∶1可以在90 min内实现完全降解,Fe@EDTA-2∶1、Fe@EDTA-3∶1和Fe@EDTA-4∶1只需要60 min即可以完全降解STZ.从图7(b)可以看 出,120 min内,Fe@MA-1∶3、Fe@MA-1∶1和Fe@MA-2∶1对STZ的降解率分别为61%、68%和92%,Fe@MA-3∶1、Fe@MA-4∶1均可以在60 min内实现完全降解.从试验结果可以看出,随着铁含量占比的增加,铁碳复合材料对STZ的降解率明显升高,然而进一步增加铁的比例,其降解率提升幅度变小.出于节省材料成本的原则,该研究的后续试验使用的铁碳复合材料分别为Fe@EDTA-2∶1和Fe@MA-3∶1.2.3.2溶液初始pH
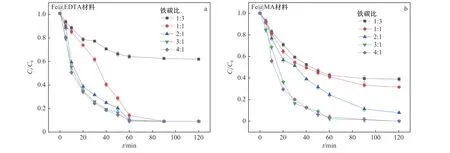
图7 铁碳比对铁碳复合材料降解STZ的影响Fig.7 Influence of Fe-C ratio on degradation of STZ by Fe-Ccomposites
Fe@EDTA和Fe@MA材料各设计5组试验,研究pH分别为3、5、7、9和11的条件下,Fe@EDTA和Fe@M材料诱发的非均相Fenton反应对STZ降解效果的影响.由图8可以看出,铁碳复合材料在酸性(pH=3)条件下拥有最佳催化性能,能够在120 min实现全部降解;在偏酸性(pH=5)条件下,Fe@EDTA材料能够在120 min内降解约40%的STZ,而Fe@MA几乎无法降解STZ;而在中性(pH=7)和碱性(pH=9和pH=11)条件下,Fe@EDTA和Fe@MA材料的催化性能均大大降低,几乎无法降解STZ.
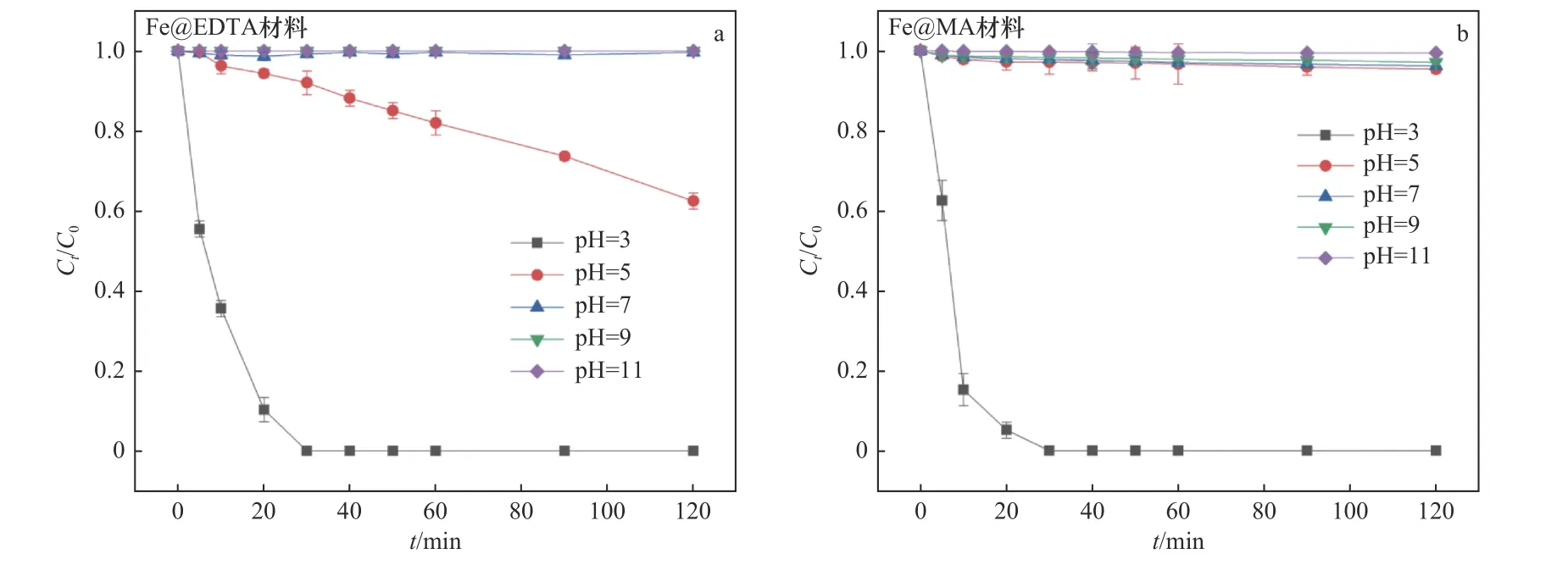
图8 初始p H对铁碳复合材料降解STZ的影响Fig.8 Influenceof initial pH on degradation of STZ by Fe-Ccomposites
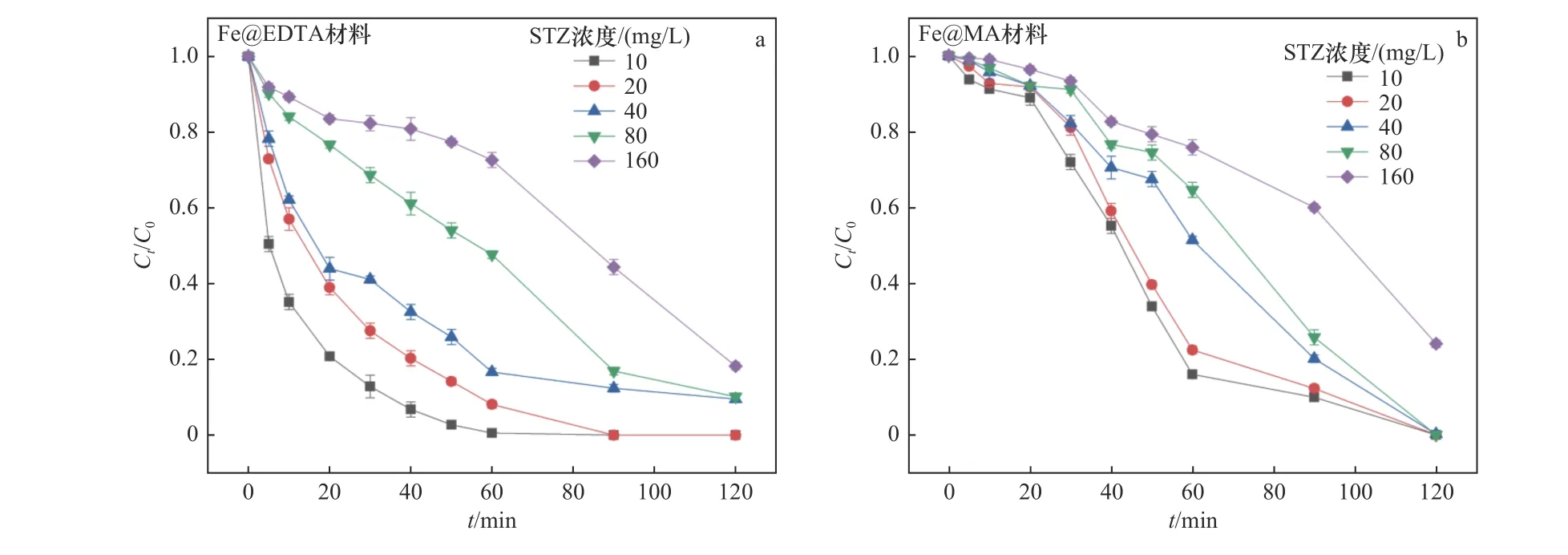
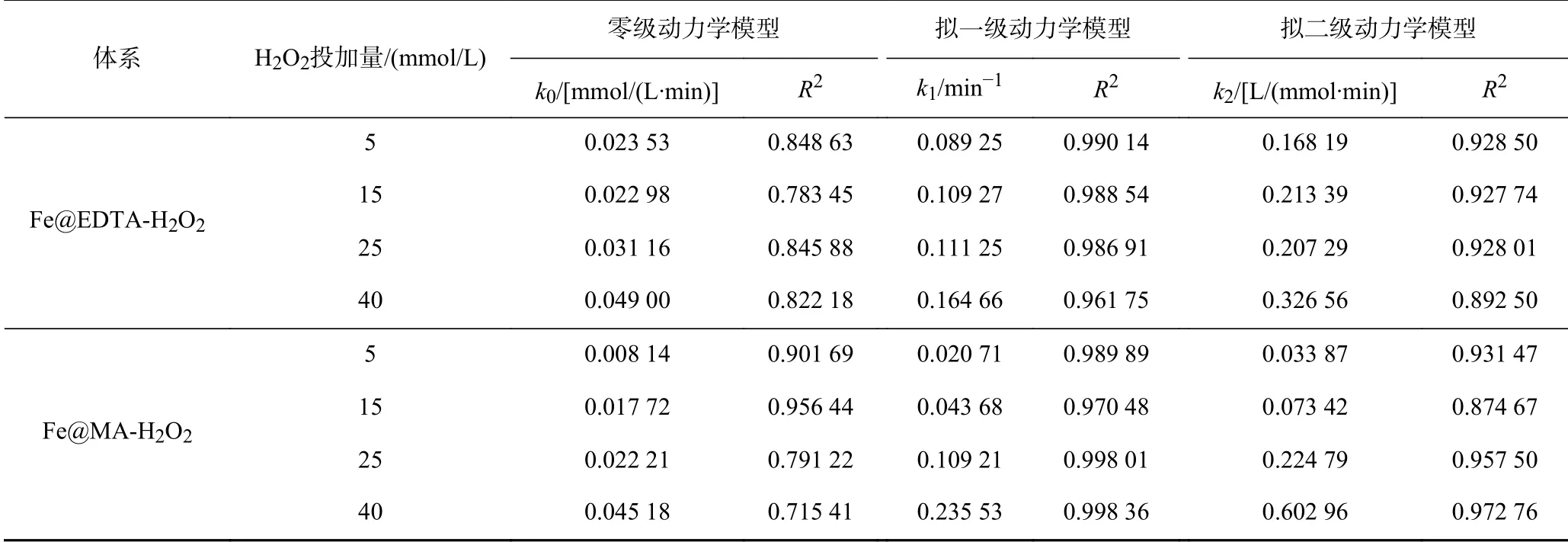
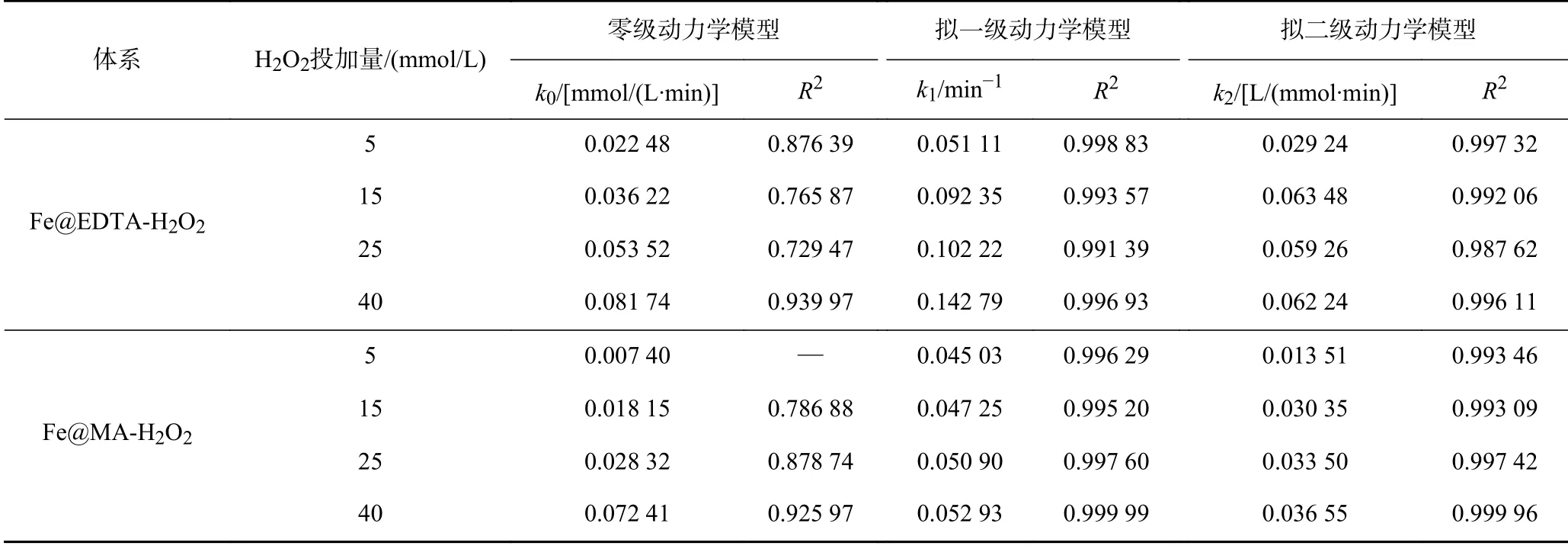
在含有溶解氧的溶液中,铁碳复合材料表面的nZVI极易氧化并在表面形成氧化层,使其具有核壳结构.根据溶液的pH条件,核壳结构的外壳生成Fe3O4或Fe(OH)2等铁氧化物,当水中溶解氧充足时,Fe3O4可以进一步反应生成羟基氧化铁(FeOOH),反应式如下[36]:
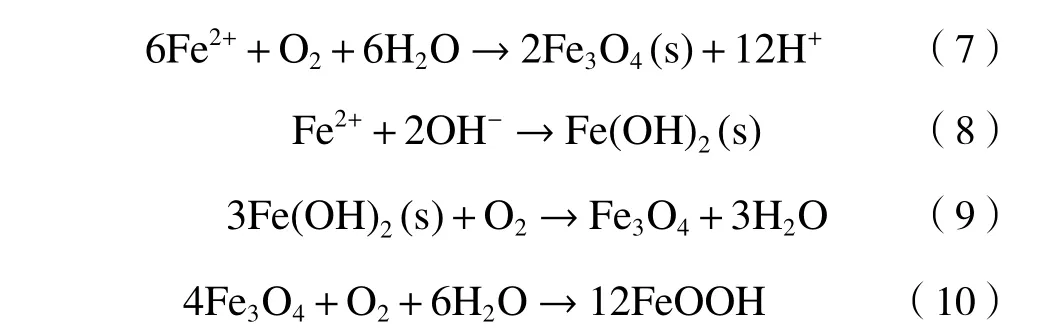
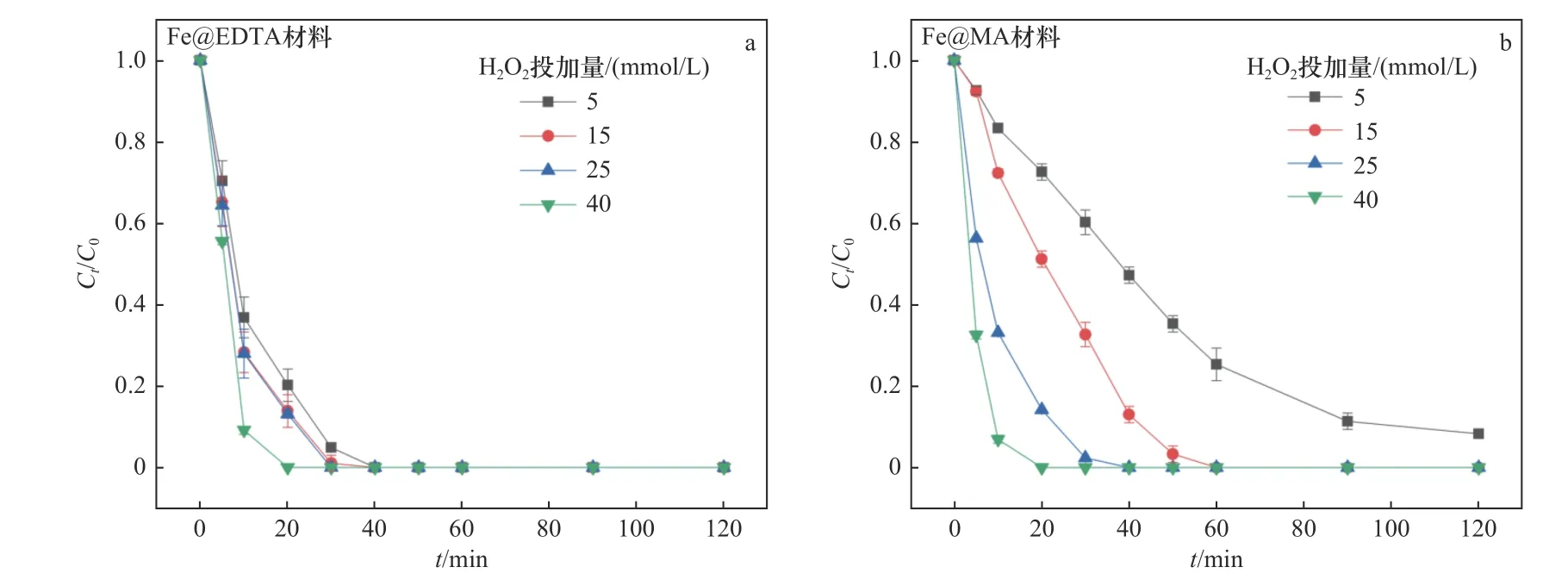
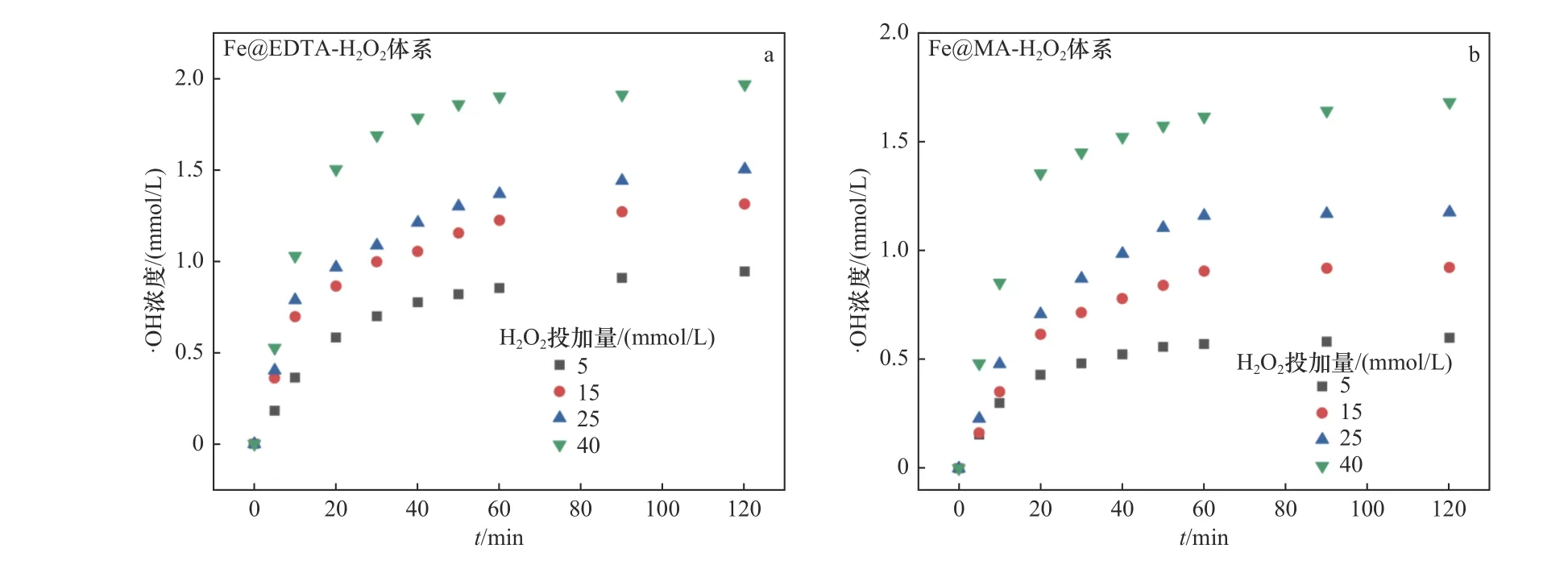
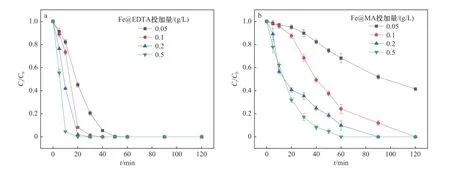
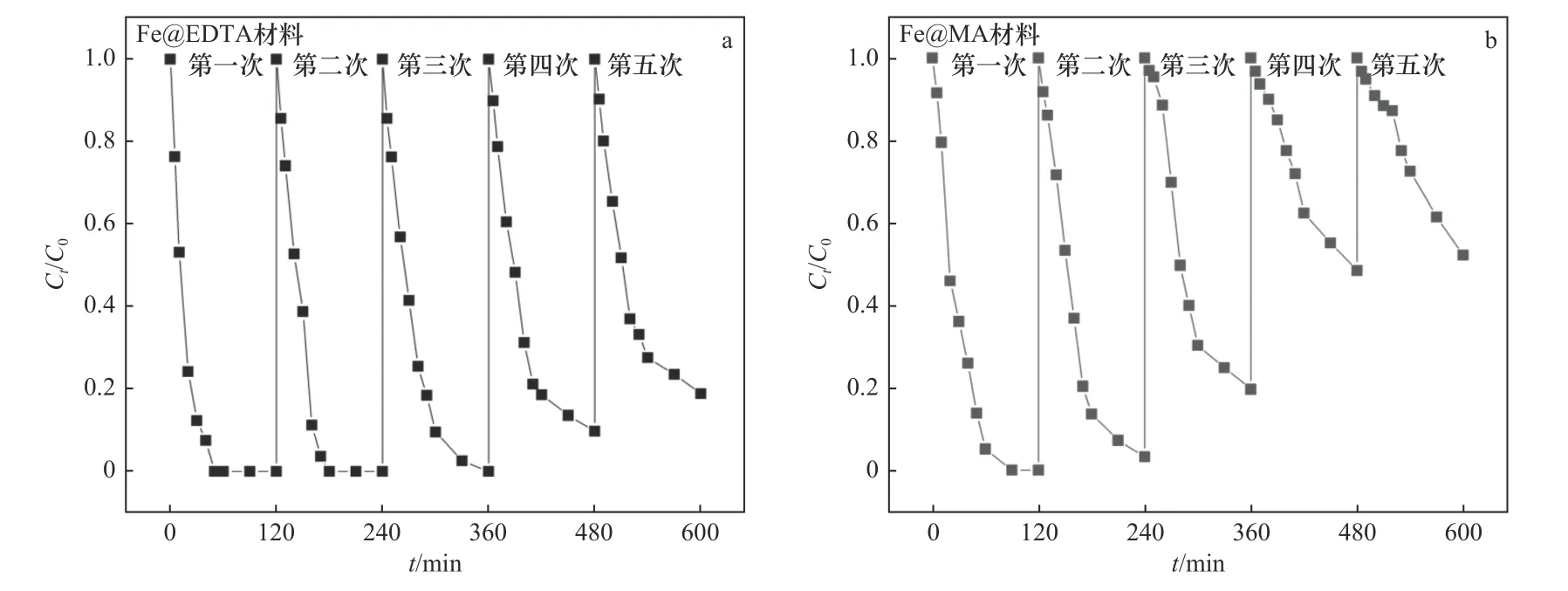
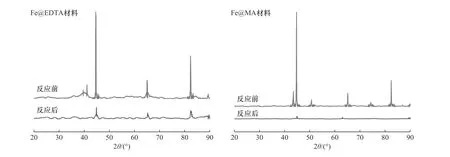
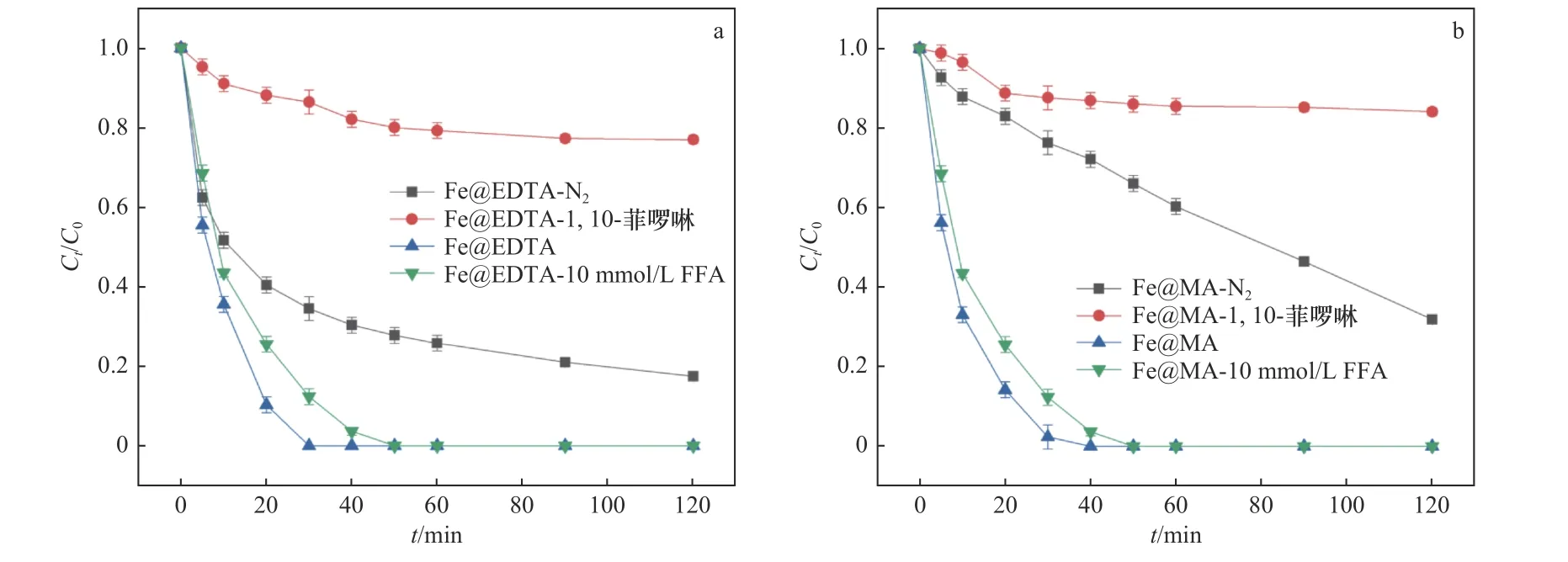
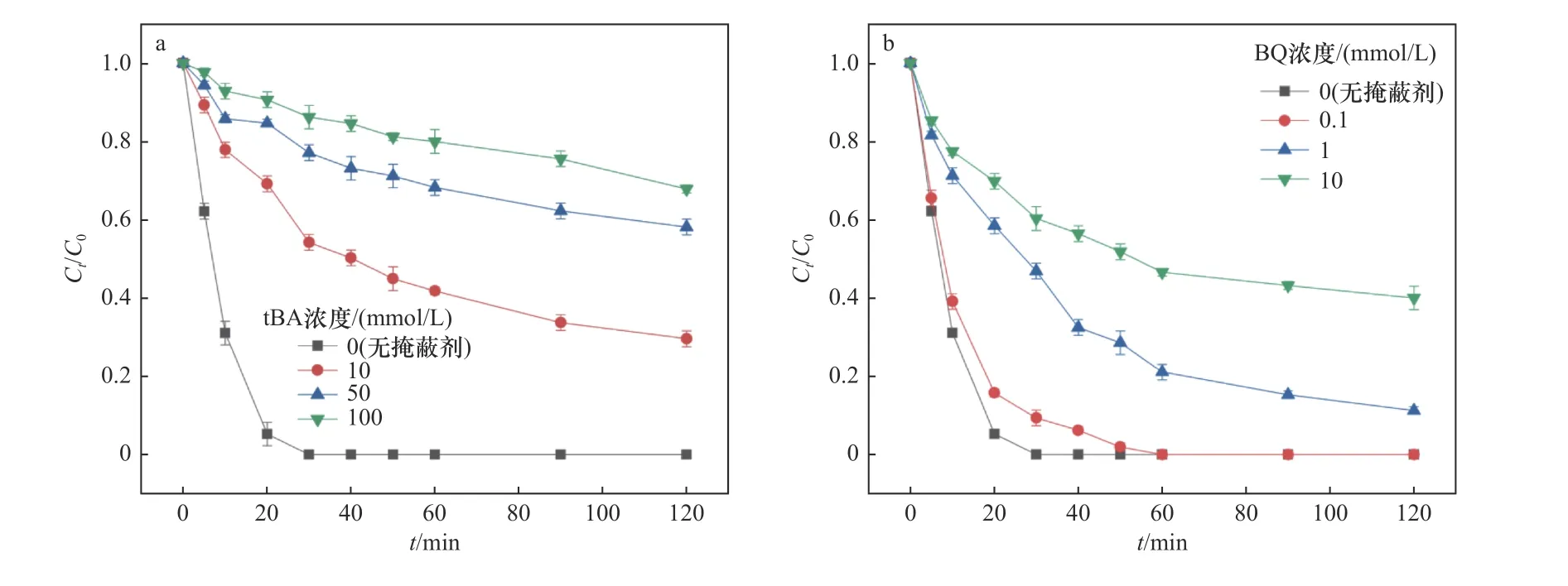
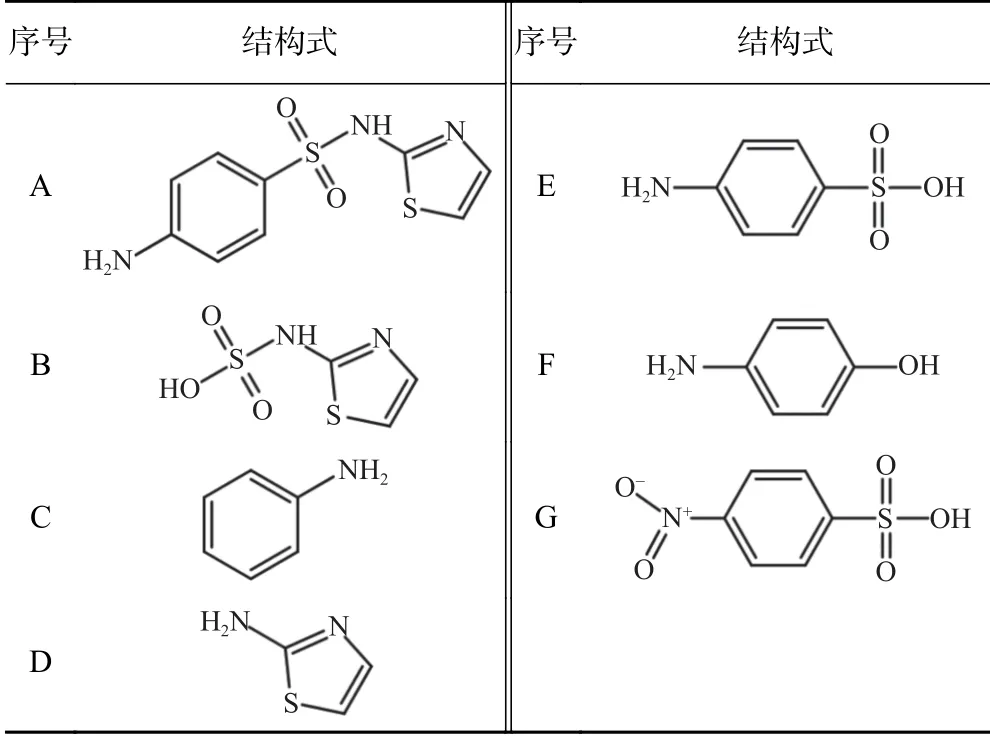
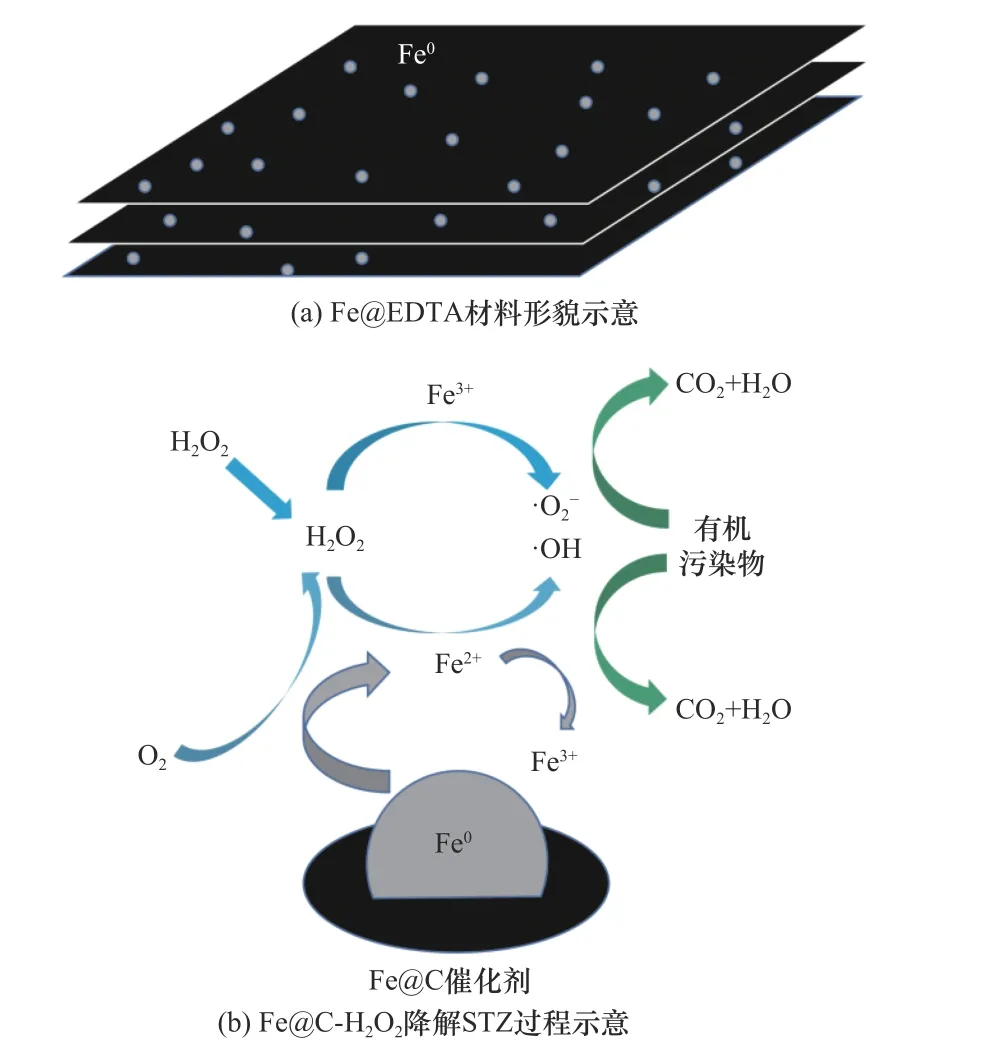
在Fe@EDTA和Fe@MA材料的非均相Fenton催化体系反应过程中,当溶液pH较低时,氧化层较薄,催化剂表面与H2O2的反应位点较多,从而促进了Fe2+与∙OH的生成,使得氧化反应的速率提升.当溶液的pH为中性和碱性时,nZVI表面的氧化层较厚,铁主要以Fe3O4或Fe(OH)2等铁氧化物的形式存在,失去了与H2O2反应的活性,导致∙OH生成量减少,最终降低了铁碳复合材料的催化性能.此外,由于STZ的结构中含有氨基等可电离基团,在水溶液中可以发生酸碱解离反应,因此,水溶液中的STZ在不同pH条件下存在多种解离形态[37].不同pH下STZ的主要解离形态分布如图9所示.STZ的解离常数(pKa)值为2.01±0.3和7.11±0.09,当pH<2.01时,STZ的主要存在形态为阳离子;当pH>7.11时,STZ的主要存在形态为阴离子;当2.01 图9 不同p H下STZ的解离形态分布Fig.9 Dissociation morphology distribution of STZ under different pH conditions 2.3.3 H2O2投加量 Fe@EDTA和Fe@MA材料各设计4组试验,考察H2O2投加量分别为5、15、25、40 mmol/L的条件下,Fe@EDTA和Fe@MA材料诱发的非均相Fenton反应对STZ降解效果的影响.由图10(a)可以看出,H2O2投加量分别为5、40 mmol/L时,Fe@EDTA材料分别能够在40、20 min内实现STZ的完全降解.由图10(b)可以看出:H2O2投加量为5 mmol/L时,Fe@MA材料对STZ的降解率约为92%;当H2O2投加量分别为15、25和40 mmol/L时,分别能够在60、40、20 min内实现STZ的完全降解.STZ的降解率和降解速率均随着H2O2投加量的增多而增加,当H2O2投加量为40 mmol/L时,Fe@EDTA和Fe@MA材料均能够在20 min内实现完全降解,可能是因为随着H2O2投加量的升高,∙OH的含量随之升高,促进了非均相Fenton反应的进行,有利于STZ的降解[40].从图10(a)可以看出,对于Fe@EDTA-H2O2体系,当H2O2投加量从5 mmol/L分别提升至15和25 mmol/L时,STZ的降解速率明显提升,然而继续升高H2O2投加量至40 mmol/L时,STZ的降解速率提升幅度变小,这可能是因为过量的H2O2会导致∙OH的猝灭,∙OH自身也会发生分解反应[41].对于Fe@MA-H2O2体系,H2O2投加量分别为25和40 mmol/L时,STZ的降解率均较高.因此从经济角度综合考虑,铁碳复合材料最佳H2O2投加量为25 mmol/L. 注:溶液初始pH为3,最终溶液pH为6.9,铁碳复合材料投加量为0.2 g/L,STZ的初始浓度为20 mg/L. 从图11可以看出,对于Fe@EDTA和Fe@MA材料,由于水中溶解氧和H2O2的作用,Fe0转化为Fe2+,10 min内均生成大量∙OH,并且Fe@EDTA材料比Fe@MA材料生成更多的∙OH,前者∙OH浓度为0.5~1 mmol/L,后者∙OH浓度为0.3~0.8 mmol/L.另外,Fe@EDTA材料在10 min后继续缓慢生成∙OH,而Fe@MA材料在10 min后∙OH浓度几乎不再发生变化,这说明Fe@EDTA材料表面均匀分布的nZVI能够有效而持久地与H2O2反应生成∙OH,而Fe@MA材料由于被碳包覆,而且自身粒径较大,相比于Fe@EDTA材料,该铁碳复合材料反应活性与持久性略有降低. 图11 Fe@EDTA-H 2O2体系和Fe@MA-H 2O2体系生成的∙OH浓度Fig.11 Concentrationsof ∙OH generated by Fe@EDTA-H2O2 system and Fe@MA-H2O2 system 2.3.4 铁碳复合材料投加量 Fe@EDTA和Fe@MA材料各设计4组试验,考察铁碳复合材料投加量分别为0.05、0.1、0.2和0.5 g/L的条件下,Fe@EDTA和Fe@MA材料诱发的非均相Fenton反应对STZ降解效果的影响.从图12(a)可以看出,在Fe@EDTA材料投加量分别为0.05、0.1、0.2和0.5 g/L的条件下,均能够在120 min内完全降解STZ.从图12(b)可以看出:当Fe@MA材料投加量为0.05 g/L时,反应120 min后STZ的降解率约为60%;当Fe@MA材料投加量分别为0.1、0.2和0.5 g/L时,均能够在120 min内完全降解STZ.这说明STZ的降解速率随铁碳复合材料投加量的增加而增加,STZ的降解率随着铁碳复合材料投加量的增加而上升,原因可能是随着铁碳复合材料投加量增加,H2O2催化分解产生∙OH的速度和∙OH总量也随之增加.对于Fe@MA材料,可以看出当铁碳复合材料投加量为0.05g/L时,反应120 min后STZ的降解率为60%;当铁碳复合材料投加量增至0.1g/L时,降解效果改善明显,能够完全降解STZ;然而当铁碳复合材料投加量继续增加时,降解速率增长幅度变小.原因可能是:①铁碳复合材料投加量过大时,会催化H2O2产生O2,从而减少了H2O2的有效利用率[42];②铁碳复合材料投加量过大时,会与H2O2产生过量的∙OH,然而∙OH稳定性较差,还未与STZ反应自身便发生分解反应或与H2O2发生猝灭反应[43]. 图12 Fe@EDTA和Fe@MA投加量对铁碳复合材料降解STZ的影响Fig.12 Influence of Fe@EDTA and Fe@MA dosage on degradation of STZ by Fe-C composites 虽然总体上随着两种铁碳复合材料投加量的增加,STZ降解率随之增长,但是值得注意的是,过多地投加铁碳复合材料只是稍微提高了反应速率,因此从经济角度考虑,铁碳复合材料降解STZ的最佳投加量为0.2 g/L. 2.3.5 STZ初始浓度 Fe@EDTA和Fe@MA材料各设计5组试验,考察STZ初始浓度分别为10、20、40、80和160 mg/L的条件下,对Fe@EDTA和Fe@MA材料诱发非均相Fenton反应降解STZ的影响. 从图13可以看出,铁碳复合材料的催化效率随着STZ初始浓度的升高而降低.对于Fe@EDTA材料,反应120 min后,STZ初始浓度分别为40、80和160 mg/L的样品组,STZ的降解率分别为91%、90%和82%;STZ初始浓度为10和20 mg/L的样品组均能够实现完全降解STZ.对于Fe@MA材料,反应120 min后,STZ初始浓度为160 mg/L的样品组,STZ的降解率为76%;STZ初始浓度为10、20、40和80 mg/L的样品组均能够完全降解STZ.当STZ初始浓度较低时,铁碳复合材料能够快速地降解STZ,这是因为铁碳复合材料与H2O2产生充足的∙OH,少量的STZ被完全降解;当STZ浓度过高时,∙OH氧化能力有限,STZ的降解速率下降.结果显示,0.2 g/L的Fe@EDTA材料能够快速降解STZ初始浓度为10和20 mg/L的样品组,而 图13 STZ浓度对铁碳复合材料降解STZ的影响Fig.13 Influence of pollutant concentration on degradation of STZby Fe-Ccomposites STZ初始浓度为10、20、40、80和160 mg/L的样品组无法被Fe@MA材料完全降解.因此,铁碳复合材料降解STZ的最佳初始浓度为20 mg/L. 2.3.6 反应动力学研究 运用3种典型的动力学模型对Fe@EDTA-H2O2体系和Fe@MA-H2O2体系中STZ的降解反应以及∙OH的生成反应进行拟合,结果分别如表1和表2所示.由表1可见,Fe@EDTA和Fe@MA材料对STZ的降解均更符合拟一级动力学模型,且随着H2O2投加量的增加,反应速率常数也随之增大.由表2可见,Fe@EDTA-H2O2体系和Fe@MA-H2O2体系的试验数据也均更符合拟一级动力学模型,这说明∙OH在STZ的降解中起主要作用. 表1 Fe@EDTA-H 2O2体系和Fe@MA-H 2O2体系降解STZ的参数Table 1 STZ degradation parametersof Fe@EDTA-H2O2 and Fe@MA-H2O2 systems 表2 Fe@EDTA-H 2O2体系和Fe@MA-H 2O2体系产生∙OH的参数Table 2∙OH generation parameters of Fe@EDTA-H2O2 and Fe@MAH2O2 systems 该研究考察了Fe@EDTA和Fe@MA材料在多次重复使用后催化性能的变化情况,每次反应结束后均用去离子水洗涤后重复使用.从图14(a)可以看出,Fe@EDTA材料具有较好的重复利用性和稳定性,前3次重复试验后均可以实现STZ完全降解,第4次和第5次重复试验的降解率也分别达到91%和82%.从图14(b)可以看出,Fe@MA材料的重复利用性和稳定性较为一般,在前3次重复试验时污染物的降解率较为理想,直到第4次和第5次重复试验时,Fe@MA材料的催化活性受到影响,STZ的降解率仅分别为52%和48%.从图15可以看出,Fe@EDTA材料在5次反应后依然具有较好的结晶度,而Fe@MA材料的衍射峰强度较弱,这说明在多次重复试验后Fe@MA的结晶度减弱,nZVI出现一定程度的溶解和脱落损失,因此影响了降解效果[44].总体而言,Fe@EDTA材料比Fe@MA材料表现出了更好的重复利用性和稳定性. 图14 Fe@EDTA和Fe@MA材料的重复降解试验Fig.14 Repeated degradation experimentsof the Fe@EDTA and Fe@MA materials 图15 Fe@EDTA和Fe@MA材料反应前后XRD衍射图谱Fig.15 XRDpatterns of the Fe@EDTA and Fe@MA materials before and after reaction 该研究考察了不同反应体系降解STZ的区别,检测了反应过程中∙OH的浓度和铁离子浸出浓度,确定了反应过程中产生的活性氧的种类.通过在反应前和反应过程中通入N2研究无氧条件下铁碳复合材料的催化性能,采用糠醇(FFA)作为单线态氧(1O2)的淬灭剂,1,10-菲啰啉作为Fe2+/Fe(Ⅱ)的掩蔽剂,对苯醌(BQ)和叔丁醇(tBA)作为掩蔽剂淬灭超氧自由基 (∙O2 −)和∙OH. 与正常条件相比,在无氧状态下,Fe@EDTA和Fe@MA材料对STZ的降解均被部分抑制,反应120 min后降解率均约为81%,同样,加入10 mmol/L的糠醇(FFA)后,对于STZ的抑制效果较为微弱,而加入1,10-菲啰啉后STZ的降解几乎被完全抑制,120 min后降解率仅为20%(见图16),这说明STZ的降解与溶解氧浓度有一定关系,与1O2几乎没有关系,铁离子在降解过程中起到较为关键的作用. 图16 无氧条件、单线态氧掩蔽和铁离子掩蔽试验Fig.16 Oxygen-free conditions,singlet oxygen masking and iron ion masking experiments 另外,该文研究了3种浓度的tBA和BQ对铁碳复合材料降解STZ的影响(见图17、18). 从图17(a)可以看出,在tBA存在的条件下,Fe@EDTA材料对STZ的降解被大幅抑制,反应120 min后浓度分别为10、50和100 mmol/L时,STZ的降解率分别降至70%、42%和30%.从图18(a)可以看出,Fe@MA材料对STZ的降解率也分别降至66%、40%和32%,这说明∙OH在铁碳复合材料诱发非均相Fenton反应降解STZ的过程中发挥着重要的作用.从图17(b)可以看出,浓度为0.1 mmol/L的BQ对Fe@EDTA材料降解STZ没有明显抑制效果,而加入1和10 mmol/L的BQ后,STZ的降解率分别降至89%和60%.从图18(b)可以看出,浓度为0.1 mmol/L的BQ同样对Fe@MA材料降解STZ没有明显抑制效果,而加入1和10 mmol/L的BQ后,STZ的降解率分别降至63%和47%,结果表明∙O2−同样参与了降解反应. 图17 掩蔽剂对Fe@EDTA材料降解STZ的影响Fig.17 Influence of masking agent on STZdegradation of the Fe@EDTA material 图18 掩蔽剂对Fe@MA材料降解STZ的影响Fig.18 Influence of masking agent on STZ degradation of the Fe@MA material 据Boreen等[45]的报道显示,STZ(A)降解共分为两步(见表3):第一步是因∙OH进攻STZ造成磺胺结构中的S−C(α)和S−N(β)键的断裂,S−C(α)断裂后形成B与C,S−N(β)键断裂后形成D与E,其中C与E进一步羟基化形成F并伴随硫酸根的释放,E中的氨基进一步被氧化为硝基,形成G;第二步是苯环的开环形成小分子有机物以及释放硫酸根、铵根和硝酸根.通过测定反应体系的总有机碳(TOC)值来评估STZ的矿化程度.对于Fe@EDTA-H2O2体系,降解120 min后,反应溶液中TOC的去除率达到93%,而Fe@MA-H2O2体系的TOC去除率相对较低,加入25 mmol/L的H2O2反应后,TOC的去除率约为73%,试验结果表明,Fe@C-H2O2体系将大部分STZ降解为无机态的CO2和H2O,并且Fe@EDTA材料的反应活性优于Fe@MA. 表3 STZ降解过程中的中间产物Table 3 Intermediates during STZdegradation 基于以上的试验结果可以看出,以EDTA和MA为前驱体配体制备的负载nZVI的铁碳材料,能够有效降解STZ,推测铁碳复合材料对STZ的降解是基于非均相Fenton反应的氧化作用,反应体系中起氧化作用的主要活性氧物种为∙OH和∙O2−,Fe2+则由2种途径产生,一种是铁碳复合材料表面的Fe0与水中的溶解氧在酸性条件下生成〔见式(14)〕,另一种是Fe0直接被H2O2腐蚀产生〔见式(15)〕,因此在无氧条件下STZ的降解速率会有所降低,而不是明显降低.非均相Fenton催化体系降解STZ等有机污染物的可能作用机制如图19所示. 图19 Fe@C-H2O2非均相Fenton催化体系的作用机制示意Fig.19 Action mechanism of the Fe@C-H2O2 heterogeneous Fenton system a)铁碳复合材料的表征结果表明,Fe@EDTA材料具有直径为4 nm的纳米铁粒子在碳层中均匀分布的结构,Fe@MA材料中的nZVI则聚集为被100 nm碳层包覆的直径为400 nm的大颗粒. b)降解试验结果显示:Fe@EDTA材料的最佳铁碳比为2∶1,Fe@MA材料的最佳铁碳比为3∶1,2种铁碳复合材料的最佳试验条件均为初始pH=3、H2O2投加量25 mmol/L、铁碳复合材料投加量0.2 g/L、STZ初始浓度20 mg/L;STZ的降解以及∙OH的生成均符合拟一级动力学模型;Fe@EDTA材料具有较好的重复利用性和稳定性,5次重复试验后,STZ的降解率仍高达82%,Fe@MA材料的重复利用性和稳定性较为一般,5次重复试验后,STZ降解率约为50%. c)通过机理探究试验,将Fe@C-H2O2体系的降解机理归因于nZVI诱导的非均相Fenton氧化,其中∙OH和∙O2−在氧化有机污染物过程中起到关键作用.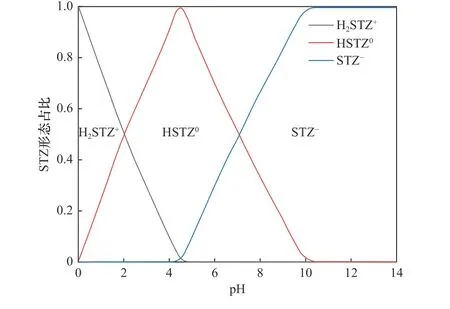
2.4 铁碳复合材料的重复利用性和稳定性
2.5 铁碳复合材料降解STZ的机理
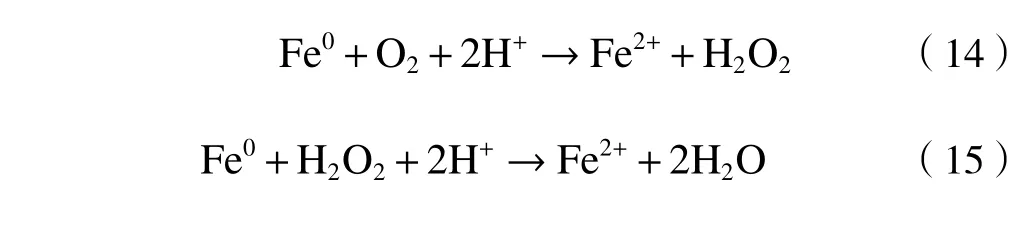
3 结论

