超声介入配合大柴胡汤加减治疗胆囊穿孔的临床效果分析
王巨義,脱小飞,刘 琳
胆囊穿孔是急性梗阻性胆囊炎的严重并发症之一,病情一般都比较危急[1-2],且胆囊穿孔并无特殊临床症状,主要表现与急性梗阻性胆囊炎类似,多为右上腹持续疼痛,多伴有局限性腹膜炎及高热、寒战,白细胞明显升高,部分伴有轻度黄疸[3]。如果未及时发现并治疗则可能引发较为严重的并发症,如胆道系统感染、胆道休克及多脏器功能衰竭等。超声诊断能较早发现胆囊穿孔的部位,由于穿孔部位不同,超声图像也各有特点。胆囊穿孔多见于老年患者,且常伴有多种内科疾病,不能耐受急症手术,故此类患者常不建议行急症手术治疗,所以超声介入在早期胆囊穿孔的治疗中能发挥很大作用。本研究选取44例胆囊穿孔患者,采用超声介入配合大柴胡汤加减治疗,效果较好,报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2020年1月—2021年12月我院收治的44例胆囊穿孔患者资料,其中男25例(56%),女19例(44%);年龄38~89岁,平均(68.4±1.9)岁,病程5~8 d,平均 (5.4±1.3) d。44例患者均有不同程度的内科疾病,全部行超声检查及超声介入治疗,术后口服大柴胡汤加减,并观察术后体征、体温、白细胞计数及胆汁引流情况。
1.2 胆囊穿孔的诊断标准 1)胆囊壁肝床面肝脏(S4或S5段)可见脓肿,经胆囊壁肝床面缺损区与胆囊相通。2)胆囊壁游离面超声二维图像可见胆囊增大、胆囊壁增厚,胆囊底部壁可见缺损区,胆囊周围有游离或包裹性积液。
1.3 仪器与治疗方法
1.3.1 诊断仪器与方法 应用Philips IU22或Philips ELITE超声诊断仪器进行诊断。使用频率为3.5 mHz的凸阵探头,患者取平卧位,重点扫查肝床面及底部胆囊壁,多断面观察胆囊壁是否存在缺损区,胆囊周围是否有游离或者包裹性积液,积液宽径,如胆囊周围肝脏(S5区)出现脓肿,观察肝脓肿是否与胆囊相通。
1.3.2 超声介入治疗方法 患者取平卧位,消毒、局麻后于超声引导下经皮经肝,一步法完成胆囊穿刺后,根据胆囊内胆汁情况,选择置入8 Fr或10 Fr猪尾引流管。若伴有肝脓肿则经肝行穿刺置管引流,对于胆囊周围宽径大于1 cm的游离积液,则行腹腔积液置管引流,对于包裹性积液则行穿刺抽吸术。
1.3.3 中药治疗 超声介入治疗后予大柴胡汤加减口服,组方为黄芩10 g,枳壳6 g,川楝子10 g,白芍10 g,木香6 g,大黄15 g,蒲公英30 g,甘草6 g,醋延胡索10 g,北柴胡10 g,1次/d,1次1付,200 mL水煎服。
1.4 统计学方法 将数据输入Excel 2010。计量资料以形式进行描述,计数资料以例(%)形式进行描述。
2 结果
2.1 全身指标 44例患者全部有右上腹压痛,Murphy征阳性37例,右上腹局限性腹膜炎19例。40例有发热,28例体温高于38 ℃,12例体温低于38 ℃。44例患者均有不同程度的白细胞计数升高,高于10×109/L共36例,高于20×109/L共8例。
2.2 胆囊穿孔的超声二维图像 本组44例患者超声二维图像均发现胆囊壁缺损,其中肝床面穿孔形成肝脓肿17例(38%),游离面穿孔27例(62%)。游离面穿孔中胆囊周围游离积液19例,包裹性积液8例。
2.3 胆囊穿孔的超声介入治疗 本组44例患者由于不能耐受急症手术治疗,均行急症超声介入治疗。
2.3.1 肝床面穿孔 行超声引导下经皮肝穿刺胆囊置管引流(UG-PTGD)及肝脓肿穿刺置管引流,同时引流出脓性浑浊胆汁,证实为胆囊穿孔合并肝脓肿形成,见图1。

图1 肝床面穿孔
2.3.2 游离面穿孔 行UG-PTGD及胆囊周围游离积液置管引流,同时引流出脓性浑浊胆汁,证实为胆囊穿孔合并腹腔积液形成,见图2。
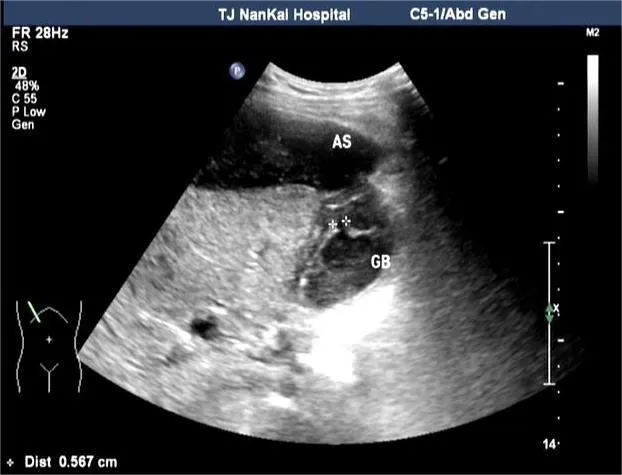
图2 游离面穿孔
2.3.3 胆囊周围少量积液 对于胆囊周围积液宽径小于1 cm或者包裹性积液,行超声引导下积液穿刺抽吸术,抽出脓性浑浊胆汁,见图3。
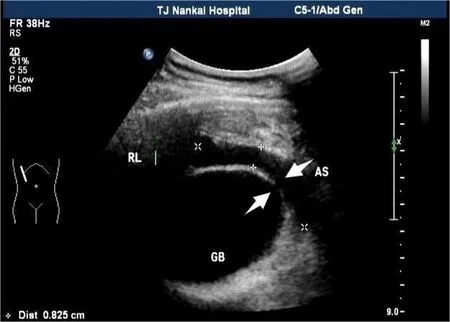
图3 胆囊周围包裹性积液
2.3.4 术后治疗 44例患者均置管成功,术后予大柴胡汤加减口服,平均12 h腹痛逐步减轻,Murphy征阴性,局限性腹膜炎消失,平均72 h后体温降至正常,白细胞降至正常水平,平均5 d后胆汁颜色转为正常,症状体征明显好转,复查超声可见肝脓肿及腹腔积液消失,后保留PTGD管,拔除其他引流管后出院,见图4。
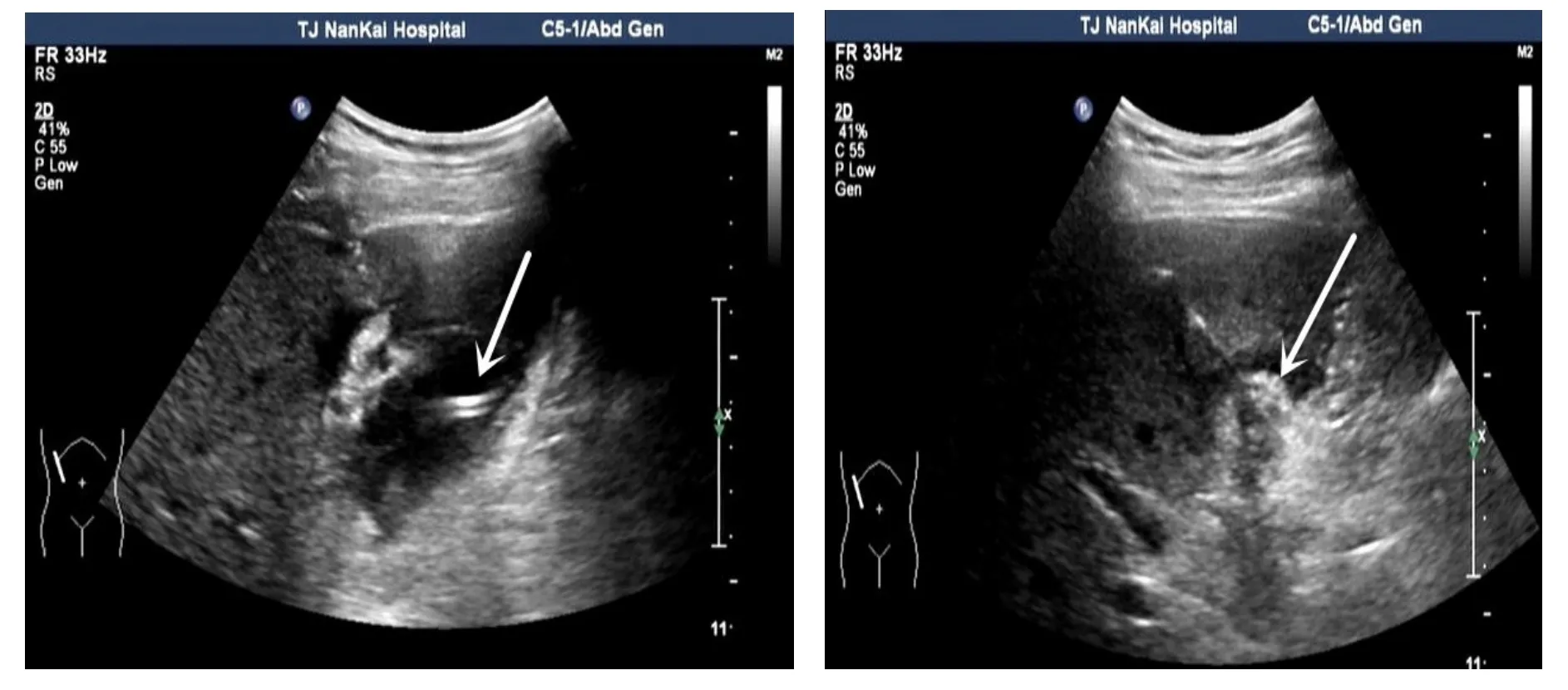
图4 超声介入治疗术后
3 讨论
胆囊穿孔是急性梗阻性胆囊炎的严重并发症,发生率约为2%~15%[4],多见于老年患者,且病程较长。本组病例中男25例(56%),女19例(44%);年龄38~89岁,平均(68.4±3.6)岁,病程 5~8 d,平均(5.4±1.3) d。朱彩鹏等[5]认为大多数胆囊穿孔患者有胆囊结石病史,胆汁排泄时,结石容易嵌顿于胆囊颈部或胆囊管引起胆囊梗阻,进而引起胆囊壁水肿、缺血坏死,淤积的胆汁继发细菌感染,胆囊壁容易发生坏疽,同时由于胆囊内压力升高,进而出现穿孔。于一龙等[6]认为罗-阿氏窦穿孔是胆囊穿孔的一种特殊形式。胆囊壁由于结石或者胆汁的刺激形成慢性炎症,从而形成罗-阿氏窦,其组织形态特点是胆囊壁黏膜变薄易膨出,胆囊内压力高时极易引起该窦穿孔。
1934年,Niemeier[7]将胆囊穿孔分为3型:急性或Ⅰ型(游离穿孔和弥漫胆汁性腹膜炎)、亚急性或Ⅱ型(胆囊周围脓肿和局限性腹膜炎)、慢性或Ⅲ型(胆囊肠瘘)。Ⅰ型穿孔主要为胆囊底部壁穿孔,此类穿孔发病急,最多见,主要临床表现为局限性腹膜炎,多位于右上腹,若穿孔时间长,胆汁可从肝右叶下方顺流至右侧腹,甚至到盆腔。超声扫查此类胆囊穿孔,应着重扫查胆囊底部周围、连续性扫查肝右叶下方至右髂窝。Ⅱ型主要为肝床面穿孔,胆囊壁肝床面发生坏疽,胆汁感染至临近肝脏,形成肝脓肿,部分漏出胆汁也可以被周围大网膜包裹,形成包裹性积液。此类穿孔急腹症症状不明显,更多为高热、寒战,血常规可见白细胞明显升高等脓毒血症表现。对于此类胆囊穿孔,超声应多扫查肝床部胆囊壁及临近肝脏(S5区),Ⅱ型穿孔较容易发现,因为多数可见明显的胆囊壁肝床面缺损,周围可见脓肿与胆囊相通。Ⅲ型一般被认为胆囊-肠瘘,属于游离面穿孔的一种特殊类型。由于胆囊壁脏器面毗邻十二指肠,因此胆囊-十二指肠瘘较多见,胆囊-胃瘘、胆囊腹壁瘘相对少见,发病主要为慢性胆囊炎迁移所致,慢性胆囊炎的胆囊壁与周围脏器长时间粘连,同时结石反复刺激胆囊壁,容易出现肠瘘。Date等[8]认为胆囊穿孔部位以胆囊底部多见,因胆囊底位于远端,血运气差易引发穿孔,其次为体部和颈部。本组病例中,胆囊壁肝床面穿孔(Ⅱ型穿孔)为17例,比例为38%,游离面穿孔(Ⅰ型穿孔)为27例,比例为62%。可见游离面穿孔占比更高,更为常见。
胆囊穿孔的诊断主要依靠影像学检查。超声是急性胆囊炎合并胆囊穿孔的首选早期检查方法[9],胆囊壁可见明显局部缺损是胆囊穿孔最直接的影像学特征,也是该疾病的特征性超声表现。胆囊穿孔的二维超声图主要表现为直接征象及间接征象,直接征象是指胆囊壁水肿、毛糙,呈现多边影或双边影,胆囊壁可见明显的缺损区,多见于肝床面穿孔,肝床部附近肝脏(S5区)形成肝脓肿,经胆囊壁缺损区与胆囊相通。间接征象是指由于部分胆囊壁缺损区直径过小,二维超声不能探及,多见于游离面穿孔。间接超声征象中,胆囊周围游离或包裹性积液往往是胆囊穿孔后漏出的胆汁所致,即使在二维超声图像下,没有发现明显的胆囊壁缺损区,也可以依据胆囊周围出现宽径大于1 cm的游离积液,推断出胆囊穿孔。胆囊穿孔超声直接征象合并其他间接征象显示胆囊穿孔的特异性和准确性较高,并可结合临床症状作出明确诊断。
虽然胆囊穿孔的影像学检查具有特征性表现,但是显示率并不高,有文献报道显示率仅61%[10],而超声诊断胆囊穿孔也存在一定的误诊及漏诊,主要是由于超声自身的限制性,如肋骨或气体干扰、体位要求、患者肥胖、医师检查手法等,导致胆囊壁缺损区并不能完全探及,因此需要多断面甚至多体位进行扫查。张锐利等[11]认为胆囊穿孔的漏诊或者误诊,主要与穿孔小、炎症重,患者及医师因素有关,主要原因为:1)穿孔面积过小,二维超声图像下超声不易发现胆囊壁的连续性中断,部分文献报道,对于直径 ≤5 mm的胆囊缺损区,超声检查较容易漏诊[12]。2)穿孔后大部分胆汁外漏,胆囊体积明显缩小,而且胆囊穿孔多是由于胆囊壁坏疽,部分发生严重坏疽的胆囊壁在超声图像下,轮廓显示不清,很难发现胆囊壁的缺损区,此时可以切换成高频探头,且多切面、多体位观察胆囊壁,可减少漏诊或误诊;3)部分患者体型肥胖,皮下或内脏脂肪过厚,肋骨或者胃肠气体干扰,超声因为衰减导致远场图像显示不清,局限性腹膜炎导致腹膜刺激征引起的肌紧张,不能完全配合超声检查,也会影响超声检查效果。4)由于胆囊穿孔不具有特征性体征,超声医师进行检查时,发现急性梗阻性胆囊炎且胆囊周围积液较少时,并未多体位、多断面的扫查胆囊壁缺损区,忽略了穿孔的可能。总之,超声医师若发现急性梗阻性胆囊炎时,需认真询问病史,扫查过程中可结合高频探头,多断面、多体位重点观察胆囊壁有无缺损、有无胆囊周围积液及肝脓肿形成,可提高超声诊断胆囊穿孔的准确率。
超声介入治疗在胆囊穿孔的早期治疗及诊断中发挥了重要作用。首先,胆囊穿孔多见于高龄患者,高龄患者对疼痛不敏感,导致早期急性梗阻性胆囊炎发作时,因体征不明显延误诊治,由于病程时间过长,胆囊张力升高,胆囊壁缺血坏死严重,出现穿孔,又因高龄患者基础内科疾病多,如呼吸系统疾病,心血管疾病等,这类患者麻醉、手术均有极高的风险,不能耐受急症手术。另外,由于胆囊穿孔的患者多存在病程较长,胆囊壁出现水肿、充血、黏膜坏死甚至坏疽,且胆囊壁炎性物质渗出,周围组织粘连严重,术中解剖结构显示不清楚,周围网膜、胆囊壁、肝床面等周围组织质地脆、接触后易出血且难以分离,术中难以将胆囊浆膜层与肝床完全分离,术中渗血过多,胆囊三角难以显示清楚,易发生胆管损伤及大出血,且术后并发症如胆漏、渗血等风险较高。羊平等[13]认为胆囊穿孔行急症手术时,损伤胆道及血管的风险较大,中转开腹率高。而患病超过72 h的患者,由于炎性渗出较多,导致手术区域炎症粘连严重,术中极易损伤胆管和血管,所以对于胆囊穿孔,急症手术并不是最理想的治疗方案,因此UG-PTGD是一种有效、快速缓解临床症状及胆道感染的较好方案。该治疗能迅速降低胆囊压力,直接快速排出脓性胆汁,且损伤小,易于操作,术后结合抗生素使用,能有效减轻胆道感染。本组44例,均行UG-PTGD,术后未出现严重并发症,短时间内减轻胆囊压力,症状明显缓解。吴昱等[14]对348例高危或高龄患者行UG-PTGD,发现通过UG-PTGD可使高危急性梗阻性胆囊炎患者胆道迅速减压,有效缓解症状,避免急症手术带来的诸多风险,明显降低了死亡率,并且为择期行胆囊切除提供了良好的手术时机。另外,UG-PTGD 充分发挥了超声微创技术创伤小、操作简便、准确安全的优势,值得临床推广。另外,对于不能耐受急症手术的患者,可以一期行UG-PTGD,择期行胆囊切除术,能有效地减少围手术期的损伤。Tan等[15]研究表明在老年急性胆囊炎患者行腹腔镜下胆囊切除术(LC)前,一期先行UG-PTGD,待炎症减轻后二期行LC,不仅可以缩短LC手术时间,减少术中出血,缩短术后康复时间,而且可以减少高龄患者急性胆囊炎的术后并发症,建议作为首选的治疗方法。王琦等[16]研究结果显示,对于急性坏疽穿孔性胆囊炎患者先行UG-PTGD,后期行LC,较急诊开腹传统胆囊切除术治疗效果更好。
中药在胆囊穿孔治疗中能起到重要作用,大柴胡汤为表里双解剂,具有和解少阳,内泻热结之功效。主治少阳阳明合病,往来寒热,胸胁苦满,呕不止,郁郁微烦,心下痞硬,或心下满痛,大便不解,或协热下利,舌苔黄,脉弦数有力。临床常用于治疗急性胰腺炎、急性胆囊炎、胆石症等属少阳阳明合病者。胡路路等[17]对22例老年胆囊穿孔的患者行UG-PTGD治疗,术后未采取中药治疗,1~3 d患者体温逐渐降至正常水平,白细胞计数逐步下降。平均6d后症状、体征好转,本组中44例术后均予大柴胡汤加减口服治疗,平均12 h腹痛逐步减轻,平均72 h后体温降至正常,白细胞降至正常水平,平均5 d后胆汁颜色转为正常,症状体征明显好转,复查超声可见胆囊内淤积胆汁消失,肝脓肿及腹腔积液消失。可见超声介入术后配合中药治疗,能有效地减轻炎症反应,恢复胆汁正常排泄。
综上所述,胆囊穿孔的超声图像特征主要表现为胆囊壁缺损,根据缺损部位分为胆囊壁肝床面穿孔、游离面穿孔。肝床面穿孔多表现为胆囊周围肝脓肿,游离面穿孔多表现为胆囊周围游离或者包裹性积液。超声介入在早期胆囊穿孔的诊治中能发挥重要作用,既能快速排出胆囊内感染性胆汁,又能对周围脓肿或积液进行穿刺引流发现外漏脓性胆汁,证实为胆囊穿孔,而且可以有效的对胆囊穿孔围手术期进行损伤控制。术后配合使用大柴胡汤加减,可以疏肝理气,和解少阳,清热散结,对胆囊穿孔能起到很好的辅助治疗作用。

