生长抑素类似物联合依维莫司治疗胰腺神经内分泌肿瘤的临床疗效观察
陈晓兰 尚庆玲 李 慧
(信阳市第一人民医院内分泌科,河南 信阳 464000)
胰腺神经内分泌肿瘤(P-NEN)在神经内分泌肿瘤属于较特殊的一类[1]。临床通常选择根治性切除原发灶来治疗P-NEN,但由于缺乏激素相关的临床表现,多数无功能患者直至肿瘤引起压迫才被诊断,此时肿瘤大多已向远处转移,患者失去最佳手术时机,因此这类患者的治疗多以延缓疾病进展、改善临床症状为主[2]。故药物治疗在P-NEN 综合治疗中必不可少。生长抑素类似物(SSAs)是目前P-NEN 的首选治疗药物[3]。而高靶向性药物依维莫司近年来也不断被用于肿瘤的治疗中[4]。本研究旨在探讨生长抑素类似物与依维莫司联合方案在PNEN 中的临床疗效。
1 资料与方法
1.1 一般资料:选取我院于2016年3月至2017年10月收治的54例无功能胰腺神经内分泌肿瘤患者,将其按随机数字表法分为观察组(n=27)与对照组(n=27)。对照组男16例,女11例;年龄26~75岁,平均(52.14±8.27)岁;WHO 消化系统肿瘤分级[5]:G1 级12例,G2 级15例。观察组男15例,女12例;年龄25~76岁,平均(51.51±7.42)岁;WHO 消化系统肿瘤分级:G1 级13例,G2 级14例。两组患者性别、年龄、肿瘤分级等一般资料差异无统计学意义(P>0.05)。纳入标准:①符合《中国胃肠胰神经内分泌肿瘤病理学诊断共识》中的相关诊断标准[6],并经CT 或MRI 影像或经活检病理及免疫组化确诊;②WHO 2010 病理分级属G1、G2 的患者;③RE CIST1.1 评价至少有一个最长径可测量的肿瘤病灶。排除标准:①功能性肿瘤患者;②合并肺间质性病变或重度慢阻肺;③多发性神经内分泌瘤病;④严重心、肝、肾功能障碍;⑤近期行过靶向治疗或化疗者;⑥合并血液系统疾病、免疫系统疾病。
1.2 方法:对照组患者肌肉注射醋酸奥曲肽微球20mg,3 周/次。或肌肉注射醋酸兰瑞肽40mg,2 周/次。观察组在对照组基础上加用依维莫司,口服,5mg/d,共治疗3 个月。
1.3 观察指标:治疗效果:比较治疗前及治疗3 个月后PET 和CT 扫描结果,采用RECIST1.1 评价标准[7]对患者治疗近期疗效进行评价。完全缓解(CR):所有目标病灶消失,任何病理性淋巴结(无论是否为目标病灶)短轴值必须<10mm;部分缓解(PR):以临界直径的总和为参照,所有目标病灶直径的总和在4 周内持续减小至少30%;病灶稳定(SD):以目标病灶直径总和最小值为参照,目标病灶最大长径之和减少高于30.0%,最大长径之和增加20.0%以下;疾病进展(PD):以目标病灶直径总和最小值为参照,所有目标病灶直径总和至少增加20%;直径总和增加的绝对值>5mm 或出现新的病灶。统计并比较两组患者疾病进展时间及治疗后l~3年复发率。实验室指标:于治疗前及治疗3 个月后使用酶联免疫吸附法检测两组血清CgA 水平。血清CgA正常值为44μg/L,上限值为870μg/L。记录比较治疗后两组不良反应类型及发生率。
1.4 统计学方法:运用SPSS19.0 统计学软件分析数据,正态分布数据计量资料以(±s)表示,采用t检验,计数资料采用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组治疗效果比较:治疗后,观察组与对照组患者均无完全缓解情况,部分缓解与病灶稳定情况差异无统计学意义(P>0.05),但观察组疾病进展情况明显少于对照组(P<0.05),详见表1。
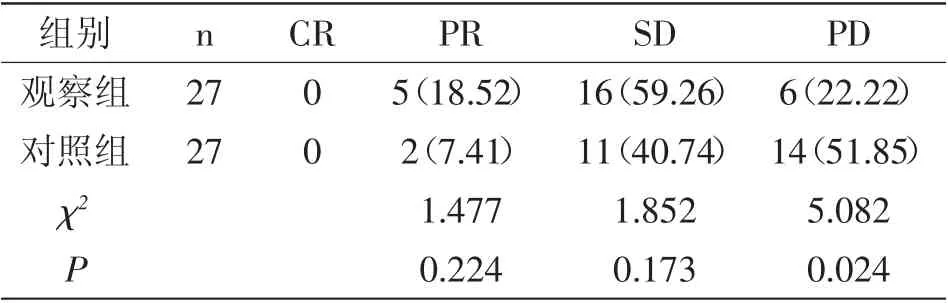
表1 两组治疗效果比较 [n(%)]
2.2 两组患者疾病进展时间与治疗后1~3年复发率比较:观察组患者疾病进展时间明显长于对照组(P<0.05),治疗后1~3年观察组患者复发率均低于对照组,且复发率差异逐年扩大,详见表2。

表2 两组患者疾病进展时间与治疗后1~3年复发率比较[n(%)]
2.3 两组患者治疗前及治疗3 个月后血清CgA 水平比较:两组患者治疗前血清CgA 水平比较差异无统计学意义(P>0.0.5),治疗3 个月后,两组患者的血清CgA 水平均明显下降,且观察组血清CgA 水平明显低于对照组(P<0.05),详见表3。
表3 两组患者治疗前及治疗3 个月后血清CgA 比较(±s)

表3 两组患者治疗前及治疗3 个月后血清CgA 比较(±s)
组别 n 治疗前 治疗后观察组 27 325.41±32.28 226.08±30.47 t P<0.001对照组 27 331.07±34.55 267.95±31.64 7.001 <0.001 t 0.622 4.953 P 0.537 <0.001 11.627
2.4 两组患者治疗后不良反应发生情况比较:治疗后,观察组不良反应明显高于对照组(P<0.05),详见表4。
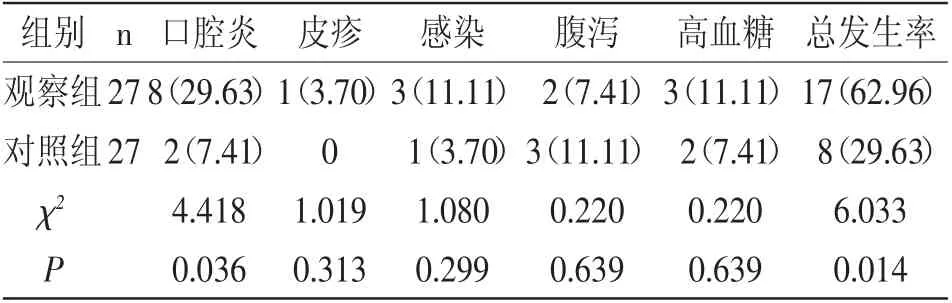
表4 两组不良反应发生情况比较 [n(%)]
3 讨论
晚期胰腺神经内分泌肿瘤的主要以生长抑素类似物、化疗、减瘤手术等方式进行治疗,因PNEN 患者大多数都存在生长抑素受体(SRRT)过度表达,故生长抑素类似物治疗是首选治疗方案,其中奥曲肽和兰瑞肽为常用治疗药物[8]。有研究表明,生长抑素类似物联合靶向药物进行治疗,其疗效明显优于单一使用生长抑素类似物[9]。
本研究中,观察组患者疾病进展情况与对照组相比有较大差异,疾病进展时间明显长于对照组,且观察组治疗1~3年期间复发率也低于对照组,说明生长抑素类似物联合依维莫司对肿瘤进展有明显的抑制作用。考虑机制为生长抑素类似物可以与SRRT 结合,诱导肿瘤细胞使其凋亡,影响肿瘤细胞的分裂生长,从而有效地抑制肿瘤细胞的增殖,控制临床症状[10]。此外,它也可抑制血管生长因子的生成和表达,增强机体免疫能力,间接阻碍肿瘤的快速增殖,降低疾病复发率[11]。而依维莫司可特异性抑制mTOR 通路,抑制肿瘤细胞生长与增殖、细胞代谢和血管新生,能显著延长晚期pNET 病人的疾病进展时间,提高pNET 患者总生存率[12]。
CgA 是一种神经内分泌肿瘤血清标志物,其表达水平可反映肿瘤的进展及复发情况,对NET 的诊断、评估疗效及预后均有重要价值[13]。SSA 可以影响血清CgA 的水平。本研究中,观察组治疗3 个月后,其血清CgA 的水平明显低于对照组,说明在使用SSA 的基础上加用依维莫司可进一步降低血清中CgA 的含量。考虑机制为依维莫司结合细胞内蛋白FKBP.12 形成特殊复合物,该复合物可降低mTOR 激酶、S6 核糖体蛋白激酶和4E-结合蛋白的活性,减少低氧诱导因子和血管内皮生长因子的表达,从而有效抑制肿瘤细胞的增殖[14]。
本研究中,观察组不良情况多于对照组,观察组口腔炎症患者明显多于对照组,表现为口腔、唇、舌黏膜的炎症反应或溃疡,伴局部疼痛或吞咽困难[15]。说明在使用SSA 的基础上加用依维莫司,会增加患者不良反应发生率。考虑机制为依维莫司作为mTOR 抑制剂,虽对癌症有明显的治疗效果,但抑制mTOR 信号的同时造成免疫抑制,导致免疫调节异常,故使患者容易感染,易引起口腔黏膜不良反应的发生[16]。
综上所述,生长抑素类似物联合依维莫司的疗效优于单纯使用生长抑素类似物,但在增强疗效的同时,也增加了不良反应的发生率。临床治疗选择联合用药时应依照患者实际情况合理选择,患者发生药物不良反应时应及时进行相应的治疗护理,努力使药物达到治疗效果的同时降低患者受到的损害。

