3种客观赋权法比较优选健胃除痞颗粒的提取工艺
李洁环,张建军,冯健英,陈雪婷,徐文杰,李智勇
[广东省第二中医院(广东省中医药工程技术研究院)/广东省中医药研究开发重点实验室,广东 广州 510095]
健胃除痞方由乌药、柴胡、白芍、佛手、豆蔻、佩兰等药味组成,具有疏肝行气、健胃除胀、消痞除满之功效,临床上用于治疗慢性胃炎、萎缩性胃炎等引起的痞满嘈杂、胃胀、嗳气、胃痛灼热等症。原方汤剂内服,临床疗效显著,但存在煎煮、携带、使用不方便等缺点,拟将其开发制成颗粒剂,现对其水提取工艺进行研究。由于中药化学成分复杂,选择单一成分的含量进行质量监测不足以全面反映制剂的质量;因此,本研究选择乌药中去甲异波尔定质量浓度、白芍中芍药苷质量浓度以及固形物质量作为评价指标,多指标综合评价优化提取工艺条件。在进行综合评价时,各指标权重系数的确定尤为关键,其合理性直接影响评价结果的可靠性和正确性[1]。客观赋权法是依据原始数据间的相关关系,通过一定的数学方法,经统计分析、计算,来获得权重的一种赋权方法,其结果不依赖于人的主观判断,不受人为主观偏好的干扰,客观性强,使评价结果更具可信性[2]。本文拟采用熵权法、标准离差法、基于指标相关性的权重确定方法(criteria impor‐tance through intercriteria correlation,CRITIC)建立权重,分析比较3种客观赋权法得到的结果,优化确定最佳提取工艺条件。
1 仪器与材料
1.1 仪器
Agilent1200 高效液相色谱仪(美国Agilent 公司);HH-8数显恒温水浴锅[邦西仪器科技(上海)有限公司];KQ-300DE 型数控超声波清洗器(昆山市超声仪器有限公司);JJ500 型电子天平(0~500 g/0.01 g,常熟市双杰测试仪器厂);XS205DU 电子分析天平(0~220 g/0.1 mg,瑞士梅特勒-托利多有限公司);PTHW 型调温电热套(巩义市予华仪器有限责任公司);Heidolph 旋转蒸发仪(德国Heidolph 公司);DHG-9203A鼓风干燥箱(上海精宏实验设备有限公司)。
1.2 试药
乌药等饮片购自广州市中芝源中药有限公司,经广东省中医药工程技术研究院刘法锦研究员鉴定,乌药(产地:浙江)为樟科植物乌药Lindera aggregata(Sims)Kos-term.干燥块根的加工炮制品,白芍(产地:安徽)为毛莨科植物芍药Paeonia lactifloraPall.干燥根的加工炮制品,其余饮片经鉴定均为正品。试验所用饮片经检验,质量均符合《中国药典》2020年版一部各饮片项下的有关规定。
去甲异波尔定(批号111825-201201)、芍药苷(批号110736-201539)对照品购自中国食品药品检定研究院;乙腈为色谱纯(德国默克),水为蒸馏水,甲酸、磷酸等其他试剂为分析纯。
2 方法与结果
2.1 评价指标的建立
2.1.1 去甲异波尔定、芍药苷的测定
2.1.1.1 色谱条件 去甲异波尔定:Kromasil 100-5-C18色谱柱,以乙腈∶(0.5%甲酸-0.1%三乙胺)(体积比9∶91)为流动相,柱温25 ℃,检测波长280 nm,流速1 mL/min。芍药苷:Agilent Eclipse Plus C18色谱柱,以乙腈-0.1%磷酸(体积比13∶87)为流动相,柱温25 ℃,检测波长230 nm,流速1 mL/min。
2.1.1.2 对照品溶液的制备 分别取去甲异波尔定、芍药苷对照品适量,精密称定,加甲醇溶解,摇匀,制成质量浓度分别为298.4、280.9 μg/mL 的储备液。取上述去甲异波尔定、芍药苷对照品储备液各0.25、0.6 mL,分别置1 mL量瓶中,加甲醇定容至刻度,摇匀,制成质量浓度分别为74.6、168.5 μg/mL 的去甲异波尔定、芍药苷对照品溶液。
2.1.1.3 供试品溶液的制备 按处方比例,称取乌药等饮片260 g,加水提取2 次,每次加8 倍量水,提取1 h,合并提取液,200 目筛滤过,滤液浓缩并定容至250 mL。精密移取浓缩液1 mL,置5 mL量瓶中,加甲醇适量,超声处理(功率300 W,频率40 kHz)25 min,放冷,加甲醇定容至刻度,摇匀,滤过,即得去甲异波尔定供试品溶液。另精密量取浓缩液1 mL,置10 mL量瓶中,加稀乙醇适量,同法操作制备芍药苷供试品溶液。
2.1.1.4 阴性对照溶液的制备 按处方比例,称取除乌药外的其余饮片,按上述供试品溶液的制备方法制备缺乌药的阴性对照溶液。同法制备缺白芍的阴性对照溶液。
2.1.1.5 专属性考察 精密吸取上述去甲异波尔定对照品、供试品和缺乌药的阴性对照溶液各8 μL 进样测定,结果表明,去甲异波尔定对照品和供试品溶液在相同位置处有一色谱峰,阴性对照溶液未见该色谱峰。另精密吸取上述芍药苷对照品、供试品和缺白芍的阴性对照溶液各5 μL 进样测定,结果表明,芍药苷对照品和供试品溶液在相同位置处有一色谱峰,阴性对照溶液未见该色谱峰。上述色谱条件下,去甲异波尔定、芍药苷基本上可达到基线分离,峰对称性良好,分离度均大于1.5,理论塔板数以去甲异波尔定峰计算不低于5 000,以芍药苷峰计算不低于2 000,表明去甲异波尔定、芍药苷的测定方法专属性良好,色谱图见图1和图2。
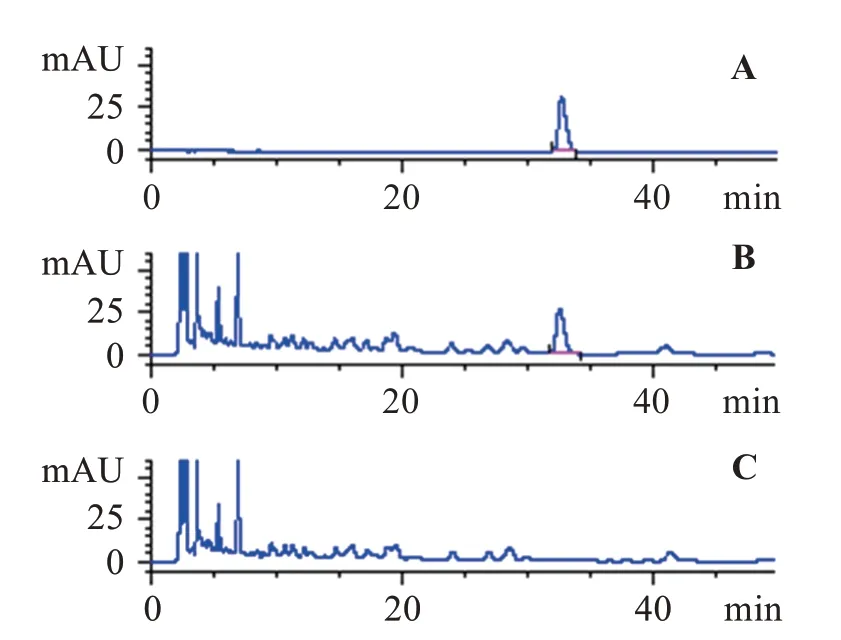
图1 去甲异波尔定对照品(A)、供试品(B)、阴性样品(C)的HPLC图Figure 1 HPLC diagrams of the reference substance(A),test substance(B)and negative sample(C)of norisoboldine
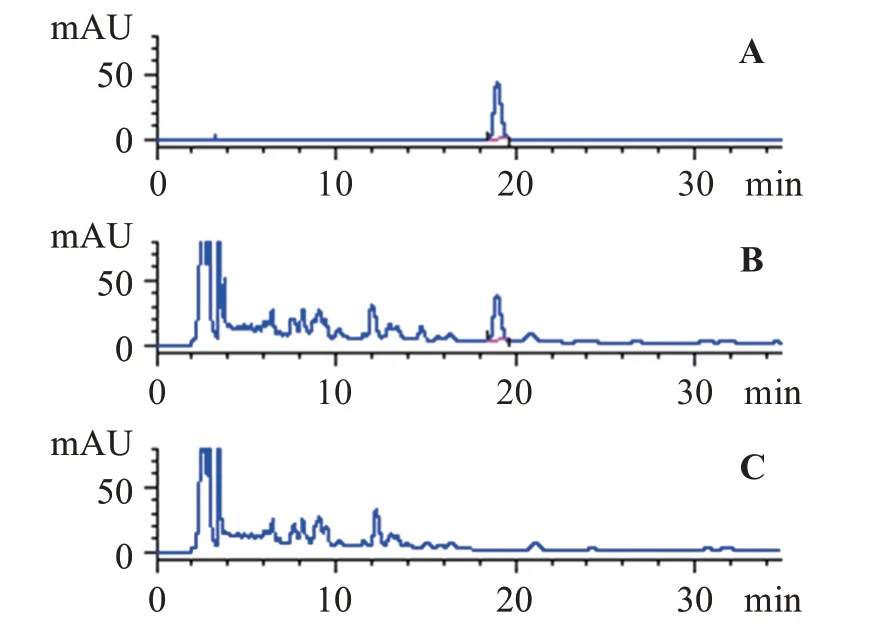
图2 芍药苷对照品(A)、供试品(B)、阴性样品(C)的HPLC图Figure 2 HPLC diagrams of the reference substance(A),test substance(B)and negative sample(C)of paeoniflorin
2.1.1.6 线性关系考察 精密量取“2.1.1.2”项下去甲异波尔定对照品储备液0.1、0.2、0.3、0.4、0.5、0.6 mL,分别置于1 mL量瓶中,加甲醇稀释至刻度,摇匀,配制成质量浓度分别为29.84、59.68、89.52、119.4、149.2、179.0 μg/mL 的对照品溶液,按上述色谱条件进样4 μL,以进样量(X,ng)对峰面积(Y)进行线性回归,得去甲异波尔定的回归方程为Y=2.282X-14.71,r=0.999 9,表明去甲异波尔定进样量在119.4~716.2 ng范围内与峰面积呈良好线性关系。
精密量取“2.1.1.2”项下芍药苷对照品储备液0.15、0.3、0.4、0.5、0.6、0.8 mL,分别置于1 mL 量瓶中,加稀乙醇稀释至刻度,摇匀,配制成质量浓度分别为42.13、84.26、112.4、140.4、168.5、224.7 μg/mL的对照品溶液,按上述色谱条件进样5 μL,以进样量(X,ng)对峰面积(Y)进行线性回归,得芍药苷的回归方程为Y=1.493X-29.47,r=0.999 9,表明芍药苷进样量在210.7~1124 ng范围内与峰面积呈良好线性关系。
2.1.1.7 方法学考察 去甲异波尔定:精密度、重复性、24 h 稳定性试验去甲异波尔定峰面积RSD 分别为1.06%、1.72%、1.93%,平均加样回收率为99.94%,RSD 为1.32%。芍药苷:精密度、重复性、24 h 稳定性试验芍药苷峰面积RSD 分别为1.34%、1.57%、1.89%,平均加样回收率为99.33%,RSD为1.14%。
2.1.2 固形物质量的测定 精密吸取各样品浓缩液50 mL,置已恒重的蒸发皿中,水浴蒸干,照干燥失重测定法(《中国药典》2020年版四部0831项)测定,按公式:固形物质量=W÷50×250 计算固形物质量,其中W为50 mL浓缩液的固形物质量。
2.2 正交试验设计及结果
2.2.1 正交试验设计
采用L9(34)正交试验法,以乌药中去甲异波尔定质量浓度、白芍中芍药苷质量浓度和固形物质量为评价指标,对影响提取工艺的提取次数、提取时间、加水量进行考察。
2.2.2 样品的制备
按处方比例,称取乌药、柴胡、白芍等饮片9份,每份260 g,按表1正交试验设计表的安排进行提取,提取液200目筛滤过,滤液浓缩并定容至250 mL。
2.2.3 样品评价指标的测定
按“2.1.1.1”项色谱条件进样测定(去甲异波尔定样品进样8 μL,芍药苷样品进样5 μL),计算9 份正交样品中去甲异波尔定和芍药苷质量浓度,并测定固形物质量,结果见表1。
2.2.4 数据的无量纲化处理[3-4]为消除各指标量纲不同对方案决策的影响,先对表1数据进行无量纲化处理,使数据处于[0,1]之间,公式如下:
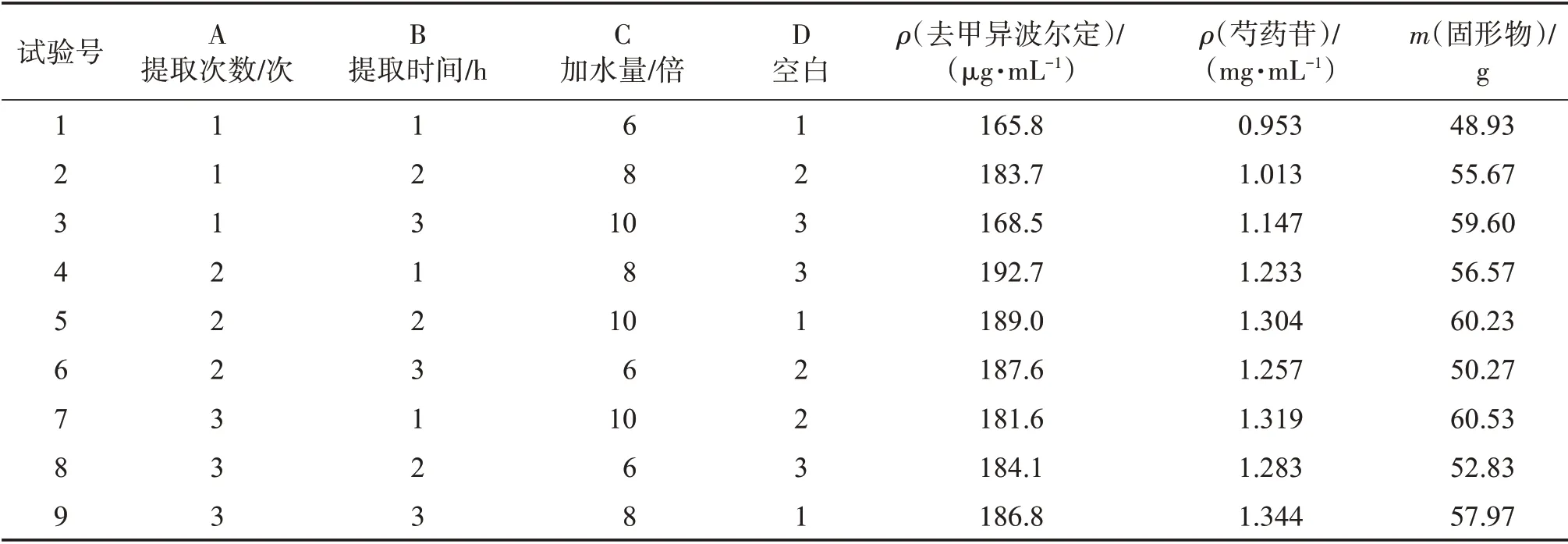
表1 正交试验设计及结果Table 1 Orthogonal experimental design and results

式中:Yij为第i个评价对象的第j个评价指标的无量纲化处理数值;Xij为第i个评价对象的第j个评价指标的原始数值;maxXij和minXij分别表示第i个评价对象在第j个评价指标上的最大值和最小值。数据处理结果见表2。
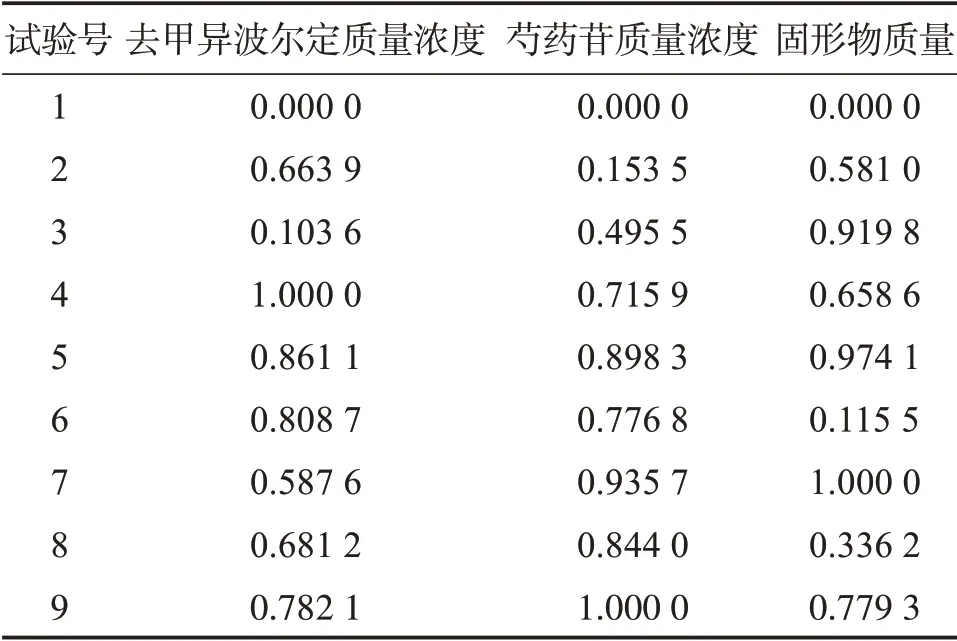
表2 数据无量纲化处理结果Table 2 Data dimensionless processing results
2.2.5 指标成分权重的确定
2.2.5.1 熵权法确定权重[5-7]熵原本是一个热力学概念,后被引入信息论中,用来度量信息量的多少。熵权法中,可以用熵值(Ej)来判断某个指标的离散程度,其信息熵Ej越小,指标的离散程度越大,变异程度越大,该指标对综合评价的影响(即权重Wj)就越大。信息熵Ej、各指标客观权重Wj的计算公式如下:
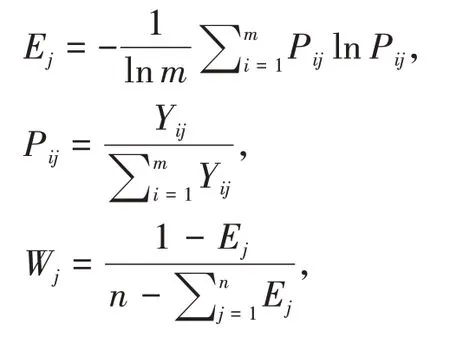
式中:Ej为第j个评价指标的熵值;Pij为第i个评价对象在j指标下的概率;m为被评价对象的数目;n为评价指标的数目;Wj为第j个评价指标的权重。计算结果见表3、4。
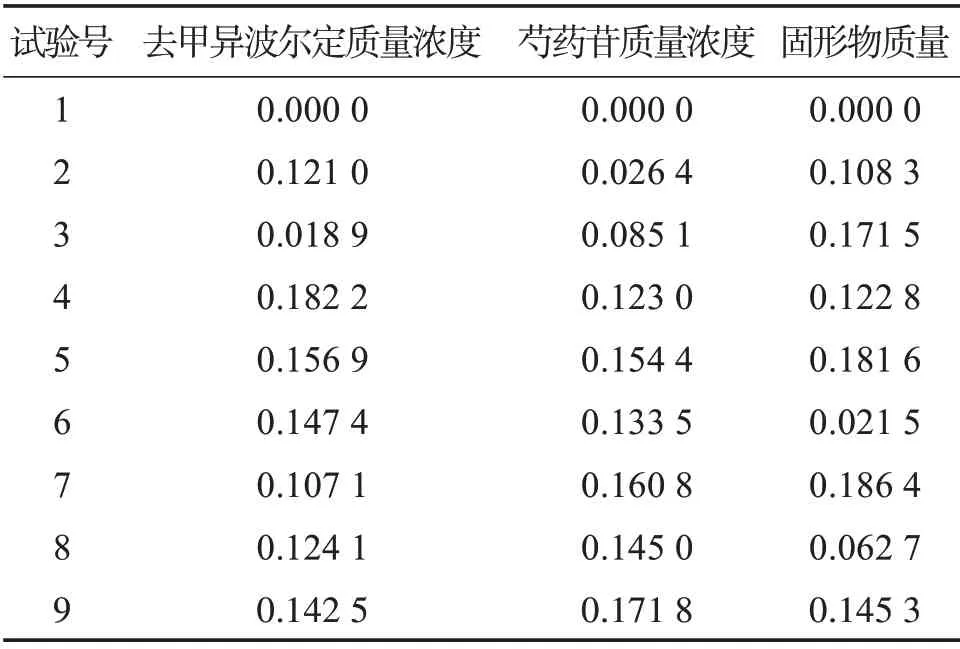
表3 各指标的Pij值Table 3 Pij value of each index
2.2.5.2 标准离差法确定权重[1,8-9]标准离差法主要是根据指标变异性的大小来确定权重。指标的标准差越大,其变异程度就越大,在综合评价中所起的作用也越大,则其权重也应越大。反之,指标的标准差越小,表明其指标值的变异程度越小,提供的信息量越小,权重也应越小。标准差(Sj)、各指标权重(Wj)的计算公式如下:
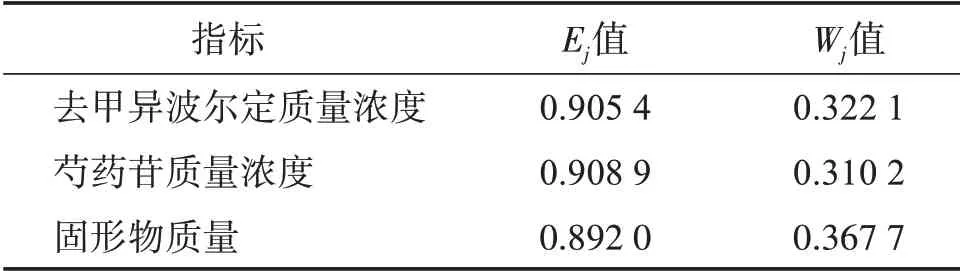
表4 各指标的Ej值和Wj值Table 4 Ej and Wj value of each index
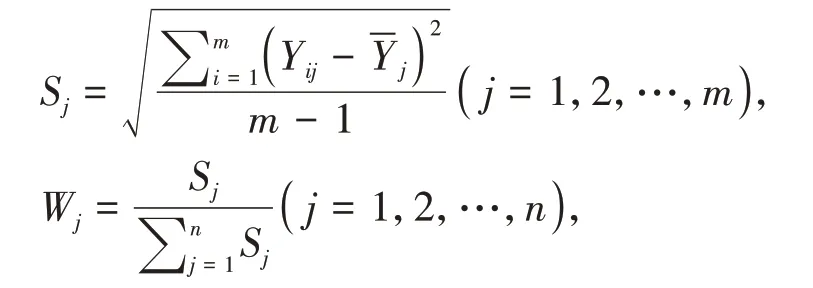
式中:Sj为第j个指标无量纲化测度值的样本标准差;Yij为第i个评价对象的第j个评价指标的无量纲化数值;为第j个指标无量纲化数值的样本平均值;Wj为第j个评价指标的权重;m为被评价对象的数目;n为评价指标的数目。计算结果见表5。
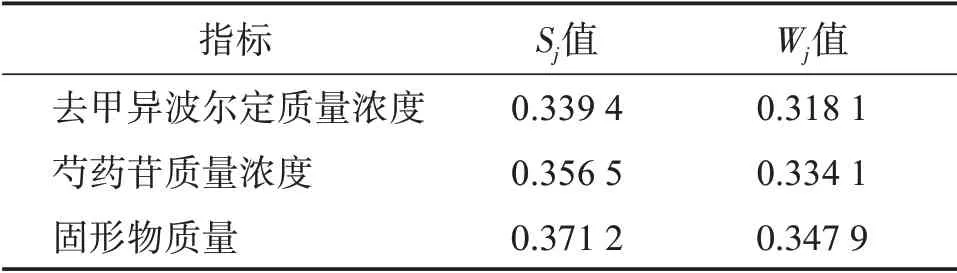
表5 各指标的Sj 值和Wj值Table 5 Sj and Wj value of each index
2.2.5.3 CRITIC 法确定权重[10-12]CRITIC 法是一种以评价指标间的对比强度及冲突性作为基础,综合衡量客观权重的计算方法。对比强度以标准差(Sj)来体现,Sj越大,各方案之间的取值差距越大。冲突性以指标间相关性为基础,以Rj的形式来体现,如果两指标之间具有较强的正相关,说明两个指标冲突性较低,表明这两个指标反应的信息较为相似。设Cj表示第j个指标所包含的信息量,Cj越大,则第j个指标所包含的信息量越大,该指标的相对重要性也就越大,客观权重(Wj)就越大。利用SPSS 软件计算出各评价指标间的相关系数(rij)矩阵,结果见表6。Rj、Cj、Wj计算公式如下:
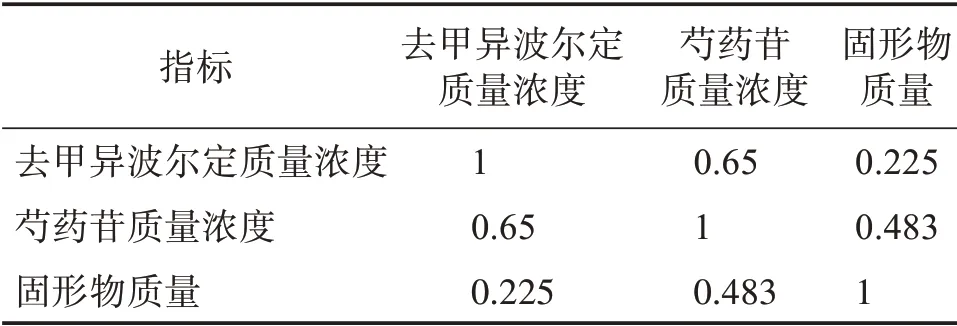
表6 各指标间的相关性Table 6 Correlation among indicators
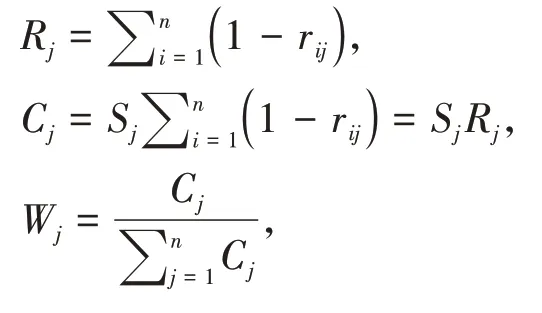
式中:rij为评价指标i和j之间的相关系数,n为评价指标的数目。计算结果见表7。
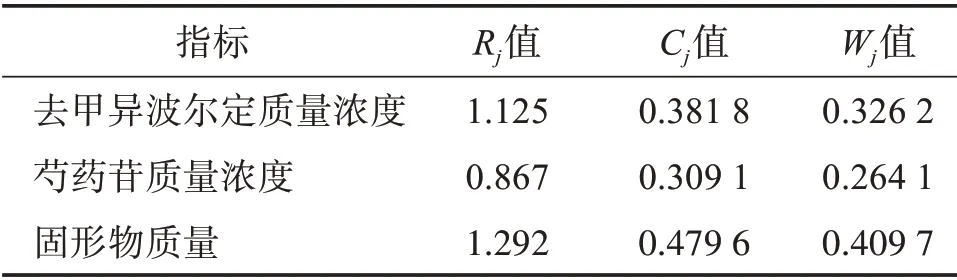
表7 各指标的Rj、Cj、Wj值Table 7 Rj、Cj、Wj value of each index
2.2.5.4 综合评价结果的比较分析 分别采用经熵权法、标准离差法、CRITIC 法分析得到的权重系数对正交试验结果进行综合加权评分,以去甲异波尔定质量浓度、芍药苷质量浓度、固形物质量9次试验的最大值为100 分,将各指标成分的总量分别转换为评分值,再乘以相应的权重系数后求和,得综合评分值,公式如下:
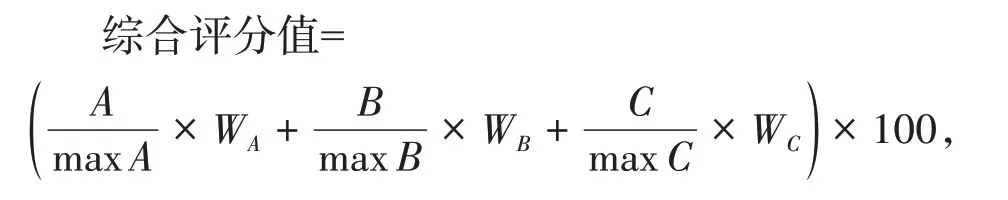
式中:A为去甲异波尔定质量浓度,B为芍药苷质量浓度,C为固形物质量,max 为正交9 次试验的最大值,W为权重系数。分析结果见表8。
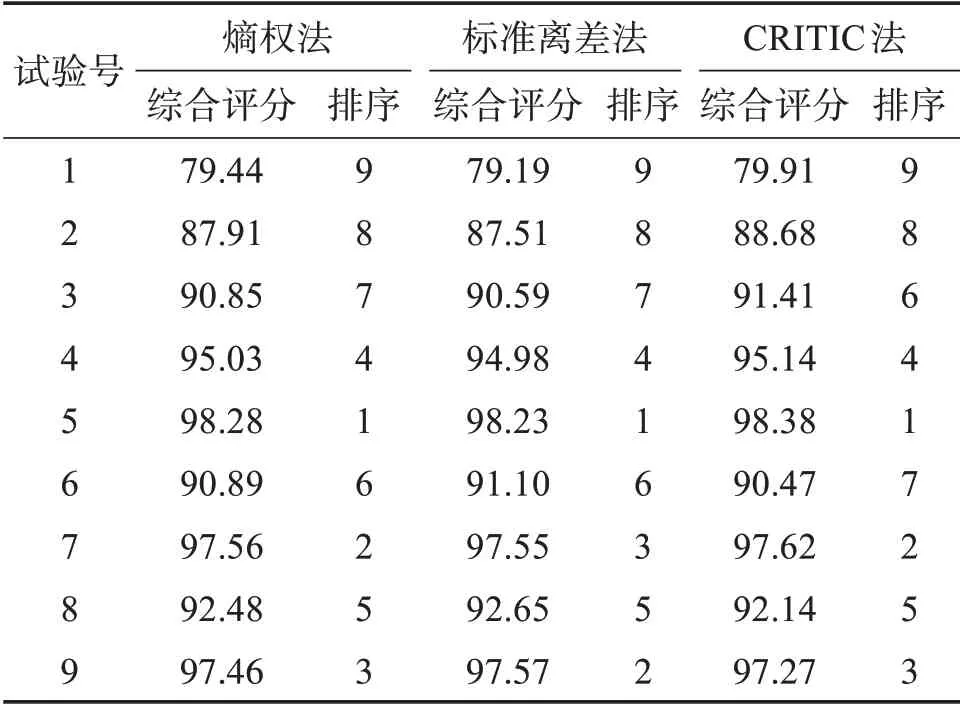
表8 3种赋权法综合评分结果分析Table 8 Analysis of comprehensive scoring results of three weighting methods
结果表明,3 种赋权法得到的综合评分值相差不大,较为接近,但各正交试验综合评分的排序存在微小的差异,分值最高的均是正交5,正交3、6、7、9 的排名有所不同。采用Kendall 协调系数W检验对3 种评分结果进行一致性检验[13-15],结果显示:Kendall 协调系数W=0.985,χ2=23.644,P=0.003<0.01,表明3 种赋权法对各正交试验的排名具有较高的一致性,其差异不具有统计学意义。由于CRITIC法不仅考虑了指标变异大小对权重的影响,还考虑到各指标之间的冲突性,更为全面,可减少指标之间信息熵的重叠,更有利于得到可信的评价结果,综合考虑,确定采用CRITIC 法确定的权重系数进行综合评分。
2.2.6 正交试验结果分析
采用CRITIC 法确定的权重系数对正交结果进行综合评分,并进行方差分析,结果见表9、10。
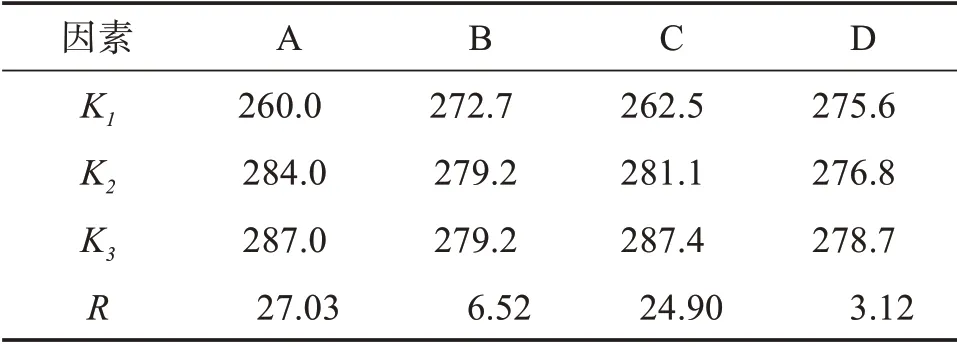
表9 直观分析表Table 9 Visual analysis
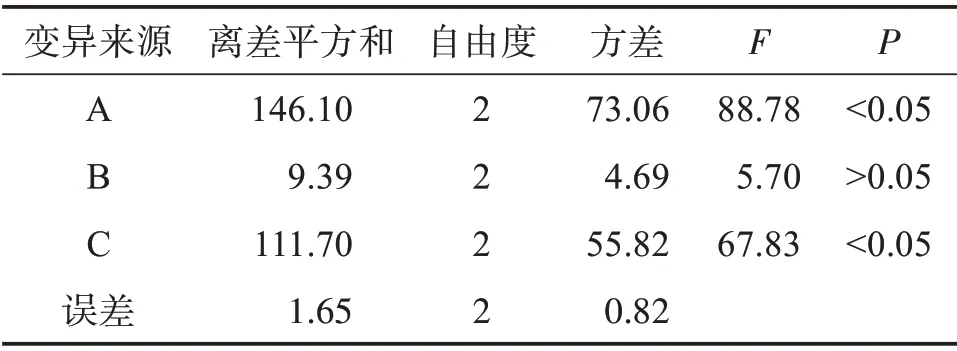
表10 方差分析表Table 10 Variance analysis
结果表明,因素A(提取次数)、因素C(加水量)对试验结果的影响有统计学意义,因素B(提取时间)对试验结果影响无统计学意义。因此,提取工艺条件确定为:A3B1C3,即加水提取3 次,每次加10倍量水,提取1 h。
2.3 验证试验
按处方比例,称取乌药、柴胡、白芍等饮片3份,每份260 g,按优选的工艺条件提取,200 目筛滤过,滤液浓缩并定容至250 mL。照上述方法测定去甲异波尔定质量浓度、芍药苷质量浓度、固形物质量,结果见表11。
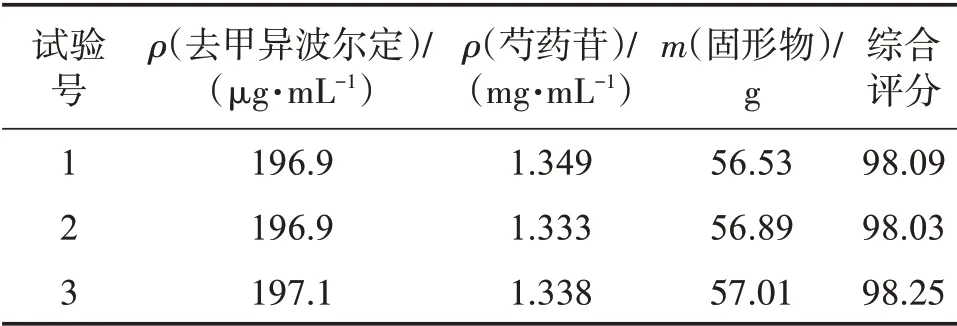
表11 提取工艺验证结果Table 11 Validation results of extraction process
结果表明:验证试验平均综合评分值为98.12,与正交试验综合评分值最大值(98.38)接近,表明优选的工艺参数稳定、合理。
3 讨论
实验前期对处方中其他药味的含量测定方法进行了考察,结果发现柴胡中柴胡皂苷a、d 的稳定性较差,这可能是由于其结构中含有环氧醚键,在高温条件下易开环发生转化;而乌药中乌药醚内脂由于属于脂溶性成分,传统水煎法或水提法不易将它溶出,使它在水提浓缩液中的煎出率低、含量很小[16];此外,佛手中橙皮苷成分含量测定方法有干扰,因此,均暂不列为评价指标。
现阶段的中药提取工艺综合评价方法常用的仍然是经验性权数法,受决策者主观上的重视程度影响较大。客观赋权法是一种建立在原始样本数据上,经数学方法统计分析、处理后获得权重的方法,它不受人为主观偏好的干扰,具有较强的数学理论依据,客观性强[2,17]。本文采用熵权法、标准离差法、CRITIC 法3 种客观赋权法,对正交试验数据分别进行分析、处理、计算,用所计算得到的权重进行综合评分,对评分结果进行一致性检验,结果表明3 种赋权法的排名具有较高的一致性。在3 种客观赋权法中,熵权法和标准离差法都是根据指标变异性的大小来确定权重,CRITIC法则不仅考虑了变异对于指标的影响,同时还考虑到各指标之间的相关性、冲突性,因此,CRITIC 法要比熵权法、标准离差法更加全面,且对于多指标多对象的综合评价问题,采用CRITIC 法可消除一些相关性较强的指标的影响,减少指标之间信息熵的重叠,更有利于得到可信的评价结果[18-19]。因此,最终确定用CRITIC法计算的权重系数进行分析,优选得到的最佳工艺条件为:提取3次,每次加10倍量水,提取1 h。该条件下,去甲异波尔定质量浓度为197.0 µg/mL、芍药苷质量浓度为1.34 mg/mL,固形物质量为56.81 g,综合评分值为98.12,与正交试验综合评分值最大值(98.38)接近,表明工艺合理可行。

