超声及超声造影引导下粗针活检在周围型肺部病变中的应用
朱鹏飞, 何 英
南通大学附属肿瘤医院, 江苏 南通 226011
在世界范围内,肺癌是最常见的癌症,是癌症死亡最主要的原因[1],在中国,肺癌是目前发病率及死亡率最高的疾病[2]。肺癌常在晚期才被诊断且5年生存率差[3]。然而,常规方法(放疗、化疗、手术)对于晚期肺癌的疗效差强人意[4]。随着肺癌的个性化医疗的发展[5],快速而精确地获取肺部病灶组织的病理结果、免疫组化及基因检测结果,更有利于诊断肺癌及制定后续治疗方案。当前获取肺部病灶组织的方法有CT、支气管镜、超声等,但对于周围型肺部病变而言,支气管镜及CT引导下的穿刺有其局限性。通常在支气管镜下活检取得的组织材料较少,因此,难以获得满意的免疫组化及基因检测结果。此外,一些老年患者无法忍受支气管镜检查,因而无法获得组织[6]。尽管CT可以提供更多肺部病变的位置信息,如肺部病变的临近组织结构及是否有纵膈淋巴结侵犯等,但其穿刺成功率低于超声,且术后并发症明显高于超声引导下穿刺[7]。而超声引导下穿刺周围型肺部病变以方便、经济、易操作、无辐射及并发率低等优点在临床上逐步成为首选方式[8]。本文主要探讨通过超声及超声造影引导下粗针穿刺活检取得患者病灶组织,从而获得精准而有效的病理结果、免疫组化及基因结果,为后续临床治疗提供有利帮助。
1 资料与方法
1.1 一般资料
研究对象随机从2018年1月至2022年3月经CT或MRI诊断为周围型肺部病变的患者中选取:超声造影组初选56例患者中,有4人经超声造影后显示不宜穿刺,其余52例患者均行超声造影,然后在其引导下经皮穿刺,作为超声造影组,其中男性38例、女性14例;平均年龄(69.3±10.4)岁。常规超声组102例,其中男性77例、女性25例;平均年龄(67.8±9.8)岁,仅在常规二维超声引导下进行穿刺。
1.2 方法
采用彩色超声仪Logiq E9,带有超声造影功能,探头频率采用3.5~5 MHz。参考CT或MRI所示病灶部位,对其行常规超声检查,观察病灶所处位置、病灶的大小、病灶的回声强弱及血流灌注等情况。造影组采用机械指数MI=0.13固定造影条件,经肘静脉注入超声造影剂2.4 mL(声诺维)。以周围的正常肺组织和胸膜软组织作为参照,着重观察病灶轮廓及增强过程,内部有无坏死区域等,穿刺时间选在造影后10~60 min内。
穿刺枪采用巴德自动活检枪,采用18G针头。常规超声组参考CT或MRI所示部位,对病变进行常规超声扫查,以确定病变的形态和大致范围、位置与其毗邻结构及其血流特征等,选取合适的进针路线,确定穿刺点;超声造影组参考造影情况,避开无增强坏死区域,尽量在明显增强区域进行穿刺取材,确定穿刺点。然后探头用无菌套隔离,装引导架,确定穿刺引导线,超声引导下进行局部麻醉,超声实时引导一次性巴德穿刺针(18G)进行穿刺,准确取到靶目标区域组织,取材需为实性组织,长度约1~2 cm,由穿刺者判断穿刺是否成功及组织条是否足够,穿刺者根据其决定取材次数,通常取材2~4次,取材后立即放入固定液中,送病理检查。穿刺结束后指示患者卧床休息,按压至少30 min,密切监测患者生命体征,特别是有无常见并发症,如气促、胸痛、咯血等。
1.3 穿刺成功判断标准
穿刺成功:(1)取出病理能分辨的、有效的病变组织;(2)取出有意义的良性细胞。
穿刺失败:(1)取出病变组织过少,病理无法确定良恶性的组织;(2)取得的病变组织为纤维结缔组织、非特异性的良性细胞或大片坏死组织等。
1.4 统计学处理
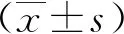
2 结果
2.1 病理结果
常规超声组:恶性病变81例,包括腺癌32例(图1)、鳞癌29例等;良性病例11例,其中炎症8例;穿刺失败10例。超声造影组:恶性病变45例,包括腺癌15例、鳞癌13例等;良性病例7例,其中炎症6例。超声造影组中有2例未能分型,亚型(分类)诊断准确率96%(50/52),常规超声组中有6例未能得出具体分型(2例诊断出非小细胞癌,4例诊断为癌),亚型(分类)诊断准确率94%(96/102)。
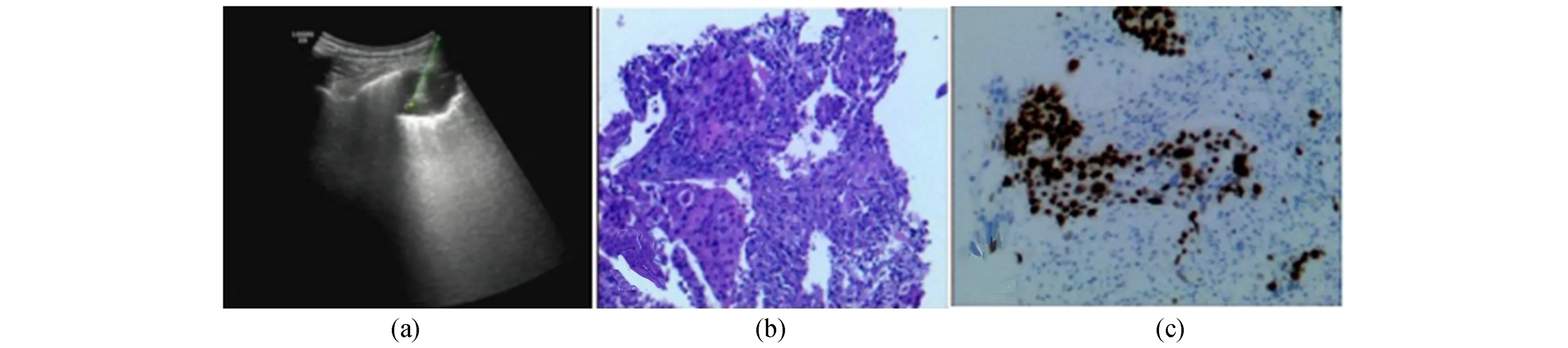
图1 常规超声引导下穿刺
2.2 免疫组化及基因检测结果
超声造影组中有19例进行基因检测,6例检测阳性,其中外显子19突变2例,外显子21突变1例,外显子20突变1例,KRAS基因突变2例,表皮生长因子受体(EGFR)阳性率32%。常规超声组中43例进行基因检测,15例阳性,其中外显子19突变7例,外显子21突变8例,EGFR阳性率35%。
2.3 两组活检参数比较
超声造影组病变最大径的平均大小为(6.2±2.0)mm,常规超声组病变最大径的平均大小为(6.2±2.5)mm。超声造影组平均大小取(2.9±0.8)针,常规超声组平均大小取(3.1±0.9)针,比较差异无统计学意义(P>0.05)。常规超声组病变内坏死显示率21%(21/102),低于超声造影组病变内坏死显示率[46%(24/52)],差异具有统计学意义(P<0.05)。影像图见图2。

图2 超声造影与常规超声坏死区域的显示
超声造影组皆取到有效组织,成功率为100%(52/52),常规超声组有10例因取到坏死组织或组织太少而无法判断病变性质,成功率为90%(92/102),超声造影组取材成功率更高,差异具有统计学意义(P<0.05),影像图见图3。超声造影组无严重并发症,而常规超声组有2例穿刺后出现咯血,并发症发生率比较,差异无统计学意义(P>0.05)。

图3 穿刺影像图
3 讨论
3.1 超声引导肺外周肿块活检
常规超声能获取肺外周病灶组织不同角度的断层图像,可以显示病灶中血流信息和坏死区域,且能实时检测穿刺过程。超声可以在安全的前提下从不同的角度选择最短最优路线,从而最大程度地获取病灶组织[9]。此外,超声可以选择多个不同的区域进行穿刺,从而获得同一病灶不同区域的组织,以此满足病理分型、免疫组化、基因诊断的要求,对临床诊断及治疗提供帮助。彩色多普勒在活检过程中可实时显示穿刺针,避免大血管撕裂。Guo等[10]研究显示,超声引导下肺外周病变活检总体诊断准确率为81.8%,对于直径≤20 mm、21~49 mm和≥50 mm的病灶,诊断准确率分别为72.0%、86.8%和79.7%。Huang等[11]利用彩色多普勒引导下穿刺外周肺、胸壁和纵膈病变,其敏感性为93.94%,特异性为100%,诊断准确性为95.04%。本研究中首次穿刺成功率90%,其中有43例进行基因突变检测,EGFR阳性率为35%,19例进行PD-LI免疫组化检测,均能满足检测需要。
3.2 超声引导肺外周肿块活检局限性
虽然彩色多普勒超声能够一定程度上反映病变的血流状况,但对于肺部病变中真实的血流灌注情况显示欠佳,并且普通超声难以提供更多的细节,例如病变内的坏死区、隐藏在不张肺叶内的病变等,另外对于其与周围大血管的关系显示欠佳,易造成假阴性和取材失败[12]。研究表明,常规超声穿刺失败率达5%~15%[13],本研究中由于大片坏死而造成取材失败者有10例。
3.3 超声造影引导肺外周肿块活检
常规超声通过观察病灶的二维灰阶图像来区分坏死区域,一般认为无回声或极低回声为坏死区域,而超声造影则是根据病灶的增强情况来区分坏死与否。通常富血供、有活力的区域在注射造影剂声诺维后会显著增强,而坏死区域在注射造影剂声诺维后表现为灌注缺损或无灌注,另外大多乏血供病变区在注射造影剂声诺维后表现为轻微增强或增强不明显。在本研究中,部分病例其肺部病灶中在超声造影下显示为灌注缺损或无灌注的区域,在其常规二维超声表现中却显示为等回声的区域(图1),而有部分病例其肺部病灶中在常规二维超声上表现为极低回声的区域却在超声造影下可表现为显著增强的区域。利用超声造影对病灶中坏死灶检出的优势,避开坏死区域,选择合适的穿刺点及穿刺路线(图2),有利于提高穿刺成功率[14]。穿刺组织中大部分为坏死组织,缺乏可用于病理诊断的有效组织是本次研究中穿刺失败的主要原因。肺部病变,尤其是较大的病变,大多伴有坏死、炎症、肺不张等,有研究表明对于显示病变内部坏死率,超声造影明显较高[15],本研究中超声造影组病变中有24例显示其内部有坏死区域,坏死显示率46%,远高于对常规超声穿刺组的21%。有研究表明,在低或无增强区域取得的组织大多数为坏死组织,而在高增强区常常能取得较好的病变组织[16]。
虽然彩色多普勒超声对于病灶内的血流分布情况在一定程度上能予以显示,但对于一些低速血流及微小血管缺乏有效的显示。另外患者的呼吸运动对彩色多普勒超声会产生较大影响,从而导致病灶内血流情况显示欠佳。而超声造影能实时清晰地显示病灶内血管分布,不受呼吸干扰,能引导穿刺时避开大血管,有效地减少并发症的发生。本研究中有一例患者术后出现咯血,其原因可能是彩色多普勒未能完全显示出病灶内及其周边的血管分布情况,导致穿破血管而引起。此外尽管穿刺成功率可随穿刺次数的增加而增大,但气胸、出血等并发症发生的可能性也会增加。有研究表明穿刺取材次数少于2次时,其并发症明显低于穿刺取材次数大于2次者[17],因此精准穿刺非常重要。而超声造影比常规超声更能显示肺部病灶的内部结构,更加精确地引导穿刺,从而减少穿刺次数。
肺为双重血液供应,有研究发现,良性肺部病变中的血流主要来自于肺动脉,而恶性病变中的血流通常来自支气管动脉,根据病灶增强时间及灌注模式,可初步判断病灶的良恶性,增强穿刺者的信心,减少穿刺针数[18],本研究中常规超声引导下穿刺平均穿刺针数(3.1±0.9)略高于超声造影引导下穿刺针数(2.9±0.8)。
3.4 结论
超声及超声造影引导下穿刺是一种安全有效的方法,对于患者的诊断、病理分型、免疫组化、基因诊断都具有重要价值。超声造影对于病灶与周边组织结构的关系及病灶内部的血流情况较常规超声更具优势,并且更有利于区分肺部病变内部的活性区域及坏死区域,能有效地提高穿刺成功率。

