有无均整器下肺癌立体定向放疗的差异性研究*
杨鹏,王伟生,徐成,宋宏昌,黎杰,康盛伟,吴骏翔
610041成都,四川省肿瘤医院·研究所,四川省癌症防治中心,电子科技大学医学院 放射肿瘤学四川省重点实验室(杨鹏、黎杰、康盛伟、吴骏翔);628000四川 广元,广元市中心医院 肿瘤科(杨鹏、王伟生、徐成);615000四川 凉山州,西昌市人民医院 肿瘤科(宋宏昌)
立体定向放射治疗(stereotactic body radiation therapy,SBRT),是通过精确聚焦射线在靶区病灶上使靶区剂量提高的同时,尽量减少正常组织接受的剂量[1]。无均整器(flattening filter free,FFF)技术是将常规加速器中均整过滤器(flattening filter,FF) 移除,从而产生锥形的剂量剖面曲线并且提升射束中心的剂量率,缩短了治疗时间[2-3]。此外,FFF技术也减少了散射线和漏射线,有效降低了靶区外正常组织的剂量[4-6]。
因此,FFF模式已逐渐应用于SBRT技术中[7-9], 尤其对不可手术的早期肺癌患者来说,极大提高了肿瘤控制率和3年内的存活率[10]。近年来,关于FFF模式和FF模式下肺癌SBRT剂量学差异的研究较多,大多数文章均是单独比较两种技术之间的物理剂量差异[4,11];或是关于肺癌SBRT生物学剂量的研究[12]。少有关于比较两种模式在肺癌SBRT治疗中的物理剂量学和放射生物学差异的研究。因此,本文旨在比较FFF模式和FF模式下,肺癌SBRT中放疗物理剂量和放射生物学的差异,为该技术的临床应用提供一定的参考价值。
1 资料和方法
1.1 患者资料
本研究随机选取2022年1月至2022年4月在四川省肿瘤医院接受SBRT放射治疗的非小细胞肺癌患者84例,患者年龄45 ~ 68岁(中位年龄61岁),所有患者均证实无放射治疗禁忌症。靶区体积大小为8.14 ~ 33.49 cm3,体积中位数为16.67 cm3。根据RTOG 0813报告[13]对于靶区体积的分类,其中靶区体积在7.4 ~ 13.2 cm3区间的24例、13.2 ~ 22.0 cm3区间的47例、22.0 ~ 34.0 cm3区间的13例;靶区位置均属于周围型(靶区距离支气管的距离大于2 cm)。
1.2 CT定位和靶区勾画
使用体部热塑膜对患者进行体位固定,所有患者均为仰卧位,双手固定于两侧。模拟定位CT为飞利浦公司的Brilliance BigBore的16排专用大孔径定位CT进行4DCT扫描,CT重建厚度为0.3 cm,获取患者的10个呼吸时相序列图像。定位完成后将患者的4DCT数据传入MIM Maestro软件,重建获得最大密度投影图像和平均密度投影(average intensity projection,AIP)图像,并由其主管医生完成靶区和危及器官的勾画。靶区勾画包括:肿瘤大体靶区(gross tumor volume,GTV)为影像所见肺部病灶,4DCT各时相上分别勾画GTV然后叠加生成内靶区(internal target volume,ITV),ITV外放5 mm生成计划靶区(planning target volume,PTV)[14]。危及器官(organ at risk,OAR)勾画包括:心脏、脊髓、食管、气管、双肺组织。PTV的处方剂量为50 Gy/5 F。
1.3 计划设计
将CT及勾画好的结构传到Pinnacle39.10 计划系统进行计划设计,所有病例分别在剂量模式为6 MV的FFF模 式(VMATFFF)和FF模 式(VMATFF)下进行容积旋转调强放疗(volumetric modulated arc therapy,VMAT)计划设计,剂量率大小分别为1 400 Mu/min和600 Mu/min,优化时靶区和危及器官均采用相同的剂量限制条件,计划的优化和计算使用4DCT的AIP图像。设计SBRT计划时VMAT采用两个往返弧,并根据靶区的位置设置相应的弧度,计算网格采用2.0 mm,共面野,间隔2°出束。优化算法为SmartArc,剂量算法为Adaptive Convolve 。加速器采用医科达公司生产的Infinity直线加速器,配备80对0.5 cm的多叶光栅。计划设计靶区和危及器官的要求为:对于PTV,50 Gy的剂量线要求至少覆盖90%体积的靶区;危及器官剂量体积限制要求见表1。

表1 危及器官剂量体积限制要求Table 1.Limitation on Dose Volumes for OARs
1.4 SBRT计划评估
靶区评估采用D90、D2、靶区覆盖率(coverage rate,CR)、适形指数(conformity index,CI)以及梯度指数(gradient index,GI)[13,15-16]。
CR的定义为式 (1):
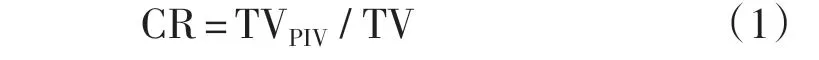
式中,TVPIV表示为处方剂量所包含的靶区体积,TV表示靶区体积;
CI的定义为式(2):
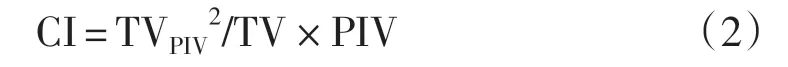
其中,PIV表示为处方剂量所覆盖的总体积。CI的值越接近1表示其适形度越好;
GI的定义为式(3):

式中,PIV50%PIV表示剂量为50%的处方剂量所包绕的体积,对于相同适形度的靶区,靶区外越陡峭的剂量梯度是其优于其他放疗计划的重要因素。
OAR的评估包括脊髓的0.25 cc、0.5 cc;左右肺的1 000 cc和1 500 cc;食管的5 cc;气管的4 cc;心脏的1 500 cc[13]。;并比较了两种模式下的机器跳数(monitor unit,MU)。
1.5 正常组织并发症概率(normal tissue complication probability,NTCP)模型
NTCP模型是一种建立在剂量-体积关系的数学模型,通过不同的参数来比较或者预测不同器官在接受一定照射剂量后出现放疗并发症的概率。通过提取剂量体积直方图(dose volume histogram,DVH)中的参数,将DVH中的物理剂量转化成生物有效剂量(biological effective dose,BED),线性二次(linear guadratic,LQ)模型可以良好地反映细胞与射线发生作用的生物学效应,公式如式(4) 所示:
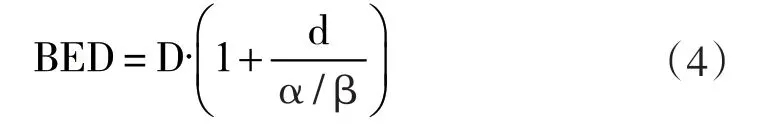
其中,D表示为处方剂量,d表示为单次剂量,α/β表示放射损伤中不可修复的部分占可修复部分的比例。经Borst等[17]论证,对于肺组织,当α/β的比值为3时,LQ模型得到的生物剂量用来评估放疗毒性发生的概率是最优的。除此之外,还需将非均匀的剂量转化为等效均匀剂量(equivalent uniform dose,EUD)进行计算。NTCP模型的公式如式(5):
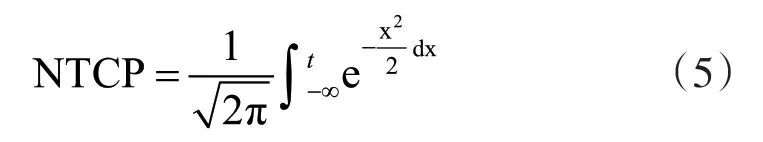
其中,
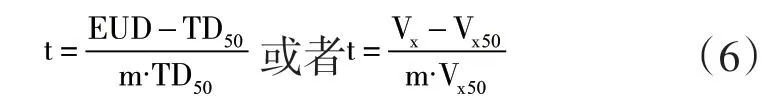
式(6)中,TD50表示50%的概率发生并发症的剂量,m为曲线的斜率参数,曲线的陡度随着m的减小而增大。Vx表示组织中接受剂量为xGy的体积,Vx50表示放疗并发症发生的概率为50%时xGy下所接受的体积。本次研究中采用的是肺平均剂量(mean lung dose,MLD)模型即EUD = MLD,所有计算的参数如表2所示[17-18]:

表2 计算NTCP所需参数Table 2.Parameters Used to Calculate NTCP
1.6 统计学方法
将两组计划的数据进行对比,使用SPSS 23.0进行统计分析,数据均以均数±标准差来表示,采用配对t检验,P<0.05差异具有统计学意义。
2 结 果
2.1 剂量学参数结果
表3所示为两组计划靶区剂量学参数的比较结果,如表所示,VMATFFF组与VMATFF组计算得到的D90、D2、CR、CI和GI的差异均无统计学意义(P > 0.05)。
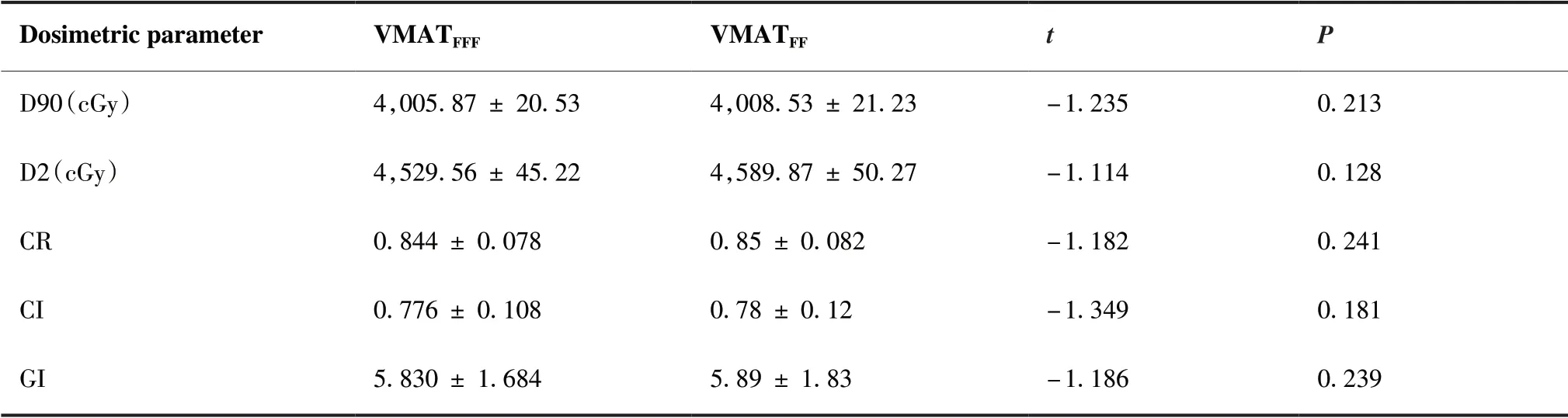
表3 计划靶区的剂量学参数比较Table 3.Dosimetric Parameters of PTV
表4所示为脊髓、食管、气管、双肺和心脏的剂量学参数统计结果,两组计划中脊髓0.25 cc的差异有统计学意义(P<0.05),且VMATFFF组计划中的脊髓0.25 cc的均值小于VMATFF组计划的结果;脊髓0.5 cc的差异有统计学意义(P<0.05),且VMATFFF组计划该参数平均值小于VMATFF组计划的结果;食管5 cc的差异有统计学意义(P<0.05),且VMATFFF组计划该参数平均值小于VMATFF组计划的结果;肺1 500 cc的差异有统计学意义(P > 0.05),且VMATFFF组计划该参数平均值小于VMATFF组计划的结果。其他结果的差异均无统计学意义(P > 0.05)。
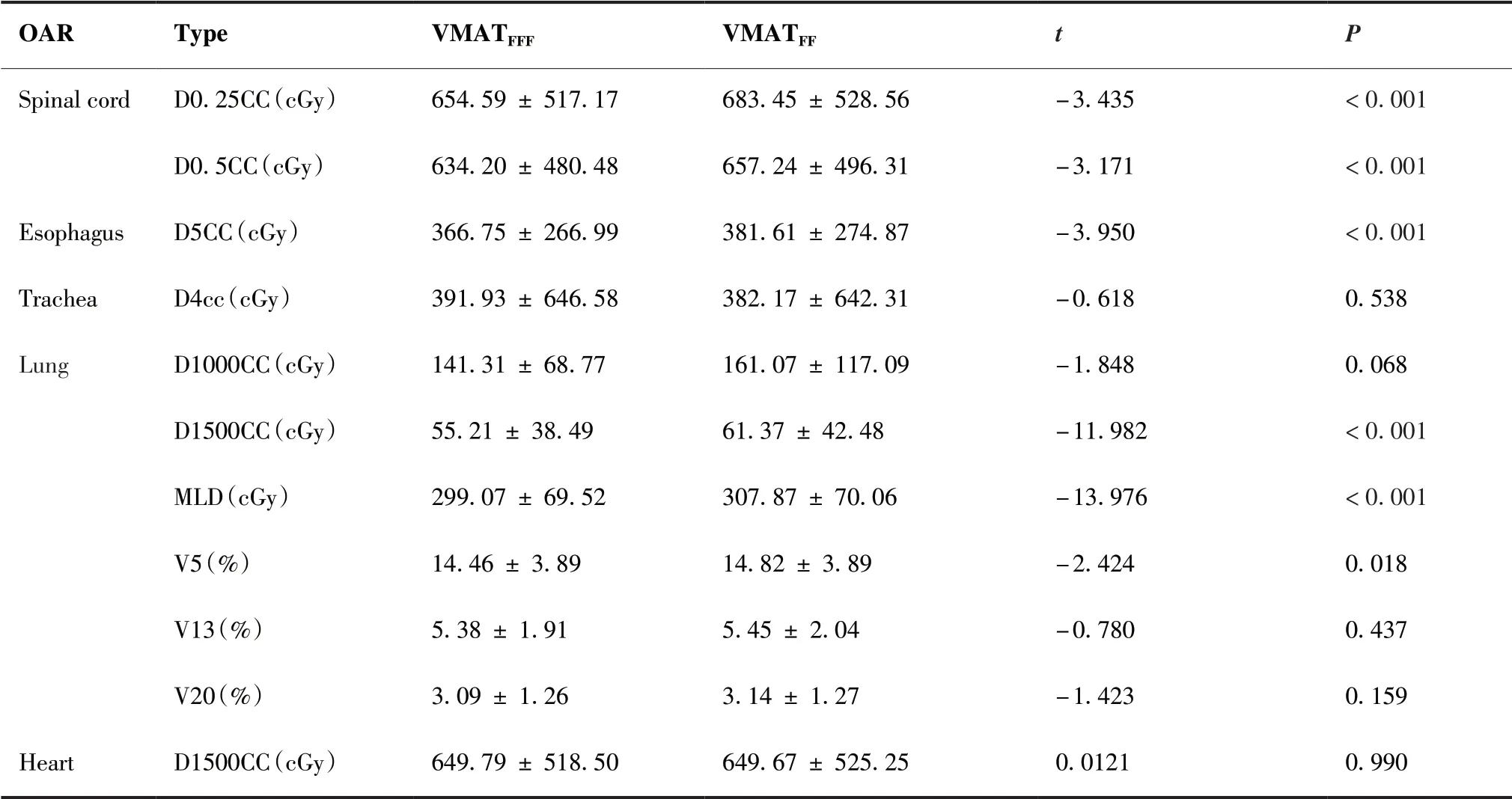
表4 危及器官的剂量学参数比较Table 4.Dosimetric Parameters of OARs
2.2 肺部放射生物学参数结果
表5为双肺的MLD、V5、V13、V20以及通过MLD 模型得到的NTCP值。其中,两组计划得到的MLD和V5的NTCP值的差异具有统计学意义(P<0.001),且VMATFFF组计划的NTCP的平均值均小于VMATFF组计划得出的结果。其余放射生物学参数的差异不具有统计学意义(P > 0.05)。
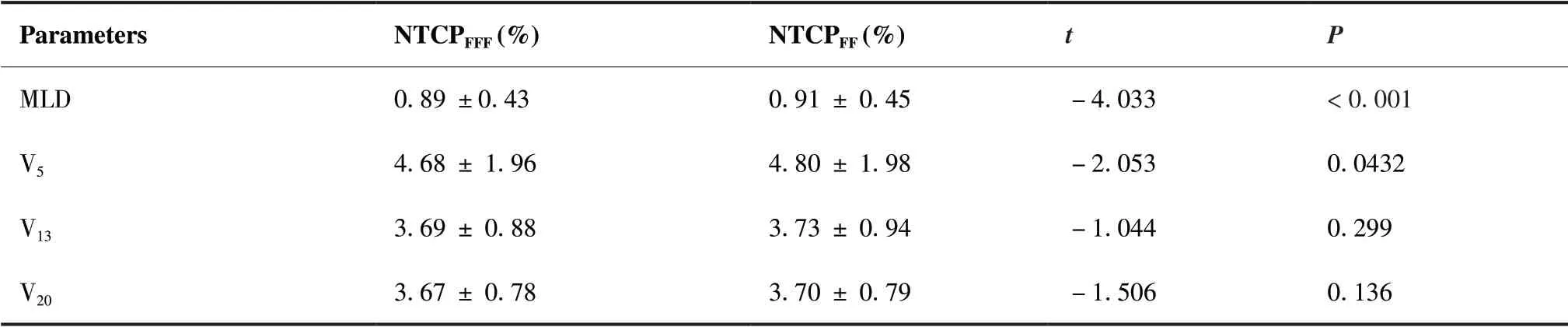
表5 肺部NTCP结果比较Table 5.NTCP of Lung
2.3 两组计划机器跳数比较
VMATFFF计划的MU为1 883.89±287.334,VMATFF计划的MU为1 897.91±266.94,经配对t检验分析,两组数据的差异无统计学意义(P > 0.05)。
3 讨 论
SBRT具有单次剂量大的特点,使用常规的剂量率照射导致治疗时间较长,对于心肺功能较差的老年患者,长时间刚性固定体位治疗的难度较大;另一方面,长时间的治疗可能增加肿瘤移位的风险(患者自身移动),因此需要额外的影像检查来确定肿瘤的位置[19]。FFF模式是在治疗中关闭均整器,均整器的作用是在靶区上产生一个平坦的剂量分布,但是在某些不平坦的部位治疗中,往往会出现靶区周围产生热点而靶区中心出现冷点。对于调强放射治疗来说,均整器的移除并不会产生影响,因其正需要剂量分布与靶区高度适形。移除均整器可以将剂量率提高两倍以上,从而减少了治疗时间;同时,散射线和漏射线的产生大大降低。Kragl等[3]研究表明,6 MV光子下,机头散射和漏射线降低了40%和52%,10 MV光子下分别为56%和65%。Gasic等[4]比较了FFF模式和FF模式下早期肺癌的放疗计划与治疗时间,评估靶区采取覆盖率、适形指数,发现两种模式下的差异无统计学意义(P > 0.05),与本研究所得结果一致;除此之外,本研究还评估了D2、D98、CR、CI和GI值,两种模式下所得结果的差异均无统计学意义,可知两种模式对靶区的影响差异不大。在危及器官评估中,Gasic等[4]对肺部SBRT评估得到FFF模式下的计划脊髓的结果要优于FF模式,肺V20之间的差异无统计学意义;本研究结合RTOG0813报告[15],评估了脊髓D0.25cc和D0.5cc,食管D5CC,气管D4cc,肺V5,V13,V20,D1000cc和D1500cc,心脏D1500cc;VMATFFF组 与VMATFF组 相 比,脊 髓D0.25cc和D0.5cc分别降低了28.86 cGy和23.04 cGy(P < 0.05);对于食管D5cc,VMATFFF组比VMATFF组降低了14.86 cGy(P < 0.05);对于肺MLD、D1500cc和V5,VMATFFF组与VMATFF组相比分别降低了8.8 cGy、6.16 cGy和0.36%(P < 0.05)。其余结果的差异无统计学意义(P > 0.05)。可以看出,FFF模式下的计划对危及器官的保护更好。
NTCP模型是一种数学模型,通过提取DVH中的数据进行计算得到相应器官接受一定剂量后出现放疗并发症的概率并以此来评估放疗计划的质 量[20]。许多研究工作借助NTCP模型,对临床和放射物理学数据进行分析,以此来优化治疗方案。目前有较多NTCP模型[21],本文采用的是MLD模型,该模型是Lyman-kutcher Burman(LKB)模型的特殊形式(体积因子n = 1)[17]。通过MLD模型得到了FFF和FF模式下MLD,V5,V13,V20的NTCP,比较得出MLD和V5的结果差异具有统计学意义,在FFF模式下,由MLD计算得到的NTCP值降低0.02%,由V5计算得到的NTCP值降低0.12%,V13和V20的结果的差异无统计学意义(P > 0.05)。由此也验证了FFF模式对危及器官的保护要优于FF模式。此外,本研究还比较了两组模式下机器跳数的情况,其差异无统计学意义,但FFF模式下的剂量率远大于FF模式下的剂量率,机器跳数相近的情况下侧面反映出FFF模式的治疗时间会更短。本次研究选取的病例中靶区体积较小且均为单靶区,不能完全体现于较大的靶区和多靶区情况,后续研究将比较两种模式在多中心靶区和大体积靶区的差异。同时,本次研究未能评估两种模式下治疗时间的差异,后续研究将对比两种模式下的治疗时间,从机器执行效率比较两种模式的差异。
综上所述,本研究通过对比84例肺癌的FFF模式和FF模式的SBRT计划的放射剂量学与放射生物学的结果表明,两组计划在靶区剂量分布的差异无统计学意义,在对OAR的保护中,FFF模式优于FF模式,使得脊髓、食管、肺的受量更小,在进行放射生物学评估中得到,FFF模式下MLD和V13的NTCP值更小,从而说明发生放射性肺炎的概率更小,进一步体现了FFF模式在肺部SBRT中的优势,临床实用性更高。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。

