速度向量成像技术评价二叶式主动脉瓣患者升主动脉弹性的价值
张 娇,纳丽莎,马 鑫,王 琴
(1.宁夏医科大学,银川 750004;2.山东省妇幼保健院,济南 250000;3.宁夏医科大学总医院心脏中心功能检查部,银川 750004)
二叶式主动脉瓣(bicuspid aortic valve,BAV)是一种常见的先天性心脏病,发病率为0.5%~2.0%[1],男性多发[2]。瓣膜功能障碍是BAV最常见的并发症,其次就是严重BAV相关的主动脉病变(BAV associated aortopathy,BAV-AA)。研究[3-4]表明,BAV-AA与胸主动脉瘤的形成、主动脉夹层高发病率和高病死率有关。尽管BAV患者发病早期是无症状的,但通常伴随着进行性瓣膜病和胸部主动脉疾病[3,5],可导致慢性心力衰竭,增加急性动脉综合征和心源性猝死的风险[3]。因而BAV相关的BAV-AA已成为目前研究的热点。近年来,速度向量成像(velocity vector imaging,VVI)技术已成为一种无创的评价心脏及大动脉管壁结构力学的超声新技术,可以用来评价大血管管壁弹性的改变。因此,本研究应用VVI技术联合M型超声检测BAV患者升主动脉弹性参数并分析二者之间相关性,探讨VVI技术评估BAV患者升主动脉弹性的临床应用价值。
1 资料与方法
1.1 研究对象
选取2017年10月至2019年8月在宁夏医科大学总医院就诊的无并发主动脉瓣功能不全(狭窄或反流)或仅有轻度主动脉瓣功能不全BAV 40例患者作为病例组。其中男性34例,女性6例,平均年龄(42.50±14.14)岁。根据STeich法和双平面Simpson法测量左室射血分数(LVEF)≥55%。排除标准:1)年龄>65岁;2)透声差;3)心律不齐、高血压、糖尿病、心肌病的患者;4)主动脉瓣中重度狭窄和(或)关闭不全的患者。选择与病例组年龄、性别相匹配的健康体检者20例作为对照组,其中男性11例,女性9例,平均年龄(37.1±10.34)岁。
1.2 研究方法
1.2.1 仪器与方法 使用西门子ACUSON SC2000超声诊断仪器,探头(4 V1),频率带宽(1.25~4.5 MHZ),深度(16~21 cm),受检对象左侧卧位,保持呼吸平稳,全程记录三导联心电图,根据2016年《中国成年人超声心动图检查测量指南》[6],先进行常规超声参数的测量。
1.2.2 采用M型超声测量计算升主动脉弹性参数 在升主动脉长轴切面,确定主动脉瓣上3 cm位置,启动M型,存储记录升主动脉M型运动曲线(图1),分别测量升主动脉舒张末期内径(aortic diastolic dimension,AoD)和升主动脉收缩末期内径(aortic systolic dimension,AoS),同步记录动脉血压。参考Nistri等[7]推荐的方法计算下列指标:1)升主动脉应变(aortic strain,AS):AS(%)=100(AoS-AoD)/AoD;2)升主动脉僵硬指数(aortic stiffness index,ASI):ASI=ln(SBP/DBP)/[(AoSAoD)/AoD];3)升主动脉扩张性(Aortic distensibility,ADIS):ADIS(10-6cm2.dyn-1)=[2(AoS-AoD)/(AoD×PP)]。
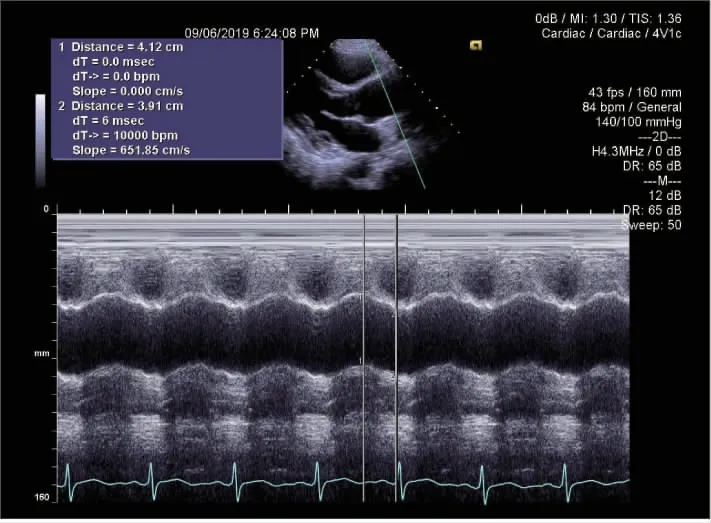
图1 左室长轴切面上经主动脉瓣上3 cm处取样获得升主动脉M型运动曲线
1.2.3 应用VVI技术测量BAV患者的升主动脉VVI参数1)图像采集:同步连接心电图,嘱受检者呼气后屏住呼吸,获得清晰的升主动脉长轴切面,存储3个心动周期动态图。2)脱机分析:启动VVI软件,选择自由轨迹切面模式,将图像停帧于收缩期,定位主动脉瓣上3 cm处,开始沿升主动脉长轴前、后管壁每隔0.5 cm选取1个标示点,前后壁各选取4个标示点,逐点手工描记,取样结束后,工作站会自动检测每个标点,并收集每个取样点的VVI相关资料,最后工作站会自动计算得出舒张期与收缩期的应变值(Smax)、应变率(SRmax)及最大纵向运动速度(Vs)、最大纵向运动位移(Ds),见图2~图5。
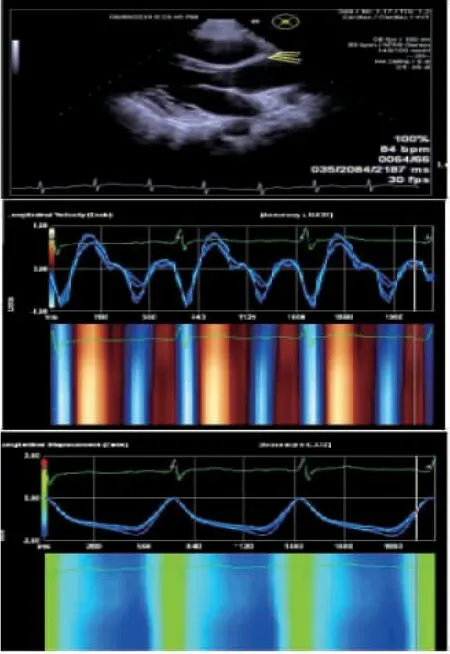
图2 应用VVI软件分析病例组升主动脉前壁纵向运动速度及位移
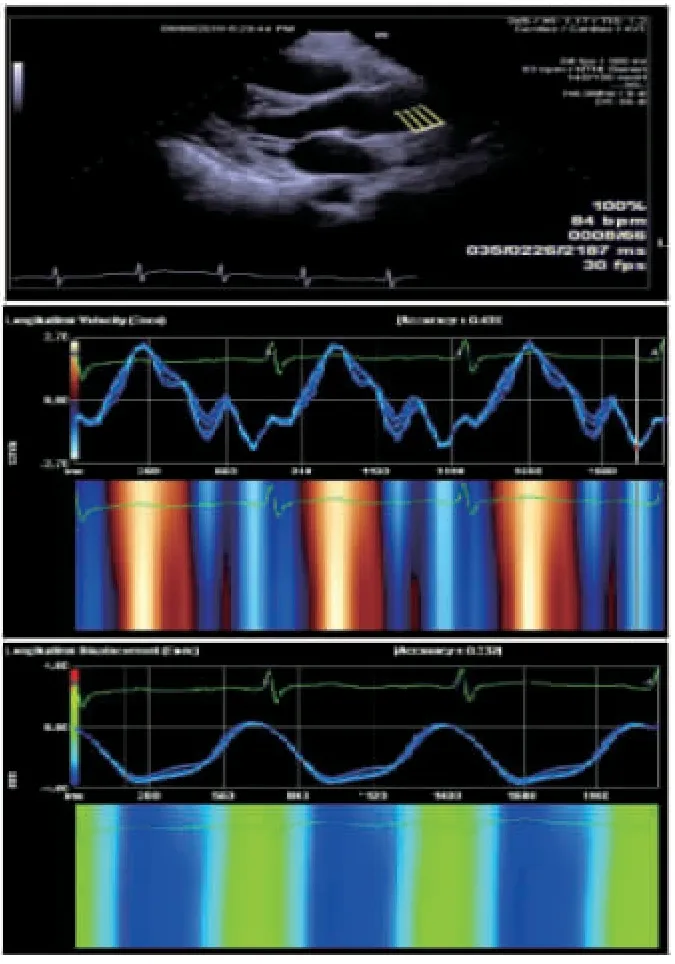
图3 应用VVI软件分析病例组升主动脉后壁纵向运动速度及位移
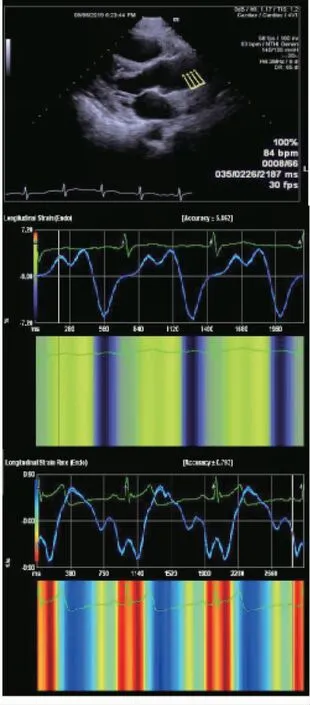
图5 应用VVI软件分析病例组升主动脉后壁应变值、应变率
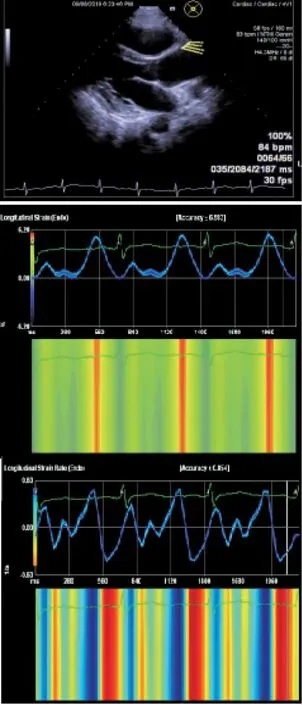
图4 应用VVI软件分析病例组升主动脉前壁应变值、应变率
1.3 统计学方法
采用SPSS 23.0软件进行统计学分析。计量资料用均数±标准差(±s)表示,两组间比较采用t检验。采用Pearson相关性分析。P≤0.05为差异有统计学意义。
2 结果
2.1 两组一般临床资料及常规超声测定指标比较
病例组左心室舒张末期内径(LVE-DD)较对照组增宽(P<0.05);年龄、体表面积、收缩压、舒张压、脉压差、LVEF、舒张早期二尖瓣口血流速度(E)、舒张晚期二尖瓣口血流速度(A)两组间差异均无统计学意义(P均>0.05),见表1。

表1 两组患者一般临床资料及常规超声测定指标比较
2.2 两组M型超声检测升主动脉弹性参数比较
病例组AoS、AoD较对照组增宽,AS、ADIS较对照组减低,ASI较对照组增加(P均<0.01),见表2。
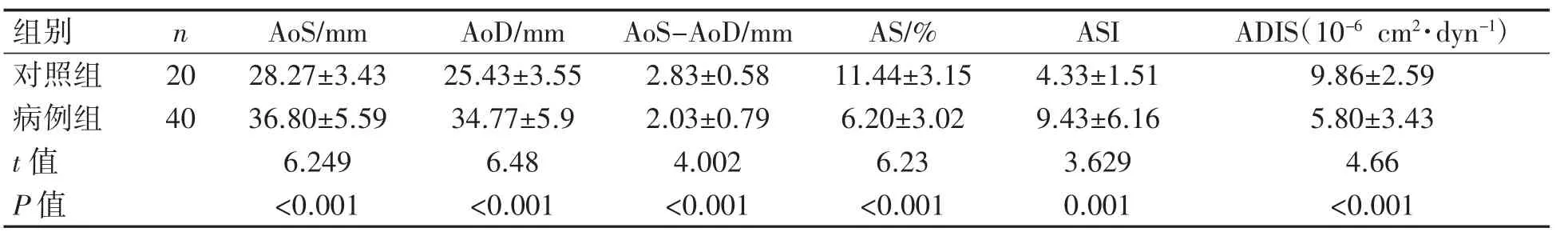
表2 两组患者M型超声检测升主动脉弹性参数比较
2.3 两组升主动脉长轴前、后壁应变参数比较
病例组与对照组升主动脉前、后壁的Vs、Ds比较差异均无统计学意义(P均>0.05);病例组升主动脉前、后壁的Ss、SRs均较对照组减低(P均<0.05),见表3。
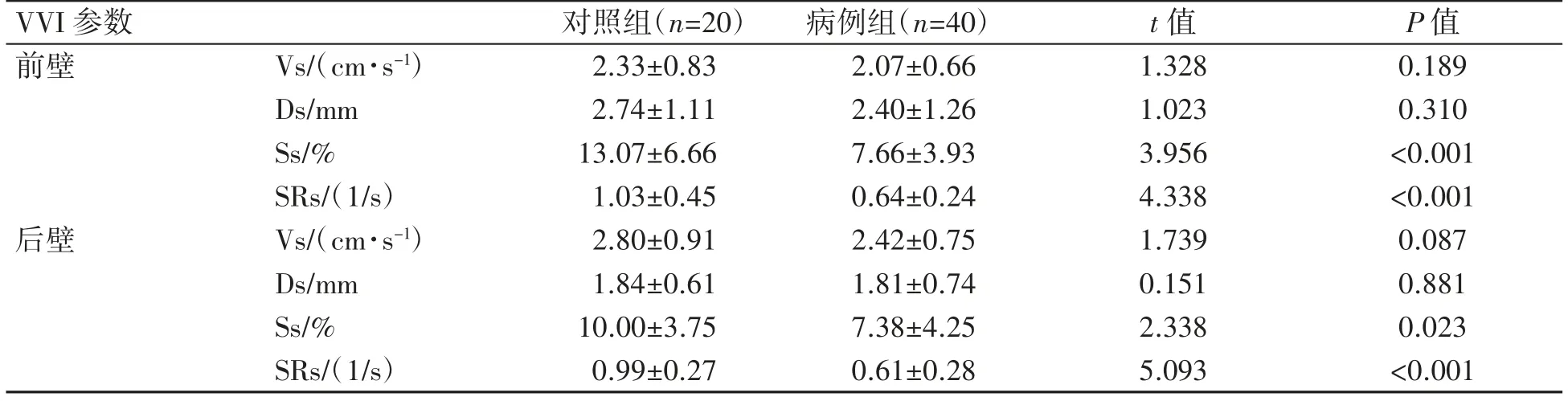
表3 两组患者升主动脉长轴前、后壁应变参数比较
2.4 升主动脉弹性参数与升主动脉前、后壁应变值相关性分析
升主动脉前壁:Ss与AS、ADIS呈正相关,与ASI呈负相关(P均<0.05);升主动脉后壁:Ss与AS呈正相关(P<0.05),与ASI、ADIS无相关性(P均>0.05),见表4。

表4 升主动脉弹性参数与升主动脉前、后壁应变值相关性分析
3 讨论
先天性BAV不仅是一种瓣膜病,也是一种主动脉疾病。研究[8]发现,BAV患者中20%~40%伴有主动脉扩张;与普通人群相比,BAV患者主动脉夹层风险增加了约8倍[9]。血管病变的发展早期通常表现为血管壁弹性的改变,动脉弹性又是临床中反应血管壁亚临床病变的重要指标。因此,在临床工作中,密切监测血管弹性变化十分重要。
本研究结果发现,BAV患者常规M型超声检测并计算的升主动脉弹性指标与对照组相比,升主动脉内径增宽,升主动脉应变和ADIS减低,ASI明显增加,这与Santaipia等[10]的研究结果相一致。与正常人群相比,成年BAV患者升主动脉的应变和扩张性均减低,而僵硬指数较正常人群增加。BAV患者动脉管壁损害的原因尚在探讨中,一方面可能是先天性主动脉壁发育缺陷[11-12]。术后病理证实,BAV患者主动脉壁中膜层结构异常,囊性坏死,其中主动脉基质金属蛋白酶异常高表达[13-14]。另一方面,考虑与主动脉瓣的形态、结构改变导致的血流动力学变化有关。本研究纳入无主动脉瓣狭窄与反流和仅轻度主动脉瓣膜狭窄与反流的患者,在一定程度上控制了血流动力学对主动脉管壁的影响因素,进一步说明BAV患者动脉管壁损害的原因更可能与先天性主动脉壁发育缺陷有关。
动脉弹性减低也高度提示患者有发生心血管疾病的风险[15]。传统对主动脉弹性的检测通常由心脏收缩引起的动脉管径的变化结合动脉压力而获得。应用公式所使用的动脉压力都是肱动脉的脉压,不能真实反映主动脉的脉压。随着超声心动图技术的发展,VVI技术作为评价心脏及大动脉管壁结构力学和弹性功能的新方法,可以简单、定量地分析血管的自身力学运动状态及血管壁的形态改变,不受切面及角度的影响,获得管壁的运动速度、位移及应变、应变率等参数,可以从微观视角辅助监测血管壁的变化,提高对心血管管壁方面亚临床改变的检出率。
本研究采用了VVI技术定量评价升主动脉管壁的应变发现,与对照组相比,病例组升主动脉前、后壁应变参数减低。同时,本研究对VVI技术测得的升主动脉前、后壁的应变值与M型超声检测并计算的升主动脉弹性参数进行了相关性分析,结果发现二者具有良好的相关性。临床上,BAV患者无论主动脉瓣和(或)升主动脉是否需要手术干预,都应积极监测主动脉内径变化及管壁功能,定期随访。形态学的改变往往滞后于功能衰退。本研究结果进一步证明VVI技术可以早期检出主动脉弹性降低这一亚临床血管病变,通过积极干预可阻止和延缓血管结构和功能的改变,从而降低心血管病事件的发生率,更有利于心血管疾病的预防。
本项研究不足之处:1)样本量不足;2)BAV患者二叶瓣融合方式不同(BAV不同表型)对升主动脉管壁造成的血流冲击影响就会不同,因而后期研究计划进一步加大样本量并将病例组依据瓣膜的不同表型分成亚组,应该会得出更有价值的结论。
综上所述,VVI技术测得的升主动脉应变参数与M型超声检测并计算的升主动脉弹性参数相关性良好,可以作为评价BAV患者升主动脉弹性的一种新技术,为临床早期提供升主动脉弹性损害的超声心动图参考依据。

