UV-LED/NaClO 工艺降解水中邻苯基苯酚的活性组分贡献和影响因素
赖成然, 李青松, 马晓雁, 李国新, 陈国元, 王吉苹 , 蔡力童
(1. 厦门理工学院 水资源环境研究所, 福建 厦门 361024;2. 浙江工业大学 土木工程学院, 浙江 杭州 310014;3. 厦门市水资源利用与保护重点实验室, 福建 厦门 361024)
1 前 言
水环境中药品和个人护理品(pharmaceuticals and personal care products,PPCPs)对人体健康的危害引起了广泛关注。据报道,水体中PPCPs 检出频次日益增多[1-3],因此有必要对其进行去除。研究表明O3氧化[4]、电化学氧化[5]、紫外协同TiO2(UV/TiO2)[6]、UV/H2O2[7]和UV/PS[8]等工艺可以有效去除水环境中PPCPs,其中UV/氯工艺被认为是处理受污染水(饮用水和再生水)的一个高效选择[9]。UV/NaClO 工艺可产生羟基自由基(HO·)、氯自由基(Cl·)、二氯自由基(Cl2-·)、氯氧自由基(ClO·)、氧自由基(O-·)及次氯酸根自由基(ClOH·)等多种氧化性自由基[10-11]。HO·可以无选择地降解有机污染物,而含氯自由基(RCS)则对于含芳香环和富电子结构的污染物具有选择性的去除。不同自由基(HO·、RCS)在UV/NaClO 工艺中的贡献取决于自由基的浓度和目标污染物的结构特性[12~15],因而自由基的浓度及其与目标物的反应速率常数是控制污染物去除效能的重要因素[16]。目前,关于UV/NaClO 工艺组分贡献的研究中自由基常被作为研究重点[17~18],但反应涉及自由基种类繁多,去除机理复杂,其中Cl·和ClO·由于缺少针对性的淬灭剂及探针物质,竞争动力学降解实验中常被简单归为RCS[19],导致其贡献难以准确评价。因此需要进一步研究Cl·和ClO·的浓度及其与目标污染物的反应速率常数,探明HO·、Cl·和ClO·等组分在UV/NaClO 工艺降解污染物过程中的贡献。
邻苯基苯酚(o-phenylphenol,OPP)是一种典型酚类PPCPs,常被添加于杀菌剂和防腐剂中,在地表水和污水污泥中均有检出[20]。OPP 具有一定的危害[21],2017 年被世界卫生组织列为致癌物[22]。紫外发光二极管(UV-LED)灯作为一种新兴的半导体技术逐渐成为基于UV 的高级氧化工艺中的紫外光源。相对于传统UV 灯,UV-LED 有独特的优势:(1) 安全无毒;(2) 灯珠寿命长,不易损坏;(3) 无需提前预热,安全可控。因此UV-LED 在水处理领域中有替换传统低压汞灯的潜力。
本研究以OPP 为目标污染物,采用紫外发光二极管(UV-LED)/NaClO 工艺对其去除进行研究。利用自由基淬灭剂和探针物质组合建立竞争动力学实验,确定了UV-LED/NaClO 工艺中HO·、Cl·和ClO·浓度及其与OPP 二级反应速率常数,对比了不同组分(UV-LED 光解、NaClO 氯化和自由基氧化等)对OPP去除的相对贡献,考察了NaClO 投加量和pH 值对OPP 降解过程中不同组分贡献的影响。以期为UV-LED/NaClO 工艺降解水环境中微量污染物提供理论支撑和基础数据。
2 实验(材料与方法)
2.1 实验试剂与仪器
OPP(德国 Dr.Ehrenstorfer 公司,质量分数w>99.9%);沙丁胺醇(salbutamol,SAL)(德国 Dr.Ehrenstorfer公司,w>99.8%);C2H7NO2、KH2PO4(HPLC 级,中国aladdin);乙腈(HPLC 级,德国Merck)、硝基苯(nitrobenzene,NB)、苯甲酸(benzoic acid,BA)、对二甲氧基苯(1,4-dimethoxybenzene,DMOB)、叔丁醇(tert-butanol,TBA)(HPLC 级,上海安谱);次氯酸钠(CP,活性氯质量分数≥5.2%);Na2S2O3·5H2O、K2HPO4·3H2O、NaHCO3、HCl 和NaOH 均为分析纯;实验室用水均为Mill-Q 超纯水(电阻≤18.2 MΩ)。
LC-20A 高效液相色谱仪(Shimadzu,日本);DZF-6050 真空干燥箱(上海精宏实验设备有限公司),纯水机(Milipore,美国),HJ-6A 型磁力恒温搅拌器(江苏金坛峥嵘仪器),pH 计(Eutevch,美国),UV-LED灯(深圳微紫科技有限公司,波长278 nm,单个100 mW)。
2.2 实验方法
实验于放置在磁力搅拌器上的石英筒管(300 mL)中进行,筒管中添加由磷酸盐缓冲液配制的OPP 溶液(浓度为3.0 μmol·L-1,pH=7.0±0.2)。考察初始pH 的影响时通过0.1 mol·L-1的HCl 或NaOH 调节溶液pH 为设定值。光源采用8 个UV-LED 小灯珠(光强为0.33 mW·cm-2)并联组成,内置于石英套管中。实验时先投加一定量的NaClO 溶液(1~7 mg·L-1),然后启动UV-LED 灯开始实验。设定时间取出3 mL 水样,经0.1 mol·L-1的Na2S2O3淬灭过膜后,采用HPLC 测定溶液中剩余OPP 浓度。所有条件下的反应均重复3 次,取平均值。
本研究采用自由基探针来确定自由基浓度和二级反应速率常数。由于UV-LED/H2O2工艺中仅生成HO·,因此采用NB 作为HO·的探针化合物,通过竞争动力学计算出HO·的浓度及其与OPP 的二级反应速率常数。在UV-LED/NaClO 工艺中,利用TBA 和NaHCO3组合淬灭HO·、Cl·、ClO·及Cl2-·,再加入SAL 排除CO3-·的影响,计算出ClO·与OPP 的二级反应速率常数。将计算出的二级反应速率常数代入含NB、BA、DMOB 的竞争动力学公式,可求得UV-LED/NaClO 工艺中HO·、Cl·和ClO·的稳态浓度及其与OPP 的二级反应速率常数。
2.3 分析方法
OPP、NB、SAL、BA 和DMOB 浓度采用HPLC 进行测定。检测波长为分别为254、262、223、230和225 nm。流动相是体积比为60:40 的乙腈和水(SAL 的水相为7.5 mmol·L-1的KH2PO4溶液,BA 的水相为0.02 mmol·L-1的C2H7NO2溶液),流速均为1.0 mL·min-1,柱温设定为40 ℃,进样量为10 μL。
3 结果与讨论
3.1 UV -LED、NaClO 和UV-LED/NaClO 对OPP 的去除
对比考察了UV-LED、NaClO和UV-LED/NaClO对OPP的去除,结果如图1 所示。cOPP,0为OPP 的初始浓度,cOPP,t为OPP 在t时刻的浓度,ρNaClO为NaClO 的质量浓度。

图1 OPP 在UV-LED、NaClO 和UV-LED/NaClO工艺中的降解动力学曲线Fig.1 OPP degradation kinetic curves under UV-LED irradiation, NaClO oxidation and UV-LED/NaClO processes cOPP,0=3 μmol·L-1, ρNaClO =3 mg·L-1, pH=7.0±0.2
实验反应900 s 后UV-LED 和NaClO 对OPP 的去除分别为56.6% 和61.3%,而同样时间内UV-LED/NaClO对OPP 的去除可达100%。拟合UV-LED 辐射、NaClO 氧化和UV-LED/NaClO 工艺的降解曲线,其拟一级动力学常数k分别为0.054 4、0.060 2 和0.275 2 min-1。联用工艺降解 OPP 的拟一级动力学常数分别为 UV-LED 和NaClO 的5 倍和4 倍,UV-LED/NaClO 工艺对OPP 的降解有协同作用。
UV-LED 对OPP 的去除原因可能是由于OPP 受UV-LED 照射后被直接光解。NaClO 通过氧化作用对OPP 也有明显的去除。UV-LED 与NaClO 联用显著提高了OPP 的去除,这是因为溶液中的HOCl/OCl-在UV-LED 的辐射下生成大量的HO·和RCS 等氧化性自由基[23-29],这些自由基可通过单电子氧化、脱H+、C─C 不饱和键加成等途径有效去除OPP[30-32],主要反应式为式(1)~(6)。Pan 等[24]、Xiong 等[33]采用UV/NaClO 降解甲硝哒唑和普萘诺尔时发现UV 与NaClO 有明显协同作用,与本研究结论类似。
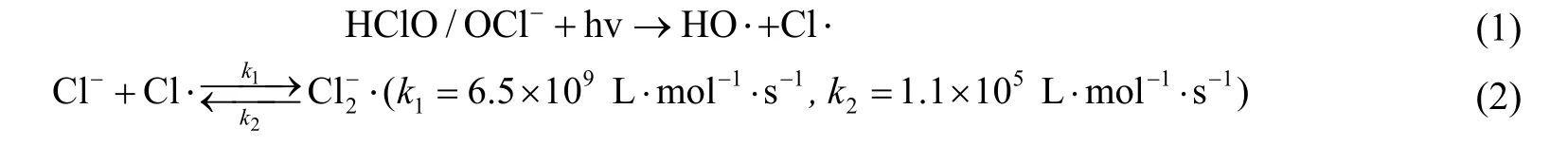

3.2 OPP 与自由基的二级反应速率常数
3.2.1 OPP 与HO·的二级反应速率常数
HO·、Cl·和ClO·等自由基对污染物去除有不同的贡献[32]。为了进一步探究HO·、Cl·及ClO·等自由基对OPP 去除贡献及其与OPP 的反应速率,采用竞争动力学模型对其进行研究。
NB 与HO·发生专一性反应(二级反应速率常数为3.9×109L·mol-1·s-1),H2O2在UV-LED 照射下仅产生HO·[25,34]。UV-LED/H2O2工艺对NB 和OPP 的降解如图2 所示。由图1、2 可知,单独UV-LED 对NB和OPP 的拟一级降解速率常数分别为0.005 2 和0.054 4 min-1,此外实验中发现单独H2O2无法去除NB和OPP。NB 和OPP 的去除则可用式(7)和(8)来表示。

式中:kNB和kOPP表示UV-LED/H2O2降解NB 和OPP 过程中的拟一级动力学常数;kUV-LED,NB和kUV-LED,OPP为UV-LED 降解NB 和OPP 的拟一级动力学常数;kHO·,NB和kHO·,OPP表示HO·与NB、OPP 的二级反应速率常数;cHO·,ss表示HO·在溶液中的稳态浓度。
由图2 可知,UV-LED/H2O2降解NB 和OPP 的拟一级动力学常数为0.035 4 及0.067 8 min-1。由式(7)和(8)计算出kHO·,OPP=1.86×109L·mol-1·s-1。OPP 为芳香环化合物,Lei 等[35]研究表明含芳香环结构的PPCPs与HO·速率常数为108~1010L·mol-1·s-1,实验中OPP 与HO·的反应速率与此范围相符。

图2 NB 和OPP 在UV-LED/H2O2 工艺中的降解动力学曲线Fig.2 Degradation kinetic curves of NB and OPP under UV-LED/H2O2 processes cOPP,0=3 μmol·L-1, cNB,0=3 μmol·L-1,ρH2O2=10 mg·L-1, pH=7.0±0.2
3.2.2 Cl·、ClO·与OPP 的二级反应速率常数
TBA 可与HO·、Cl·和ClO·反应,常用于测定AOPs 中RCS 的贡献[30-31]。NaHCO3能有效淬灭HO·、Cl·及Cl2-·。UV-LED/NaClO 工艺投加TBA 和NaHCO3可以淬灭相应自由基。但NaHCO3会消耗HO·和Cl·生成CO3-· (式(9)和(10))。

CO3-·是一种高选择性自由基(氧化还原电位E0=1.78 V),与含富电子基团的化合物及苯酚、苯胺等含芳香环结构的物质反应具有较高的反应速率[36-37]。实验中HCO3-可明显促进OPP 的降解,为排除CO3-·的影响,UV-LED/NaClO 工艺中添加TBA、NaHCO3、SAL 和OPP 进行竞争动力学实验,结果如图3 所示。SAL 与HO·、ClO·和CO3-·的二级反应速率常数kHO·,SAL=2.62×109L·mol-1·s-1、kClO·,SAL=1.21×108L·mol-1·s-1及kCO3-·,SAL=2.29×108L·mol-1·s-1[34-38]。UV-LED 和NaClO 降解SAL 的拟一级动力学常数为0.011 8 min-1。单独投加NaHCO3时,OPP 和SAL 的降解动力学可表示为式(11)和(12)。

图3 OPP 和SAL 在含TBA 和NaHCO3 的UV-LED/NaClO工艺中的降解动力学曲线Fig.3 Degradation kinetic curves of OPP and SAL under UV-LED/NaClO processes containing TBA and NaHCO3 cOPP,0=3 μmol·L-1, cSAL,0=3 μmol·L-1, ρNaClO=3 mg·L-1,cTBA=100 mmol·L-1, cNaHCO3=50 mmol·L-1, pH=7.0±0.2
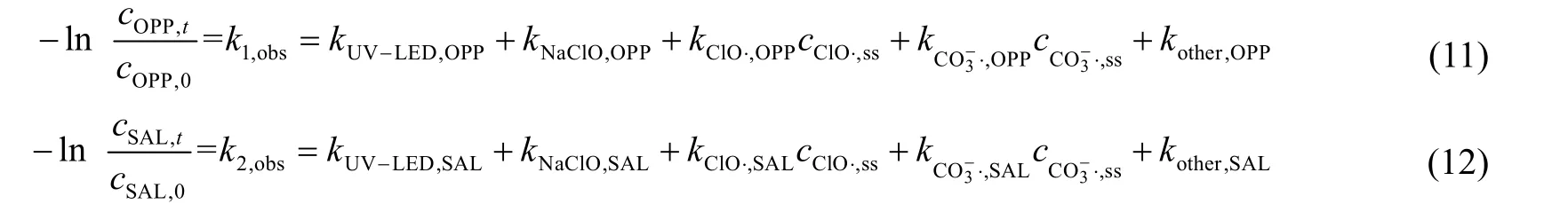
式中:kother,OPP和koher,SAL为其他未被淬灭的活性组分对OPP 和SAL去除的拟一级动力学速率常数;cClO·,ss和cCO3-·,ss为ClO·和CO3-·在溶液中的稳态浓度;kUV-LED,SAL和kUV-LED,OPP为单独UV-LED 降解SAL 和OPP的拟一级动力学常数;kNaClO,SAL和kNaClO,OPP表示单独NaClO 降解SAL 和OPP 的拟一级动力学常数。
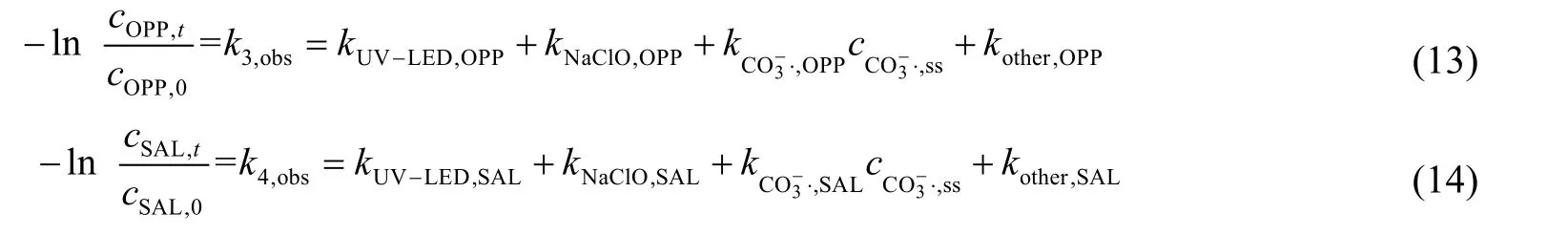
式中:k1,obs、k2,obs、k3,obs、k4,obs分别为SAL 和OPP 在不同条件下的拟一级动力学常数,分别为0.823 2、0.787 5、0.315 8 和0.501 4 min-1。通过式(11)~(14)则可推出式(15)和(16)

由式(15)和(16)可求出cClO·,ss=3.88×10-11mol·L-1,kClO·,OPP=2.18×108L·mol-1·s-1。Yang 等[39]采用竞争动力学计算出苯并噻唑和苯并三唑与ClO·的二级反应速率常数分别为2.22×108和2.40×108L·mol-1·s-1,其速率常数略大于本实验中的kClO·,OPP,但仍为同一数量级。
采用NB、BA 和DMOB 作为探针化合物,NB、BA 和DMOB 在UV-LED/NaClO 工艺中的去除如图4 所示。
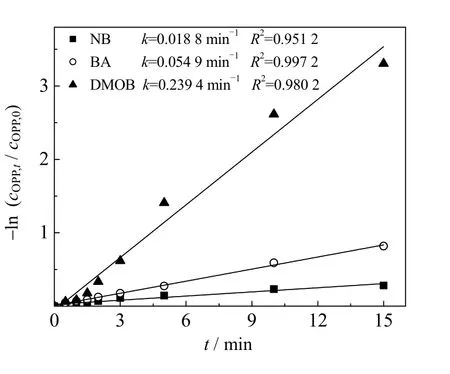
图4 NB、BA 和DMOB 在UV-LED/NaClO工艺中的降解动力学曲线Fig.4 Degradation kinetic curves of NB, BA and DMOB under UV-LED/NaClO processes cOPP,0=3 μmol·L-1, cNB,0=3 μmol·L-1,cBA,0=3 μmol·L-1, cDMOB,0=3 μmol·L-1,ρNaClO=3 mg·L-1, pH=7.0±0.2
DMOB 可以与HO·、Cl·和ClO·进行反应,其二级反应速率常数分别为7.0×109、1.8×1010及2.1×109L·mol-1·s-1,而BA 与ClO·不发生反应,其与HO·、Cl·的二级反应速率常数为5.9×109和1.8×1010L·mol-1·s-1[25]。单独UV-LED 和NaClO无法降解BA 和DMOB[25],其反应式如式(17)~(19)。

式中:kUV-LED,NB表示单独UV-LED 降解NB 的拟一级动力学常数;kHO·,NB表示NB 与HO·的二级反应速率常数;kHO·BA、kCl·,BA表示BA 与HO·、BA 与Cl·的二级反应速率常数;kHO·,DMOB、kCl·,DMOB、kClO·,DMOB表示DMOB 与HO·、DMOB 与Cl·、DMOB 与ClO·的二级反应速率常数。利用上式计算可得到UV-LED/NaClO 工艺中HO·、Cl·及ClO·的稳态浓度分别为1.22×10-13、1.08×10-14及1.38×10-12mol·L-1。
OPP 的去除可用式(20)表示:

式中:kUV-LED,OPP和kNaClO,OPP表示单独UV-LED 和单独NaClO 降解OPP 的拟一级动力学常数;kobs,OPP表示UV-LED/NaClO 降解OPP 的拟一级动力学常数;kother表示其他组分(Cl2-·、O-·、ClOH·和水合电子eaq等)对OPP 的降解贡献。TBA 对其他组分无淬灭效果,其贡献可用式(21)表示。

由式(20)和(21)计算得到kCl·,OPP=1.33×1011L·mol-1s-1。Cl·与OPP 反应速率最快,HO·次之,ClO·与OPP 的反应速率最小,由此可知增大Cl·的浓度可以提高OPP 的去除。研究表明卡马西平和氟康唑与Cl·的二级速率常数均大于其与HO·的速率常数[16,40],本实验具有类似的结论,这可能是因为3 种污染物皆属芳香环化合物,HO·和Cl·都能将其去除,但Cl·的选择性导致其与含芳香环的物质反应更快,因此3 种污染物去除过程中其与Cl·的二级反应速率常数大于HO·。
3.3 UV -LED/NaClO 降解OPP 过程中不同组分的贡献
基于上述实验中已确定HO·、Cl·和ClO·与OPP 的二级反应速率常数、自由基稳态浓度,kother的贡献值可通过式(21)计算得到。为了考察不同组分对OPP 降解的贡献,采用OPP、NB、BA 和DMOB 的混合竞争动力学模型对其进行研究,通过拟一级动力学常数确定降解过程中不同组分的相对贡献,可用式(20)表示,结果如图5 所示。NaClO、UV-LED、HO·、ClO·、Cl·和其他组分对OPP 降解的贡献率分别为22.17%、19.15%、5.01%、6.44%、31.13% 和16.1%。活性自由基(HO·、ClO·和Cl·)对OPP 的去除贡献占58.56%,贡献值HO·<ClO·<Cl·,其中Cl·贡献占自由基总贡献的53.16%,这可能是因为HO·与ClO·二级反应速率常数远小于Cl·,导致HO·与ClO·对OPP 的降解贡献仅为11.45%,低于单独Cl·贡献。

图5 UV-LED/NaClO 工艺中不同组分对OPP 降解的贡献Fig.5 Effects of different species on OPP degradation under UV-LED/NaClO processes cOPP,0=3 μmol·L-1, ρNaClO=3 mg·L-1,pH=7.0±0.2
RCS 与UV-LED 对OPP 降解起重要作用[41],其对OPP的降解贡献为56.72%,其中Cl·和UV-LED 的相对降解贡献占主要部分,这是因为一方面由于Cl·氧化还原电位高于ClO·[42],与OPP 反应速率高于HO·;另一方面OPP 摩尔吸光系数为4 620 L·mol-1·cm-1(紫外波长=278 nm),光量子产率φ为0.001 9(pH=7 时)[43],吸收UVC 后易被直接光解。这与Kong 等[44]采用UV/氯工艺降解丁二烯时发现UV 和RCS 相对贡献远大于HO·的结论类似。实际水体中由于天然有机物(NOM)和阴离子(Br-、NO2-和I-等)的存在,会抑制紫外/氯工艺中活性组分(HO·和RCS)的产生,降低OPP的去除[45]。
3.4 pH 与 NaClO 投加量对UV-LED/NaClO 工艺去除OPP 的影响
3.4.1 pH 对不同组分去除OPP 贡献的影响
pH 影响UV-LED/NaClO 工艺中活性基团的浓度和存在形式[46],因此考察了pH 对OPP 降解中各组分贡献的影响,结果如图6 所示。
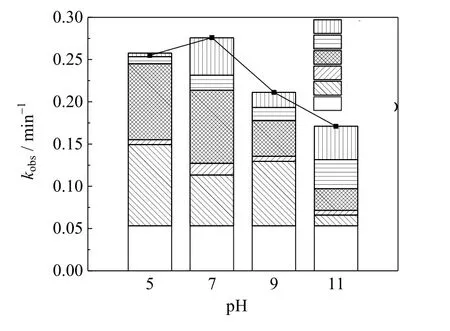
图6 pH 值对UV-LED/NaClO去除OPP 的影响Fig.6 Effects of pH on OPP degradation under UV-LED/NaClO processes cOPP,0=3 μmol·L-1, ρNaClO =3 mg·L-1,pH=7.0±0.2
不同pH 值时OPP 的降解均符合拟一级动力学模型(R2>0.97),当pH 值为5、7、9 和11 时,OPP 降解的拟一级动力学速率常数分别为0.255 0、0.275 2、0.211 2 和0.171 0 min-1,降解速率常数随pH 值的增大先增加后减少。中性时有利于OPP 的去除。实验中Cl·的贡献率随pH 值增加由35.29% 降到15.05%,而ClO·贡献率则从3.29% 增大至20.07%,HO·的贡献几乎不受pH 值的影响。这是因为一方面碱性溶液中OCl-浓度增大,而OCl-会与HO·及Cl·反应生成氧化电位较低的Cl2-·[46]。另一方面pH 增大使溶液中Cl·被H+以及低电位的eaq大量消耗,而少部分氯会因磁力搅拌作用形成Cl2挥发[44],导致溶液中Cl·浓度降低,与OPP 反应速率较低的ClO·取代Cl·成为OPP 降解的主要活性组分(式(5)、(22)和(23)),同时OPP 的量子产率随pH 升高而降低[41],因而碱性环境对OPP 的降解起抑制作用。中性环境下,溶液中的HOCl 浓度增大,与OCl-反应生成更多的HO·和Cl·,进而更有效地去除OPP。溶液呈酸性时,Cl·浓度增大,但eaq与H+以2.4×109L·mol-1·s-1的速率相互消耗[47],导致其他组分贡献显著减少,因此溶液在pH=5 时降解速率略低于pH=7 时。李博强等[48]在研究UV-LED/NaClO 去除AAP 时得到类似降解规律,AAP 在中性环境中降解效果最好。Kim 等[49]研究UV-LED/NaClO 工艺降解红霉素时,发现ClO·的贡献随着pH 的增加而增加,而Cl·贡献随着pH 的增加而减少,结论与本研究具有同样的结论。然而Kong 等[50]使用UV/NaClO 工艺降解吉非贝齐时发现HO·的贡献随pH 增大而增加,RCS 的贡献随pH 增大而减少。这可能是因为RCS 浓度增大时其高选择性导致对污染物去除效果增加不明显,从而使贡献减小,但本实验并未观察到这一现象。

3.4.2 NaClO 投加量对不同组分去除OPP 贡献的影响
氧化剂的投加量对AOPs 的去除污染物的性能有着重要的影响[51]。因此考察了NaClO 投加量对OPP去除的影响(见图7)。
由图7 可知,当NaClO 质量浓度为1、3、5 及7 mg·L-1时,OPP 降解的拟一级动力学常数为0.171 6、0.275 7、0.415 2 及0.637 2 min-1。同时,OPP 的降解速率常数与NaClO 的投加量呈线性关系(R2=0.998 5),UV-LED/NaClO 工艺中OPP 的降解速率常数随着NaClO 投加量增大而增大,这是因为HO·和RCS 的浓度随着NaClO 浓度增加而增多[25],NaClO 的氧化去除效果也因投加量增加而去除更多的OPP,这与Gao 等[52]研究UV-LED/NaClO 工艺降解碘帕醇时所得结论相同。

图7 NaClO 投加量对UV-LED/NaClO 下不同组分去除OPP 贡献的影响Fig.7 Effects of different species on OPP degradation under UV-LED/NaClO processes at different NaClO concentrations cOPP,0=3 μmol·L-1, pH=7.0±0.2
当NaClO 的质量浓度为1、3、5 及7 mg·L-1时,HO·对OPP 的降解贡献率分别为7.62%、5.01%、3.79% 及2.69%,Cl·对OPP 的降解贡献率为33.50%、31.13%、27.19% 及16.10%,ClO·对OPP的降解贡献率为5.87%、6.44%、8.63% 及17.04%。HO·、Cl·的相对贡献随NaClO浓度增高而减小,ClO·的相对贡献则随之增大。这是由于当NaClO 浓度增大时,溶液中HOCl/OCl-增多,加快与HO·和Cl·的反应生成大量ClO·,如式(3)~(6),导致HO·和Cl·浓度增幅变小,ClO·浓度增幅变大,因此其相对贡献也随之变化。Wu 等[53]采用UV/NaClO 降解CAF和NDA 时发现Cl·浓度增量会随着NaClO 投加量增加而减小,ClO·则会随之增大,结论与本实验类似。
4 结 论
(1) UV-LED/NaClO 工艺对OPP 的去除符合拟一级动力学(k=0.275 2 min-1),UV-LED/NaClO 工艺能有效去除OPP。
(2) Cl·与OPP 反应最快,HO·次之,ClO·与OPP 反应最慢。Cl·、HO·和ClO·与OPP 的二级反应速率常数分别为1.86×109、1.33×1011和2.18×108L·mol-1·s-1,其稳态浓度分别为1.22×10-13、1.08×10-14及1.38×10-12mol·L-1。
(3) UV-LED/NaClO 工艺降解OPP 过程中,不同组分贡献依次为:Cl·>NaClO>UV-LED>其他组分>HO·>ClO·,自由基是主要贡献组分,占总体贡献53.16%。
(4) 中性环境能够促进UV-LED/ NaClO 工艺中OPP 降解。酸性和中性环境中Cl·对OPP 的降解起主要作用,而碱性环境中ClO·起主要作用。OPP 降解速率常数和ClO·的贡献率随NaClO 投加量的增大而增大,而HO·和Cl·的贡献率则随NaClO 投加量的增大而减小。

