ER+/HER2-乳腺癌多基因阵列检测应用:ASCO指南解读与瑞金医院临床实践
舒 兰,陈小松
(上海交通大学医学院附属瑞金医院外科 乳腺疾病诊治中心,上海 200025)
雌激素受体(estrogen receptor,ER)阳性/人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)阴性乳腺癌在内分泌治疗基础上,是否需辅助化疗,存在较大争议。既往研究发现,基于多基因阵列表达谱,如21基因复发分数(recurrence score,RS)和 70 基因预后分型,较常规临床病理指标,更好地预测ER+/HER2-乳腺癌的预后和化疗获益[1]。美国临床肿瘤协会(American Society of Clinical Oncology,ASCO)从2016年开始针对ER+/HER2-早期乳腺癌分子标志物和术后辅助治疗的合理选择制定指南,并分别在2017年、2019年和2022年3次更新[2-5]。同时,对于具体的乳腺癌病人,需结合其常规临床病理指标、多基因阵列检测结果、年龄和个人意愿等,综合判别,制定合适的辅助治疗方案。本文就多基因阵列在ER+/HER2-乳腺癌应用的系列ASCO指南,并结合瑞金医院实际临床应用经验,作一解读和评述。
多基因阵列表达谱在ER+/HER2-乳腺癌病人中的应用
ER+/HER2-乳腺癌病人,目前报道的多基因阵列表达谱主要包括21基因RS、70基因预后分型、PAM50 ROR、EndoPredict 和乳腺癌指数(breast cancer index,BCI)等[6],其中针对 21 基因 RS 和 70基因预后分型已开展前瞻性临床研究,并获得Ⅰ级循证医学证据。故本文主要讨论21基因RS和70基因预后分型在ER+/HER2-乳腺癌中的应用。
21基因RS是根据NSABP B20、RUSH大学医学中心和Providence St.Josephs医院的三项研究[7],采用cDNA微阵列进行多基因检测,筛选获得21基因(16个癌基因以及5个参考基因)。根据其表达计算相应得分(0~100 分),并划分为低危(<18 分)、中危(18~30分)和高危(>30分)。在 NSABP B14 和B20两项研究只接受单纯内分泌治疗的病人中,验证其对预后的预测。NSABP B20研究进一步证实21基因RS可预测辅助化疗的获益。低危病人只需单纯内分泌治疗,而高危病人可从化疗中获益[8]。2005年,美国食品药品监督管理局(FDA)批准21基因RS用于ER+/HER2-、淋巴结阴性乳腺癌病人的临床应用。同期开展的前瞻性临床研究TAILORx[9],入组ER+/HER2-、淋巴结阴性乳腺癌病人,验证21基因RS对预后和辅助化疗疗效的预测价值。低危(<11分)病人单独接受内分泌治疗;高危(>25分)病人接受内分泌治疗+化疗;中危(11~25分)病人,随机接受内分泌治疗或内分泌治疗+化疗。需说明的是,TAILORx研究选用11分和25分作为21基因RS危险度分级的界定值,依据其10年无远处转移生存率(distant metastasis free survival,DMFS)为10%和20%对应RS数值95%可信区间(confidence interval,CI)的下限值,而原先选定的18分和30分界定值则直接对应10年DMFS为10%和20%的RS数值。
70基因预后分型是荷兰癌症研究所利用cDNA微阵列技术,在117例腋窝淋巴结阴性、年龄<55岁乳腺癌病人中,检测发现70个基因与病人预后相关。之后在独立的295例Ⅰ/Ⅱ期乳腺癌病人中,验证其可预测预后[8]。2007年,美国FDA批准70基因预后分型用于早期乳腺癌的检测。同期开展的前瞻性MINDACT临床研究[10],对于入组的病人(包括ER-、HER2+和淋巴结阳性),首先根据临床病理指标(T、N、组织学分级)(见表1)分为临床风险(C)高危和C低危,之后再根据70基因预后分型(G)结果,将病人分为G高危和G低危。C/G均低危的病人,则接受单纯内分泌治疗;C/G均高危的病人,则推荐内分泌治疗+化疗;C/G不符合(C高危/G低危或C低危/G高危)的病人,随机接受内分泌治疗或内分泌治疗+化疗。MINDACT的主要研究终点指标为C高危/G低危病人,如不接受辅助化疗,其5年DMFS的95%CI下限>92%。70基因预后分型最初需使用新鲜标本检测,限制其临床推广应用。技术改良更新后,其亦可用石蜡包埋的标本进行检测[11],该更新方案在2015年被美国FDA批准。
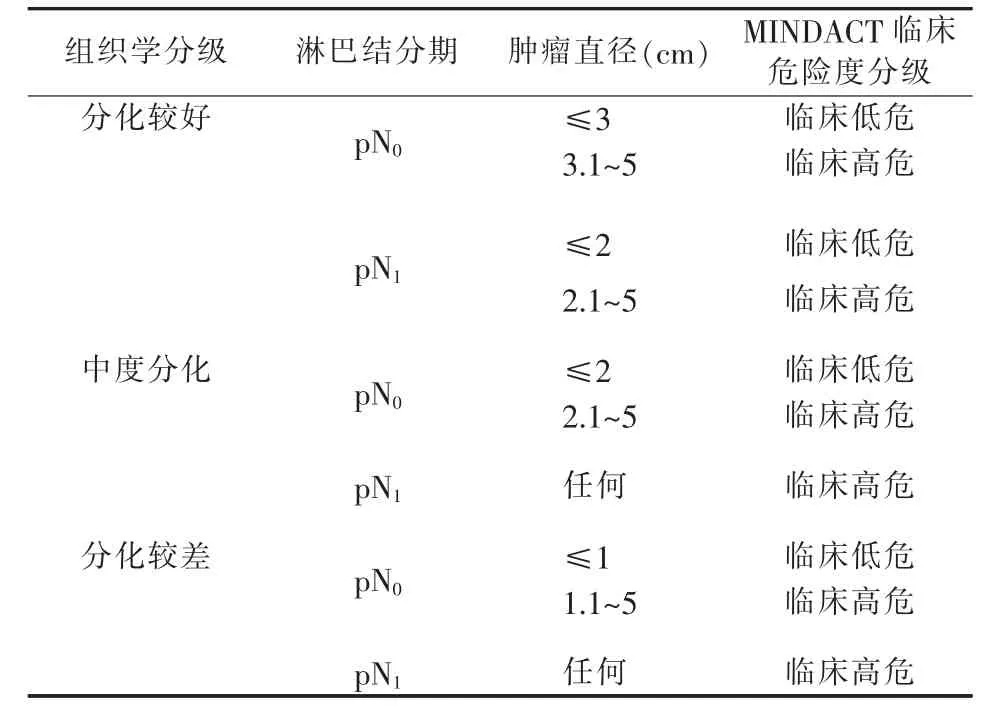
表1 乳腺癌临床危险分级
ASCO早期乳腺癌标志物与辅助治疗指南更新与实践:21基因RS
TAILORx从2006年开始入组,2010年截止,共纳入10 253例病人。2015年首次报道了TAOLORx研究低危病人的随访结果,发现其单独接受内分泌治疗,5年DMFS为99.3%。提示对于21基因RS低危的病人,可安全豁免化疗[12]。2016年ASCO早期乳腺癌分子标志物与术后辅助治疗决策的指南,对于ER+/HER2-、淋巴结阴性的乳腺癌病人,推荐21基因RS检测(证据级别:高;推荐强度:强)。笔者中心从2014年探索基于逆转录聚合酶链反应技术检测的21基因RS在临床应用,并在大型队列中验证,其能独立预测预后。相应检测平台对ER和PR检测的结果与免疫组织化学结果的符合率分别为98.7%和87.8%,与既往NSABP B14研究报道的数据[13]相似。故从2014年起,笔者中心对于肿瘤直径>1 cm或T1b期、组织学2~3级的ER+/HER2-、淋巴结阴性的病人,常规推荐21基因RS检测,帮助制定术后辅助治疗方案。
在2018年,TAILORx更新并公布了RS中危病人接受辅助化疗疗效的数据。在所有人群中,内分泌治疗+化疗对比内分泌治疗,并不改善预后。进一步分析发现RS分值、年龄与化疗获益存在交互作用。年龄>50岁的病人,化疗不改善预后;但年龄≤50岁、RS为16~25分的病人,化疗可改善预后;而年龄≤50岁但RS为11~15分的病人,则不能从化疗中获益[9]。2019年ASCO基于TAILORx的8年随访结果,更新了早期乳腺癌分子标志物与辅助治疗的指南推荐,在ER+/HER2-、淋巴结阴性的病人中[4]:①年龄>50岁且RS为11~25分,或年龄≤50岁且RS为11~15分,辅助化疗获益较少,可使用单独内分泌治疗(证据级别:高;推荐强度:强);②年龄≤50岁且RS为16~25分,可考虑内分泌治疗+化疗(证据级别:中;推荐强度:中);③RS为26~30分,无论年龄大小,可考虑内分泌治疗+化疗(证据质量:不足;推荐强度:中);④RS≥31分,则推荐辅助化疗(证据质量:高;推荐强度:强)。
基于TAILORx研究结果和ASCO指南的更新,是否仅凭21基因RS和年龄,就可以决策辅助化疗?答案是否定的!对于RS为26~30分的病人,根据TAILORx临床研究设计,均需辅助化疗;但年龄>50岁,特别是老年乳腺癌病人,是否同样需要化疗?笔者中心对于RS为26~30分的ER+/HER2-、淋巴结阴性的病人,在21基因RS检测前后均进行多学科团队(multi-disciplinary team,MDT)讨论,发现只有70%的病人最终推荐辅助化疗。影响其推荐的独立因素包括年龄和分子分型状态。年龄≤50岁和Luminal B型的病人更多推荐辅助化疗[14]。对于预后较好的黏液癌、浸润性乳头状癌等特殊类型乳腺癌病人,ASCO指南推荐是否仍合适?笔者中心分析了1 736例ER+/HER2-乳腺癌病人,在接受21基因RS检测前后进行MDT讨论,发现21基因RS分值显著影响浸润性导管癌和浸润性小叶癌病人的辅助化疗决策,但并不影响其他特殊类型乳腺癌病人辅助化疗决策,需待进一步研究证实[15]。最后对于年龄≤50岁、RS为16~25分的病人,辅助化疗的获益是否来自化疗诱导的闭经?对于这部分病人,特别是无其他临床高危因素的情况下,是否可采用卵巢功能抑制+内分泌治疗来替代化疗?笔者认为可与病人充分沟通化疗的绝对获益以及不良反应,再根据病人的意愿、年龄以及临床复发风险等,选择辅助化疗或卵巢功能抑制+内分泌治疗[6](见图1)。
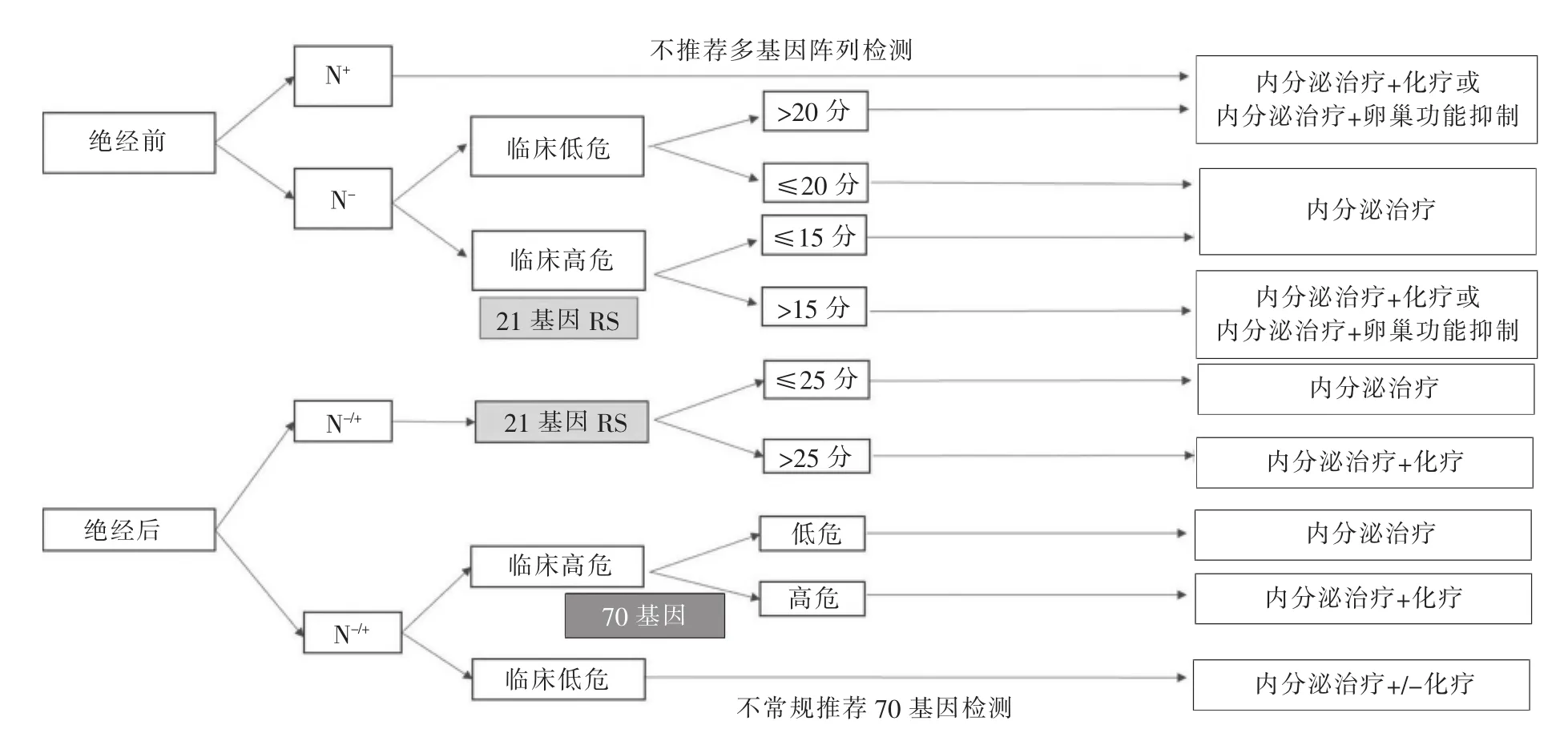
图1 多基因阵列在ER+/HER2-乳腺癌的应用:瑞金医院临床诊疗流程
2019年ASCO会议更新了TAILORx中危组病人根据临床风险以及年龄、RS分值预测辅助化疗获益的结果,发现对于临床低危、年龄≤50岁且RS为16~20分的病人,辅助化疗获益较少,可考虑单独内分泌治疗[16]。2019年欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)会议公布了TAILORx研究中RS≥26分队列病人的预后,其中43%的病人RS为26~30分,全组有6%的病人实际未接受辅助化疗,未接受化疗病人的预后显著差于接受化疗的病人,提示RS为26~100分的病人可从辅助化疗中获益[17]。RS为26~30分的病人中,虽然不是随机接受化疗或不化疗,但发现未接受化疗病人的5年和9年DMFS分别为89.6%和80.6%,低于接受化疗病人的94.6%和88.5%,提示在内分泌治疗基础上,可考虑推荐辅助化疗[17]。2022年ASCO更新了早期乳腺癌分子标志物与辅助治疗的指南中,对于ER+/HER2-、淋巴结阴性的病人,并未根据临床风险进行21基因RS检测的额外推荐,与2019年的指南保持一致。可能与临床风险分析的数据是非计划的亚组分析而该组人群较少有关[5]。但在临床实践中,需综合考虑月经状态、临床风险和RS分值,推荐合理的辅助治疗方案(见图1)。
对于淋巴结阳性的病人,21基因RS是否可指导辅助化疗的选择?前瞻性RxPONDER临床研究是针对淋巴结N1期、ER+/HER2-且21基因RS分值≤25分的病人,随机接受内分泌治疗或内分泌治疗+化疗。2020年圣安东尼奥乳腺癌研讨会(San Antonio Breast Cancer Symposium,SABCS)公布了中位5.3年的随访结果,发现两组病人预后差异无统计学意义,同时21基因RS分值的高低也不能预测辅助化疗的获益。进一步分析发现病人的月经状态与辅助化疗的获益相关。在绝经后病人中,辅助化疗不提高其预后 [无浸润性癌生存率(invasive disease free survival,iDFS)绝对获益为-0.6%];对于绝经前病人,辅助化疗可显著提高病人预后(iDFS绝对获益为4.9%)[18]。基于这项研究,2022年ASCO更新的早期乳腺癌分子标志物与辅助治疗指南,对于ER+/HER2-和淋巴结阳性的病人进行了下述推荐。①对于N1期病人,如病人为绝经后,则推荐21基因RS检测,以帮助辅助化疗决策(证据质量:高;推荐强度:强),但对于绝经前病人,则不应推荐21基因RS检测(证据质量:高;推荐强度:中);②对于RS≥26分的病人,需推荐辅助化疗(证据质量:高;推荐强度:强);③在N2~3期的病人中,缺乏21基因RS使用的前瞻性研究数据,临床上不推荐使用(证据质量:不足;推荐强度:中)[5]。笔者中心在RxPONDER研究结果公布前,分析发现影响ER+/HER2-、淋巴结阳性病人辅助化疗的独立因素包括年龄、并发症以及21基因RS,年龄>50岁、并发症≥2个以及RS为低危的病人,更少推荐辅助化疗[19]。在RxPONDER研究结果公布后,对于N1期病人,更多参考其结果,绝经前病人不常规推荐21基因RS检测;而对于绝经后21基因RS≤25分的病人,一般不推荐辅助化疗。但考虑到RxPONDER研究入组病人中,3枚淋巴结转移(9.1%)和组织学3级(11.3%)的较少,在上述人群中检测21基因RS指导辅助化疗的选择需慎重[18]。
ASCO早期乳腺癌标志物与辅助治疗指南更新与实践:70基因预后分型
2016年公布了MINDACT研究5年随访结果,发现对于C高危/G低危病人,不接受辅助化疗的5年 DMFS为 94.7%(95%CI 92.%~96.2%),超过预设的92%,提示可根据临床风险和70基因预后分型检测结果,指导术后辅助化疗的选择[10]。故2017年ASCO指南推荐在临床高危、ER+/HER2-且淋巴结阴性(证据级别:高;推荐强度:强)或N1期(证据级别:高;推荐强度:中)的病人中,可考虑70基因预后分型检测(证据级别:高;推荐强度:强);但对于淋巴结转移>1枚的N1期病人,应用70基因预后分型需谨慎;而对于临床低危的病人,则不推荐70基因预后分型检测(证据级别:高;推荐强度:强)[3]。MINDACT虽然入组了ER-或HER2+等病人,但目前尚不推荐70基因预后分型检测,主要原因如下:①MINDACT入组的ER-或三阴性乳腺癌病人,G低危比例低。ER-病人只有4.2%为G低危,88.4%三阴性病人为G和C均高危。②对于HER2+乳腺癌,目前已有较明确的分层治疗选择,特别是抗HER2靶向药物治疗。针对这部分病人,豁免化疗缺乏高等级循证医学证据。③对于淋巴结转移2~3枚病人应用70基因预后分型需谨慎,淋巴结转移1枚病人的预后可能好于转移2~3枚的病人,且其在MINDACT研究中入组较少,只占所有人群的6.9%。
MINDACT研究在2020年ASCO会议上更新了8年的随访结果。同样对于C高危/G低危组病人,未化疗病人的5年DMFS为 95.1%(95%CI 93.1%~96.6%),提示70基因预后分型可指导化疗的选择。但在HR+/HER2-、C高危/G低危组病人中,辅助化疗可提高2.6%绝对DMFS。根据年龄分析发现,在年龄≤50岁的病人中,辅助化疗DMFS改善的绝对值为5.0%;>50岁的病人,其绝对获益只有0.2%。该结果提示,对于C高危但年龄≤50岁的病人,即使70基因预后分型为低危,仍需考虑辅助化疗,因此不常规推荐其检测[20]。2022年更新的ASCO指南,对于临床高危、年龄>50岁、HR+/HER2-且淋巴结N0~1期的病人,推荐70基因预后分型指导后续辅助治疗(证据质量:中;推荐强度:强);而对于年龄≤50岁、临床高危的病人,不推荐70基因预后分型检测(证据质量:高;推荐强度:强);对于临床低危的病人,无论年龄或淋巴结状态,不推荐70基因预后分型检测(证据质量:中;推荐强度:中)[5]。由于70基因预后分型在国内于2019年才上市,笔者中心临床应用相对于21基因RS检测较少。对于HR+/HER2-且淋巴结N0~1期者,可考虑在临床高危的绝经后病人、多形性浸润性小叶癌等特殊类型乳腺癌或21基因RS检测为中危的绝经前病人中应用[21]。
在 ER+/HER2-、N0~1期乳腺癌病人中,21 基因RS和70基因预后分型均在回顾性和前瞻性临床研究中,验证其可预测病人的预后以及辅助化疗的获益,目前已获批在上述病人中应用且被ASCO等指南所推荐。在临床实践中,需整合上述多基因阵列的最新循证医学证据,考虑每例病人具体的临床风险、基因风险、年龄、并发症、治疗反应以及病人意愿等因素,制定适合每个中心实际情况的临床诊疗常规,从而为ER+/HER2-乳腺癌病人制定个体化辅助治疗方案。

