曲妥珠单抗联合常规化疗对HER2阳性晚期乳腺癌患者外周血T淋巴细胞亚群及生存率的影响
吴景艳,谢菲菲
1河南科技大学第一附属医院临床试验病房,洛阳 471000;2焦作市第二人民医院妇产科,焦作 454150
乳腺癌是多发于中老年女性群体的恶性肿瘤之一,约占女性全部恶性肿瘤的10%,居女性恶性肿瘤发病率首位[1]。多数患者早期无典型症状,首次确诊时已为晚期,从而失去手术根治的最佳时机,临床多以化疗为主要治疗手段[2],常用化疗方案为吉西他滨(gemcitabine,GEM)联合卡培他滨(capecitabiue,CAP),但该方案不良反应发生风险高,且成本较高[3-4]。随着乳腺癌生物学水平研究的不断深入,分子靶向治疗因可直接作用于肿瘤细胞的特定位点、对正常细胞的损伤较小而为临床治疗乳腺癌提供了新的治疗选择[5-6]。曲妥珠单抗是治疗HER2阳性乳腺癌的1代单克隆抗体,可靶向作用于HER2而灭杀肿瘤细胞[7]。基于此,本研究拟探究曲妥珠单抗联合常规化疗对HER2阳性晚期乳腺癌患者的疗效,现报道如下。
1 资料与方法
1.1 一般资料
选取2017年3月~2019年3月本院收治的78例晚期乳腺癌患者为研究对象,依据随机数字表法分为对照组和观察组,每组39例。对照组:年龄43~66岁,平均年龄(54.51±5.86)岁;病程 1~4年,平均病程(3.06±0.64)年;肿瘤转移( tumor node metastasis,TNM)分期:Ⅲ期24例,Ⅳ期15例。观察组:年龄40~69岁,平均年龄(53.81±7.75)岁;病程1~5年,平均病程(3.19±0.77)年;TNM分期:Ⅲ期28例,Ⅳ期11例。两组一般资料比较无统计学差异(P>0.05),具有可比性。本研究经本院医学伦理委员会批准(伦理批号:hnfsyy20170158),患者或家属均签署知情同意书。
纳入标准:①符合《中国抗癌协会乳腺癌诊治指南与规范》(2015版)[8]相关诊断标准,确诊为乳腺癌者。②TNM分期为Ⅲ~Ⅳ期者。③HER2阳性者。④女性,年龄为40~70岁者。
排除标准:①合并心、肝、肾脏器功能严重障碍者。②患血液系统或免疫系统疾病者。③对研究药物过敏者。④同时接受其他研究试验者。⑤预计生存期少于6个月者。⑥依从性较差、中途退出研究者。
1.2 治疗方法
对照组给予GEM联合CAP治疗:注射用盐酸吉西他滨[连云港杰瑞药业有限公司,国药准字H20123362,规格0.2g(按C9H11F2N3O4计)]静脉滴注,剂量为1000mg/m2,于第1天、第8天用药;第1天、第14天给予卡培他滨片(江苏恒瑞医药股份有限公司,国药准字H20133365,规格0.5g)口服,剂量为2000mg/m2。21天为1个治疗周期,共治疗2个周期。
观察组在对照组治疗基础上加用注射用曲妥珠单抗(上海复宏汉霖生物医药有限公司,国药准字S20200019,规格150mg/瓶),静脉滴注,首次治疗剂量为8mg/kg,第2次治疗降低剂量为6mg/kg,后期保持此剂量直至治疗结束,每周治疗1次,共治疗 2 个月[7]。
1.3 观察指标
①T淋巴细胞亚群。于治疗前后采集患者空腹静脉血5ml,采用DT5-3低速台式离心机(河北医众医疗器械有限公司,d=10cm)以2500r/min离心10min,分离上清液置于-80℃条件下保存。采用FACSCalibur流式细胞分析仪(美国BD公司)测定CD3+、CD4+、CD8+、CD4+/CD8+水平。②肿瘤标记物。取上述分离血清,运用酶联免疫吸附法测定血清中癌相关糖蛋白抗原(cancer-associated glycoprotein antigen,CA153)、组织多肽特异性抗原(tissue polypeptide specific antigen,TPS)、癌胚抗原(carcinoembryonic antigen,CEA)水平。③临床疗效。治疗结束后采用《实体瘤疗效评价标准》(1.1版)[9]评估两组疾病控制率。其中,肿瘤完全消失为完全缓解,肿瘤体积缩小50%及以上为部分缓解,肿瘤体积缩小50%以下或增加25%以下为稳定,肿瘤体积增加25%及以上或出现新病灶为进展。疾病控制率=(完全缓解+部分缓解)例数/总例数×100%。④生存率。随访3年,截止时间为2022年3月31日,记录所有患者的生存情况。⑤不良反应发生情况。观察两组治疗期间出现的不良反应,包括恶心呕吐、贫血、肝功能异常、心脏毒性等。
1.4 统计学方法
2 结果
2.1 T淋巴细胞亚群
治疗前,两组CD3+、CD4+、CD8+、CD4+/CD8+等T淋巴细胞亚群水平比较无统计学差异(P>0.05);治疗后,两组CD8+水平无明显变化(P>0.05),CD3+、CD4+、CD4+/CD8+均降低,但观察组高于对照组(P<0.05)。见表1。
表1 两组T淋巴细胞亚群水平比较 n=39, x±s
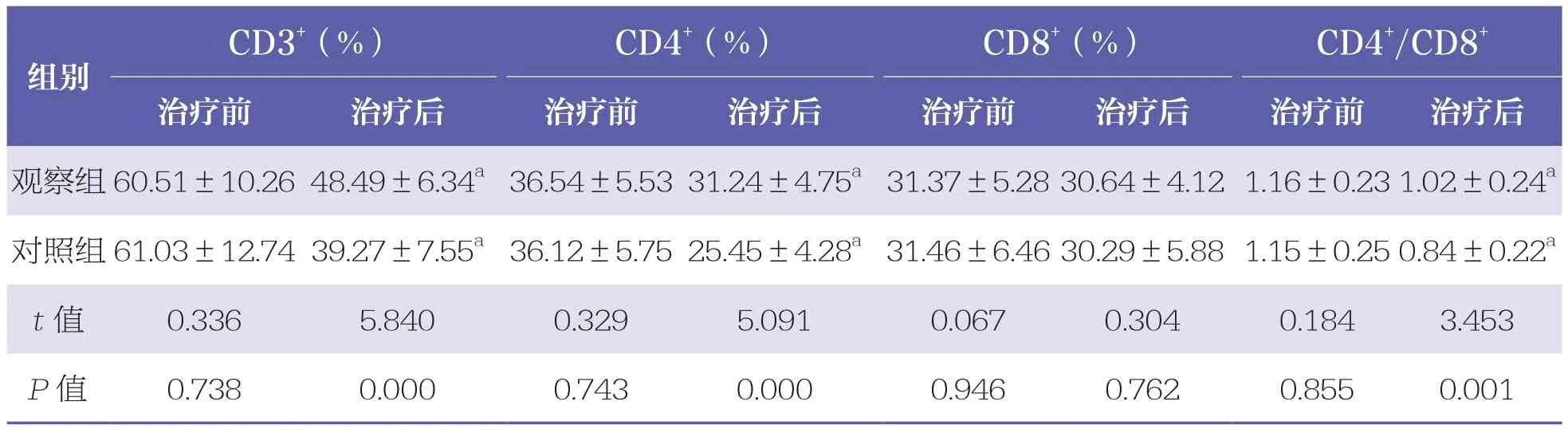
表1 两组T淋巴细胞亚群水平比较 n=39, x±s
与同组治疗前比较,a:P<0.05。下同
CD3+(%) CD4+(%) CD8+(%) CD4+/CD8+治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组60.51±10.26 48.49±6.34a36.54±5.53 31.24±4.75a31.37±5.28 30.64±4.12 1.16±0.23 1.02±0.24a对照组61.03±12.74 39.27±7.55a36.12±5.75 25.45±4.28a31.46±6.46 30.29±5.88 1.15±0.25 0.84±0.22a t值 0.336 5.840 0.329 5.091 0.067 0.304 0.184 3.453 P值 0.738 0.000 0.743 0.000 0.946 0.762 0.855 0.001组别
2.3 肿瘤标记物
治疗前,两组CA153、TPS、CEA水平比较无统计学差异(P>0.05);治疗后,两组CA153、TPS、CEA水平均降低,且观察组低于对照组(P<0.05)。见表2。
表2 两组肿瘤标记物水平比较 n=39, x±s
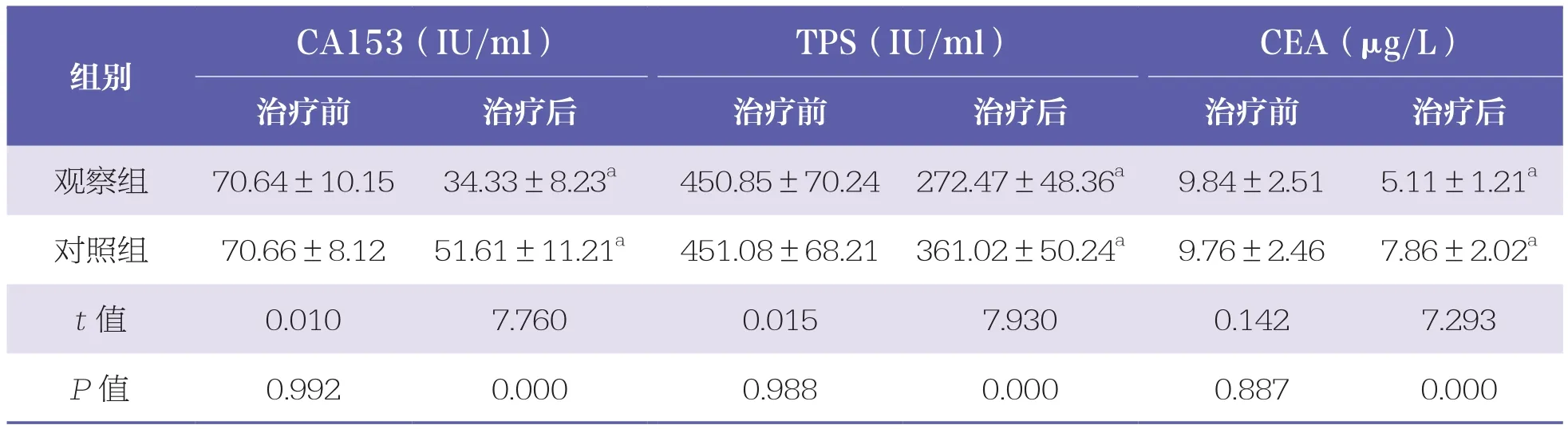
表2 两组肿瘤标记物水平比较 n=39, x±s
CA153(IU/ml) TPS(IU/ml) CEA(μg/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 70.64±10.15 34.33±8.23a 450.85±70.24 272.47±48.36a 9.84±2.51 5.11±1.21a对照组 70.66±8.12 51.61±11.21a 451.08±68.21 361.02±50.24a 9.76±2.46 7.86±2.02a t值 0.010 7.760 0.015 7.930 0.142 7.293 P值 0.992 0.000 0.988 0.000 0.887 0.000组别
2.4 临床疗效
观察组的疾病控制率(89.74%)高于对照组(69.23%,χ2=5.032,P<0.05)。见表3。
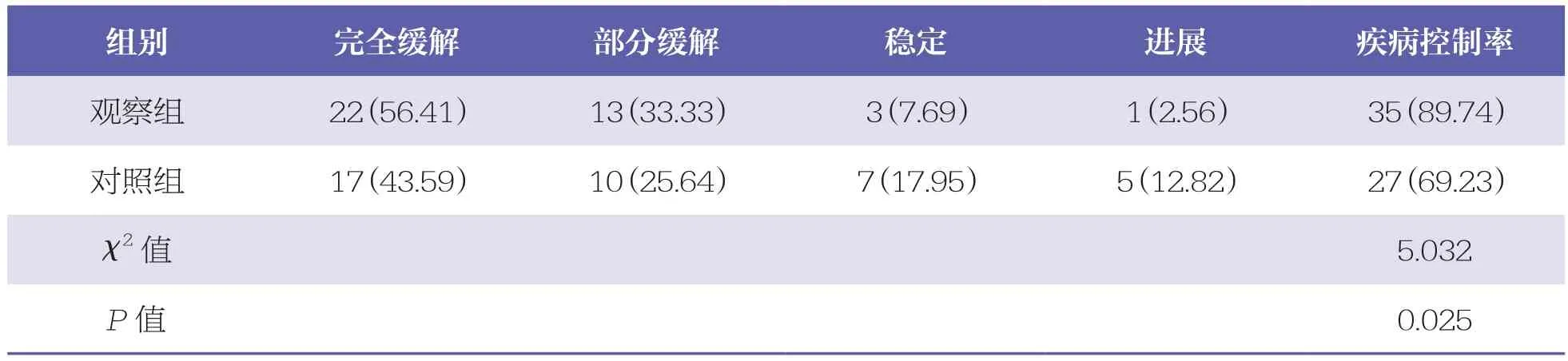
表3 两组临床疗效比较 n=39,n(%)
2.5 生存率
观察组的1年、2年、3年生存率均高于对照组(P<0.05)。见表4。
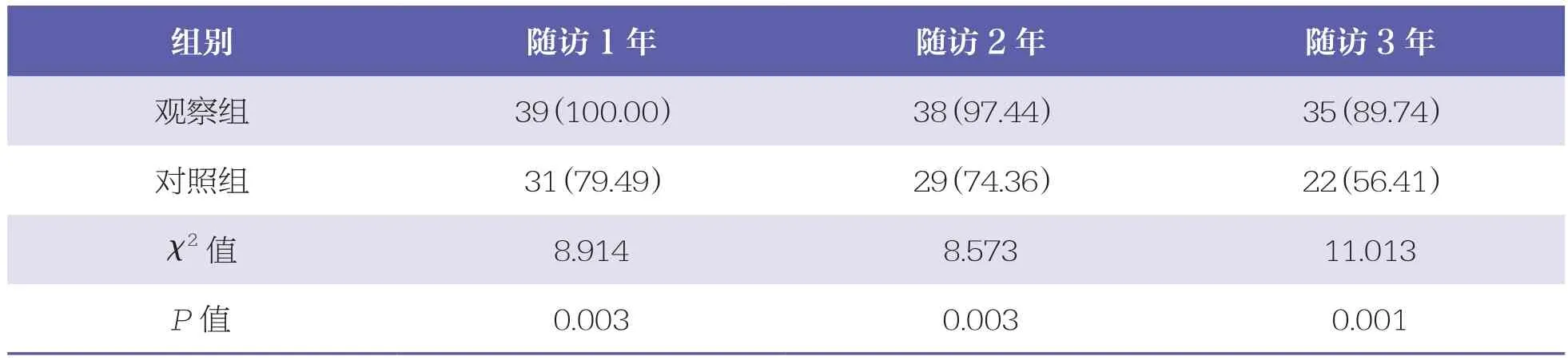
表4 两组生存率比较 n=39,n(%)
2.6 不良反应发生率
治疗期间,两组均发生恶心呕吐、贫血、肝功能异常、心脏毒性等不良反应,但两组比较无统计学差异(P>0.05),且经对症处理后均缓解。见表5。
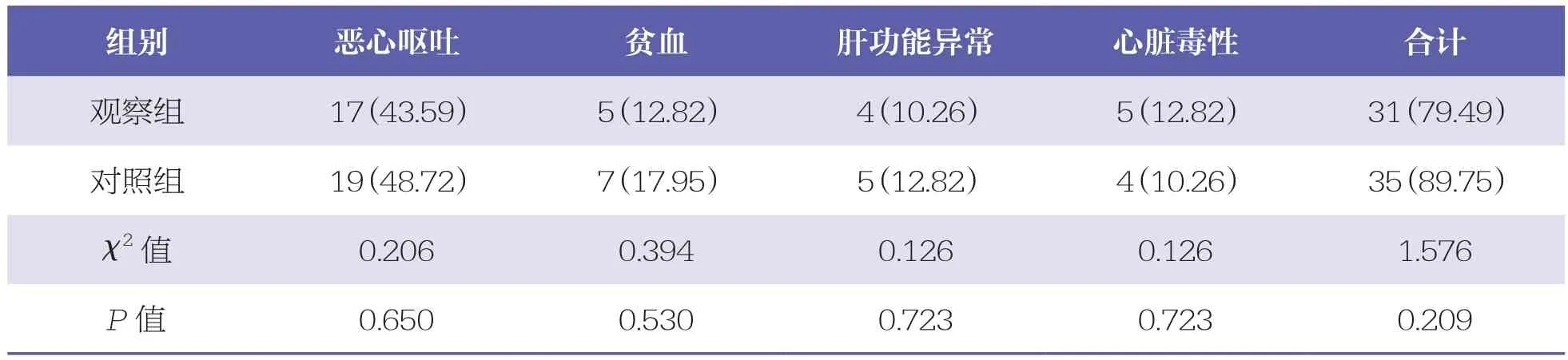
表5 两组不良反应发生率比较 n=39,n(%)
3 讨论
晚期乳腺癌通常具有恶性程度高、进展速度快、病死率较高等特点。对于HER2阳性晚期乳腺癌患者,其肿瘤增殖率、转移率、病死率更高,因此受到临床高度重视[10-11]。现阶段,多种化疗方案对乳腺癌肿瘤细胞均具有较强的杀伤力,可延长晚期乳腺癌患者的生存期,但化疗通常是全身性的,且在杀死肿瘤细胞的同时会对机体正常细胞造成不同程度损伤,导致机体免疫功能下降,影响疗效及生存率[12-13]。因此,临床开始倾向于结合靶向药物治疗以减轻化疗对机体免疫功能的损伤。曲妥珠单抗对HER2具有较高的靶向性,已成为治疗乳腺癌的首选靶向药物。已有多项研究证实,曲妥珠单抗可有效延长HER2阳性乳腺癌患者的生存期,减轻不良反应[14];曲妥珠单抗术前辅助治疗可有效改善HER2阳性乳腺癌患者的病灶组织相关指标、减少术后肿瘤复发转移[15]。但关于曲妥珠单抗联合GEM、CAP化疗对乳腺癌患者的效果及安全性如何,尚缺乏研究考察。
本研究考察了曲妥珠单抗联合GEM、CAP化疗对晚期乳腺癌患者T淋巴细胞亚群、生存率及安全性的影响。研究结果显示,治疗后两组CD3+、CD4+、CD4+/CD8+水平均降低,但观察组各指标水平高于对照组,提示化疗可影响患者免疫功能,但曲妥珠单抗可减轻这种影响,与文献报道一致[16]。分析原因可能是曲妥珠单抗可靶向结合HER2而灭杀肿瘤细胞,而对HER2以外的组织细胞损伤较少,因此对免疫功能的影响较小。肿瘤标记物是肿瘤细胞发生、发展、浸润、转移过程中分泌的活性物质,其水平异常升高能够反映肿瘤的进展。CA153、TPS、CEA是临床判断乳腺癌肿瘤细胞增殖活性、临床疗效及预后的常用指标。本研究中,治疗后两组CA153、TPS、CEA水平均降低,且观察组低于对照组,而疾病控制率及1年、2年、3年生存率均高于对照组,表明曲妥珠单抗联合常规化疗方案疗效较佳,可有效降低肿瘤标记物水平、提高患者生存率、改善预后,与既往研究结果一致[17],有较高的临床价值。此外,两组均发生恶心呕吐、贫血、肝功能异常、心脏毒性等不良反应,但两组比较无统计学差异,且经对症处理后均缓解,表明在常规化疗方案基础上应用曲妥珠单抗安全性较高。
综上所述,在常规化疗基础上应用曲妥珠单抗治疗能有效提高晚期HER2阳性乳腺癌患者的临床疗效,可在一定程度上改善患者免疫功能、降低肿瘤标记物水平、提高患者的疾病控制率及生存率,且安全性较高。但由于本研究样本数量及随访时间有限,并未对患者的5年甚至更远期生存率进行探究,后续仍需通过大量大样本、前瞻性研究进一步证实。

